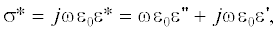Электрохимия, 2019, T. 55, № 3, стр. 366-372
Определение высокочастотной электропроводности растворов NaCl и KCl по скорости их нагрева электрическим полем с частотой 27 МГц
А. Е. Луньков a, *, Д. Г. Ковалёв a, Н. Б. Шестопалова a, Ю. А. Фомина a
a Саратовский государственный медицинский университет
410012 Саратов, ул. Б. Казачья, 112, Россия
* E-mail: aelunkov@mail.ru
Поступила в редакцию 16.07.2018
После доработки 14.09.2018
Принята к публикации 01.11.2018
Аннотация
Предложена методика определения высокочастотной электропроводности водных растворов электролитов, основанная на измерении скорости одновременного нагрева ВЧ-электрическим полем двух жидкостей в зазоре конденсатора. Равенство напряженностей электрического поля обеспечивалось параллельным размещением кювет с растворами и соединением их двумя общими электродами. Отношение скоростей нагрева электролита и воды, измеренное при этом условии, позволяет определить отношение их электропроводностей. Для ВЧ-нагрева использовали аппарат УВЧ-терапии, позволяющий воздействовать на объекты как электрическим, так и магнитным полем с частотой 27.12 МГц. Приводятся особенности экспериментального определения скорости нагрева исследуемых жидкостей электрическим и магнитным полями. Определены скорости нагрева ВЧ-электрическим полем воды и растворов NaCl и KCl в диапазоне концентраций 0.004–20%. Установлено, что скорость нагрева растворов многократно превышает скорость нагрева дистиллированной воды. Максимальная скорость нагрева и предельная ВЧ электропроводность, соответствующая для обоих растворов концентрации 0.5%, превышают эти параметры воды примерно в 60 раз. В диапазоне концентраций 1–20% экспериментально подтверждена прямая пропорциональность между статической электропроводностью электролитов и скоростью их нагрева ВЧ-магнитным полем.
ВВЕДЕНИЕ
Тепловой эффект воздействия электромагнитной энергии ВЧ- и СВЧ-диапазонов широко используется для промышленных, исследовательских, бытовых и лечебных целей. В настоящее время для этого чаще всего используются выделенные частоты 27.12 и 2455 МГц, в связи с чем сохраняется научный интерес к измерениям кинетики высокочастотного разогрева различных сред и значений их электрофизических параметров на этих частотах. При этом как возможности практического применения, так и методики исследований определяются различиями в получении электромагнитных колебаний ВЧ- и СВЧ-диапазонов, поскольку на ВЧ используются колебательные системы с сосредоточенными параметрами, а на СВЧ – объемные резонаторы. Поэтому, несмотря на повышение теплового эффекта с ростом частоты электромагнитных полей, ВЧ-диапазон широко используется в силу большей глубины прогрева, а также больших конструктивных возможностей для разогрева объектов разных размеров и формы, так как конденсаторные и индукционные нагреватели легче приспособить к разным объектам по сравнению с объемными резонаторами.
В публикациях, посвященных изучению высокочастотных значений электрофизических параметров воды и водных растворов, обычно рассматриваются частоты СВЧ-диапазона, близкие к области максимального поглощения. Отсутствуют данные об использовании экспериментальных значений скорости нагрева для определения высокочастотных значений электропроводности жидкостей. Все эти обстоятельства и определили проведение исследований, результаты которых приводятся в данной работе.
Теоретический анализ. При ВЧ-разогреве веществ в электрическом поле конденсатора удельная мощность потерь энергии – Р [Вт/м3] выражается формулой
где Е – напряженность электрического поля, σ – высокочастотная электропроводность вещества [1, 2].В переменном электрическом поле существуют два механизма нагрева вещества – за счет токов проводимости свободных носителей заряда и за счет диэлектрических потерь, вызываемых поляризацией связанных зарядов. Поэтому высокочастотные параметры электролитов, где присутствуют оба вида потерь, представляют в виде комплексной электропроводности σ* = σ' + jσ" или комплексной диэлектрической проницаемости ε* = ε' – jε", связанных соотношением
где ω = 2πf – круговая частота поля, ε0 = 8.85 × × 10–12 Ф/м – абсолютная диэлектрическая проницаемость вакуума [3]. В общем случае удельная электропроводность σ, входящая в выражение (1), имеет значение комплексной электропроводности вещества на данной частоте переменного электрического поля.Частотную зависимость диэлектрической проницаемости воды и водных растворов обычно исследуют, используя уравнении Дебая [4]:
(3)
$\begin{gathered} \varepsilon {\text{'}} = {{\varepsilon }_{\infty }} + \frac{{{{\varepsilon }_{S}} - {{\varepsilon }_{\infty }}}}{{1 + (\omega ){{\tau }^{2}}}}, \hfill \\ \varepsilon '' = \frac{{{{\varepsilon }_{S}} - {{\varepsilon }_{\infty }}}}{{1 + (\omega ){{\tau }^{2}}}}(\omega )\tau , \hfill \\ \end{gathered} $(4)
$\sigma {\text{'}} = \frac{{{{\sigma }_{\infty }}}}{{{\text{1}} + {\text{(}}\omega {\text{)}}{{\tau }^{{\text{2}}}}}}(\omega ){{\tau }^{2}},$Для воды область дисперсии диэлектрической проницаемости лежит в диапазоне 109–1011 Гц, для которого опубликовано большое число работ по высокочастотной диэлектрической проницаемости и электропроводности воды и водных растворов электролитов, например, работы [5–8]. В частности, показано [9], что на частоте 2455 МГц электропроводность водного раствора NaCl меньше высокочастотной электропроводности воды ($\sigma '$ = 1.35 См/м) и уменьшается с ростом концентрации до 0.31 См/м при концентрации 5 М. Эти данные получены с использованием выражения (4) и значений εS и τ, приведенных в справочнике [10] и работе [6]. Значения диэлектрической проницаемости и электропроводности, вычисляемые на основе соотношений Дебая, дают значения только дипольной составляющей, в то время как в растворах электролитов присутствует и ионная составляющая проводимости. В работе [8] приводятся значения мнимой составляющей диэлектрической проницаемости ε" и ее ионной (ε")ион и дипольной (ε")дип составляющих 4 М раствора NaCl в диапазоне частот 3–100 ГГц. Показано, что вклад ионной составляющей в ε" возрастает от 29% на 100 ГГц до 98% на 3ГГц, причем с уменьшением частоты разность ε"–(ε")ион становится еще меньше.
Для частоты 27 МГц ωτ $ \ll $ 1 и выражение (4) дает $\sigma '$ = ωε0εSωτ, что для воды соответствует значению 1.65 × 10–4 См/м, которое получается на основе данных, приведенных в справочнике [10]. Это значение, соответствующее дипольной составляющей электропроводности, практически совпадает с известным значением остаточной ионной электропроводности очищенной воды – 2 × 10–4 См/м. На этом фоне водные растворы электролитов по сравнению с водой должны иметь существенно большие значения электропроводности именно за счет роста ее ионной составляющей. При этом значения статической электропроводности растворов электролитов, возрастающие с ростом концентрации, не соответствуют значениям ионной составляющей высокочастотной электропроводности в силу сложного механизма взаимодействия ионов и молекул воды и, в первую очередь, процесса гидратации ионов. Поэтому экспериментальное определение значений комплексной высокочастотной электропроводности (ВЧ ЭП) электролитов имеет не только практическое, но и теоретическое значение.
Все виды электропроводности приводят к потерям энергии высокочастотного электрического поля, которая расходуется на нагревание жидкости, причем удельная мощность потерь пропорциональна комплексной электропроводности среды, помещенной в электрическое поле и квадрату напряженности поля (1).
Сама удельная мощность потерь Р может измеряться по скорости нагрева жидкости в силу очевидной зависимости [11]
(5)
$P = {{c}_{{\text{p}}}}\rho \left( {{{\Delta T} \mathord{\left/ {\vphantom {{\Delta T} {\Delta t}}} \right. \kern-0em} {\Delta t}}} \right)\,\,\,[{\text{В т /}}{{{\text{м }}}^{{\text{3}}}}],$Тогда (1) и (5) дают соотношение, непосредственно связывающее скорость нагрева и ВЧ ЭП объекта, помещенного в переменное электрическое поле с напряженностью Е
(6)
${{c}_{{\text{p}}}}\rho \left( {{{\Delta T} \mathord{\left/ {\vphantom {{\Delta T} {\Delta t}}} \right. \kern-0em} {\Delta t}}} \right) = \sigma {{E}^{2}}.$Измерение скорости нагрева – достаточно простая экспериментальная задача, но для определения по ней высокочастотной электропроводности необходимо также определять и напряженность электрического поля Е, действующего на объект. Эта задача осложняется тем, что напряженность поля, необходимая для заметного нагрева, может достигать нескольких кВ/м. Кроме того, ее величина зависит от электрофизических параметров самой нагреваемой среды в силу особенностей реализации воздействия электрическим полем, которые обсуждаются ниже. Поэтому нами была использована методика относительных измерений, позволяющая избежать необходимости измерения напряженности ВЧ-электрического поля Е. Главная идея методики состоит в одновременном нагреве в одном электрическом поле двух жидкостей, для одной из которых значение электропроводности известно. Наиболее логично при исследовании водных растворов брать в качестве этой “опорной” жидкости воду.
МЕТОДИКА ЭКСПЕРИМЕНТА
Для высокочастотного нагрева использовался физиотерапевтический аппарат УВЧ-70-1, работающий на частоте 27.12 МГц и имеющий максимальную выходную мощность 70 Вт. У всех аппаратов УВЧ-терапии имеется вторичный (терапевтический) колебательный контур, индуктивно связанный с основным колебательным контуром LC-генератора, находящимся при работе под высоким напряжением питания. Воздействие осуществляется помещением объекта между круглыми электродами (диаметром 110 мм) основного конденсатора терапевтического контура, расстояние между которыми можно изменять. В терапевтический контур входит также переменный конденсатор для настройки его в резонанс перед началом процедуры.
При необходимости дополнительная настройка может проводиться за счет возможности изменения расстояния между основными электродами в пределах толщины защитных пластиковых футляров, в которые они помещены. Она позволяет регулировать потери, вносимые в измерительный контур за счет перераспределения напряженности поля, приложенной к исследуемым объектам и к переходными емкостями зазоров между ними и электродами конденсатора. Увеличение этих зазоров приводит к уменьшению их емкости и, в силу последовательного соединения, к увеличению напряженности на них. Соответственно уменьшается напряженность поля Е, приложенная к объекту, и потери, вносимые в контур объектом. Все эти особенности работы аппарата неизбежно приводят к зависимости напряженности поля, приложенного непосредственно к объекту, от его электрофизических параметров. Исключение этой зависимости является еще одним преимуществом относительной методики измерений.
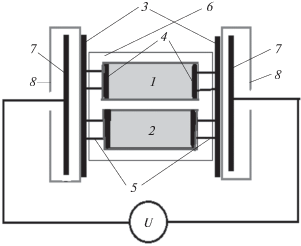
Две жидкости объемом по 40 мл (дистиллированная вода и раствор электролита) в двух прямоугольных пластиковых кюветах размещались между основными электродами вторичного колебательного контура аппарата. Главное условие практической реализации предлагаемой методики – обеспечение равной напряженности электрического поля, действующего на обе жидкости. Это достигалось электрическим соединением жидкостей обеих кювет навесными металлическими электродами. При параллельном размещении кювет использовались два электрода, состоящие из общей внешней пластины, к которой припаяны два разнесенных электрода, входящих вдоль внутренней стороны стенки в каждую из кювет. Шунтирующие электроды навешивались на торцевые стенки кювет, одновременно соединяя находящиеся в них объемы жидкостей. Внешние электроды имели площадь основных электродов и контактировали с плоскостями их защитных футляров. Для минимизации теплообмена между жидкостями соединяющие их внешние электроды изготавливались из фольгированного стеклотекстолита, у которого толщина медного слоя не превышает 50 мкм, а внешний и внутренние электроды соединялись лишь двумя припаянными проволочными контактами. Схема размещения исследуемых жидкостей между электродами УВЧ-аппарата приведена на рис. 1.
Рис. 1.
Размещение исследуемых жидкостей в электрическом поле УВЧ-аппарата: 1 – кювета с водой; 2 – кювета с электролитом; 3 – внешние электроды; 4 – внутренние электроды; 5 – соединения внешнего и внутренних электродов; 6 – контейнер из пенопласта; 7 – основные электроды УВЧ-аппарата; 8 – защитные футляры основных электродов.
Термоизоляции кювет обеспечивалась помещением в контейнер из пенопласта с разделяющей их внутренней перегородкой. Сверху контейнеры закрывались крышкой из пенопласта, в которой имелись отверстия для помещения в жидкости двух спиртовых термометров. Температура воды измерялась термометром с максимальной регистрируемой температурой 40°C при цене деления 0.2°С. Для измерения более высоких температур нагрева электролитов использовался термометр до 100°С с ценой делений 1°.
Измерения проводились при номинальной мощности аппарата 40 Вт с регистрацией температуры жидкостей через 1 мин. Перед началом измерений измерительный контур настраивался в резонанс с помощью подстроечного конденсатора и индикатора настройки. Исследовались растворы NaCl и KCl с концентрациями 0.5, 1, 2, 4, 10, 20%, для приготовления которых использовали бидистиллированную воду.
Используемый УВЧ-аппарат предусматривает также воздействие переменным магнитным полем с помощью подключения к ВЧ-выходу резонансного индуктора в виде плоской катушки диаметром 60 мм, помещенной в защитный пластиковый корпус. В этом случае измерительный контур образуют индуктивность индуктора вместе с соответствующей постоянной емкостью и емкостью того же подстроечного конденсатора. Эта возможность использовалась для исследования зависимости от концентрации скорости нагрева электролитов переменным магнитным полем той же частоты. В этих измерениях не использовалась относительная методика, но обеспечивалась термоизоляция кювет с растворами в процессе нагрева.
РЕЗУЛЬТАТЫ ИЗМЕРЕНИЙ
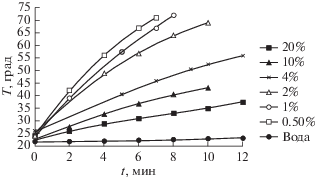
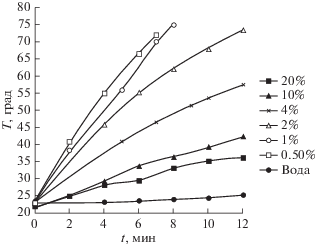
Полученные зависимости температуры жидкостей от времени нагрева приведены на рис. 2 для растворов NaCl и на рис. 3 для растворов KCl.
Согласно приведенным зависимостям скорость нагрева электролитов всегда превосходит скорость нагрева воды, уменьшаясь при увеличении их концентрации. Сами зависимости сохраняют линейность вплоть до температур порядка 50°C, несмотря на 50%-ное увеличение статической электропроводности растворов в температурном интервале 20–50°С [12]. Это косвенно свидетельствует о различии между статической электропроводностью и ионной составляющей высокочастотной электропроводности. Нарушение линейности нагрева при более высоких температурах скорее всего связано с уменьшением значений составляющих комплексной диэлектрической проницаемости [10].
Так как максимальная скорость нагрева наблюдалась при минимальной концентрации обоих электролитов – 0.5%, были проведены дополнительные серии измерений скорости нагрева для сверхмалых концентраций. Для этого использовали растворы, полученные последовательным двукратным разведением дистиллированной водой 0.5%-ных растворов до концентрации 0.0039%.
Полный объем полученных данных, включающий результаты для малых концентраций растворов приведен в табл. 1. Приведенные значения абсолютной скорости нагрева растворов получены усреднением по всем промежуточным временным интервалам.
Таблица 1.
Абсолютные и отнесенные к скорости нагрева воды значения скоростей нагрева растворов в зависимости от их концентрации
| Концентрация растворов, % | NaCl | KCl | ||
|---|---|---|---|---|
| (ΔT/Δt)абс, град/мин | (ΔT/Δt)отн. воды, разы | (ΔT/Δt)абс, град/мин | (ΔT/Δt)отн. воды, разы | |
| 20 | 1.2 | 9.4 | 1.2 | 8.4 |
| 10 | 2.0 | 14.6 | 1.7 | 14.6 |
| 4 | 3.0 | 30.5 | 3.4 | 24.3 |
| 2 | 5.4 | 36.3 | 5.0 | 26.4 |
| 1 | 6.0 | 48.0 | 6.6 | 48.3 |
| 0.5 | 7.2 | 55.7 | 6.9 | 63 |
| 0.25 | 6.2 | 50.6 | 6.7 | 56.7 |
| 0.125 | 5.6 | 47.8 | 6.7 | 48.6 |
| 0.0625 | 5.8 | 38.3 | 6.9 | 35.8 |
| 0.0312 | 7.4 | 26.8 | 10.9 | 31.3 |
| 0.0156 | 6.2 | 22.5 | 7.0 | 24.7 |
| 0.0078 | 5.2 | 7.1 | 5.1 | 15.3 |
| 0.0039 | 2.7 | 6.2 | 3.9 | 11.6 |
В силу близости значений теплопроводности и плотности исследованных жидкостей относительные скорости нагрева фактически показывают, во сколько раз электропроводность раствора больше электропроводности дистиллированной воды (6). Значение абсолютных и относительных скоростей нагрева не всегда коррелируют, что объясняется изменением напряженности поля в зазоре конденсатора при изменении потерь, вносимых в контур разными растворами. Как правило, с увеличением скорости нагрева и электропроводности электролита уменьшается острота настройки контура в резонанс и снижается скорость нагрева воды за счет уменьшения резонансной амплитуды напряженности поля Е. Именно поэтому более точными являются относительные значения скорости нагрева, при которых исключается зависимость от изменения действующего значения напряженности электрического поля.
Оба электролита демонстрируют близкие значения относительной (к скорости нагрева Н2О) скорости нагрева для всех исследованных концентраций, за исключением двух самых малых значений (0.0078 и 0.0039%), для которых значения KCl вдвое выше чем у NaCl.
Полученный максимум концентрационной зависимости фактически соответствует предельному значению ВЧ-электропроводности водных растворов NaCl и KCl на частоте 27 МГц. Если в качестве опорного использовать значение электропроводности воды 1.65 × 10–4 См/м, то предельные значения электропроводности будут равны 0.92 × 10–2 См/м у NaCl и 1.04 × 10–2 См/м у KCl (соответственно их значениям относительной скорости нагрева). С учетом отмеченной выше тенденции к увеличению ионной составляющей ВЧ-электропроводности опорное значение электропроводности воды можно увеличиться на величину ее статической электропроводности – 2 × 10–4 См/м.
Использование в ВЧ-диапазоне колебательных контуров с сосредоточенными элементами (емкостью и индуктивностью) позволяет реализовывать раздельное воздействие на исследуемые объекты только электрическим или только магнитным высокочастотным полем. В случае электролитов поглощение энергии переменного магнитного поля происходит только за счет токов проводимости, а удельная мощность потерь пропорциональна статической электропроводности [1], которая увеличивается с ростом концентрации раствора. Для подтверждения этой очевидной особенности была проведена серия измерений скорости нагрева электролитов переменным магнитным полем с использованием вышеуказанной возможности применения аппаратов УВЧ-терапии. В этих измерениях 30 мл исследуемого раствора заливалось в круглую пластиковую чашку, которая для термоизоляции воздушным слоем помещалась в чашку большего диаметра с крышкой. Эта система устанавливалась на корпусе горизонтально расположенного магнитного индуктора, а термометр вставлялся в отверстие общей крышки, закрывающей обе чашки. В начале измерения индуктор также настраивался в резонанс. Все измерения проводились при номинальной мощности аппарата 70 Вт в течение 10 мин. Полученные значения скорости нагрева для растворов разных концентраций приведены в табл. 2.
Таблица 2.
Скорости нагрева переменным магнитным полем электролитов с разной концентрацией
| Концентрация растворов, % | (ΔT/Δt), град/мин NaCl |
(ΔT/Δt), град/мин KCl |
|---|---|---|
| 1 | 0.35 | 0.4 |
| 2 | 0.6 | 0.8 |
| 4 | 1.35 | 1.7 |
| 10 | 3.05 | 3.9 |
| 20 | 5.35 | 6.4 |
Приведенные в таблице скорости нагрева практически пропорциональны статической электропроводности, соответствующей концентрациям растворов. Нарушение линейности зависимости при 20%-ных концентрациях можно также объяснить уменьшением амплитуды магнитного поля индуктора за счет увеличения потерь, вносимых раствором во вторичный колебательный контур. Главный вывод, который можно сделать на основе сравнения данных табл. 1 и 2, состоит в том, что концентрационные зависимости скорости нагрева электролитов ВЧ-электрическим и ВЧ-магнитным полями носят прямо противоположный характер.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Предложенная методика позволила успешно применить кинетику ВЧ-нагрева для изучения электропроводности электролитов. Полученные результаты показывают, что исследование электрофизических параметров электролитов на частоте, далекой от области их дисперсии, дает интересные результаты, имеющие практическое значение в силу достаточно широкого использования частоты 27 МГц. К этим результатам следует отнести прежде всего значительное увеличение скорости ВЧ-нагрева воды, содержащей малые концентрации ионов. Это означает, что энергозатраты при ВЧ-сушке изделий могут оказаться в десятки раз меньше рассчитанных с использованием справочных данных, которые приводятся для дистиллированной воды. В подтверждение этого можно привести результаты дополнительных измерений, которые показали, что скорость нагрева водопроводной воды оказывается в 20–30 раз больше скорости нагрева дистиллированной воды.
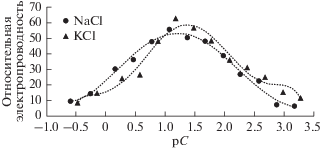
Теоретический интерес может представлять зависимость скорости нагрева и высокочастотной электропроводности исследованных электролитов от их концентрации, в частности максимум этой зависимости при концентрации 0.5%, который означает существование предельных значений ВЧ ЭП растворов хлоридов натрия и калия в ВЧ-диапазоне. Этот результат согласуется с данными, полученными в работе [13], для водного раствора NaCl на частоте 25 МГц. В работе исследовалась ВЧ-электропроводность NaCl, K2SO4 и K3Fe(CN)6 путем измерения импеданса конденсаторной ячейки, содержащей исследуемый раствор. В выражение для комплексной проводимости ячейки вводилась зависимость электропроводности электролита от концентрации по теории Дебая–Фалькенгагена. Теоретически и экспериментально исследовались максимумы зависимости комплексной проводимости ячейки с электролитом от его концентрации. Так как данные измерений приведены в виде зависимости относительного значения электропроводности от логарифма молярной концентрации, на рис. 4 данные табл. 1 приведены в таких же координатах (рС = –lgC(М)). На рис. 4, максимальное значение электропроводности NaCl соответствует рС = 1.1 (0.08 М). В работе [13] соответствующее значение рС для NaCl на частоте 25 МГц порядка 1.3 (0.05 М) с совпадением общего вида зависимости электропроводности от концентрации. Это можно рассматривать как хорошее совпадение с учетом того, что максимум концентрационной зависимости, приведенной в работе [13], можно определить не по экспериментальным точкам, а по аппроксимирующему их полиному. Кроме этого, на частоте 25 МГц, по оценке авторов, существенно возрастают погрешности расчетов в силу увеличения вклада в эквивалентную схему неучитываемой индуктивной составляющей цепи.
Рис. 4.
Зависимость относительных значений электропроводности от молярной концентрации по данным табл. 1.
Максимумы концентрационной зависимости скорости нагрева (а, следовательно, высокочастотной электропроводности) электролитов на частоте 2455 МГц получены и в работе [14], которые соответствовали концентрации 1–1.5 М для NaCl и 1 М для MgCl2. В этой работе использовался нагрев электролитов в СВЧ-поле объемного резонатора, что могло внести методические погрешности, причина которых обсуждается ниже. Однако эти погрешности не должны отразиться на общем виде экспериментальной кривой.
Таким образом, с использованием разных методик измерений и разных частотных диапазонов получены экспериментальные данные, показывающие наличие максимума в зависимости высокочастотной электропроводности электролитов от их концентрации. Сопоставление полученных нами данных и данных работы [13] с данными работы [14] позволяет предположить, что максимальные значения ВЧ-электропроводности электролитов получаются при близких значениях диэлектрических потерь, зависящих от частоты электрического поля, и ионной составляющей электропроводности, зависящей от концентрации. В частности, теоретическое значение максимума зависимости относительной ВЧ-электропроводности от концентрации, приведенное в работе [13], фактически соответствует условию равенства активной и реактивной составляющих комплексной проводимости исследуемого раствора электролита.
На основе этого можно ожидать, что при переходе в ВЧ- (а точнее, в УВЧ) диапазон наиболее интересные результаты могут быть получены при исследовании ВЧ ЭП водных растворов малых концентраций.
Полезным в методическом плане является сопоставление зависимости кинетики нагрева электролитов переменными электрическими и магнитными полями от их концентрации и, соответственно, статической электропроводности. Их различие имеет важное значение при переходе в СВЧ-диапазон, где становится возможным одновременное воздействие на объект, помещенный в объемный резонатор, электрической и магнитной составляющих электромагнитного поля. Этим можно объяснить несоответствие между расчетными значениями электропроводности и экспериментальными значениями скорости нагрева растворов NaCl на частоте 2455 МГц, приведенными в работах [7, 8]. При расчетных значениях электропроводности, изменяющихся от 1.35 См/м для воды до 0.31 См/м для 5 М раствора NaCl (в 4.35 раз) экспериментальные значения скорости нагрева, полученные авторами, менялись для тех же пределов от 0.3 до 0.26 град/с (всего в 1.15 раз). При нагреве жидкости помещали в цилиндрический объемный резонатор, в котором невозможно полное пространственное разделение электрического и магнитного полей, особенно при вносимом с объектом возмущении картины поля. Поэтому совместное противоположное воздействие электрической и частично магнитной составляющих электромагнитного поля уменьшило скорость нагрева, которая в электрическом поле любой частоты должна быть прямо пропорциональной электропроводности.
Для понимания механизма взаимодействия ионной и диэлектрической составляющих электропроводности в переменном электрическом поле представляет интерес продолжение исследований по нагреву электролитов и в СВЧ-диапазоне, где для этих целей доступна частота 2455 МГц. Однако при этом необходимо использовать резонаторы с сосредоточенной емкостью [15], чтобы избежать совместного воздействия на электролит электрической и магнитной составляющих электромагнитного поля.
В заключении можно отметить, что возможности данной методики измерений далеко не ограничиваются исследованными объектами. Исследовательский интерес представляет и возможность сравнительного исследования разных объектов в поле одинаковой напряженности, и используемая частота, которая может оказаться в области дисперсии электрофизических параметров более высокомолекулярных жидкостей.
Список литературы
Глуханов, Н.П. Физические основы высокочастотного нагрева. М.-Л., Машиностроение. 1965, С. 68.
Княжевская, Г.С., Фирсова, М.Г. Высокочастотный нагрев диэлектрических материалов. Л., Машиностроение, 1980, С. 11, 12.
Нетушил, А.В., Жуховицкий, Б.Я., Кудин, В.Н., Парини, Е.П. Высокочастотный нагрев диэлектриков и полупроводников. М.-Л., Госэнергоиздат, 1959.
Дебай, П. Полярные молекулы. М.-Л., ГНТИ, 1931.
Щербаков, В.В. Дисперсия высокочастотной проводимости полярных растворителей. Электрохимия. 1994. Т. 30. № 11. С. 1367.
Засецкий, А.Ю., Лилеев, А.С., Лященко, А.К. Диэлектрические свойства водных растворов NaCl в СВЧ-диапазоне. Журн. неорган. химии. 1994. Т. 39. № 6. С. 1035.
Щербаков, В.В., Артемкина, Ю.М., Короткова, Е.Н. Диэлектрические свойства и высокочастотная проводимость системы хлорид натрия–вода. Журн. неорган. химии. 2014. Т. 59. № 9. С. 1153.
Артемкина, Ю.М., Ермаков, В.И., Коваленко, Л.В., Короткова, Е.Н., Поливанова, А.Г., Щербаков, В.В. Особенности поглощения электромагнитной энергии водными растворами на частоте 2455 МГц. I. Растворы электролитов. Химия и хим. технология. 2014. Т. 57. Вып. 6. С. 86.
Ахадов, Я.Ю. Диэлектрические свойства бинарных растворов. М., Наука, 1977, С. 400.
Ахадов, Я.Ю. Диэлектрические параметры чистых жидкостей. М., Изд-во МАИ, 1999, 856 с.
Пюшнер, Г. Нагрев энергией сверхвысоких частот. М., Энергия, 1968, 310 с.
Добош, Д. Электрохимические константы. Справ. для электрохимиков. М., Мир, 1980, 365 с.
Ghowsi, R.K., Gale Same Aspects of the High Frequency Conductance of Electrolytes, J. Electrochem. Soc., 1989, vol. 136, no. 10, p. 1806.
Артемкина, Ю.М., Коваленко, Л.В., Короткова, Е.Н., Поливанова, А.Г., Щербаков, В.В. Исследование высокочастотного нагревания некоторых водных растворов электролитов и неэлектролитов. Успехи в химии и хим. технологии. 2013. Т. XXVII. № 2. С. 9.
Лебедев, И.В. Техника и приборы СВЧ. Т. 1. М., Высшая школа, 1970, С. 417.
Дополнительные материалы отсутствуют.