Электрохимия, 2019, T. 55, № 3, стр. 335-340
Влияние толщины активного слоя на характеристики электродов из феррофосфата лития
Е. К. Тусеева a, Т. Л. Кулова a, А. М. Скундин a, *, А. К. Галеева b, А. П. Курбатов c
a Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
Москва, Ленинский просп., 31, корп. 4, Россия
b Центр физико-химических методов исследования и анализа
Алматы, Казахстан
c Казахский национальный университет им. Аль-Фараби
Алматы, Казахстан
* E-mail: askundin@mail.ru
Поступила в редакцию 08.06.2018
После доработки 01.09.2018
Принята к публикации 16.10.2018
Аннотация
Методами гальваностатического циклирования и циклической вольтамперометрии впервые исследовано влияние толщины активного слоя (количества активного материала на единице площади электрода) на характеристики электродов на основе феррофосфата лития. При рассмотрении электрода как системы с дважды распределенными параметрами (распределение состава материала по радиусу индивидуального зерна LiFePO4 и распределение процесса по глубине всего активного слоя) сделан вывод, что намного сильнее проявляется неравномерность распределения процесса по глубине активного слоя, чем по объему индивидуальных зерен феррофосфата лития. Предполагается, что этот вывод будет справедлив и для электродов из других материалов.
ВВЕДЕНИЕ
Феррофосфат лития LiFePO4 рассматривается большинством исследователей как наиболее перспективный материал положительного электрода крупномасштабных литий-ионных аккумуляторов, предназначенных, в частности, для электротранспорта и интеллектуальных электросетей. Основные преимущества этого материала – высокая стабильность, способность работать при высоких зарядных и разрядных токах, относительно низкая себестоимость, безопасность, экологичность и т.п. В то же время феррофосфату лития присущи существенные недостатки, прежде всего низкая электронная проводимость и низкий коэффициент диффузии лития. В последние два десятилетия была проведена огромная работа по преодолению этих недостатков путем различных усовершенствований технологии синтеза, различным модификациям и т.д. (см. обзоры [1‒5]). В подавляющем большинстве случаев характеристики феррофосфата лития оценивают по измерениям в дисковых элементах с тонкими электродами, когда толщина активного слоя составляет единицы микрон. Между тем, в реальных аккумуляторах толщина активного слоя на электродах составляет десятки микрон, а с увеличением толщины активного слоя удельные характеристики заметно падают. Сам по себе этот факт известен (см., например, [6, 7]), но далеко не самоочевиден. Действительно, обычный активный слой интеркаляционного электрода представляет собой пористую систему с дважды распределенными параметрами – распределение концентрации лития по радиусу каждого зерна активного материала и распределение концентрации ионов, а также омических потерь в электролите в межзеренном пространстве. С учетом того, что коэффициент диффузии лития в твердой фазе на несколько порядков меньше, чем коэффициент диффузии ионов в жидком электролите, часто предполагают, что неравномерность распределения процесса по толщине активного слоя намного меньше, чем неравномерность распределения концентрации по радиусу индивидуального зерна, однако это предположение в общем виде не оправдывается [8]. В настоящей работе методами гальваностатического циклирования и циклической вольтамперометрии исследовано влияние толщины активного слоя на характер разряда и заряда электродов на основе феррофосфата лития, причем диапазон исследованных толщин охватывал как электроды, типичные для лабораторных исследований функциональных материалов, так и электроды, характерные для реальных литий-ионных аккумуляторов. В определенной степени эта работа является продолжением исследований влияния температуры на характеристики электродов на основе феррофосфата лития [9].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Методика изготовления электродов и сборки ячеек была, в общем, такой же, как описано в [9]. Рабочие электроды изготавливали по стандартной намазной технологии из коммерческого LiFePO4 марки KJ2. По данным поставщика, 50% всех частиц этого материала имеют размер менее 4 мкм, а 10% частиц меньше 0.7 мкм. Содержание углерода в материале составляет 4.7%. В качестве токоотвода использовали сетку из нержавеющей стали квадратного плетения. Диаметр жилок сетки 50 мкм, просвет 100 мкм. Активную массу готовили смешением порошка LiFePO4 (85 мас. %), сажи (10 мас. %, Timcal, Бельгия) и поливинилиденфторида (5 мас. %, Aldrich), предварительно растворенного в N-метилпирролидиноне (Aldrich). Количество активного вещества на электроде размером 15 × 15 мм составляло 5, 14 и 30 мг (что соответствовало 2.22, 6.22 и 13.33 мг/см2). Электроды прессовали давлением 1000 кг/см2 с последующей сушкой под вакуумом при температуре 120°С. Поскольку подложкой рабочего электрода была сетка, а не фольга, точно оценить толщину активного слоя практически невозможно (часть активного материала находится в ячейках сетки). Эффективная плотность активного материала может быть оценена в 1.5 г/см3, так что толщина активного слоя упомянутых выше электродов оценивается в 15, 40 и 90 мкм, что сопоставимо с толщиной сетки. Электрохимические измерения проводили в трехэлектродных герметичных ячейках с литиевым вспомогательным и литиевым электродом сравнения. Ячейки собирали и заполняли электролитом в перчаточном боксе с атмосферой сухого аргона (ОАО “Спектроскопические системы”, Россия). Содержание воды и кислорода в боксе не превышало 1 ppm. В качестве электролита использовали 1 М LiPF6 в смеси этиленкарбонат–диэтилкарбонат–диметилкарбонат (1 : 1 : 1) (все компоненты электролита имели квалификацию “extra dry” и были приобретены в Aldrich). Содержание воды в электролите, определенное кулонометрическим титрованием по К. Фишеру (установка типа 917 Ti-Touch фирмы Metrohm), не превышало 20 ppm. В качестве сепаратора использовали нетканый полипропилен толщиной 15 мкм (НПО “Уфим”).
Гальваностатические измерения проводили с помощью компьютеризированного стенда АЗРВРИК 50 mA–10 V (ОАО “НТЦ Бустер”, Россия) при токе от 0.1 до 22 мА. Во всех случаях ток заряда был равен току разряда. Циклические вольтамперограммы регистрировали с использованием потенциостата-гальваностата Р-20Х8 фирмы “Элинс” (Россия) при скорости развертки потенциала от 0.1 до 4.2 мВ/с. Известно, что деградация феррофосфатных электродов при циклировании не столь значительна, чтобы повлиять на результаты экспериментов с изменяющейся токовой нагрузкой.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Гальваностатические измерения
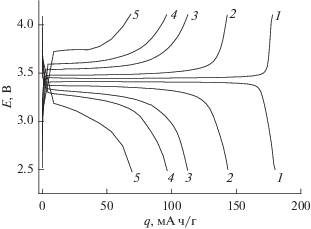
На рис. 1 приведены гальваностатические разрядные и зарядные кривые, полученные на электроде с наиболее тонким активным слоем (2.2 мг/см2). Видно, что на таком электроде при достаточно малом токе 20 мА/г, что соответствует примерно С/8, разрядные и зарядные кривые близки к равновесным, а разрядная емкость близка к теоретической. При более интенсивных режимах гальваностатические кривые сильно отклоняются от равновесных, что связано, в частности, с образованием неравновесных твердых растворов в системе LiFePO4–FePO4. С ростом тока разрядная емкость уменьшается, что свидетельствует о неравномерности распределения процесса по объему электрода, однако рис. 1 еще не позволяет определить, какая неравномерность здесь играет основную роль – неравномерность распределения по радиусу индивидуальных частиц LiFePO4, или неравномерность по толщине активного слоя электрода.
Рис. 1.
Гальваностатические кривые на электроде с содержанием феррофосфата лития 2.2 мг/см2 при токах 100 мкА (20 мА/г, 0.044 мА/см2) (1), 1 мА (200 мА/г, 0.44 мА/см2) (2), 4 мА (800 мА/г, 1.78 мА/см2) (3), 8 мА (1.6 А/г, 3.55 мА/см2) (4) и 16 мА (3.2 А/г, 7.11 мА/см2) (5).
Гальваностатические кривые, полученные на электроде с наиболее толстым активным слоем (13.3 мг/см2), приведены на рис. 2.
Рис. 2.
Гальваностатические кривые на электроде с содержанием феррофосфата лития 13.3 мг/см2 при токе 616 мкА (20 мА/г, 0.275 мА/см2) (1), 3.08 мА (103 мА/г, 1.37 мА/см2) (2), 6.16 мА (205 мА/г, 2.75 мА/см2) (3), 12.32 мА (411 мА/г, 5.47 мА/см2) (4) и 24.64 мА (821 мА/г, 10.95 мА/см2) (5).
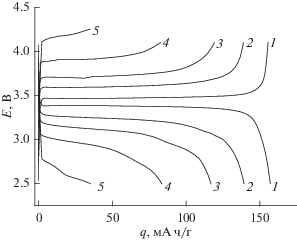
Видно, что увеличение толщины активного слоя не приводит к качественному изменению характера гальваностатических кривых. Основное различие заключается в сильном увеличении поляризации (при одинаковом токе в расчете на массу активного вещества) с ростом толщины активного слоя.
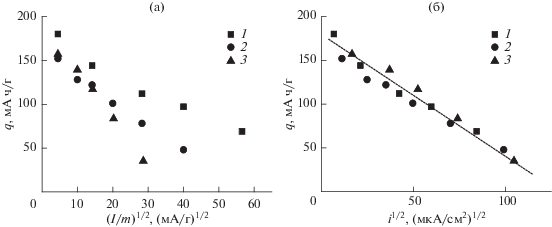
Рисунок 3 показывает характер изменения разрядной емкости с увеличением тока. При одинаковом токе в расчете на массу феррофосфата лития (рис. 3а) емкость заметно падает с увеличением толщины активного слоя. При одинаковой плотности тока в расчете на площадь поверхности электрода (рис. 3б) емкость практически не зависит от толщины активного слоя. Интересно, что в этом случае емкость снижается линейно с корнем квадратным из величины плотности тока. (Аналогичная корневая зависимость емкости электродов на основе феррофосфата лития следует также из данных, приведенных в [10], однако в этой статье такая зависимость не обсуждается). Сопоставление рис. 3а и 3б позволяет сделать вывод о том, что в этих условиях именно неравномерность распределения процесса по глубине активного слоя электрода определяет характеристики электрода в целом. Корневая зависимость емкости Q от плотности тока i, характерная вообще для пористых электродов, соответствует известному уравнению Пейкерта
Рис. 3.
Зависимость разрядной емкости от плотности тока в расчете на массу феррофосфата лития (а) и от плотности тока в расчете на площадь поверхности электрода (б) для электродов с количеством феррофосфата лития 2.2 (1), 6.2 (2) и 13.3 мг/см2 (3).
Некоторое представление о зависимости разрядной емкости от толщины активного слоя (при постоянной плотности тока в расчете на массу феррофосфата лития) дает рис. 4.
Рис. 4.
Зависимость разрядной емкости от толщины активного слоя электрода при плотности тока 20 (1), 200 (2) и 800 мА/г (3). Зависимости линеаризованы по методу наименьших квадратов.
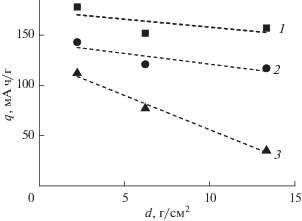
Абсолютное значение наклона прямых на рис. 4 возрастает с ростом плотности тока и составляет 1.59, 2.13 и 6.81 мА ч/см2 при плотности тока 20, 200 и 800 мА/г. В работе [6] приводятся данные о разрядной емкости электрода на основе феррофосфата лития от толщины активного слоя в интервале от 25 до 120 мкм, что в пересчете соответствует диапазону от 5.5 до 26.4 мг/см2 при токе 2 С (около 320 мА/г). Здесь также получена линейная зависимость с абсолютным значением наклона 6.25 мА ч/см2, что хорошо соответствует результатам настоящей работы.
Вывод о доминирующей роли распределения процесса по глубине активного слоя по сравнению с неравномерностью распределения лития по объему индивидуального зерна подтверждается также данными о поляризации электродов. В качестве количественной меры поляризации здесь, как обычно, принята поляризация в середине разрядных или зарядных кривых. Зависимость потенциала на середине гальваностатической кривой от плотности тока приведена на рис. 5. На рис. 5а плотность тока отнесена к единице массы феррофосфата лития, а на рис. 5б – к единице площади электрода.
Рис. 5.
Зависимость поляризации от плотности тока в расчете на единицу массы феррофосфата лития (а) и на единицу площади электрода (б) для электродов с количеством активного вещества 2.2 (квадраты), 6.2 (кружки) и 13.3 мг/см2 (треугольники).
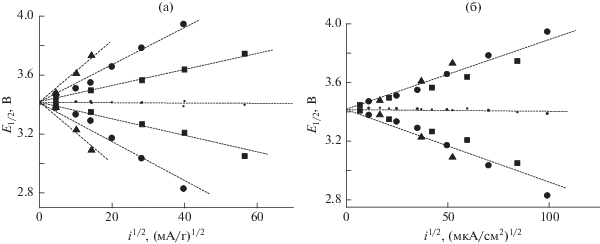
Сравнение рис. 5а и 5б показывает, что поляризация по толщине активного слоя намного превышает поляризацию по отдельным зернам.
Циклическая вольтамперометрия
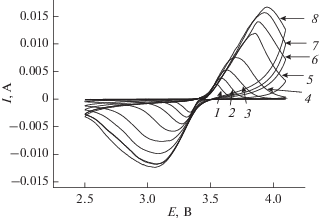
Типичные вольтамперограммы на электроде с наиболее тонким активным слоем (2.2 мг/см2) показаны на рис. 6. В общем, характер этих вольтамперограмм не отличается от приводимых в литературе (см., например, [10–12]). Даже для электрода со столь тонким активным слоем и даже для минимальной использованной в работе скорости развертки потенциала (0.1 мВ/с) сказывается необратимость процесса: разность потенциалов анодного и катодного максимума составляет в этом случае 0.21 В. По мере роста скорости развертки потенциала необратимость возрастает – увеличивается полуширина максимумов, а сами максимумы смещаются, соответственно, в анодную и катодную стороны.
Рис. 6.
Вольтамперограммы на электроде с содержанием феррофосфата лития 2.2 мг/см2 при скоростях развертки потенциала 0.1 (1), 0.2 (2), 0.4 (3), 0.8 (4), 1.6 (5), 2.4 (6), 3.2 (7) и 3.6 мВ/с (8).
Увеличение толщины активного слоя приводило к увеличению необратимости. Для электрода с активным слоем 13.3 мг/см2 в диапазоне потенциалов 2.5−4.1 В удалось получить вольтамперограммы только при скоростях развертки потенциала не более 0.4 мВ/с (рис. 7).
Рис. 7.
Вольтамперограммы на электроде с содержанием феррофосфата лития 13.3 мг/см2 при скоростях развертки потенциала 0.1 (1), 0.2 (2) и 0.4 мВ/с (3).
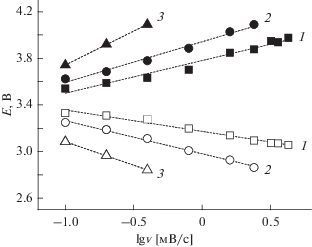
Увеличение необратимости с ростом толщины активного слоя проявляется, в частности, в увеличении поляризации, т.е. в смещении потенциалов максимумов в анодную и катодную стороны. На рис. 8 показаны зависимости потенциалов анодных и катодных максимумов от логарифма скорости развертки потенциала для электродов с разной толщиной активного слоя.
Рис. 8.
Зависимость потенциалов анодных (темные значки) и катодных (светлые значки) максимумов от скорости развертки потенциала для электродов с содержанием активного материала 2.2 (1), 6.2 (2) и 13.3 мг/см2 (3).
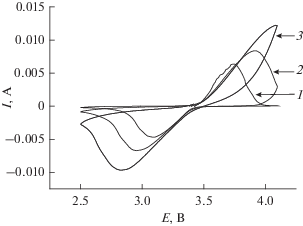
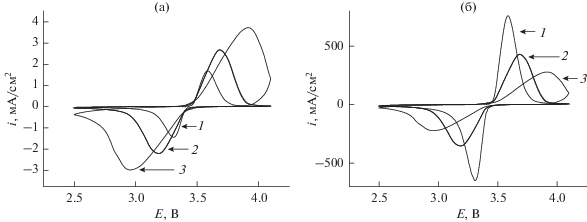
Очень наглядно влияние толщины активного слоя на характеристики электродов на основе феррофосфата лития видно из сопоставления вольт-амперных кривых разных электродов при одной и той же скорости развертки потенциала и при нормировании тока на единицу площади поверхности электрода и на массу активного материала. Такое сопоставление приведено на рис. 9. Увеличение массы активного материала на электроде сопровождается снижением тока (и количества электричества), приходящегося на единицу массы, что свидетельствует о неравномерности распределения процесса по толщине активного слоя.
Рис. 9.
Вольтамперограммы, полученные при скорости развертки потенциала 0.2 мВ/с на электродах с количеством активного материала 2.2 (1), 6.2 (2) и 13.3 мг/см2 (3). Ток нормирован на единицу площади электрода (а) и на единицу массы активного материала (б).
Метод циклической вольтамперометрии часто используют для измерения коэффициентов диффузии в твердой фазе активного материала. Результаты настоящей работы показывают, что такие исследования можно проводить только на электродах с очень тонким активным слоем. Анализ циклических вольтамперограмм настоящей работы показывает, что зависимости тока в максимуме от корня из скорости развертки потенциала линейны и проходят через начало координат. Из наклона таких зависимостей обычно и вычисляют значение коэффициента диффузии. Очевидно, что при равномерном распределении процесса по толщине активного слоя наклон зависимостей тока в максимуме от корня из скорости развертки потенциала должен быть пропорционален площади внутренней поверхности активного слоя, или пропорционален массе активного материала в степени 2/3. В настоящей работе для электродов с содержанием феррофосфата лития 2.2, 6.2 и 13.3 мг/см2 соотношение площадей внутренней поверхности составляет 1.00 : 1.99 : 3.30.
Соотношение наклонов для анодного процесса оказалось 1.00 : 1.86 : 2.14, а для катодного процесса 1.00 : 1.91 : 2.48. Эти данные также свидетельствуют о росте неравномерности распределения процесса по глубине активного слоя с ростом толщины этого слоя.
ЗАКЛЮЧЕНИЕ
В настоящей работе впервые методами гальваностатического циклирования и циклической вольтамперометрии исследовано влияние толщины активного слоя (количества активного материала на единице площади электрода) на характеристики электродов на основе феррофосфата лития. Электрод рассматривается как система с дважды распределенными параметрами – распределение состава материала по радиусу индивидуального зерна LiFePO4 и распределение процесса по глубине всего активного слоя. Количество активного материала изменялось от 2.2 до 13.3 мг/см2, что охватывает диапазон от лабораторных ячеек для изучения свойств собственно активного материала до практических аккумуляторов. Гальваностатическое циклирование проводили при токах от 20 до 3200 мА/г, а циклические вольтамперограммы регистрировали при скоростях развертки потенциала от 0.1 до 3.6 мВ/с. Сделан вывод, что в таких условиях намного сильнее проявляется неравномерность распределения процесса по глубине активного слоя, чем по объему индивидуальных зерен феррофосфата лития.
Приведенные рассуждения, вероятно, будут справедливы и для электродов из других материалов, в том числе для электродов, функционирующих полностью по однофазному механизму.
Список литературы
Yuan, L.-X., Wang, Z.-H., Zhang, W.-X., Hu, X.-L., Chen, J.-T., Huang, Y.-H., and Goodenough, J.B., Development and challenges of LiFePO4 cathode material for lithium-ion batteries, Energy Environ. Sci., 2011, vol. 4, p. 269.
Wang, Y., He, P., and Zhou, H., Olivine LiFePO4: development and future, Energy Environ. Sci., 2011, vol. 4, p. 805.
Wang, J. and Sun, X., Olivine LiFePO4: the remaining challenges for future energy storage, Energy Environ. Sci., 2015, vol. 8, p. 1110.
Gong, C., Xue, Z., Wen, S., Ye, Y., and Xie, X., Advanced carbon materials/olivine LiFePO4 composites cathode for lithium ion batteries, J. Power Sources, 2016, vol. 318, p. 93.
Eftekhari, A., LiFePO4/C nanocomposites for lithium-ion batteries, J. Power Sources, 2017, vol. 343, p. 395.
Yu, D.Y.W., Donoue, K., Inoue, T., Fujimoto, M., and Fujitani, S., Effect of Electrode Parameters on LiFePO4 Cathodes, J. Electrochem. Soc., 2006, vol. 153, p. A835.
Ke, L., Lv, W., Fang-Yuan Su, F-Y., He, Y-B., You, C.-H., Li, B., Li, Z., Yang, Q-H., and Kang, F., Electrode thickness control: Precondition for quite different functions of graphene conductive additives in LiFePO4 electrode, Carbon, 2015, vol. 92, p. 311.
Roberts, M.R., Madsen, A., Nicklin, C., Rawle, J., Palmer, M.G., Owen, J.R., and Hecto, A.L., Direct Observation of Active Material Concentration Gradients and Crystallinity Breakdown in LiFePO4 Electrodes During Charge/Discharge Cycling of Lithium Batteries, J. Phys. Chem. C, 2014, vol. 118, p. 6548.
Тусеева, Е.К., Кулова, Т.Л., Скундин, А.М., Галеева, А.К., Курбатов, А.П. Влияние температуры на поведение электродов из феррофосфата лития, Электрохимия (в печати)
Avci, E., Mazman, M., Uzun, D., Biçer, E., and Şener, T., High performance LiFePO4/CN cathode material promoted by polyaniline as carbon–nitrogen precursor, J. Power Sources, 2013, vol. 240, p. 328.
Gao, H., Jiao, L., Yang, J., Qi, Z., Wang, Y., and Yuan, H., High rate capability of Co-doped LiFePO4/C, Electrochim. Acta, 2013, vol. 97, p. 143.
Du, J., Jiao, L., Wu, Q., Liu, Y., Qi, Z., Guo, L., Wang, Y., Huatang, and Yuan, H., Mesoporous LiFePO4 microspheres for rechargeable lithium-ion batteries, Electrochim. Acta, 2013, vol. 98, p. 288.
Дополнительные материалы отсутствуют.


