Электрохимия, 2019, T. 55, № 5, стр. 619-628
Восстановление бромат-аниона на вращающемся дисковом электроде в стационарных условиях: сравнение численного и аналитического решений уравнений конвективной диффузии при избытке протонов
А. Е. Антипов a, b, *, М. А. Воротынцев a, b, c, d, **, Д. В. Конев a, c, Е. М. Антипов a, b
a Российский химико-технологический университет им. Д.И. Менделеева
125047 Москва, А-47, Миусская пл., 9, Россия
b Московский государственный университет им. М.В. Ломоносова
119992 Москва, ГСП-1, Ленинские горы, 1, Россия
c Институт проблем химической физики РАН
142432 Московская обл., Черноголовка, просп. академика Семенова, 1, Россия
d Институт молекулярной химии университета Бургундии
Дижон, Франция
* E-mail: 89636941963antipov@gmail.com
** E-mail: mivo2010@yandex.com
Поступила в редакцию 25.12.2017
После доработки 27.11.2018
Принята к публикации 03.12.2018
Аннотация
Статья содержит результаты численного анализа конвективно-диффузионных транспортных уравнений для компонентов электрохимического процесса восстановления бромат-аниона на вращающемся дисковом электроде по механизму редокс-медиаторного автокатализа (ЕС"). Задача решена с учетом различия в величинах их коэффициентов диффузии. Предполагается постоянство концентрации протонов внутри раствора, включая диффузионный слой, благодаря ее достаточно большой величины по сравнению с концентрацией бромат-ионов. Сравнение полученных результатов с предсказаниями приближенного аналитического исследования той же системы [Vorotyntsev M.A., Antipov A.E. Electrochim. Acta. 2017. V. 246. P. 1217] подтверждает адекватность разработанного аналитического подхода для расчетов как распределений концентраций компонентов системы (за исключением очень больших толщин диффузионного слоя), так и максимальной плотности тока для широкого интервала значений внешних параметров - состава раствора, скорости реакции конпропорционирования, интенсивности конвекции (частоты вращения электрода), проходящего тока.
ВВЕДЕНИЕ
В последние годы активный поиск экологически чистых способов получения электроэнергии привлек дополнительное внимание к проблематике электрохимических источников тока. Одним из таких источников является водородно-броматная проточная редокс-батарея [1]. От своих ближайших аналогов – проточных-редокс батарей на основе ванадия, цинка, меди и др. [2, 3] – ее отличают высокие показатели по мощности и плотности энергии [1].
Известно, что бромат-анион, выступающий в такой системе в роли основного окислителя, в исследуемом интересном с практической точки зрения интервале потенциалов не может быть восстановлен на электроде напрямую без значительного перенаряжения [4, 5]. В работе [6] впервые было показано, что в достаточно кислой среде в присутствии даже очень небольшого количества молекулярного брома (на несколько порядков меньшего, чем объемная концентрация бромат-аниона) благодаря медиаторному автокатализу (EC'' механизму) можно решить эту проблему через каталитический цикл, состоящий из обратимой окислительно-восстановительной гетерогенной реакции (1) на электроде и необратимой (в кислых растворах) гомогенной химической стадии – реакции конпропорционирования (2):
(1)
${\text{B}}{{{\text{r}}}_{2}} + 2{{{\text{e}}}^{ - }} \rightleftarrows \,\,2{\text{B}}{{{\text{r}}}^{ - }},$(2)
${\text{BrO}}_{3}^{ - } + 5{\text{B}}{{{\text{r}}}^{ - }} + 6{{{\text{H}}}^{ + }} \to 3{\text{B}}{{{\text{r}}}_{2}} + 3{{{\text{H}}}_{{\text{2}}}}{\text{O}}.$Следует отметить, что процесс в целом демонстрирует при оптимальной интенсивности конвекции быструю кинетику за счет автокаталитического эффекта [6], и лимитирующей его стадией в стационарных условиях оказывается диффузионный транспорт бромат-аниона из объема раствора в приэлектродную область, где он расходуется в ходе реакции (2). В результате разрядный ток может достигать величин, сравнимых и даже превышающих величину предельного диффузионного тока по основному окислителю – бромат-аниону. Так, например, при объемной концентрации бромат-аниона в воде порядка нескольких моль/л и сопоставимой концентрации протонов плотность разрядного тока на электроде может достигать нескольких А/см2 [1, 6]. Не менее многообещающие теоретические оценки можно получить и для плотности энергии (более 500 Вт/кг) такой системы, что обусловлено высокой растворимостью водного раствора бромата и шестиэлектронной природой процесса электровосстановления бромат-аниона до бромид-аниона благодаря сочетанию реакций (1) и (2) [7].
Так как этот процесс лежит в основе указанного электрохимического механизма, который представляется весьма перспективным для электрохимической энергетики, данной работой авторский коллектив продолжает систематическое изучение закономерностей ионного транспорта в рассматриваемых системах, выполняемое методами численного анализа соответствующих транспортных уравнений [6, 7], со сравнением этих результатов с предсказаниями приближенного аналитического расчета.
В работах [8, 9] используется модель неподвижного слоя Нернста [10, 11] для вращающегося дискового электрода, поверхность которого обладает свойством равнодоступности, а все профили концентрации реагентов зависят только от нормальной к поверхности электрода координаты z. Таким образом, учет эффекта конвективного переноса компонентов раствора за счет гидродинамического движения раствора около поверхности диска осуществляется путем определения слоя толщины zd, внутри которого перенос компонентов происходит только за счет диффузионного транспорта, а вне слоя (при z ≥ zd) концентрации компонентов постоянны и равны значениям в объеме раствора. Толщина диффузионного слоя zd связана с частотой вращения дискового электрода f по формуле Левича [12],
(3)
${{z}_{{\text{d}}}} = 1.61{{D}^{{1{\text{/}}3}}}{{\nu }^{{1{\text{/}}6}}}{{\left\{ {({{2\pi } \mathord{\left/ {\vphantom {{2\pi } {60}}} \right. \kern-0em} {60}})f\left[ {{\text{rpm}}} \right]} \right\}}^{{ - 1{\text{/}}2}}}.$Несмотря на то, что такая модель хорошо описывает основные закономерности для указанной системы на качественном уровне, она является чрезмерно упрощенной и, например, не учитывает того обстоятельства, что в системе с несколькими реагентами в формуле (3) наступает неопределенность в выборе значения коэффициента диффузии D (если коэффициенты диффузии реагентов различаются). Также модель Нернста не позволяет учесть влияние конвективного переноса на распределения концентраций компонентов во внешней части диффузионного слоя в такой системе.
Недавно впервые была развита аналитическая теория для конвективно-диффузионного транспорта в ходе броматного процесса, причем для различающихся величин коэффициентов диффузии для различных реагентов системы [13]. Та же система уравнений конвективно-диффузионного транспорта, учитывающих как электрохимический процесс (1), протекающий на поверхности электрода, так и реакцию конпропорционирования (2), была решена численными методами при условии одинаковых коэффициентов диффузии для различных компонентов [14]. В данной работе представлены результаты численного анализа указанной системы уравнений при произвольных значениях величин коэффициентов диффузии для компонентов. Полученные результаты сравниваются с предсказаниями приближенного исследования [13] для этой системы, имея в виду, что их согласие означает правильность обоих подходов.
ОПИСАНИЕ СИСТЕМЫ
На вращающемся дисковом электроде происходит процесс электровосстановления бромата ${\text{BrO}}_{3}^{ - }$ (реагент A концентрации A) с участием бромид-аниона Br– (реагент B концентрации B) до молекулярного брома Br2 (реагент C концентрации C) в кислой среде посредством автокаталитического цикла (1)–(2) (механизм EC'') благодаря присутствию молекулярного брома Br2. В объеме раствора концентрация бромат-аниона A° на несколько порядков превышает (следовую) концентрацию брома C° (A° $ \gg $ C°); бромид-анион Br– (реагент B), образующийся на поверхности электрода по реакции (1), в объеме раствора отсутствует из-за реакции (2).
В общем случае транспорт реагентов в системе обусловлен совокупностью диффузионного, конвекционного и миграционного вкладов. Рассматривая, как и ранее [6, 8, 13, 14], случай, когда протоны в виде ионов гидроксония находятся в избытке по сравнению со всеми другими компонентами (H° $ \gg $ A°), можно показать [14], что изменением локальной концентрации протонов можно пренебречь и считать ее постоянной. В этом случае протоны играют роль фонового электролита (совместно с неактивными ионными компонентами в объеме раствора), что позволяет пренебречь миграционным членом в транспортных уравнениях.
Комбинация реакций (1)–(2) представляет собой каталитический цикл, основанный на редокс-паре бромид/бром, благодаря которому бромат A участвует в реакции электровосстановления, несмотря на его неэлектроактивность на электроде в исследуемом интервале потенциалов. Известно, что реакция конпропорционирования (2) состоит из последовательных элементарных стадий и ее скорость V имеет первый порядок по бромат- и бромид-анионам [15–18]:
(4)
$V \equiv {{--{\text{d}}A} \mathord{\left/ {\vphantom {{--{\text{d}}A} {{\text{d}}t}}} \right. \kern-0em} {{\text{d}}t}} = kAB,$Таким образом, учитывая конвективный и диффузионный транспорт в системе, запишем систему уравнений для пространственных профилей концентрации бромат-аниона A(z), бромид-аниона B(z) и брома C(z):
(5)
${{D}_{A}}{{{\text{d}}}^{2}}{{A\left( z \right)} \mathord{\left/ {\vphantom {{A\left( z \right)} {{\text{d}}{{z}^{2}}}}} \right. \kern-0em} {{\text{d}}{{z}^{2}}}} = {{v}_{z}}\left( z \right){\text{d}}A{{\left( z \right)} \mathord{\left/ {\vphantom {{\left( z \right)} {{\text{d}}z}}} \right. \kern-0em} {{\text{d}}z}} + V\left( z \right),$(6)
${{D}_{B}}{{{\text{d}}}^{2}}{{B\left( z \right)} \mathord{\left/ {\vphantom {{B\left( z \right)} {{\text{d}}{{z}^{2}}}}} \right. \kern-0em} {{\text{d}}{{z}^{2}}}} = {{v}_{z}}\left( z \right){\text{d}}B{{\left( z \right)} \mathord{\left/ {\vphantom {{\left( z \right)} {{\text{d}}z}}} \right. \kern-0em} {{\text{d}}z}} + V\left( z \right),$(7)
${{D}_{C}}{{{\text{d}}}^{2}}{{C\left( z \right)} \mathord{\left/ {\vphantom {{C\left( z \right)} {{\text{d}}{{z}^{2}}}}} \right. \kern-0em} {{\text{d}}{{z}^{2}}}} = {{v}_{z}}\left( z \right){\text{d}}C{{\left( z \right)} \mathord{\left/ {\vphantom {{\left( z \right)} {{\text{d}}z}}} \right. \kern-0em} {{\text{d}}z}} - 3V\left( z \right),$На бесконечном удалении от поверхности электрода профили концентраций стремятся к величинам концентраций в объеме раствора:
На поверхности электрода балансовые соотношения между потоками реагентов и величиной плотности катодного тока j принимают вид:
(9)
$\begin{gathered} {{{\text{d}}A} \mathord{\left/ {\vphantom {{{\text{d}}A} {{\text{d}}z}}} \right. \kern-0em} {{\text{d}}z}} = 0,\,\,{{D}_{{\text{B}}}}{{{\text{d}}B} \mathord{\left/ {\vphantom {{{\text{d}}B} {{\text{d}}z}}} \right. \kern-0em} {{\text{d}}z}} = - {j \mathord{\left/ {\vphantom {j F}} \right. \kern-0em} F},\,\,\,{{D}_{{\text{C}}}}{{{\text{d}}C} \mathord{\left/ {\vphantom {{{\text{d}}C} {{\text{d}}z}}} \right. \kern-0em} {{\text{d}}z}} = {j \mathord{\left/ {\vphantom {j {2F}}} \right. \kern-0em} {2F}},\,\, \\ j \geqslant 0\,\,{\text{д л я }}\,\,z = 0, \\ \end{gathered} $ПРОЦЕДУРА ОБЕЗРАЗМЕРИВАНИЯ
Процедура обезразмеривания повторяет работу [14], поэтому представлена здесь кратко. Характерной длиной вдоль z направления является толщина кинетического слоя zk, которая, по определению, представляет собой расстояние, на которое бромид-анионы B при режиме слабых токов успевают за счет диффузии отойти от поверхности электрода, прежде чем большинство из них вступит в гомогенную реакцию (2) с броматом A.
(10)
${{z}_{{\text{k}}}} = {{\left( {{{{{D}_{{\text{B}}}}} \mathord{\left/ {\vphantom {{{{D}_{{\text{B}}}}} {5kA^\circ }}} \right. \kern-0em} {5kA^\circ }}} \right)}^{{0.5}}}.$Обезразмеривая пространственную координату z на указанную характерную длину zk, получим
(11)
$x = {z \mathord{\left/ {\vphantom {z {{{z}_{{\text{k}}}}}}} \right. \kern-0em} {{{z}_{{\text{k}}}}}}.$В соответствии с выводами работы [19] следует определить индивидуальные толщины диффузионного слоя zdi для каждого из реагентов в соответствии с формулой (3) и соответствующие безразмерные величины xdki, равные отношениям толщин диффузионного и кинетического слоев для i-го реагента:
(12)
${{x}_{{{\text{dkA}}}}} = {{{{z}_{{{\text{dA}}}}}} \mathord{\left/ {\vphantom {{{{z}_{{{\text{dA}}}}}} {{{z}_{{\text{k}}}}}}} \right. \kern-0em} {{{z}_{{\text{k}}}}}},\,\,{{x}_{{{\text{dkB}}}}} = {{{{z}_{{{\text{dB}}}}}} \mathord{\left/ {\vphantom {{{{z}_{{{\text{dB}}}}}} {{{z}_{{\text{k}}}}}}} \right. \kern-0em} {{{z}_{{\text{k}}}}}},\,\,{{x}_{{{\text{dkC}}}}} = {{{{z}_{{{\text{dC}}}}}} \mathord{\left/ {\vphantom {{{{z}_{{{\text{dC}}}}}} {{{z}_{{\text{k}}}}}}} \right. \kern-0em} {{{z}_{{\text{k}}}}}}.$Последние в соответствии с формулой (3) связаны между собой отношениями коэффициентов диффузии реагентов:
(13)
$\begin{gathered} {{z}_{{{\text{dA}}}}}:{{z}_{{{\text{dB}}}}}:{{z}_{{{\text{dC}}}}} = {{x}_{{{\text{dkA}}}}}:{{x}_{{{\text{dkB}}}}}:{{x}_{{{\text{dkC}}}}} = \\ = D_{{\text{A}}}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}:D_{{\text{B}}}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}:D_{{\text{C}}}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}. \\ \end{gathered} $Профили концентраций обезразмерены аналогично работе [8]
(14)
$\begin{gathered} a\left( x \right) = {{A\left( z \right)} \mathord{\left/ {\vphantom {{A\left( z \right)} {A^\circ }}} \right. \kern-0em} {A^\circ }},\,\,b\left( x \right) = {{B\left( z \right)} \mathord{\left/ {\vphantom {{B\left( z \right)} {B^\circ }}} \right. \kern-0em} {B^\circ }}, \\ c\left( x \right) = {{{{D}_{{\text{C}}}}C\left( z \right)} \mathord{\left/ {\vphantom {{{{D}_{{\text{C}}}}C\left( z \right)} {{{D}_{{\text{B}}}}B^\circ }}} \right. \kern-0em} {{{D}_{{\text{B}}}}B^\circ }},\,\,\,B^\circ \equiv {{j{{z}_{{\text{k}}}}} \mathord{\left/ {\vphantom {{j{{z}_{{\text{k}}}}} {F{{D}_{{\text{B}}}}}}} \right. \kern-0em} {F{{D}_{{\text{B}}}}}}. \\ \end{gathered} $Безразмерная плотность катодного тока равна
(15)
$J = {j \mathord{\left/ {\vphantom {j {j_{{\text{A}}}^{{\lim }}}}} \right. \kern-0em} {j_{{\text{A}}}^{{\lim }}}},\,\,\,\,\quad{{J}_{{{\text{CA}}}}} = {{j_{{\text{C}}}^{{\lim }}} \mathord{\left/ {\vphantom {{j_{{\text{C}}}^{{\lim }}} {j_{{\text{A}}}^{{\lim }}}}} \right. \kern-0em} {j_{{\text{A}}}^{{\lim }}}},\,\,\,\,\quad{{J}_{{{\text{CA}}}}} \ll 1,$Величина J ограничена сверху безразмерной величиной Jmax= jmax/$j_{{\text{A}}}^{{\lim }},$ которая отвечает максимальной плотности катодного тока jmax. Ранее было показано [6, 7], что величина тока, протекающего в системе, зависит от концентрации брома в приэлектродной области, а ситуация, когда на поверхности электрода (при z = x = 0) гетерогенная реакция (1) протекает настолько интенсивно, что локальная концентрация брома на электроде c(0) становится равной нулю, отвечает максимальной плотности тока J = Jmax (и j = jmax, соответственно) [6].
Поскольку реагент A не восстанавливается напрямую на электроде в указанном интервале потенциалов, то и толщина диффузионного слоя zdА для бромат-аниона, равно как и величина $j_{{\text{A}}}^{{\lim }},$ определены здесь формально из соображений наглядности, как это будет показано ниже при обсуждении полученных результатов.
Уравнения (5–6) с граничными условиями (8), (9) можно переписать в безразмерном виде [13]:
(16)
$\begin{gathered} {{{{{\text{d}}}^{2}}a\left( x \right)} \mathord{\left/ {\vphantom {{{{{\text{d}}}^{2}}a\left( x \right)} {{\text{d}}{{x}^{2}}}}} \right. \kern-0em} {{\text{d}}{{x}^{2}}}} = - \left( {{{\alpha ^\circ } \mathord{\left/ {\vphantom {{\alpha ^\circ } {x_{{{\text{dkA}}}}^{3}}}} \right. \kern-0em} {x_{{{\text{dkA}}}}^{3}}}} \right){{x}^{2}}{{{\text{d}}a\left( x \right)} \mathord{\left/ {\vphantom {{{\text{d}}a\left( x \right)} {{\text{d}}x}}} \right. \kern-0em} {{\text{d}}x}} + \\ + \,\,\left( {{J \mathord{\left/ {\vphantom {J {{{x}_{{{\text{dkA}}}}}}}} \right. \kern-0em} {{{x}_{{{\text{dkA}}}}}}}} \right)a\left( x \right)b\left( x \right), \\ \end{gathered} $(17)
$\begin{gathered} {{{{{\text{d}}}^{2}}b\left( x \right)} \mathord{\left/ {\vphantom {{{{{\text{d}}}^{2}}b\left( x \right)} {{\text{d}}{{x}^{2}}}}} \right. \kern-0em} {{\text{d}}{{x}^{2}}}} = - \left( {{{\alpha ^\circ } \mathord{\left/ {\vphantom {{\alpha ^\circ } {x_{{{\text{dkB}}}}^{3}}}} \right. \kern-0em} {x_{{{\text{dkB}}}}^{3}}}} \right){{x}^{2}}{{{\text{d}}b\left( x \right)} \mathord{\left/ {\vphantom {{{\text{d}}b\left( x \right)} {{\text{d}}x}}} \right. \kern-0em} {{\text{d}}x}} + \\ + \,\,a\left( x \right)b\left( x \right), \\ \end{gathered} $(18)
$\begin{gathered} {{{{{\text{d}}}^{2}}c\left( x \right)} \mathord{\left/ {\vphantom {{{{{\text{d}}}^{2}}c\left( x \right)} {{\text{d}}{{x}^{2}}}}} \right. \kern-0em} {{\text{d}}{{x}^{2}}}} = - \left( {{{\alpha ^\circ } \mathord{\left/ {\vphantom {{\alpha ^\circ } {x_{{{\text{dkC}}}}^{3}}}} \right. \kern-0em} {x_{{{\text{dkC}}}}^{3}}}} \right){{x}^{2}}{{{\text{d}}c\left( x \right)} \mathord{\left/ {\vphantom {{{\text{d}}c\left( x \right)} {{\text{d}}x}}} \right. \kern-0em} {{\text{d}}x}} - \\ - \,\,0.6a\left( x \right)b\left( x \right), \\ \end{gathered} $(19)
$\begin{gathered} a\left( x \right) \to 1,\,\,b\left( x \right) \to 0,\,\, \\ c\left( x \right) \to c^\circ = {{F{{D}_{{\text{C}}}}C^\circ } \mathord{\left/ {\vphantom {{F{{D}_{{\text{C}}}}C^\circ } {j{{z}_{{\text{k}}}}}}} \right. \kern-0em} {j{{z}_{{\text{k}}}}}} = {{{{x}_{{{\text{dkC}}}}}{{J}_{{{\text{CA}}}}}} \mathord{\left/ {\vphantom {{{{x}_{{{\text{dkC}}}}}{{J}_{{{\text{CA}}}}}} {2J}}} \right. \kern-0em} {2J}}\,\,{\text{д л я }}\,\,x \to \infty , \\ \end{gathered} $(20)
${{{\text{d}}a} \mathord{\left/ {\vphantom {{{\text{d}}a} {{\text{d}}x}}} \right. \kern-0em} {{\text{d}}x}} = 0,\,\,{{{\text{d}}b} \mathord{\left/ {\vphantom {{{\text{d}}b} {{\text{d}}x}}} \right. \kern-0em} {{\text{d}}x}} = - 1,\,\,\,{{{\text{d}}c} \mathord{\left/ {\vphantom {{{\text{d}}c} {{\text{d}}x}}} \right. \kern-0em} {{\text{d}}x}} = {1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}\,\,\,{\text{д л я }}\,\,x = 0.$В результате получим систему дифференциальных уравнений с граничными условиями для пространственных профилей концентрации основных реагентов, содержащую следующие безразмерные параметры: набор отношений толщин диффузионного и кинетического слоев для каждого из компонентов xdkA, xdkB и xdkC; отношение JCA для предельных диффузионных токов по брому и бромат-аниону (JCA $ \ll $ 1 при условии низкой концентрации брома по сравнению с концентрацией бромат-аниона в объеме раствора); величину безразмерной плотности тока J, выступающую в качестве дополнительного параметра для гальваностатического режима.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Настоящее исследование ставит целью получить решение поставленной выше задачи конвективно-диффузионного транспорта численными методами и сравнить результаты численных расчетов с полученными ранее в работе [13] асимптотическими решениями для основных характеристик системы – пространственных профилей концентрации основных реагентов и зависимости максимальной плотности тока Jmax от отношения толщин диффузионного и кинетического слоев для брома C, xdkC.
В работе [13] были получены формулы для основных характеристик системы в рамках двух асимптотических приближений: для режимов “слабого тока” и “тонкого кинетического слоя”.
Первый из режимов предполагает, что для достаточно слабого катодного тока можно пренебречь изменением концентрации бромат-аниона A в приэлектродной области, т.е. считать, что концентрация A приближенно постоянна во всех точках и равна объемному значению, т.е. a(x) ≈ 1. При подстановке указанного значения a(x) = 1 в уравнения (16) система упрощается, и возможно записать асимптотические формулы для пространственных профилей концентрации основных реагентов, выражения (14a), (14c), (15a) в [13], а также сделать вывод, что для xdkC < 1 и для xdkC ~ 1 в таком приближении максимальная плотность тока Jmax ~ JCA, а для 1 < xdkC < 6 величина Jmax зависит от параметра xdkC, но остается малой (Jmax$ \ll $ 1).
В случае, когда толщина кинетического слоя значительно превышает толщины диффузионных слоев для всех реагентов, т.е., если выполняется условие xdkA, xdkB, xdkC$ \ll $ 1, асимптотические выражения для профилей концентрации a(x), b(x), c(x) принимают еще более простой вид (16c) из [13]. Сравнение численных результатов для a(x) свидетельствует о малости потребления бромат-аниона в приэлектродной области, и, следовательно, малой величине отклонения пространственного профиля концентрации бромат-аниона a(x) от соответствующего объемного значения, равного 1 (1 – a(0) $ \ll $ 1), что отлично согласуется с аналитическими приближениями. Сравнение результатов для профилей b(x) и c(x) с выводами, полученными на основе формулы (16c) из [13] для xdkC = 0.1, также показывает хорошую сходимость (рис. 1). Такое совпадение ожидаемо: максимальная величина тока J = Jmax ≅ JCA, т.е. очень мала, что свидетельствует о чрезвычайно малом потреблении реагента A в ходе гомогенной реакции (2).
Рис. 1.
Безразмерные пространственные профили концентрации для бромид-аниона b(x) и брома c(x) для xdkC = 0.1. Параметры xdkB = 0.09, xdkA = 0.11 рассчитаны по формуле (13), где DA = 1.48 × 10–5 см2 с–1, DB = 2.08 × 10–5 см2 с–1 [20], DC = 1.18 × 10–5 cм2 с–1 [21]. Сплошные кривые рассчитаны аналитически в рамках приближения “слабого тока” для достаточно толстого кинетического слоя согласно (16c) из [13], штриховые кривые – результат численного решения системы уравнений (16), (17), (18). Расчеты проведены для максимального тока Jmax = JCA = 10–4.

Концентрация брома C при приближении к поверхности электрода демонстрирует квазилинейный спад, тогда как концентрация бромид-аниона B, наоборот, квазилинейный рост на масштабах толщины диффузионного слоя xdkC или xdkВ. Такое поведение близко к зависимости, выведенной Левичем [12] для окислительно-восстановительного процесса на поверхности электрода за счет редокс-пары бром/бромид, т.е. отвечает ситуации, когда бромат-анион A практически не участвует химических превращениях в ходе реакции (2) в приэлектродной области из-за очень малой концентрации бромида B, образовавшегося из брома C. Нулевая концентрация брома на поверхности электрода показывает, что в данном случае величину катодного тока лимитирует диффузионный перенос брома из объема раствора, а величина этого тока (в безразмерных единицах), которая соответствует максимальной катодной плотности тока в системе J = Jmax, равна предельной диффузионной плотности тока брома, т.е. JCA. Из-за усиления влияния конвекции при удалении от поверхности электрода наблюдается отклонение от линейной зависимости на расстояниях, сопоставимых с толщиной диффузионного слоя как для реагента B, так и для C.
При увеличении толщины диффузионного слоя по сравнению с толщиной кинетического (увеличении параметра xdkC) растет и величина максимального тока Jmax, так как все большее количество бромид-анионов B успевает прореагировать с бромат-анионами A по реакции (2) в ходе диффузионного транспорта в приэлектродной области, что приводит к увеличению потребления A и, как следствие, отклонению профиля a(x) от 1, т.е. его объемного значения при приближении к поверхности электрода (рис. 2а). Тем не менее, даже для случая, когда толщина диффузионного слоя в несколько раз превышает толщину кинетического (xdkC = 4), формула (14c) предсказывает, что условие c(0) = 0, отвечающее максимальному току Jmax, достигается уже при слабом токе J = Jmax = 9 JCA, т.е. ток в системе можно еще считать слабым и использовать формулы для “режима слабого тока”. Из согласия численных и аналитических кривых, представленных на рис. 2, можно сделать вывод, что приближение слабых токов [13] с хорошей точностью (отклонение между численными и аналитическими результатами не превышает 5%) воспроизводит численное решение даже для случая, когда J превышает JCA практически на порядок (рис. 2 отвечает случаю J = 7 JCA).
Рис. 2.
Безразмерные пространственные профили концентрации для бромат-аниона a(x), бромид-аниона b(x) и брома c(x) при xdkC = 4.0. Сплошные кривые рассчитаны в рамках приближения “слабого тока” для достаточно тонкого кинетического слоя согласно формулам (17a), (18b) из [13], штриховые кривые – результат численного решения системы уравнений (16), (17), (18). Расчеты проведены для тока J = 7 × 10–4, JCA = 10–4.
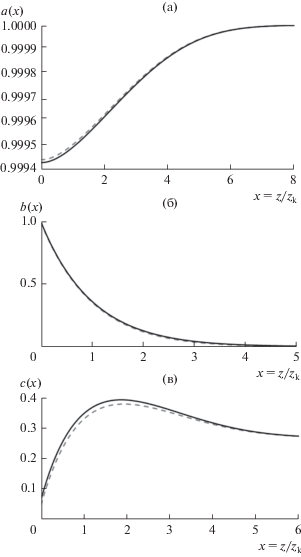
Для xdkC$ \gg $ 1 в работе [13] методом сращивания асимптотических приближений получены асимптотические формулы (21f) и (21h) для случая “тонкого кинетического слоя”, в рамках которого концентрацию бромат-аниона внутри кинетического слоя можно считать постоянной и равной a(0). При значениях параметра xdkC, меньших его критического значения, равного 6, толщина кинетического слоя в безразмерных единицах xkj практически равна ее значению для слабых токов, т.е. 1, что сводит общие формулы (21f), (21h) к формулам (17a), (18b). Соответствующие результаты для профилей концентраций уже были показаны на рис. 2.
На рис. 3 представлено сравнение пространственных профилей концентрации a(x), b(x) и c(x) для A, B- и C-реагентов, соответственно, построенных аналитически по формулам (21f) и (21h) с результатами численного моделирования для значения параметра xdkC, равного 8 (т.е., превышающего критическое значение 6) для случая максимального тока Jmax = 0.5. Потребление бромат-аниона в приэлектродной области в ходе реакции (2) становится в этом случае большим и приводит к значительному градиенту концентрации профиля a(x) в приэлектродной области (рис. 3а).
Рис. 3.
Безразмерные пространственные профили концентрации для бромат-аниона a(x), бромид-аниона b(x) и брома c(x) при xdkC = 8.0. Сплошные кривые рассчитаны аналитически в рамках приближения “тонкого кинетического слоя” согласно (21f) и (21h) из [13], штриховые кривые – результат численного решения системы уравнений (16), (17), (18). Расчеты проведены для максимального тока Jmax = 0.5, JCA = 10–4.
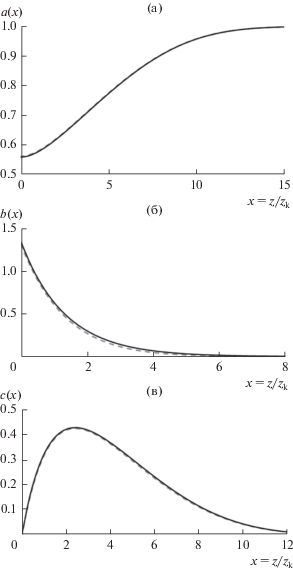
В результате реализации автокаталитического цикла (1)–(2) происходит интенсивное (сопоставимое с величиной a(0)) накопление компонентов редокс-пары в приэлектродной области, о чем свидетельствует немонотонное поведение профиля концентрации c(x) для брома C с максимумом в приэлектродной области (рис. 3в): при утонении кинетического слоя (xdkC > 6) бром C, образованный в результате реакции (2) в основном диффундирует обратно к электроду, а лишь небольшая его часть (около 1/6) уходит в объем раствора. Концентрационный профиль b(x) для бромида B демонстрирует близкий к экспоненциальному рост при приближении к поверхности электрода (рис. 3б), но в отличие от случая xdkC < 6, величина b(0) становится больше 1, что также является следствием сопоставимого с величиной a(0) накопления компонентов редокс пары.
Из согласия аналитических и численных результатов можно сделать вывод, что предложенный аналитический подход адекватно описывает указанные выше особенности поведения профилей концентраций основных реагентов и хорошо воспроизводит численные результаты, когда толщина диффузионного слоя становится гораздо больше толщины кинетического слоя, в частности когда их отношение xdkC превышает его критическое значение, равное 6. Заметим, что в этом случае максимальный ток jmax становится сопоставимым с предельным диффузионным током бромат-иона $j_{{\text{A}}}^{{\lim }},$ т.е. в безразмерных величинах Jmax порядка 1, а толщины диффузионных слоев для компонентов zdi начинают зависеть от величины проходящего тока J. Как видно из рис. 3, даже при максимальной плотности тока это изменение распределения концентраций адекватно описывается приближенными аналитическими формулами для “режима тонкого кинетического слоя”.
Однако при еще более высоких значениях xdkC, когда безразмерный максимальный ток приближается к своей верхней границе (равной 1.2), аналитические предсказания, основанные на приближении тонкого кинетического слоя", показывают отклонение от численных результатов при прохождении очень сильного тока, близкого к максимальному (рис. 4). Причиной отклонения является нарушение условия постоянства профиля концентрации a(x) = a(0) для бромат-аниона A внутри тонкого кинетического слоя, которое наблюдается с увеличением параметра xdkC. Для xdkC $ \gg $ 6 максимальная плотность катодного тока Jmax приближается к 1.2, что отвечает большой величине размерной максимальной плотности тока jmax ≅ 1.2 $j_{{\text{A}}}^{{\lim }}.$ Потребление бромат-аниона А в приэлектродной области в ходе реакции (2) настолько увеличивается, что концентрация A вблизи электрода a(0) падает до столь малой величины, что даже небольшое (по сравнению с 1) ее изменение внутри тонкого кинетического слоя становится сначала сопоставимым с абсолютным значением a(0), а при дальнейшем увеличении xdkC – много большим, чем a(0). При этом аналитические выражения для профилей концентраций, выведенные в “приближении тонкого кинетического слоя”, начинают все более отличаться от корректных (полученных численным интегрированием, см. ниже), поскольку величина a(x) существенно изменяется по сравнению с a(0) внутри кинетического слоя – несмотря на малую толщину этого слоя по сравнению с диффузионным. В таком случае система может быть описана аналитическими формулами, выведенными в рамках приближения “сильных токов” [22], когда реакция (2) из-за отсутствия бромат-аниона A вблизи поверхности электрода прекращается, и образуется тонкая реакционная зона, отодвинутая от поверхности электрода, внутри которой локализована гомогенная реакция конпропорционирования (2).
Рис. 4.
Безразмерные пространственные профили концентрации для бромат-аниона a(x), бромид-аниона b(x) и брома c(x) при xdkC = 20.0. Сплошные кривые рассчитаны аналитически в рамках приближения “тонкого кинетического слоя” согласно (21f) и (21h) из [13], штриховые кривые – результат численного решения системы уравнений (16), (17), (18). Расчеты проведены для фиксированной величины JCA = 10–4 и различных величин плотности тока J: максимальной плотности тока J = Jmax = 1.07; J ≈ 0.8 Jmax = 0.85; J ≈ 0.5 Jmax = 0.5.
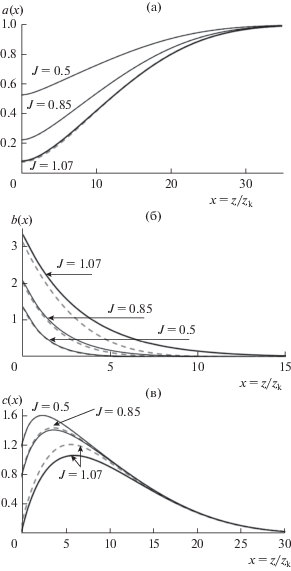
Численные расчеты подтверждают нарушение условия постоянства профиля концентрации a(x) = a(0) для достаточно больших xdkC (например, xdkC = 20), что приводит к росту расхождения между численными и аналитическими расчетами для пространственных профилей концентраций основных реагентов с увеличением величины плотности тока J (рис. 4). Так, при фиксированном значении xdkC = 20 для предельного тока J = = Jmax = 1.07 величина a(0) достаточно мала – не превышает 0.1, тогда как максимальное отклонение аналитических предсказаний распределений концентраций от численных результатов составляет около 7%. В то же время для значения плотности тока J меньшего, чем максимальное, например, J = 0.8 Jmax = 0.85, которой соответствует величина a(0) ≈ 0.2, относительное отклонение аналитических профилей концентрации по сравнению с численными результатами уже не превышает 2% (рис. 4).
Численные результаты для зависимости безразмерной максимальной плотности катодного тока Jmax от параметра xdkC, т.е. отношения толщин диффузионного и кинетического слоев для брома С представлены на рис. 5. Соответствующая аналитическая кривая на рис. 5 построена интерполяцией выведенных в работе [13] приближений:
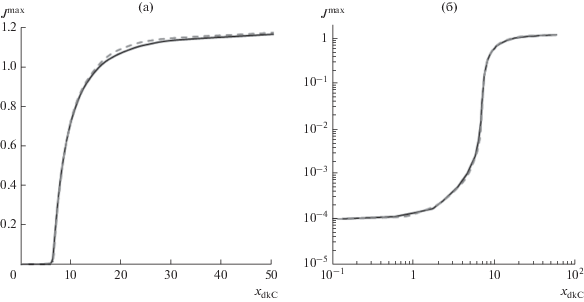
Рис. 5.
Зависимость безразмерной максимальной плотности катодного тока Jmax от параметра xdkC, т.е. от отношения толщин диффузионного и кинетического слоев для брома при JCA = 10–4. Сплошные кривые рассчитаны аналитически для xdkC < 1 по формуле (16e) из [13] и формуле (21) данной работы, 1 < xdkC < 3 в рамках приближения “слабого тока”, формула (19) из [13], и xdkC > 3 в рамках приближения “тонкого кинетического слоя”, формулы (21j) и (21k) из [13]; штриховые кривые – результат численного решения системы уравнений (16), (17), (18).
• для xdkC < 0.5 использована формула (16e) из [13],
• для 0.5 < xdkC < 1 величину Jmax можно получить, подставляя условие c(0) = 0 в (15a) из [13]
(21)
${{J}^{{\max }}} = J_{{{\text{CA}}}}^{*}{{\left( {1 - 1.2{{I}_{2}}\left( {0,{{x}_{{{\text{dkC}}}}}} \right){\text{/}}{{x}_{{{\text{dkC}}}}}} \right)}^{{ - 1}}},$• для 1 < xdkC < 3 использована формула (19) из [13], основанная на приближении “слабого тока”,
• для xdkC > 3 – формулы (21j) и (21k) из [13], выведенные в приближении “тонкого кинетического слоя”.
Совпадение численных и аналитических результатов на рис. 5 позволяет рассматривать предложенные в [13] аналитические подходы для оценки максимальной плотности тока в системе не только на качественном, но и количественном уровне, не прибегая к численным расчетам. Отметим, что аналитическое выражение для максимального тока, выведенное в “приближении тонкого кинетического слоя”, очень хорошо (отклонение не превышает 2%) воспроизводит данные численного интегрирования в области даже очень больших значений параметра xdkC, когда наблюдается уже значительное расхождение для профилей концентраций (рис. 4).
ЗАКЛЮЧЕНИЕ
В работе впервые получены численные решения для задачи конвективно-диффузионного транспорта реагентов при электровосстановлении бромат-аниона на равнодоступной поверхности вращающегося дискового электрода в стационарных условиях в случае избытка протонов. Полученные численными методами профили концентраций основных реагентов (бромат-аниона A, бромид-аниона B и брома C) хорошо согласуются с аналитическими формулами для того же набора уравнений конвективно-диффузионного транспорта, выведенными ранее в работе [13], в рамках областей применимости соответствующих аналитических приближений, перекрывающих основные области изменения задаваемых параметров системы (кроме очень больших значений параметра xdkC). Такое согласие результатов позволяет использовать предложенный в [13] аналитический подход для оценки основных характеристик системы не только на качественном, но и количественном уровне, не прибегая к численным расчетам. В частности, продемонстрировано прекрасное совпадение аналитических предсказаний и результатов численного анализа для величины максимальной катодной плотности тока Jmax в зависимости от ключевого параметра системы – отношения толщин диффузионного и кинетического слоев для брома C (параметра xdkC). Разработанный в рамках данной работы алгоритм численного расчета может быть использован для численного анализа более сложных электрохимических систем, подобных представленной в работе.
Сравнение решений уравнений конвективно-диффузионного транспорта и их приближенных вариантов (модели “неподвижного слоя Нернста” [6, 8] и “Обобщенной модели слоя Нернста” [19]) было дано в работе [13], где было продемонстрировано, что при существенном различии коэффициентов диффузии компонентов (в частности, уже при различии в 2 раза) невозможно выбрать единую толщину “неподвижного слоя Нернста” zd так, чтобы полученные таким образом профили всех концентраций воспроизводили бы результаты конвективно-диффузионной теории хотя бы внутри кинетического слоя. Напротив, “Обобщенная модель слоя Нернста”, позволяющая выбирать индивидуальную толщину диффузионного слоя zdi для каждого компонента i (по формуле Левича), хорошо воспроизводит как профили всех концентраций во внутренней части диффузионного слоя. По очевидной причине обе модели не могут воспроизвести плавного вывода концентраций на их значения в объеме раствора.
Список литературы
Tolmachev, Y.V., Piatkivskyi, A., Ryzhov, V.V., Konev, D.V., and Vorotyntsev, M.A., Energy cycle based on a high specific energy aqueous flow battery and its potential use for fully electric vehicles and for direct solar-to-chemical energy conversion, J. Solid State Electrochem., 2015, vol. 19, p. 2711.
Толмачев, Ю.В., Воротынцев, М.А. Топливные элементы с химически регенерируемыми редокс-катодами. Электрохимия. 2014. Т. 50, С. 451. [Tolmachev, Yu. V. and Vorotyntsev, M. A., Fuel Cells with Chemically Regenerative Redox Cathodes, Russ. J. Electrochem., 2016, vol. 50, p. 403–411.]
Tanaka, Y., Chapter in Ion exchange membranes. Fundamentals and applications. (Second Edition), Elsevier B.V., 2015.
Трушкина, O.A., Федорович, H.B., Ботухова, Г.Н. Скрытые предельные токи при восстановлении анионов второй группы. Электрохимия. 1995. Т. 32. С. 832. [Trushkina, O.A., Fedorovich, N.V., and Botuchova G.N., Hidden limiting currents for electroreduction of the second group anions, Russ. J. Electrochem., 1995, vol. 32, p. 857.]
Skunik, M. and Kulesza, P.J., Phosphomolybdate-modified multi-walled carbon nanotubes as effective mediating systems for electrocatalytic reduction of bromate, Anal. Chim. Acta, 2009, vol. 631, p. 153.
Vorotyntsev, M.A., Konev, D.V., and Tolmachev, Y.V., Electroreduction of halogen oxoanions via autocatalytic redox mediation by halide anions: novel EC" mechanism. Theory for stationary 1D regime, Electrochim. Acta, 2015, vol. 173, p. 779.
Vorotyntsev, M.A., Antipov, A.E., and Konev, D.V, Bromate anion reduction: novel autocatalytic (EC") mechanism of electrochemical processes, Its implication for redox flow batteries of high energy and power densities, Pure Appl. Chem., 2017, vol. 89, doi https://doi.org/10.1515/pac-2017-0306
Антипов, А.Е., Воротынцев, М.А. Электровосстановление бромат-аниона на неактивном ВДЭ в стационарных условиях. Численное исследование процессов ионного транспорта и реакции конпропорционирования. Электрохимия. 2016. Т. 52. С. 1039. [Antipov, A.E. and Vorotyntsev, M.A., Bromate anion electroreduction on inactive RDE under steady-state conditions. Numerical study of ion transport processes and comproportionation reaction, Russ. J. Electrochem., 2016, vol. 52, p. 925.]
Антипов, А.Е., Воротынцев, М.А., Толмачев, Ю.В., и др. Электровосстановление бромат-аниона в кислых растворах на неактивном ВДЭ в стационарных условиях. Численное моделирование процесса в условиях избытка бромат-аниона по сравнению с протонами. Доклады Академии наук. 2016. Т. 468. С. 37. [Antipov, А.Е., Vorotyntsev, M.A., Tolmachev, Y.V., et al., Electroreduction of bromate anion in acidic solutions at the inactive rotating disc electrode under steady-state conditions: Numerical modeling of the process with bromate anions being in excess compared to protons, Doklady Physical Chemistry, 2016, vol. 468, p. 141.]
Nernst, W., Theorie der Reaktionsgeschwindigkeit in heterogenen Systemen, Z. Phys. Chem., 1904, vol. 47, p. 52.
Nernst, W. and Merriam, E.S., Zur Theorie des Reststroms, Z. Phys. Chem., 1905, vol. 53, p. 235.
Левич, В.Г. Физико-химическая гидродинамика. М.: Физматгиз, 1959. 700 с.
Vorotyntsev, M.A. and Antipov, A.E., Bromate electroreduction from acidic solution at rotating disc electrode. Theory of steady-state convective-diffusion transport, Electrochim. Acta, 2017, vol. 246, p. 1217.
Антипов, А.Е., Воротынцев, М.А. Восстановление бромат-аниона на ВДЭ в стационарных условиях при избытке протонов: численное решение уравнений конвективной диффузии при одинаковых коэффициентах диффузии компонентов. Электрохимия. 2017. Т. 54. С. 72. [Antipov, A.E. and Vorotyntsev, M.A., Bromate anion electroreduction on RDE under steady state conditions in excess of protons: numerical solution of the convection-diffusion equations with equal diffusion coefficients of components, Russ. J. Electrochem., 2017, vol. 54, p. 62.]
Cortes, C.E.S. and Faria, R.B., Revisiting the kinetics and mechanism of bromate-bromide reaction, J. Brazilian Chem. Soc., 2001, vol. 12, p. 775.
Cortes, C.E.S. and Faria, R.B., Kinetics and mechanism of bromate-bromide reaction catalyzed by acetate, Inorg. Chem., 2004, vol. 43, p. 1395.
Schmitz, G., Kinetics of the bromate-bromide reaction at high bromide concentrations, Intern. J. Chem. Kinet., 2007, vol. 39, p. 1721.
Pugh, W., The stability of bromic acid and its use for the determination of bromide in bromates and in chlorides, Trans. R. Soc. S. Afr., 1932, vol. 20, p. 327.
Vorotyntsev, M.A. and Antipov, A.E., Reduction of bromate anion via autocatalytic redox-mediation by Br2/Br− redox couple. Theory for stationary 1D regime. Effect of different Nernst layer thicknesses for reactants, J. Electroanal. Chem., 2016, vol. 779, p. 146.
Bruno, T.J. and Lide, D.R., CRC Handbook of Chemistry and Physics, 97th Edition, ed. W.M. Haynes, CRC Press, Boca Raton, FL, 2015.
Cussler, E.L., Diffusion: Mass Transfer in Fluid Systems, second ed. Cambridge University Press, New York, 1997.
Антипов, А.Е., Воротынцев, М.А. Максимальная плотность тока при восстановлении бромат-аниона на вращающемся дисковом электроде: асимптотическое поведение при больших толщинах диффузионного слоя. Электрохимия. 2018. Т. 54. С. 214. [Antipov, A.E. and Vorotyntsev, M.A., Maximum current density for bromate anion electroreduction on RDE: asymptotic behavior for large diffusion layer thicknesses, Russ. J. Electrochem., 2018, vol. 54, In press.]
Дополнительные материалы отсутствуют.



