Электрохимия, 2019, T. 55, № 7, стр. 841-853
Высокочувствительное определение меламина в молоке электрохимическим датчиком MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ
Руичи Чжао a, Шушонг Сун a, Венвен Хао a, Хуимей Гуо a, Инин Гао a, Лей Ши a, *
a Колледж химии и химической технологии, Ляонинский педагогический университет
116029 Далянь, КНР
* E-mail: shilei515dl@126.com
Поступила в редакцию 20.09.2018
После доработки 26.11.2018
Принята к публикации 22.12.2018
Аннотация
Методом самосборки успешно изготовлен высокочувствительный электрохимический датчик меламина, содержащий композиционный материал хитозан – диспергированный в поливинилпирролидоне восстановленный оксид графена (ХТЗ-ПВП-вОГ), наночастицы золота (Au-НЧ) и металлоорганический каркас MIL-101. Для исследования характеристик модифицированных материалов и электродов использованы рентгеновская дифракция (РД), инфракрасная спектроскопия с преобразованием Фурье (ИКС-ПФ), просвечивающая электронная микроскопия (ПЭМ), сканирующая электронная микроскопия (СЭМ), энергодисперсионная рентгеновская спектроскопия (ЭДРС), циклическая вольтамперометрия (ЦВ), спектроскопия электрохимического импеданса (СЭИ) и дифференциальная импульсная вольтамперометрия (ДИВ). Результаты показали, что датчик MIL‑101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ проявляет высокую чувствительность и селективность, а также хорошую устойчивость и воспроизводимость для определения меламина, поскольку ХТЗ‑ПВП-вОГ или Au-НЧ может существенно повышать проводимость датчика, кроме того MIL‑101 может значительно способствовать адсорбции меламина на поверхности модифицированного электрода. При pH 7.0, скорости развертки потенциала 100 мВ/с и частоте 50 Гц предел определения меламина был низким, составляя лишь 5.00 × 10–11 М с диапазоном линейности от 5.00 × 10–11 до 1.00 × 10–8 М и коэффициентом корреляции (R) 0.996. На основе электрохимического поведения меламина на MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ предложен возможный механизм окисления–восстановления меламина. Датчик MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ применен для определения меламина в молочных продуктах, и получен удовлетворительный результат.
1. ВВЕДЕНИЕ
Меламин, тример цианамида, часто незаконно добавляют в молочные продукты и корм для животных в целях искусственного повышения измеряемого содержания белка вследствие своего высокого содержания азота в нем (66 мас. %) и низкой стоимости [1]. Сама по себе токсичность меламина является низкой, однако если его введение превышает предел безопасности, он может вызывать некоторые серьезные проблемы для здоровья, такие как слепота, камни в почках, поражение репродуктивной системы и т.д. [2]. Чрезмерный прием меламина может даже вызывать расстройство мочевой системы, почечную недостаточность, рак или смерть [3]. До настоящего времени многие младенцы и дети испытывали расстройства мочевой системы вследствие потребления детских питательных смесей или родственных молочных продуктов с добавками меламина [4]. Таким образом, чтобы контролировать добавление меламина в продукты, Управление по пищевым продуктам и лекарственным средствам США, Европейская комиссия и другие страны установили критерии максимального уровня остаточного меламина [5].
До настоящего времени были разработаны многочисленные аналитические методы обнаружения меламина в пищевых продуктах и материалах, вступающих в контакт с пищей, такие как газовая хроматография (ГХ) [6], жидкостная хроматография/масс-спектрометрия (ЖХ/МС) [7], высокоэффективная жидкостная хроматография (ВЭЖХ) [8], твердофазный иммуноферментный анализ (ТИФА) [9], спектроскопия усиленного поверхностью комбинационного рассеяния (СУПКР) [10], технология электрохемилюминесценции [11] и т.д. Однако перечисленные выше методы, как правило, страдают от таких проблем, как сложность обработки образцов, значительный расход времени, высокая стоимость приборов и т.д.
В последнее время электрохимический метод привлекает усиленное внимание благодаря своим выдающимся преимуществам, таким как простота предварительной обработки, короткое время анализа, портативность, высокая чувствительность и т.д. [12]. В целях повышения чувствительности и селективности электрохимических датчиков разработаны многочисленные подходящие модифицированные материалы [13–15]. MIL-101 представляет собой превосходный металлоорганический каркасный материал, имеющий выдающиеся характеристики, такие как огромная удельная площадь поверхности и высокий поровый объем, и успешно применяемый во многих областях, таких как катализ [16], хранение газа [17], датчики [18], люминесценция [19], ионный обмен [20], аккумуляторы [21] и т.д. Важно отметить, что применение MIL-101 в электрохимических датчиках быстро растет в последние годы, поскольку он имеет высокодоступную поверхностную пористость и центры координационной ненасыщенности [13, 18]. Например, Ye и др. [13] изготовили электрохимический датчик на основе модифицированного угольного пастового электрода MIL-101, который проявляет повышенную электрокаталитическую активность по отношению к окислению дофамина и мочевой кислоты. Модифицированный датчик MIL-101(Cr)/XC-72 проявляет высокую чувствительность и селективность в определении хлорамфеникола [18]. Кроме того, наночастицы золота (Au-НЧ) и восстановленный оксид графена (вОГ) признаны в качестве весьма перспективных кандидатов для модификации электродов вследствие своих превосходных свойств, таких как простота изготовления, хорошая способность переноса электронов, легкость модификации, высокая совместимость и т.д., и они были успешно применены во многих конструкциях электрохимических датчиков [15, 22, 23]. В целях улучшения диспергирования вОГ в водном растворе и дополнительного повышения его проводимости в водный раствор вОГ может быть добавлен гидрофильный полимер поливинилпирролидон (ПВП), чтобы ингибировать перекристаллизацию вОГ, поскольку ПВП проявляет значительную силу связывания вОГ с образованием комплекса, в результате чего вОГ может быть хорошо диспергирован в водном растворе и устойчиво существует [24]. В последнее время применение хитозана в области электрохимии также привлекает огромное внимание [25], поскольку он может образовывать мембрану, имеющую хорошую электрохимическую устойчивость, с проводящими материалами химическим методом, и, таким образом проводимость композиционных материалов, содержащих проводящие материалы с хитозаном, выше, чем проводимость самих проводящих материалов [26].
В настоящей работе электрохимический датчик на основе композиционного материала, содержащего хитозан, диспергированный в поливинилпирролидоне восстановленный оксид графена (ХТЗ-ПВП-вОГ), наночастицы золота и металлоорганический каркас MIL-101, впервые изготовлен в процессе самосборки и применен для обнаружения меламина с достижением удовлетворительного результата. Модифицированные материалы электродов охарактеризованы методами РД, ИКС-ПФ и ПЭМ. Кроме того, модифицированные электроды охарактеризованы и исследованы методами СЭМ, ЭДРС, СЭИ, ЦВ и ДИВ соответственно. Предложен механизм окисления-восстановления меламина на датчике MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ, и исследовано применение датчика для образца молока.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
2.1. Реагенты и материалы
Меламин и HAuCl4 · 4H2O были получены от компании Sigma-Aldrich (США). Цитрат натрия, графитовый порошок, хитозан, Na2HPO4, NaH2PO4, K3Fe(CN)6, терефталевая кислота, Cr(NO3)3 · 9H2O, фтористоводородная кислота, диметилформамид (ДМФ), хлорид калия и поливинилпирролидон были получены от компании Sinopharm Chemical Reagent Co., Ltd. Glucose (ГЛЮ), лимонная кислота (ЛК), хлоруксусная кислота и ацетат свинца были приобретены от компании Tianjin Kermel Chemical Reagent Co., Ltd. Все химические реагенты относились к категории “ч. д. а.” и были использованы без дополнительной очистки. Все эксперименты в фосфатно-солевом буферном растворе (ФСБР) были осуществлены при комнатной температуре (25°C).
2.2. Приборы и методы
Электрохимические измерения были осуществлены на электрохимической рабочей станции CHI760E от компании Chenhua Instruments Co. (Шанхай, КНР). Для всех электрохимических измерений традиционная трехэлектродная система представляла собой: немодифицированный или модифицированный стеклоуглеродный электрод (СУЭ, диаметр 3 мм) в качестве рабочего электрода, насыщенный каломельный электрод (НКЭ) в качестве сравнительного электрода и платиновый (Pt) дисковый электрод в качестве противоэлектрода. Рентгеновские дифрактограммы (РД) регистрировали, используя рентгеновский дифрактометр D8 Advance от компании Bruker Co. (Германия). Инфракрасные спектры с преобразованием Фурье (ИКС-ПФ), зарегистрированные на спектрометре от компании Perkin Elmer Co. (США), использовали для характеристики составов модифицированных материалов. Морфологическое исследование модифицированных электродов и определение Au в составе Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ осуществляли методом сканирующей электронной микроскопии в сочетании с энергодисперсионной рентгеновской спектроскопии (СЭМ-ЭДРС) на приборе SU8010 от компании Hitachi. Просвечивающая электронная микроскопия (ПЭМ) была выполнена на приборе JEM-2100F от компании JEOL (Япония).
2.3. Получение модифицированных материалов для электродов
Оксид графена (ОГ) синтезировали классическим методом Хаммерса из порошка природного графита [27]. Восстановленный оксид графена (вОГ) получали, используя модифицированный метод термического восстановления [28]. Вкратце, фарфоровую лодочку с порошком ОГ помещали в трубку из полевого шпата и образец нагревали в потоке N2 (15 мл/мин) от 20 до 300°C с запрограммированным линейным изменением температуры со скоростью 5°C/мин, и температуру выдерживали в течение 30 мин. Диспергированный в поливинилпирролидоне восстановленный оксид графена (ПВП-вОГ) получали, смешивая в определенном массовом соотношении поливинилпирролидон (ПВП) и раствор восстановленного оксида графена (вОГ) и обрабатывая смесь ультразвуком при 30°C в течение 2 ч. После добавления определенного количества хитозана в раствор ПВП-вОГ и ультразвуковой обработки в течение 2 ч при 25°C получали устойчивый композиционный материал, содержащий хитозан и диспергированный в поливинилпирролидоне восстановленный оксид графена (ХТЗ-ПВП-вОГ).
Раствор Au-НЧ получали, восстанавливая HAuCl4 цитратом натрия согласно методу, описанному в литературе [29]. Как правило, 100 мл бидистиллированной деионизированной воды и 4 мл раствора 50 мМ HAuCl4 добавляли в круглодонную колбу объемом 250 мл. После встряхивания в течение 2 мин при 25°C в смешанный раствор добавляли 4 мл раствора 200 М цитрата натрия. Раствор затем перемешивали в течение получаса до тех пор, пока он не приобрел темно-красный цвет; в конечном счете был получен раствор Au-НЧ, который хранили в холодильнике при 4°C.
MIL-101 получали согласно хорошо известному методу [13]. Для этого дисперсию 6 г Cr(NO3)3 · · 9H2O в 90 мл воды, 2.5 г H2BDC (1,3-бензолдикарбоновая кислота) и 0.75 мл раствора HF помещали в лабораторный стакан и интенсивно встряхивали в течение 30 мин. Смешанный раствор затем помещали в автоклав, имеющий объем 150 мл и внутреннее покрытие из политетрафторэтилена (ПТФЭ), и нагревали от 20 до 220°C с запрограммированным линейным изменением температуры со скоростью 1°C/мин и выдерживали температуру в течение 8 ч. После охлаждения до комнатной температуры полученное в результате зеленое твердое вещество дважды промывали в течение 3 ч ДМФ при 77°C и спиртом при 80°C, соответственно. В заключение образец высушивали в вакууме при 60°C в течение 15 ч.
2.4. Изготовление MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ
Прежде чем стеклоуглеродный электрод (СУЭ) был модифицирован, его полировали влажным оксидом алюминия с размером частиц 0.05 мкм и промывали в ультразвуковой ванне смесью спирта и бидистиллированной воды в объемном соотношении 1 : 1, а затем высушивали в естественных условиях на воздухе. После этого определенный объем раствора ХТЗ-ПВП-вОГ с помощью микрошприца равномерно наносили на поверхность СУЭ, и электрод высушивали при 25°C, получая электрод ХТЗ-ПВП-вОГ/СУЭ. ХТЗ-ПВП-вОГ/СУЭ, затем вымачивали в растворе наночастиц золота в течение соответствующего времени и высушивали на воздухе, получая Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ. Наконец, соответствующее количество раствора MIL-101 (0.01 г MIL-101 растворяли в 2 мл ДМФ) наносили каплями на поверхность Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ с помощью микрошприца, и электрод высушивали естественным образом, получая модифицированный электрод MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ.
2.5. Приготовление образцов
В 5 мл раствора молока добавляли 15 мл раствора хлоруксусной кислоты (ρ = 10 г/л) и 1 мл раствора ацетата свинца (ρ = 10 г/л). После ультразвуковой обработки в течение 30 мин смесь центрифугировали в течение 5 мин при скорости 10 000 об/мин. Прозрачный надосадочный раствор собирали и использовали для экспериментального анализа.
3. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
3.1. Описание структуры и состава модифицированных материалов для электродов
Рисунок 1а представляет рентгеновские дифрактограммы ОГ, вОГ, ПВП-вОГ (массовое соотношение ПВП и вОГ составляет 2.0 : 1.0) и ХТЗ-ПВП-вОГ (массовое соотношение ХТЗ и ПВП-вОГ составляет 2.0 : 1.0). В случае ОГ наблюдался сильный дифракционный пик приблизительно при 12°, который был отнесен к отражению ОГ (001) [30], в то время как никакие сильные пики не были обнаружены в случае вОГ, ПВП-вОГ или ХТЗ-ПВП-вОГ, доказывая, что вОГ, ПВП-вОГ или ХТЗ-ПВП-вОГ находился в аморфном состоянии. Рисунок 1б представляет собой спектры в среднем диапазоне ИК-ПФ для ПВП, ХТЗ, ОГ, вОГ, ПВП-вОГ (массовое соотношение ПВП и вОГ составляет 2.0 : 1.0) и ХТЗ-ПВП-вОГ (массовое соотношение ХТЗ и ПВП-вОГ составляет 2.0 : 1.0). В случае ПВП наблюдались характеристические пики при 1659, 1424 и 1292 см–1, отнесенные к валентным колебаниям C=O, C–N и содержащихся в кольцах C–C [31]. В случае ХТЗ характеристические пики поглощения наблюдались при 1658 см–1 (амид I), 1597 см–1 (–NH2), 1381 см–1 (амид III), 1158 см–1 (C–O–C) и 1076 см–1 (–C–O) [32]. В случае образца ОГ пик при 1729 или 1619 см–1 был отнесен к валентным колебаниям карбонильных фрагментов C=O групп –COOH или к скелетным колебаниям неокисленных графитовых доменов, в то время как полосы при 1381 и 1095 см–1 соответствовали деформационным колебаниям C–O–H и валентным колебаниям алкоксильных групп, соответственно [33, 34]. После того, как ОГ был подвергнут термической обработке в N2 при 300°C в течение 0.5 ч, пик поглощения в инфракрасном спектре при 1729 см–1 слегка сдвинулся в сторону меньших частот, а интенсивность пика при 1381 см–1 значительно уменьшилась. Кроме того, появились два сильных пика при 1568 (ν(C=C)) и 1208 (δip(C=C)) см–1 [28], свидетельствуя, что ОГ в основном восстановился до вОГ. Пики поглощения в спектре ИК-ПФ в случае ПВП-вОГ или ХТЗ-ПВП-вОГ могут быть обусловлены вкладом вОГ, ПВП или ХТЗ. На рис. 1в представлено полученное методом ПЭМ изображение Au-НЧ, у которых диаметр составляет приблизительно 13 нм. На рис. 1г представлен спектр ЭДР Au-НЧ/ПВП-вОГ/СУЭ в случае мелких частиц, и результаты подтвердили присутствие Au-НЧ на поверхности модифицированного электрода. На рис. 1д представлена рентгеновская дифрактограмма кубической структуры MIL-101. Характеристические дифракционные пики кристалла приблизительно при 2.86°, 3.34°, 5.21°, 8.47° и 9.10°, отнесенные к дифракционным отражениям (022), (113), (115), (228) и (357), находятся в хорошем соответствии с данными литературы [35]. На рис. 1е представлен спектр ИК-ПФ в среднем диапазоне для MIL-101. Острый пик при 1628 или 1403 см–1 обусловлен колебаниями карбоксильной группы или симметричными колебаниями (O−C−O) дикарбоксилата в каркасе. Относительно слабые полосы при 1019 и 748 см–1 могут быть отнесены к колебаниям δ(C−H) и γ(C−H) ароматических колец соответственно. Пик при 1511 см–1 соответствует колебаниям группы C−C, связанной с ароматическим кольцом. Пик при 589 см–1 соответствует колебаниям Cr−O, что полностью подтверждает образование металлоорганического каркаса [36]. Из рис. 1а–1е можно определить, что успешно получены все модифицированные материалы электродов.
Рис. 1.
(а) Рентгеновские дифрактограммы ОГ, вОГ, ПВП-вОГ и ХТЗ-ПВП-вОГ. (б) Спектры ИК-ПФ в среднем диапазоне ПВП, ХТЗ, ОГ, вОГ, ПВП-вОГ и ХТЗ-ПВП-вОГ. (в) Полученное методом ПЭМ изображение Au-НЧ. (г) Спектр ЭДР Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ с помещенными на него мелкими частицами. (д) Рентгеновская дифрактограмма MIL-101. (е) Спектр ИК-ПФ в среднем диапазоне MIL-101.

На рис. 2а–г представлены полученные методом СЭМ изображения СУЭ и модифицированных электродов ХТЗ-ПВП-вОГ/СУЭ, Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ и MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ. На рис. 2б легко видеть, что ХТЗ-ПВП-вОГ, находящийся в гофрированном и скрученном состоянии, напоминая смятые шелковые вуали, диспергирован на поверхности стеклоуглеродного электрода. На рис. 2в можно наблюдать, что многочисленные мелкие Au-НЧ равномерно распределены на поверхности ХТЗ-ПВП-вОГ/СУЭ. На рис. 2г можно видеть, что кристаллическая морфология MIL-101 представляет собой правильные октаэдрические структуры с гладкой поверхностью и одинаковым размерам, что вполне согласуется с данными литературы [18]. Данные, представленные на рис. 2а–2г, позволяют сделать вывод, что датчик MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ успешно получен.
3.2. Оптимизация условий модификации электродов
Чтобы получить оптимальное соотношение для композиционного материала хитозана с диспергированным в поливинилпирролидоне восстановленным оксидом графена (ХТЗ-ПВП-вОГ), сначала было исследовано массовое соотношение ПВП и вОГ, и на рис. 3а представлены ЦВ ПВП-вОГ/СУЭ, модифицированного с различными массовыми соотношениями ПВП и ВОГ (в растворе 5.00 мМ K3Fe(CN)6). Когда массовое соотношение ПВП и вОГ увеличивается, проводимость датчика сначала увеличивается, а затем уменьшается. Когда массовое соотношение ПВП и вОГ составляет 2.0 : 1.0, достигается максимальная проводимость ПВП-вОГ/СУЭ. Когда массовое соотношение ПВП и вОГ продолжает увеличиваться, проводимость уменьшается. Это объясняется тем, что соответствующее количество ПВП может существенно способствовать диспергированию вОГ, и в результате этого проводимость датчика заметно улучшается. Однако проводимость датчика уменьшается, когда количество ПВП является избыточным, поскольку ПВП имеет низкую проводимость.
Рис. 3.
(а) ЦВ ПВП-вОГ/СУЭ, модифицированного при различных массовых соотношениях ПВП и вОГ. (б) ЦВ ХТЗ-ПВП-вОГ/СУЭ, модифицированного при различных массовых соотношениях ХТЗ и ПВП-вОГ. (в) СЭИ Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ при различных сроках выдерживания ПВП-вОГ/СУЭ в растворе Au-НЧ. (г) СЭИ MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ с различными объемами нанесенного раствора MIL-101 на Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ при pH 7.0 и скорости развертки потенциала 100 мВ/с.

На рис. 3б представлены ЦВ ХТЗ-ПВП-вОГ/СУЭ, модифицированного с различными массовыми соотношениями ХТЗ и ПВП-вОГ (в растворе 5.00 мМ K3Fe(CN)6 при массовом соотношении ПВП и вОГ, составляющим 2.0 : 1.0). Можно видеть, что сила тока в случае ХТЗ-ПВП-вОГ/СУЭ достигает максимума, когда массовое соотношение ХТЗ и ПВП-вОГ составляет 2.0 : 1.0, при этом сила тока достигает меньшего значения, когда массовое соотношение ХТЗ и ПВП-вОГ составляет больше или меньше, чем 2.0 : 1.0. Причина может заключаться в том, что из соответствующего количества хитозана в сочетании с ПВП-вОГ может образовываться мембрана, имеющая хорошую электрохимическую устойчивость [26], и, таким образом, проводимость модифицированного электрода может дополнительно улучшаться. Однако если количество хитозана является избыточным, проводимость модифицированного электрода уменьшается, поскольку сам по себе хитозан не является хорошим проводником.
Модифицированный электрод ХТЗ-ПВП-вОГ/СУЭ замачивали в растворе наночастиц золота (Au-НЧ) в течение некоторого времени, а затем помещали в раствор K3Fe(CN)6 (5.0 мМ) для сканирования методом СЭИ, причем полученные методом СЭИ результаты для различного времени выдерживания представлены на рис. 3в. Можно видеть, что наилучшее время выдерживания для модифицированного электрода ХТЗ-ПВП-вОГ/СУЭ в растворе наночастиц золота составляет 50 мин. Чрезмерно продолжительное или чрезмерно короткое время выдерживания представляет собой недостаток и препятствует получению хорошего электрода Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ. Это объясняется тем, что чрезмерно короткое время выдерживания приводит к уменьшению числа наночастиц золота, которые адсорбируются на электроде ХТЗ-ПВП-вОГ/СУЭ, что создает относительно низкую проводимость модифицированного электрода. Однако если время выдерживания является чрезмерно продолжительным (составляет более чем 50 мин), наночастицы золота на поверхности электрода агрегируются друг с другом, поскольку агрегация мелких частиц в крупные частицы представляет собой самопроизвольный термодинамический процесс, и в результате этого импеданс датчика увеличивается, и ухудшается перенос электронов.
В оптимальных условиях модификации, в которых массовое соотношение ХТЗ и ПВП-вОГ составляет 2.0 : 1.0 и время выдерживания ХТЗ-ПВП-вОГ/СУЭ в растворе Au-НЧ составляет 60 мин, на поверхность Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ помещали различные объемы раствора MIL-101, а затем помещали электрод в раствор K3Fe(CN)6 (5.0 мМ) для сканирования методом СЭИ. На рис. 3г видно, что сопротивление модифицированного электрода снижается до минимума, составляющего 16.93 Ом, когда количество наносимого объема раствор MIL-101 составляет 8 мкл, показывая, что MIL-101 представляет собой перспективный материал для модификации электрода. Это обусловлено высокой доступной поверхностной пористостью, причем центры координационной ненасыщенности на MIL-101 являются проводящими и обеспечивают быструю адсорбцию электролита на поверхности электрода [13, 18], и, таким образом, проводимость модифицированного электрода значительно увеличивается. Однако если количество MIL-101 является избыточным, сопротивление модифицированного электрода увеличивается, и не проявляется превосходная проводимость вОГ и Au-НЧ.
3.3. Сравнение различных модифицированных электродов
На рис. 4 представлены полученные методом СЭИ результаты для СУЭ, модифицированного последовательно ХТЗ-ПВП-вОГ/СУЭ, Au-НЧ и MIL-101 в растворе 5.00 М K3Fe(CN)6. Проводимость значительно увеличивается, СУЭ модифицирован ХТЗ-ПВП-вОГ, причем электрохимическая эффективность модифицированного электрода дополнительно улучшается, когда ХТЗ-ПВП-вОГ/СУЭ модифицирован Au-НЧ. Проводимость модифицированного электрода оказывается наилучшей, когда Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ последовательно модифицирован MIL-101, и в таком случае сопротивление модифицированного электрода составляет лишь 16.93 Ом. Кроме того, из наклонных линий, проведенных приблизительно под углом 45 град при низких частотах на рис. 4, можно видеть, что в данной системе действует элемент Варбурга. Вставка на рис. 4 представляет соответствующую эквивалентную схему. Параметры аппроксимации для различных модифицированных электродов, такие как сопротивление раствора (Rohm), сопротивление переносу заряда (Rct), емкость модифицированного электрода (C) и импеданс Варбурга, обусловленный массопереносом (W), представлены в качестве подтверждающей информации в табл. 1.
Рис. 4.
Диаграмма Найквиста СЭИ на различных модифицированных электродах в растворе 5.00 М K3Fe(CN)6 при pH 7.0 и скорости развертки потенциала 100 мВ/с.
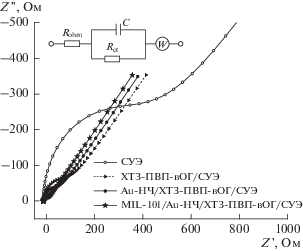
Таблица 1.
Сравнительное определение меламина на различных модифицированных электродах
| Рабочий электрод | Диапазон линейности, мкМ |
Предел определения, мкМ | Литература |
|---|---|---|---|
| Олигонуклеотиды/Au | 3.90 × 10–2 ~ 3.30 | 9.60 × 10–3 | [39] |
| Гидроксиапатит (ГАП) многостенные углеродные нанотрубки (МСУНТ)/СУЭ | 0.01 ~ 0.35 | 1.50 × 10–3 | [40] |
| 3,4-Дигидрофенилуксусная кислота (ДГФУК)/СУЭ | 0.01 ~ 5.00 | 3.00 × 10–3 | [41] |
| Изготовленный методом трафаретно печати углеродный электрод (ТПУЭ) | 5.00 ~ 200 | 0.80 | [42] |
| Поли(парааминобензойная кислота)/СУЭ | 450 ~ 4000 | 0.36 | [43] |
| Au@полианилин (ПАНИ)/СУЭ | 1.00 × 10–5 ~ 10.0 | 1.39 × 10–6 | [44] |
| Упорядоченный мезопористый углерод (УМУ)/СУЭ (комплекс Mel–Cu) | 1.0 × 10–5 ~ 5.0 × 10–4 | 2.0 × 10–6 | [45] |
| Медный электрод | 5 ~ 90 | 0.85 | [46] |
| Модифицированный электрод МСУНТ (комплекс Mel–Cu) | 1.2 × 10–3 ~ 1.9 × 10–2 | 2.5 × 10–4 | [47] |
| MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ | 5.00 × 10–5 ~ 1.00 × 10–2 | 5.00 × 10–5 | Настоящая работа |
3.4. Электрохимическое поведение и механизм окисления-восстановления меламина на MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ
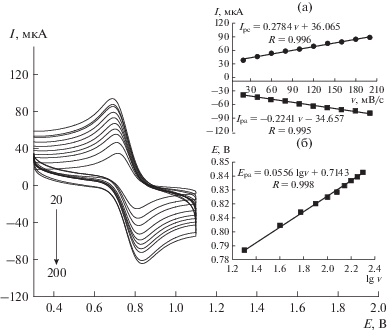
В условиях pH 7.0 и времени обогащения 100 с модифицированный электрод MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ сканировали в растворе 1.00 × 10–10 М меламина, и полученные в результате циклические вольтамперограммы для различных скоростей развертки потенциала представлены на рис. 5. Можно видеть, что пара пиков окисления-восстановления появляется в диапазоне от 0.67 до 0.84 В. На вставке рис. 5а представлено хорошее линейное соотношение между током пика и скоростью развертки потенциала, причем соответствующие уравнения представляют собой Ipc = 0.2784v + 36.065 (R = 0.996) и Ipa = = –0.2241v – 34.657 (R = 0.995), показывая, что процесс окисления–восстановления меламина на модифицированном электроде – это контролируемый адсорбцией процесс [37]. Кроме того, на вставке рис. 5б можно видеть, что потенциал пика увеличивается в зависимости от логарифма скорость развертки потенциала согласно линейному уравнению Epa = 0.0556lg v + 0.7143 (R = = 0.998). Согласно теории Лавирона [38], соотношение между Epa и lg v в контролируемом адсорбцией окислительно-восстановительном процессе соответствует следующей формуле:
Рис. 5.
Циклические вольтамперограммы MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ при различных скоростях развертки потенциала в 0.1 M ФСБР, содержащем 1.00 × 10–10 М меламина при pH 7.0 и времени обогащения 100 с. Вставка a : соотношение между током анодного пика и скоростью развертки потенциала. Вставка б : график зависимости E от lg v.
3.5. Оценка эффективности датчика MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ
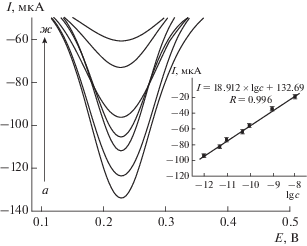
Эффективность MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ оценивали в экспериментальных условиях, включающих pH 7.0 в ФСБР (0.1 М), скорость развертки потенциала 100 мВ/с и частоту 50 Гц. На рис. 7 представлены отклики ДИВ растворов меламина (5.00 × 10–11, 1.00 × 10–10, 1.00 × 10–9, 2.00 × 10–9, 5.00 × 10–9, 8.00 × 10–9, 1.00 × 10–8 М) на MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ. Из вставки на рис. 7 можно видеть, что существует хорошее линейное соотношение между током пика и концентрацией меламина в диапазоне от 5.00 × 10–11 до 1.00 × 10–8 М. Уравнение регрессии представляет собой I = –18.912lg C + 132.69, и коэффициент корреляции (R) составляет 0.996.
Рис. 7.
Кривые ДИВ на MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ для различных концентраций меламина при pH 7.0, скорости развертки потенциала 100 мВ/с и частоте 50 Гц; a → ж: 5.00 × 10–11, 1.00 × 10–10, 1.00 × 10–9, 2.00 × 10–9, 5.00 × 10–9, 8.00 × 10–9, 1.00 × × 10–8 М. Вставка : линейное соотношение между током пика и концентрацией меламина.
В приведенных выше оптимизированных условиях образец раствора 1.00 × 10–10 М меламина исследовали пять раз на одном и том же электроде MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ, причем электрод MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ промывали в растворе ФСБР при pH 7.0 и в растворе этанола (объемное соотношение 1 : 1), а затем промывали большим количеством раствора ФСБР до тех пор, пока потенциал датчика не восстанавливался до значения отклика перед использованием. Относительное среднеквадратическое отклонение (ОСО) составляло 4.35%. Кроме того, были исследованы также пять модифицированных электродов MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ, и ОСО составляло менее чем 2.02%, показывая очень хорошую воспроизводимость MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ. Уменьшение тока пика составляло менее чем 10.56% после выдерживания электрода в течение месяца при 4°C, показывая, что электрод имеет хорошую надежность и устойчивость. По сравнению с большинством других датчиков, приведенных в табл. 1, MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ проявлял меньший предел определения с диапазоном линейности от 5.00 × 10–11 до 1.00 × 10–8 М.
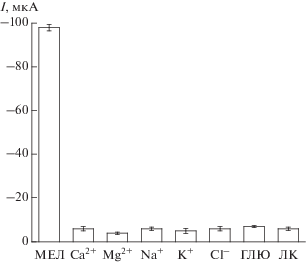
Для оценки селективности MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ было проведено исследование на влияние примесей с использованием некоторых возможных примесных веществ, таких как Ca2+, Mg2+, Na+, K+, Cl–, глюкоза (ГЛЮ) и лимонная кислота (ЛК). Перечисленные выше примеси присутствующие в одинаковой концентрации, составляющей 1.00 × 10–8 М, добавляли в раствор меламина (1.00 × 10–10 М). На рис. 8 можно видеть, что электрохимический датчик проявлял хорошую устойчивость к примесям, влияние которых было незначительным, а также улучшенную способность определения меламина.
3.6. Анализ реальных образцов
Практическая применимость датчика MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ для анализа реальных образцов молока исследована методом дифференциальной импульсной вольтамперометрии, где стандартный раствор меламина добавляли в раствор молока. Результаты, представленные в табл. 2, показывают, что MIL-101/Au-НЧ/ХТЗ-ПВП-ВОГ/СУЭ представляет собой весьма полезный инструмент для обнаружения меламина в образцах молока.
Таблица 2.
Коэффициент обнаружения меламина в молоке (n = 3)
| Добавлено, М | Найдено, М | Коэффициент обнаружения, % | ОСО, % |
|---|---|---|---|
| 1.00 × 10–9 | 0.92 × 10–9 | 92.0~104.0 | 8.9 |
| 1.01 × 10–9 | |||
| 1.04 × 10–9 | |||
| 5.00 × 10–9 | 4.88 × 10–9 | 97.6~102.4 | 2.5 |
| 4.97 × 10–9 | |||
| 5.12 × 10–9 | |||
| 8.00 × 10–9 | 7.68 × 10–9 | 96.0~101.3 | 4.3 |
| 8.05 × 10–9 | |||
| 8.11 × 10–9 |
4. ВЫВОДЫ
Для определения меламина изготовлен превосходный электрохимический датчик на основе MIL-101, Au-НЧ и ХТЗ-ПВП-вОГ, в котором MIL-101 может существенно способствовать адсорбции меламина на поверхности модифицированного электрода вследствие своей высокой доступной поверхностной пористости и центров координационной ненасыщенности, и Au-НЧ или ХТЗ-ПВП-вОГ может значительно повышать скорость переноса электронов для Au-НЧ, или диспергированный в ПВП вОГ представляет собой превосходный проводящий материал, и ХТЗ с ПВП-вОГ может образовывать мембрану, имеющую хорошую электрохимическую устойчивость. В результате этого MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ проявляет высокую эффективность определения меламина, пониженный предел определения меламина 5.00 × 10–11 М и диапазон линейности от 5.00 × 10–11 до 1.00 × 10–8 М (R = 0.996). Предложен вероятный механизм окисления–восстановления меламина на основе участия двух электронов и двух протонов в процессе окисления-восстановления меламина. Кроме того, MIL-101/Au-НЧ/ХТЗ-ПВП-вОГ/СУЭ исследован для определения меламина в молочных продуктах, и хороший результат показал, что он представляет собой перспективный датчик для обнаружения меламина в образцах молока.
Список литературы
Zhu, L., Gamez, G., Chen, H., Chingin, K., and Zenobi, R., Rapid detection of melamine in untreated milk and wheat gluten by ultrasound-assisted extractive electrospray ionization mass spectrometry (EESI-MS), Chem. Commun., 2009, vol. 0, p. 559. https://doi.org/10.1039/B818541G
Puschner, B., Poppenga, R.H., Lowenstine, L.J., Filigenzi, M.S., and Pesavento, P.A., Assessment of melamine and cyanuric acid toxicity in cats, J. Vet. Diagn. Invest., 2007, vol. 19, p. 616. https://doi.org/10.1177/104063870701900602
Dai, H.C., Shi, Y., Wang, Y.L., Sun, Y.J., Hu, J.T., Ni, P.Q., and Li, Z., A carbon dot based biosensor for melamine detection by fluorescence resonance energy transfer, Sensor. Actuat. B Chem., 2014, vol. 202, p. 201. https://doi.org/10.1016/j.snb.2014.05.058
Jia, J.Y., Shen, X.W., Wang, L.Y., Zhang, T.J., Xu, M.S., Fang, X.L., Xu, G.F., Qian, C., Wu, Y., Qian, C., Wu, Y.M., and Geng, H.Q., Extracorporeal shock wave lithotripsy is effective in treating single melamine induced urolithiasis in infants and young children, J. Urol., 2013, vol. 189, p. 1498. https://doi.org/10.1016/j.juro.2012.11.109
Guo, Z., Xu, X.F., Li, J., Liu, Y.W., Zhang, J., and Yang, C., Ordered mesoporous carbon as electrode modification material for selective and sensitive electrochemical sensing of melamine, Sensor. Actuat. B Chem., 2014, vol. 200, p. 101. https://doi.org/10.1016/j.snb.2014.04.031
Yokley, R.A., Maye, L.C., Rezaaiyan, R., Manuli, M.E., and Cheung, M.W., Analytical method for the determination of cyromazine and melamine residues in soil using LC-UV and GC-MSD, J. Agric. Food Chem., 2000, vol. 48, p. 3352. https://doi.org/10.1021/jf991231w
Yu, H., Tao, Y.F., Chen, D.M., Wang, Y.L., Liu, Z.Y., Pan, Y.H., Huang, L.L., Peng, D.P., Dai, M.H., Liu, Z.L., and Yuan, Z.H., Development of a high performance liquid chromatography method and a liquid chromatography–tandem mass spectrometry method with pressurized liquid extraction for simultaneous quantification and confirmation of cyromazine, melamine and its metabolites in foods of animal origin, Anal. Chim. Acta, 2010, vol. 682, p. 48. https://doi.org/10.1016/j.aca.2010.09.032
Zhang, S.J., Yu, Z.Q., Hu, N., Sun, Y.P., Suo, Y.R., and You, J.M., Sensitive determination of melamine leached from tableware by reversed phase high-performance liquid chromatography using 10-methyl-acridone-2-sulfonyl chloride as a pre-column fluorescent labeling reagent, Food Control, 2014, vol. 39, p. 25. https://doi.org/10.1016/j.foodcont.2013.10.037
Cao, B.Y., Yang, H., Song, J., Chang, H.F., Li, S.Q., and Deng, A.P., Sensitivity and specificity enhanced enzyme-linked immunosorbent assay by rational hapten modification and heterogeneous antibody/coating antigen combinations for the detection of melamine in milk, milk powder and feed samples, Talanta, 2013, vol. 116, pp. 173–180. https://doi.org/10.1016/j.talanta.2013.05.009
Zhang, X.F., Zou, M.Q., Qi, X.H., Liu, F., Zhu, X.H., and Zhao, B.H., Detection of melamine in liquid milk using surface-enhanced Raman scattering spectroscopy, J. Raman Spectrosc., 2010, vol. 41, p. 1655. https://doi.org/10.1002/jrs.2629
Zhou, L.M., Huang, J.S., Yang, L., Li, L.B., and You, T.Y., Enhanced electrochemiluminescence based on ${\text{Ru}}\left( {{\text{bpy}}} \right)_{{\text{3}}}^{{{\text{2}} + }}$-doped silica nanoparticles and graphene composite for analysis of melamine in milk, Anal Chim Acta, 2014, vol. 824, p. 57. https://doi.org/10.1016/j.aca.2014.03.035
Cao, Q., Zhao, H., Zeng, L.X., Wang, J., Wang, R., Qiu, X.H., and He, Y.J., Electrochemical determination of melamine using oligonucleotides modified gold electrodes, Talanta, 2009, vol. 80, p. 484. https://doi.org/10.1016/j.talanta.2009.07.006
Li, Y.Z., Chao, H.F., Du, H.J., Liu, W.B., Li, Y.W., and Ye, J.S., Electrochemical behavior of metal-organic framework MIL-101 modified carbon paste electrode: An excellent candidate for electroanalysis, J. Electroanal. Chem., 2013, vol. 709, p. 65. https://doi.org/10.1016/j.jelechem.2013.09.017
Tığ, G.A., Günendi, G., and Pekyardımcı, Ş., A selective sensor based on Au nanoparticles- graphene oxidepoly (2,6-pyridinedicarboxylic acid) composite for simultaneous electrochemical determination of ascorbic acid, dopamine, and uric acid, J. Appl. Electrochem., 2017, vol. 47, p. 607. https://doi.org/10.1007/s10800-017-1060-7
Hatami, Z. and Jalali, F., Voltammetric Determination of Immunosuppressive Agent, Azathio- prine, by Using a Graphene–Chitosan Modified Glassy Carbon Electrode, Russ. J. Electrochem., 2015, vol. 51, p. 70. [Хатами, З., Жалали, Ф. Вольтамперометрическое определение иммунодепрессивного агента азатиоприна на стеклоуглеродном электроде, модифицированном композитом графен–хитозан. Электрохимия. 2015 г. Т. 51. С. 81. doi 10.7868/S0424857015010090.]https://doi.org/10.1134/S1023193515010097
Yang, K.Z., Zhou, L.Q., Xiong, X., Ye, M.L., Li, L., and Xia, Q.H., RuCuCo nanoparticles supported on MIL-101 as a novel highly efficient catalysts for the hydrolysis of ammonia borane, Micropor. Mesopor. Mater., 2016, vol. 225, p. 1. https://doi.org/10.1016/j.micromeso.2015.12.018
Kayal, S., Sun, B., and Chakraborty, A., Study of metal-organic framework MIL-101(Cr) for natural gas (methane) storage and compare with other MOFs (metal-organic frameworks), Energy, 2015, vol. 91, p. 772. https://doi.org/10.1016/j.energy.2015.08.096
Zhang, W.Q., Zhang, Z.Y., Li, Y.C., Chen, J., Li, X.B., Zhang, Y.D., and Zhang, Y.P., Novel nanostructured MIL-101(Cr)/XC-72 modified electrode sensor: A highly sensitive and selective determination of chloramphenicol, Sensor. Actuat. B Chem., 2017, vol. 247, p. 756. https://doi.org/10.1016/j.snb.2017.03.104
Cheplakova, A.M., Solovieva, A.O., Pozmogova, T.N., Vorotnikov, Y.A., Brylev, K.A., Vorotnikova, N.A., Vorontsova, E.V., Mironov, Y.V., Poveshchenko, A.F., Kovalenko, K.A., and Shestopalov, M.A., Nanosized mesoporous metal-organic framework MIL-101 as a nanocarrier for photoactive hexamolybdenum cluster compounds, J. Inorg. Biochem., 2017, vol. 166, p. 100. https://doi.org/10.1016/j.jinorgbio.2016.11.014
He, X.Y., Gang, M.Y., Li, Z., He, G.W., Yin, Y.H., Cao, L., Zhang, B., Wu, H., and Jiang, Z.Y., Highly conductive and robust composite anion exchange membranes by incorporating quaternized MIL–101(Cr), Sci. Bull., 2017, vol. 62, p. 266. https://doi.org/10.1016/j.scib.2017.01.022
Li, G.H., Li, F.C., Yang, H., Cheng, F.Y., Xu, N., Shi, W., and Cheng, P., Graphene oxides doped MIL–101(Cr) as anode materials for enhanced electrochemistry performance of lithium ion battery, Inorg. Chem. Commun., 2016, vol. 64, p. 63. https://doi.org/10.1016/j.inoche.2015.12.017
Idrisa, A.O., Mafaa, J.P., Mabubab, N., and Arotiba, O.A., Nanogold Modified Glassy Carbon Electrode for the Electrochemical Detection of Arsenic in Water, Russ. J. Electrochemistry, 2017, vol. 53, p. 170. [Идрис, А.О., Мафа, Дж.П., Мабуба, Н., Аротиба, О.А. Модифицированный наночастицами золота стеклоуглеродный электрод для электрохимического определения мышьяка в воде. Электрохимия. 2017 г. Т. 53. С. 190. doi 10.7868/S0424857017020086.]https://doi.org/10.1134/S1023193517020082
Wang, Y., Sun, Y.M., Liao, H.B., Sun, S.N., Li, S.Z., Ager III, J.W., and Xu, Z.C.J., Activation effect of electrochemical cycling on gold nanoparticles towards the hydrogen evolution reaction in sulfuric acid, Electrochim. Acta, 2016, vol. 209, p. 440. https://doi.org/10.1016/j.electacta.2016.05.095
Liu, Q., Zhu, X., Huo, Z.H., He, X.L., Liang, Y., and Xu, M.T., Electrochemical detection of dopamine in the presence of ascorbic acid using PVP/graphene modified electrodes, Talanta, 2012, vol. 97, p. 557. https://doi.org/10.1016/j.talanta.2012.05.013
Devnani, H., Satsangee, S.P., and Jain, R., A novel graphene-chitosan-Bi2O3 nanocomposite modified sensor for sensitive and selective electrochemical determination of a monoamine neurotransmitter epinephrine, Ionics, 2016, vol. 22, p. 943. https://doi.org/10.1007/s11581-015-1620-y
Yavuz, A.G., Uygun, A., and Bhethanabotla, V.R., Substituted polyaniline/chitosan composites: synthesis and characterization carbohydrate polymers, Carbohyd. Polym., 2009, vol. 75, p. 448. https://doi.org/10.1016/j.carbpol.2008.08.005
Ma, Y.W., Liu, Z.R., Wang, B.L., Zhu, L., Yang, J.P., and Li, X.A., Preparation of graphene-supported Pt‒Co nanoparticles and their use in oxygen reduction reactions, New Carbon Mater., 2012, vol. 27, p. 250. https://doi.org/10.1016/S1872-5805(12)60016-X
Christopher, D.Z., Preparation and evaluation of graphite oxide reduced at 220°C, Chem. Mater., 2010, vol. 22, p. 5625. https://doi.org/10.1021/cm102005m
Yang, F., Wang, P.L., Wang, R.G., Zhou, Y., Su, X.O., He, Y.J., Shi, L., and Yao, D.S., Label free electrochemical aptasensor for ultrasensitive detection of ractopamine, Biosens Bioelectron., 2016, vol. 77, p. 347. https://doi.org/10.1016/j.bios.2015.09.050
Nasirpouri, F., Pourmahmoudi, H., Abbasi, F., Littlejohn, S., Chauhan, A.S., and Nogaret, A., Modification of chemically exfoliated graphene to produce efficient piezoresistive polystyrene-graphene composites, J. Electron. Mater., 2015, vol. 44, p. 3512. https://doi.org/10.1007/s11664-015-3799-0
Ebadi, A., Rafati, A.A., Bavafa, S., and Mohammadi, M., Kinetic and theoretical studies of novel biodegradable thermo-sensitive xerogels based on PEG/PVP/silica for sustained release of enrofloxacin, Appl. Surf. Sci., 2017, vol. 425, p. 282. https://doi.org/10.1016/j.apsusc.2017.07.046
Ma, F.M., Li, P., Zhang, B.Q., and Wang, Z.V., The facile synthesis of a chitosan Cu(II) complex by solution plasma process and evaluation of their antioxidant activities, Int. J. Biol. Macromol., 2017, vol. 103, p. 501. https://doi.org/10.1016/j.ijbiomac.2017.04.082
Uddin, Md.E., Layek, R.K., Kim, N.H., Hui, D., and Lee, J.H., Preparation and properties of reduced graphene oxide/polyacrylonitrile nanocomposites using polyvinyl phenol, Compos. Part. B, 2015, vol. 80, p. 238. https://doi.org/10.1016/j.compositesb.2015.06.009
Zhang, W.J., Li, Y.J., Zhang, X.X., and Li, C.L., Facile synthesis of highly active reduced graphene oxide-CuI catalyst through a simple combustion method for photocatalytic reduction of CO2 to methanol, J. Solid State Chem., 2017, vol. 253, p. 47. https://doi.org/10.1016/j.jssc.2017.05.022
Yang, J.F., Zhao, Q., Li, J.P., and Dong, J.X., Synthesis of metal–organic framework MIL-101 in TMAOH-Cr(NO3)3-H2BDC-H2O and its hydrogen-storage behavior, Micropor. Mesopor. Mater., 2010, vol. 130, p. 174. https://doi.org/10.1016/j.micromeso.2009.11.001
Fazaeli, R., Aliyan, H., Moghadam, M., and Masoudinia, M., Nano-rod catalysts: building MOF bottles (MIL-101 family as heterogeneous single-site catalysts) around vanadium oxide ships, J. Mol. Catal. A Chem., 2013, vol. 374–375, p. 46. https://doi.org/10.1016/j.molcata.2013.03.020
Dong, S.Y., Zhang, P.H., Liu, H., Li, N., and Huang, T.L., Direct electrochemistry and electrocatalysis of hemoglobin in composite film based on ionic liquid and NiO microspheres with different morphologies, Biosens. Bioelectron., 2011, vol. 26, p. 4082. https://doi.org/10.1016/j.bios.2011.03.039
Laviron, E., Adsorption, autoinhibition and autocatalysis in polarography and in linear potential sweep voltammetry, J. Electroana. Chem., 1974, vol. 52, p. 355. https://doi.org/10.1016/S0022-0728(74)80448-1
Xu, Q., Wei, H.P., Du, S., Li, H.B., Ji, Z.P., and Hu, X.Y., Detection of subnanomolar melamine based on electrochemical accumulation coupled with enzyme colorimetric assay, J. Agr. Food Chem., 2013, vol. 61, p. 1810. https://doi.org/10.1021/jf304034e
Li, J.H., Kuang, D.Z., Feng, Y.L., Zhang, F.X., Xu, Z.F., and Liu, M.Q., A novel electrochemical method for sensitive detection of melamine in infant formula and milk using ascorbic acid as recognition element, B Kor. Chem. Soc., 2012, vol. 33, p. 2499. https://doi.org/10.5012/bkcs.2012.33.8.2499
Cao, Q., Zhao, H., He, Y.J., Ding, N., and Wang, J., Electrochemical sensing of melamine with 3,4-dihydroxyphenylacetic acid as recognition element, Anal. Chim. Acta, 2010, vol. 675, p. 24. https://doi.org/10.1016/j.aca.2010.07.002
Liao, C.W., Chen, Y.R, Chang, J.L., and Zen, J.M., Single-run electrochemical determination of melamine in dairy products and pet foods, J. Agr. Food Chem., 2011, vol. 59, p. 9782. https://doi.org/10.1021/jf201989f
Liu, Y.T., Deng, J., Xiao, X.L., Ding, L., Yuan, Y.L., Li, H., Li, X.T., Yan, X.N., and Wang, L.L., Electrochemical sensor based on a poly (para -aminobenzoic acid) film modified glassy carbon electrode for the determination of melamine in milk, Electrochim. Acta, 2011, vol. 56, p. 4595. https://doi.org/10.1016/j.electacta.2011.02.088
Rao, H.B., Chen, M., Ge, H.W., Lu, Z.W., Liu, X., Zou, P., Wang, X.X., He, H., Zeng, X.Y., and Wang, Y.Y., A novel electrochemical sensor based on Au@PANI composites film modified glassy carbon electrode binding molecular imprinting technique for the determination of melamine, Biosens. Bioelectron., 2017, vol. 87, p. 1029. https://doi.org/10.1016/j.bios.2016.09.074
Guo, Z., Zhao, Y.T., Li, Y.H., Bao, T., Sun, T.S., Li, D.D., Luo, X.K., and Fan, H.T., A Electrochemical Sensor for Melamine Detection Based on Copper-Melamine Complex Using OMC Modified Glassy Carbon Electrode, Food Anal. Methods, 2018, vol. 11, p. 546. https://doi.org/10.1007/s12161-017-1025-9
Araujo, William R., and Paixão, Thiago R.L.C., Use of copper electrode for melamine quantification in milk, Electrochim. Acta, 2014, vol. 117, p. 379. https://doi.org/10.1016/j.electacta.2013.11.160
Zhu, H., Zhang, S.H., Li, M.X., Shao, Y.H., and Zhu, Z.W., Electrochemical sensor for melamine based on its copper complex, Chem. Commun., 2010, vol. 46, p. 2259. https://doi.org/10.1039/B924355K
Дополнительные материалы отсутствуют.