Электрохимия, 2019, T. 55, № 9, стр. 1133-1146
Разработка электрохимического сенсора ZIF-8/AuNPs/PVP–rGO/GCE и высокочувствительное определение сальбутамола с его помощью
Ш. Сун a, Р. Жао a, В. Хао a, Х. Гуо a, Л. Ши a, *, С. Су b, **
a Ляонинский педагогический Университет
116029 Далян, КНР
b Институт стандартов качества и технологии тестирования агропродуктов
Китайской Академии сельскохозяйственных наук
100081 Пекин, КНР
* E-mail: shilei515dl@126.com
** E-mail: suxiaoou@caas.cn
Поступила в редакцию 12.04.2018
После доработки 30.06.2018
Принята к публикации 25.07.2018
Аннотация
Собран прекрасный электрохимический сенсор для высокочувствительного определения сальбутамола на основе стеклоуглеродного электрода, модифицированного восстановленным оксидом графена, распределенным в поливинилпирролидоне, наночастицами золота и металл-органическим структурированным материалом ZIF-8. Модификаторы и электроды охарактеризованы методами рентгеновской дифракции, ИК-спектроскопии с преобразованием Фурье, просвечивающей электронной микроскопии, сканирующей электронной микроскопии, энергодисперсионного рентгено-спектрального микроанализа, спектроскопии электрохимического импеданса, циклической вольтамперометрии и дифференциальной импульсной вольтамперометрии. Показано, что этот сенсор обладает превосходными характеристиками: высокими чувствительностью и избирательностью, а также удовлетворительной стабильностью и воспроизводимостью при определении сальбутамола, благодаря тому, что самоорганизованный сенсор содержит множество пор, что способствует адсорбции сальбутамола на поверхности электрода и образует благоприятную среду для переноса электрона, что во много раз ускоряет электрохимическую окислительно-восстановительную реакцию сальбутамола. При определении сальбутамола в оптимальных условиях наименьшая определяемая концентрация очень низка: 1.00 × 10–12 моль/л, область линейности от 1.00 × 10–12 до 5.00 × 10–9 моль/л, коэффициент корреляции 0.9985. Предложен возможный механизм окислительно-восстановительной реакции сальбутамола на электроде сенсора, в которой переносятся один электрон и один протон. Описанный электрохимический сенсор использован для определения сальбутамола в реальных образцах свинины с вполне удовлетворительным результатом.
1. ВВЕДЕНИЕ
Сальбутамол, один из агонистов β2-адренергических рецепторов, обычно используется для лечения болезней, приводящих к одышке, таких как хроническое обструктивное заболевание легких, бронхиальная астма, аллергия и др. [1]. Его также часто неправильно используют в качестве вещества, усиливающего рост домашнего скота. Поскольку сальбутамол может легко входить в организм человека через пищевую цепь и накапливаться в его органах, это может наносить существенный ущерб здоровью [2]. Например, прием внутрь значительной дозы сальбутамола может вызвать морскую болезнь, мигрень, дрожание рук, боль во всем организме и другие симптомы отравления. Более того, долговременное контактирование с сальбутамолом может вызвать даже хромосомную аберрацию, рак и другие нарушения [3]. Поэтому очень важно разработать эффективные методы для определения сальбутамола.
До настоящего времени сообщалось о многих методах определения сальбутамола, таких как жидкостная хроматография высокого разрешения, газовая хроматография/масспектрометрия, капиллярый электрофорез, иммуносорбентный анализ с применением антител, меченных ферментом, применение мембран с молекулярными отпечатками и др. [4]. Хотя вышеперечисленные методы вошли в практику, но они отличаются некоторыми недостатками: они дороги, требуют больших затрат времени, а также подготовки образцов с помощью усовершенствованных устройств [5]. Таким образом, совершенно необходимо разработать простой, дешевый и быстрый способ для анализа сальбутамола.
Недавно большой интерес привлек электрохимический метод, благодаря таким его характеристикам, как дешевизна, высокая чувствительность, хорошая стабильность и простота операций [6]. До настоящего времени этот метод успешно применялся для определения сальбутамола [7]. Большие усилия по исследованию модифицирования электродов были приложены с целью усовершенствовать чувствительность и избирательность этого метода [8]; было разработано много хороших модифицирующих материалов, позволяющих усилить электрический сигнал электродов или ускорить процесс адсорбции определяемого вещества на поверхности электрода [9].
Графен – прекрасный проводящий углеродный материал с чрезвычайно большой площадью поверхности и хорошей электронной проводимостью [10]. Поскольку графен демонстрирует хорошую чувствительность по сравнению с другими углеродными материалами, он является очень многообещающим кандидатом в модификаторы электродов [11]. Однако, из-за плохой диспергируемости графена в водных растворах его применение в электрохимии носит ограниченный характер. Поливинилпирролидон (PVP) – гидрофильный полимер, обладающий способностью образовывать устойчивые комплексы с множеством других соединений. В присутствии поливинилпирролидона частицы графена нелегко собрать воедино, он может быть диспергирован в воде устойчиво и равномерно; как результат, это сильно расширило электрохимическое применение графена [12].
Наночастицы золота (AuNPs) – это тоже материал с прекрасной электропроводностью. В самое последнее время он вызывает все растущий интерес в связи с исследованиями модифицирования электрохимических сенсоров наночастицами золота, потому что они обладают выдающимися свойствами: легкость приготовления, хорошая сочетаемость с другими объектами, высокая проводимость и др. [13]. В настоящее время наночастицы золота успешно применяются при конструировании электрохимических сенсоров для определения различных веществ [14].
В последние годы привлекают внимание и очень быстро развиваются исследования структур с металл-органическим каркасом – развивающийся класс гибридных пористых материалов [15]. Цеолитные имидазольные структурированные материалы (ZIFs), подсемейство металл-органических структур, обладают прекрасными характеристиками, а именно, большой площадью поверхности, большим объемом пор, прекрасными химической стабильностью и термоустойчивостью и др. [16]. Они успешно применяются в таких областях, как хранение газа, разделение, катализ, нанотехнологические устройства, электрохимические сенсоры и др. [17]. По сравнению с другими цеолитными структурированными материалами, у ZIF-8 более гибкая структура, что бывает полезно в области электрохимического модифицирования поверхности [18–20]. Например, Ag/ZIF-8/угольно-пастовый электрод – это хороший электрохимический сенсор на H2O2 с низкой наименьшей определяемой концентрацией и высокой чувствительностью [19]. А SnO2-квантовые точки@ZIF-8 в качестве электродного материала для суперконденсаторов в электролите KOH показывает хорошее электрохимическое поведение [20].
В настоящей работе мы впервые описываем изготовление прекрасного электрохимического сенсора на сальбутамол на основе стеклоуглеродного электрода (GCE), модифицированного последовательно поливинилпирролидоном с восстановленным оксидом графена (PVP–rGO), наночастицами золота и ZIF-8. В этой комбинации ZIF-8 может обеспечить большое количество пор с тем, чтобы усилить адсорбцию сальбутамола на таком модифицированном электроде, а восстановленный оксид графена, диспергированный в поливинилпирролидоне, может сильно увеличить электроактивность этого сенсора. Модифицирующие материалы охарактеризованы методами рентгеновской дифракции, ИК-спектроскопии с преобразованием Фурье и просвечивающей электронной микроскопии. Модифицированные электроды охарактеризованы методами сканирующей электронной микроскопии, энергодисперсионного рентгено-спектрального микроанализа, спектроскопии электрохимического импеданса, циклической вольтамперометрии и дифференциальной импульсной вольтамперометрии. Кроме того, предложен механизм окисления сальбутамола на ZIF-8/AuNPs/PVP–rGO/GCE, и исследовано поведение сенсора при анализе реальных образцов.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
2.1. Реактивы и материалы
Сальбутамол, кленбутерол и наночастицы золота были приобретены у компании Sigma–Aldrich (США). Мочевая кислота, аскорбиновая кислота, L-цистеин, L-аргинин, FeCl3 · 6H2O, Ca(NO3)2 · 4H2O, Zn(NO3)2 · 6H2O, хлористый калий и гидрохлорид аммония были приобретены у компании Tianjin Kermel Chemical Reagent Co., Ltd.; гидразингидрат, диметилимидазол, диметилформамид и поливинилпирролидон – у компании Sinopharm Chemical Reagent Co., Ltd. Все остальные использованные реактивы (Merck) имели квалификацию “ч. д. а.”; все растворы готовили на дважды перегнанной деионизованной воде.
2.2. Приборы
Синтезированные структуры и композиции оксида графена (GO), восстановленного оксида графена (rGO) и PVP–rGO были охарактеризованы с помощью рентгеновской дифракции (Bruker Co., Германия) и ИК-спектроскопии с преобразованием Фурье (Perkin Elmer Co., США). Изображения наночастиц золота были получены методом просвечивающей электронной микроскопии (ТЕМ) на микроскопе JEOL JEM-2100F (Япония). Морфологию поверхности модифицированных электродов и анализ на Au структур AuNPs/PVP–rGO/GCE исследовали сочетанием методов сканирующей электронной микроскопии и энергодисперсионного рентгено-спектрального микроанализа (SEM-EDX, SU8010, Hitachi). Электрохимические измерения проводили на комплексе CHI760E (Chenhua Instruments Co., Шанхай, КНР) в трехэлектродной системе, в которой стеклоуглеродный электрод (GCE, 3 мм в диаметре, с чистой поверхностью или модифицированный) служил рабочим электродом, насыщенный каломельный электрод (SCE) – электродом сравнения, а дисковыйd Pt-электрод – вспомогательным электродом.
2.3. Приготовление материалов для модифицирования электродов
Оксид графена готовили из порошка природного графита по модифицированному методу Хаммерса [21]. Восстановленный оксид графена (rGO), диспергированный в поливинилпирролидоне (PVP–rGO), был синтезирован по методике, подобной описанной ранее [22], но с некоторыми усовершенствованиями. 0.0666 г GO вначале растворяли в 40 мл дистиллированной воды и выдерживали 12 ч в ультразвуковой ванне до получения устойчивой водной дисперсии GO. Затем к этой дисперсии добавляли 0.15 мл раствора гидразингидрата (массовое отношение 1 : 1) и 0.15 мл водного раствора аммиака (массовое отношение 1 : 4), и смесь энергично встряхивали в течение нескольких минут. Затем этот раствор перемешивали при 95°C в течение 1 ч и центрифугировали для получения rGO. Наконец, к 10 мл раствора rGO (1.66 мг/мл) добавляли нужное количество поливинилпирролидона. Через 2 ч ультразвуковой обработки при 30°C получали устойчивую дисперсию PVP–rGO черного цвета. ZIF-8 готовили по хорошо опробованной методике, описанной в работе [23].
2.4. Изготовление электродной структуры ZIF-8/AuNPs/PVP–rGO/GCE
Прежде, чем модифицировать стеклоуглеродный электрод, его полировали влажным оксидом алюминия (зерно 0.05 мкм) и тщательно промывали дважды перегнанной водой. После этого электрод ополаскивали последовательно спиртом и дважды перегнанной водой в ультразвуковой ванне и сушили на воздухе. Затем на поверхность стеклоуглеродного электрода с помощью микрошприца аккуратно наносили раствор PVP–rGO, после чего электрод сушили при 20°C. Таким способом был приготовлен модифицированный электрод PVP–rGO. Затем электрод PVP–rGO/GCE в течение некоторого времени вымачивали в растворе AuNPs (1.00 ммоль/л) и сушили на воздухе для того, чтобы получить AuNPs/PVP–rGO/GCE. После этого нужное количество раствора ZIF-8 (0.02 г ZIF-8, растворенного в 2 мл диметилформамида) капали с помощью микрошприца на поверхность AuNPs/PVP–rGO/GCE-электрода, и сушили электрод на воздухе. В конце концов, получали модифицированный стеклоуглеродный электрод ZIF-8/AuNPs/PVP–rGO/GCE. Процедуру приготовления ZIF-8/AuNPs/PVP–rGO/GCE иллюстрирует рис. 1.
2.5. Подготовка образцов свинины для анализа
Образцы свинины брали от здоровых свиней из деревенской свинарни. 1.0 г свежего свиного фарша помещали в трубку центрифуги объемом 30 мл и прибавляли 5 мл раствора ацетонитрила для того, чтобы удалить белок из свинины. Затем образец центрифугировали в течение 25 мин при 4000 об/мин, и этот процесс повторяли трижды. Прозрачный раствор над осадком собирали и выпаривали, продувая струей азота для того, чтобы удалить кислород. Полученные таким образом образцы анализировали.
3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
3.1. Получение характеристик модифицированных материалов и электродов
На рис. 2 приведены фотографии свежего раствора и растворов после выдержки с rGO (a, б) и PVP–rGO (в, г). Видно, что свежие rGO и PVP–rGO равномерно диспергированы в воде, однако, после месячной выдержки rGO почти целиком осел на дно сосуда, в то время, как раствор PVP–rGO все еще оставался гомогенным. Последнее происходит потому, что в растворе PVP–rGO возникает положительный заряд, препятствующий агрегированию rGO, и в результате этого усиливается диспергирование rGO в воде [24].
Рис. 2.
Фотографии свежего раствора или раствора после месячной выдержки rGO (a, б) и PVP–rGO (в, г).

Рисунок 3 иллюстрирует характеристики модифицированных материалов и электродов методами рентгеновской дифракции, ИК-спектроскопии с преобразованием Фурье и просвечивающей электронной микроскопии. Там же приведен энергодисперсионный рентгеновский спектр для электрода AuNPs/PVP–rGO/GCE на том участке его поверхности, где присутствуют мелкие частицы. Как видно на рис. 3а, для GO имеется весьма интенсивный пик при 2θ = 12°, который можно объяснить отражением грани GO (001) [25]. В то же время для GO наблюдается также очень слабый пик дифракции при 26.5°, который можно приписать графиту. В случае rGO или PVP–rGO этот пик при 26.5° также существует, но он шире и ниже; в то же время пик при приблизительно 12° совершенно исчез, показывая этим, что rGO или диспергированный в PVP rGO присутствуют в аморфизированном состоянии.
Рис. 3.
(а) Рентгеновская дифрактограмма GO, rGO, PVP–rGO. (б) ИК-спектры с преобразованием Фурье GO, rGO, PVP и PVP–rGO. (в) TEM-изображение AuNPs. (г) энергодисперсионный рентгеновский спектр AuNPs/PVP–rGO/GCE в месте, где находятся мелкие частицы. (д) Рентгеновская дифрактограмма ZIF-8. (е) ИК-спектр с преобразованием Фурье ZIF-8.

На рис. 3б представлены ИК-спектры с преобразованием Фурье GO, rGO, PVP и rGO–PVP. Для всех четырех образцов наблюдается широкий интенсивный пик приблизительно при 3450 ~ 3480 см–1, который связан с валентными колебаниями гидроксильной группы O–H. Пики при 1730 и 1617 см–1 для образца GO можно приписать, соответственно, связи C=O карбоксильной части молекулы – группам COOH, или колебаниям остова не окисленных графитовых доменов, в то время, как полосы поглощения при 1386 и 1071 см–1 отвечают, соответственно, деформационным колебаниям C–O–H и валентным колебаниям в алкокси-группах [26, 27]. Пик поглощения в ИК-спектрах с преобразованием Фурье rGO при 1632 см–1 можно приписать ароматической связи C=C [27]. Наблюдаемые для образцов PVP характерные пики при 1659 и 2948 см–1 отвечают ароматической (бензольной) части молекулы и валентным колебаниям ароматической связи C–H, а пики при 1238 и 823 см–1 – фенольным группам –OH [26]. Пики поглощения в ИК-спектрах rGO–PVP с преобразованием Фурье при 1632 и 1324 см–1 – это характеристические пики rGO и PVP [26].
На рис. 3в представлено TEM-изображение наночастиц золота AuNPs, диаметр которых составляет около 13 нм. Для того, чтобы проверить, действительно ли наночастицы золота модифицируют PVP–rGO/GCE-электрод, мы снимали энергодисперсионные рентгеновские (EDX) спектры, характеризующие AuNPs/PVP–rGO/GCE-электрод, в том его месте, где присутствуют мелкие частицы (рис. 3г) или где мелкие частицы отсутствуют (рис. S1B ). Результаты доказали присутствие наночастиц AuNPs на поверхности PVP–rGO/GCE.
Рисунок 3д показывает характеристические пики кристаллической дифракции ZIF-8. Пики, находящиеся приблизительно при 7.5°, 10.5°, 12.8° и 18.1°, можно приписать отражениям от граней кристалла (110), (200), (211) и (222), что находится в хорошем согласии с литературой [28]. На рис. 3е представлен ИК-спектр с преобразованием Фурье ZIF-8. Пик при 421 см–1 вызван валентными колебаниями Zn–N, а пик при 1586 см–1 – валентными колебаниями связи C=N. Пики при 1453 или 1429 см–1 связаны с растяжением кольца, а пики при 1307, 1180 и 992 см–1 с его изгибанием под влиянием сил, действующих в его плоскости [29].
Из рис. 3а–3е можно с уверенностью заключить, что все материалы для модифицирования стеклоуглеродного электрода были успешно приготовлены.
На рис. 4а–4г представлены SEM-изображения стеклоуглеродного электрода с чистой поверхностью (GCE) и такого же электрода, модифицированного с помощью PVP–rGO, AuNPs/PVP–rGO и ZIF-8/AuNPs/PVP–rGO. Легко заметить, что частицы PVP–rGO, сморщенные и скрученные, напоминающие смятый шелк, равномерно распределены по поверхности стеклоуглеродного электрода, а частицы AuNPs равномерно распределены по поверхности PVP–rGO/GCE. Более того, ZIF-8 представляет такую же структуру и морфологию кристалла, которая была описана в литературе [30]; множество частиц ZIF-8 прикреплены к поверхности AuNPs/PVP–rGO/GCE-электрода и равномерно распределены по ней.
3.2. Оптимизация условий эксперимента
3.2.1. Условия модифицирования электрода. Условия модифицирования электродов могут оказывать серьезное влияние на их электрохимическое поведение. На рис. 5 представлены результаты исследования электродов, модифицированных при различных условиях, проведенных с помощью метода электрохимического импеданса. Известно, что спектры импеданса состоят из полуокружностей и линейных участков, причем диаметр полуокружностей дает сопротивление переноса электрона (Ret), в то время, как линейные участки относятся к процессу диффузии. На рис. 5 приведены результаты исследования импеданса модифицированных PVP–rGO/GCE-электродов с различным массовым отношением PVP и rGO. Эти изменения выполнены в растворе 5.00 ммоль/л K3Fe(CN)6. Видно, что при массовом отношении PVP и rGO равном 0.5 : 1.0 (конкретно, 0.5 PVP и 1.0 rGO) модифицированный стеклоуглеродный электрод дает большую полуокружность с Ret = = 195.2 Ом/см2. Если же массовое отношение PVP и rGO равно 2.0 : 1.0, то значение Ret уменьшается до 103.4 Ом/см2. При дальнейшем увеличении массового отношения PVP и rGO величина Ret модифицированного электрода растет. Это происходит потому, что соответствующее количество PVP может активно способствовать диспергированию rGO и, как результат, электропроводность электрода заметно возрастает. Однако, при избытке PVP проводимость электрода вновь падает, потому что сам по себе PVP не электропроводен.
Рис. 5.
Годографы импеданса модифицированных электродов, приготовленных при различных условиях модифицирования. (а) PVP–rGO/GCE с различным массовым отношением PVP к rGO. (б) AuNPs/PVP–rGO/GCE с различным временем погружения PVP–rGO/GCE в раствор AuNPs. (в) ZIF-8/AuNPs/PVP–rGO/GCE с различным нанесенным объемом раствора ZIF-8 на AuNPs/PVP–rGO/GCE.

Модифицированный PVP–rGO/GCE-электрод с массовым отношением PVP и rGO равным 2.0 : 1.0 некоторое время вымачивали в растворе AuNPs, а затем помещали в раствор K3Fe(CN)6 (5.00 ммоль/л) и сканировали для измерения электрохимического импеданса. Рисунок 5б иллюстрирует влияние различного времени вымачивания. Видно, что наилучшее время вымачивания модифицированного AuNPs/PVP–rGO/GCE-электрода составляет 60 мин. Слишком короткое или слишком долгое время вымачивания не позволяет получить хороший модифицированный электрод. Это происходит потому, что при чересчур коротком времени вымачивания на поверхности электрода оказывается мало частиц AuNPs, а при слишком долгом времени вымачивания частицы золота могут агрегироваться на поверхности электрода, что снижает проводимость модифицированного электрода.
При оптимальных условиях модифицирования (массовое отношение PVP и rGO 2.0 : 1.0, время вымачивания PVP–rGO/GCE-электрода в растворе AuNPs 60 мин) по поверхности AuNPs/PVP–rGO/GCE-электродов распределяли различные объемы раствора ZIF-8, а затем помещали эти электроды в раствор K3Fe(CN)6 (5.00 ммоль/л) для измерения электрохимического импеданса. На рис. 5в можно видеть, что с ростом нанесенного объема раствора ZIF-8 от 4 до 8 мкл ток явно возрастает; в то же время значение Ret уменьшается с 49.6 до 19.5 Ом/см2. Если объем раствора ZIF-8 превышает 8 мкл, значение Ret снова растет.
Хорошо известно, что ZIF-8 – это материал с трехмерной пористой металл-органической структурой, с большой площадью поверхности и хорошо доступными порами, и это делает данный материал прекрасным “хозяином” для адсорбции на нем слабо полярных групп реагентов, что ускоряет окислительно-восстановительные реакции этих реагентов на поверхности электрода [8]. Однако, при избытке наносимого раствора ZIF-8 (например, если его объем превышает 8 мкл, как показано на рис. 5в) проводимость модифицированного электрода уменьшается потому, что на поверхности AuNPs/PVP–rGO/GCE-электрода оказывается слишком много молекул ZIF-8, в результате чего PVP–rGO и AuNPs не могут сыграть свою роль в создании хорошей проводимости. Таким образом, объем 8 мкл раствора ZIF-8 был выбран как наилучший.
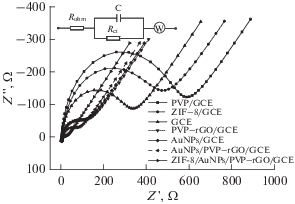
На рис. 6 показаны спектры импеданса в растворе 5.00 ммоль/л K3Fe(CN)6 различных электродов, модифицированных при одних и тех же оптимальных условиях; на врезке представлена соответствующая эквивалентная цепь. Наклонные линии при низких частотах на рис. 6, с наклоном приблизительно 45 градусов относятся к импедансу Варбурга, показывая, что этот элемент присутствует в нашей системе. В табл. S1 (приложение) приведены параметры фитинга для различных модифицированных электродов: сопротивление раствора (Rohm), сопротивление переноса заряда (Rct), емкость модифицированного электрода (C) и импеданс Варбурга, связанный с массопереносом (W). Можно выявить тенденцию в изменении Rct на различных электродах. По сравнению с величиной Rct на стеклоуглеродном электроде с чистой поверхностью (Rct = 214.9 Ом/cм2), значение Rct на PVP/GCE-электроде значительно выросло (Rct = 423.0 Ом/cм2), свидетельствуя о том, что сам по себе PVP не проводит электрический ток. На стеклоуглеродном электроде, модифицированном PVP–rGO или AuNPs, значение Rct заметно уменьшилось (соответственно, 88.7 и 80.9 Ом/cм2), показывая этим, что и rGO, диспергированный в PVP, и наночастицы золота – это материалы с хорошей проводимостью [31, 32], и поэтому скорости переноса электрона в реакции сильно увеличились. Интересный факт: значение Rct на ZIF‑8/GCE-электроде очень велико (Rct = 332.8 Ом/cм2), однако, оно уменьшается до 16.6 Ом/cм2 при модифицировании AuNPs/PVP–rGO/GCE-электрода с помощью ZIF-8. Это означает, что ZIF-8 создает такое окружение для переноса электрона на rGO, диспергированном в PVP, и на наночастицах золота, которое способно ускорять электрохимическую реакцию, хотя само по себе это соединение не способно улучшить электрохимическое поведение модифицированного электрода. Электрохимическое поведение модифицированного электрода улучшается в следующем порядке: PVP–rGO, AuNPs and ZIF-8.
Рис. 6.
Годографы импеданса различных модифицированных электродов в растворе 5.00 ммоль/л K3Fe(CN)6.
3.2.2. Условия определения. Для того, чтобы найти наилучшие условия аналитического определения, мы исследовали ряд факторов, таких как продолжительность обогащения, pH и скорость развертки потенциала. На рис. 7а показано влияние времени обогащения на дифференциальную импульсную вольтамперограмму, снятую в растворе сальбутамола (1.00 × 10–12 моль/л) на ZIF-8/AuNPs/PVP–rGO/GCE-электроде при pH 7.5 в фосфатном буферном растворе (0.1 моль/л) при следующих параметрах: скорость развертки потенциала 100 мВ/с, частота 50 Гц, амплитуда импульса 0.10 В, амплитуда напряжения 0.010 В. Видно, что в течение первых 2 мин ток в пике быстро растет. При увеличении времени обогащения сверх 2 мин не наблюдалось никакого дальнейшего изменения кривой; это указывает на то, что электрохимическая реакция достигла баланса. Поэтому мы выбрали 2 мин, как оптимальное время обогащения в настоящей работе.
Рис. 7.
(а) Ток дифференциальных импульсных вольтамперограмм сальбутамола при различном времени погружения. (б) Циклические вольтамперограммы ZIF-8/AuNPs/PVP–rGO/GCE-электрода в фосфатном буферном растворе с различными значениями pH. Врезка на рис. 7б: иллюстрация линейного соотношения между потенциалами окисления сальбутамола и pH. (в) Циклические вольтамперограммы ZIF-8/AuPs/PVP–rGO/GCE при различной скорости развертки потенциала в 0.1 M фосфатном буферном растворе (pH 7.5), содержащем 1.00 × 10–12 моль/л сальбутамола. Врезка рис. 7в: (a) связь между анодным пиковым током и скоростью развертки потенциала, (б) график зависимости E от lg v.
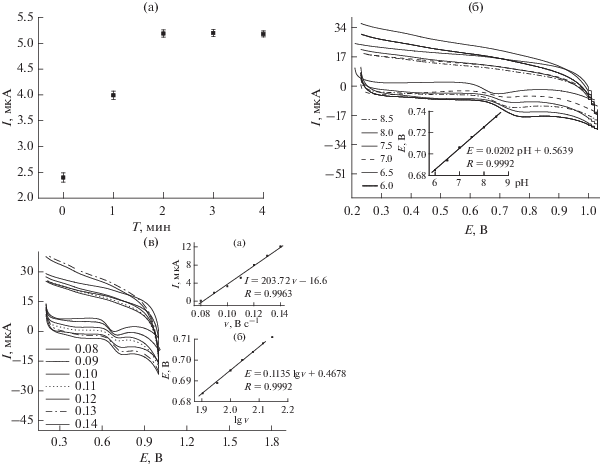
Мы исследовали влияние pH на пиковый ток сальбутамола (1.00 × 10–12 моль/л) при скорости развертки потенциала 100 мВ/с; в качестве индифферентного электролита был выбран фосфатный буферный раствор (0.1 моль/л), а значение pH меняли от 3.0 до 10.0, используя для подгонки растворы HCl или NaOH. Из рис. 7в видно, что для данной реакции лучше всего подходит pH 7.5, при этом потенциал пика тока окисления сальбутамола равен 0.68 В. Как видно на врезке к рис. 7б, между E и pH существует линейная зависимость E = 0.0202 pH + 0.5639 с коэффициентом корреляции (R) 0.9992. Это говорит о том, что в реакции окисления сальбутамола на ZIF-8/AuNPs/PVP–rGO/GCE-электроде принимают участие протоны [9].
На рис. 7в показано влияние скорости развертки потенциала на электрохимическое поведение ZIF-8/AuNPs/PVP–rGO/GCE-электрода в 1.00 × 10–12 моль/л растворе сальбутамола: показано, что пик тока окисления пропорционален скорости развертки потенциала. Как видно на врезке (a) к рис. 7в, пик тока окисления (I) растет с ростом скорости развертки потенциала (v) по линейному закону согласно уравнению: I (мкA) = = 203.72v − 16.61 (R = 0.9963). Отсюда следует вывод о том, что окисление сальбутамола на модифицированном электроде – это типичный процесс, находящийся под адсорбционным контролем [33]. Одновременно, врезка (б) к рис. 7в показывает, что потенциал пика тока окисления (E) сдвигается вперед с ростом скорости развертки потенциала по линейному закону, согласно уравнению E (В) = 0.1135 lgv + 0.4678 (R = 0.9992).
Поскольку электрохимическая реакция сальбутамола на ZIF-8/AuNPs/PVP–rGO/GCE-электроде находится под адсорбционным контролем и является полностью необратимой, соотношение между потенциалом (E) и натуральным логарифмом скорости развертки потенциала (lgv) следует уравнению Лавирона [34]:
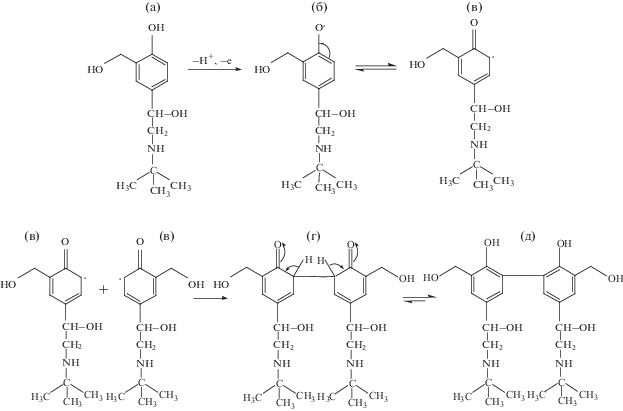
Что касается реакции окисления сальбутамола, то на основании его молекулярной структуры можно предположить, что наиболее вероятная позиция для окисления – это фенольная гидроксильная группа, а метильная группа в его молекуле должна адсорбироваться на электроде ZIF-8/AuNPs/PVP–rGO/GCE и инкапсулироваться в порах ZIF-8. Поэтому при рассмотрении электрохимического поведения сальбутамола на электроде ZIF-8/AuNPs/PVP–rGO/GCE был предложен следующий механизм окисления сальбутамола на модифицированном электроде: вначале фенольная гидроксильная группа в молекуле сальбутамола (a) теряет протон водорода и один электрон, образуя свободнорадикальное промежуточное соединение (б). Затем электрон на бензольной двойной связи в этом промежуточном продукте (б) переносится на орто связь углерода с кислородом с образованием другого свободнорадикального промежуточного соединения (в). Два промежуточных соединения (в) образуют промежуточное соединение (г) через связь C–C, и в конце концов, это промежуточное соединение (г) легко превращается в стабильный димер сальбутамола (д). Этот возможный механизм окисления сальбутамола представлен на рис. 8.
3.3. Электрохимическое поведение, воспроизводимость, стабильность и избирательность электрода ZIF-8/AuNPs/PVP–rGO/GCE
Для того, чтобы исследовать электрохимическое поведение ZIF-8/AuNPs/PVP–rGO/GCE-электрода, мы снимали дифференциальные импульсные вольтамперограммы так, чтобы измерить амперометрический отклик сальбутамола при pH 7.5 в фосфатном буферном растворе (0.1 моль/л), скорости развертки потенциала 100 мВ/с и частоте 50 Гц. На рис. 9 представлены такие дифференциальные импульсные вольтамперограммы, снятые на модифицированном электроде в растворах сальбутамола с концентрациями 1.00 × 10–12, 5.00 × 10–11, 1.00 × 10–11, 5.00 × × 10–10, 1.00 × 10–10, 1.00 × 10–9 и 5.00 × 10–9 моль/л. Пик тока окисления сальбутамола находится приблизительно при +0.68 В; с ростом концентрации сальбутамола пиковый ток уменьшается.
Рис. 9.
Дифференциальные импульсные вольтамперограммы, снятые на ZIF-8/AuNPs/PVP–rGO/GCE-электроде при различных концентрациях сальбутамола (моль/л): (a) 1.00 × 10–12; (б) 5.00 × 10–11; (в) 1.00 × 10–11; (г) 5.00 × 10–10; (д) 1.00 × 10–10; (е) 1.00 × 10–9; (ж) 5.00 × 10–9. Врезка: линейная связь между пиковым током и логарифмом концентрации сальбутамола.
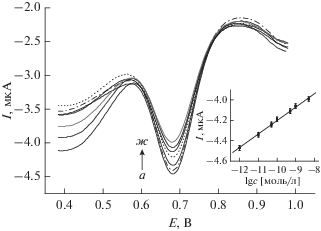
На врезке к рис. 9 также видно, что имеется хорошая линейная связь между пиковым током и логарифмом концентрации сальбутамола в интервале от 1.00 × 10–12 до 5.00 × 10–9 моль/л. Уравнение линейной регрессии таково: I = 0.1356lgс – – 2.7765 (моль/л) с коэффициентом корреляции (R) 0.9985.
Для оценки воспроизводимости нашего электрохимического сенсора были выбраны пять электродов для определения сальбутамола (1.00 × × 10–9 моль/л). Относительное стандартное отклонение измерений для пяти электродов составило 2.15%, что указывает на вполне хорошую воспроизводимость разработанного нами сенсора. Далее, проверяли срок службы и стабильность электрохимического сенсора; было показано, что после 10 использований сенсор все еще находился в хорошем состоянии, ошибка определения не превышала 8.6%. По прошествии одного месяца отклик сенсора сохранился на уровне 89.01% от его первоначального значения, что указывает на хорошие срок службы и стабильность сенсора. По сравнению с другими методами определения сальбутамола, приведенными в табл. 1, модифицированный сенсор на основе ZIF-8/AuNPs/PVP–rGO/GCE-электрода имеет более низкую наименьшую определяемую концентрацию и более широкий интервал линейности электродной функции.
Таблица 1.
Сравнение электрохимических рабочих характеристик сенсора ZIF-8/AuNPs/PVP–rGO/GCE и других модифицированных электродов при определении сальбутамола
| Рабочий электрод | Область рабочих концентраций, мкM | Наименьшая определяемая концентрация, нM | Ссылка |
|---|---|---|---|
| CNTs | 5~100 | 1000 | [35] |
| GP-PEDOT:PSS/SPCE | 100~500 | 1250 | [36] |
| Poly-ACBK/GO–Нафион/GCE | 8.36 × 10–3~1.50 × 10–1 | 6.02 | [37] |
| SMWCNT–NF/GCE | 0.10~33.3 | 100 | [38] |
| AuGN–HRP–AAb/GCE | 3.30 × 10–2~4.18 | 0.17 | [39] |
| SAL–Cu2+–MAAternary(MIP)/CPE | 1.00 × 10–3~5.50 × 10–2 | 0.60 | [40] |
| Pd@SBA-15/Ab2/ BMIM · Br/SDBS-GS | 8.40 × 10–5~6.30 × 10–2 | 0.03 | [5] |
| ZIF-8/AuNPs/PVP–rGO/GCE | 1.00 × 10–12~5.00 × 10–9 | 0.001 | Настоящая работа |
Примечания. CNTs: углеродные нанотрубки, PEDOT:PSS: поли(3,4-этилендиокситиофен) поли(стиролсульфонат), SMWCNT–NF/GCE: одно- и многостенные углеродные нанотрубки–Нафион/стеклоуглеродный электрод, AuGN–HRP–AAb/GCE: Au-гибрид графеновый нанокомпозит–пероксидаза хрена–сальбутамол–антитело/стеклоуглеродный электрод, SAL–Cu2+–MAA/CPE: сальбутамол–Cu2+–метилметакриловая кислота/угольно-пастовый электрод, Pd@SBA-15/Ab2/BMIM·Br/SDBS-GS: Pd-наночастицы в функционализированном SBA-15/антитело 2/1-бутил-3-метилимидазолий бромид/графеновые листы, функционализированные додецилбензолсульфонатом натрия.
Для того, чтобы оценить избирательность ZIF-8/AuNPs/PVP–rGO/GCE-электрода, были испробованы возможные соединения-помехи, такие, как кленбутерол (CLB), мочевая кислота (UA), аскорбиновая кислота (AA), L-цистеин (L‑cy), L-аргинин (L-ar), Fe3+ и Ca2+; измеряли их влияние на пик тока окисления дифференциальных импульсных вольтамперограмм, находящийся приблизительно при +0.68 В. При этом соединения-помехи добавляли в одной и той же концентрации 1.00 × 10–7 моль/л к раствору сальбутамола (1.00 × 10–9 моль/л). Высота пика тока сальбутамола была очень большой, в то время, как ток соединений-помех – таких как, мочевая кислота (UA), аскорбиновая кислота (AA), L‑цистеин (L-cy), L-аргинин (L-ar), Fe3+ и Ca2+ – при этом потенциале очень небольшой. Интересно отметить, что наблюдался и пиковый ток окисления кленбутерола (представитель того же семейства соединений, что и сальбутамол, другой тип агонистов β2-адренергических рецепторов), но соответствующий ему потенциал – 0.76 В, а не 0.68 В. Поэтому можно утверждать, что электрохимический сенсор ZIF-8/AuNPs/PVP–rGO/GCE представляет собой прекрасный метод для определения сальбутамола; результаты показаны на рис. 10.
3.4. Анализ реальных образцов
Для того, чтобы оценить практическую применимость сенсора ZIF-8/AuNPs/PVP–rGO/GCE к анализу реальных образцов свинины, к раствору-вытяжке из свинины добавляли стандартный раствор сальбутамола, который затем определяли методом дифференциальной импульсной вольтамперометрии. Результаты, представленные в табл. 2, показывают, что сенсор ZIF-8/AuNPs/PVP–rGO/GCE – это очень полезный инструмент для определения сальбутамола в образцах свинины.
Таблица 2.
Процент обратного извлечения сальбутамола при различных концентрациях в реальных образцах (n = 3)
| Добавлено, моль/л | Найдено, моль/л | Процент обратного извлечения, % |
|---|---|---|
| 1.00 × 10–9 | 0.94 × 10–9 | 94.0~107.0 |
| 1.03 × 10–9 | ||
| 1.07 × 10–9 | ||
| 2.91 × 10–9 | ||
| 3.00 × 10–9 | 3.01 × 10–9 | 97.0~103.0 |
| 3.10 × 10–9 | ||
| 5.00 × 10–9 | 4.81 × 10–9 | 96.3~103.6 |
| 5.06 × 10–9 | ||
| 5.15 × 10–9 |
4. ЗАКЛЮЧЕНИЕ
Сконструирован прекрасный сенсор на базе ZIF-8/AuNPs/PVP–rGO/GCE-электрода для высокочувствительного определения сальбутамола, в котором ZIF-8 предоставляет многочисленные поры, способствующие адсорбции сальбутамола на модифицированном электроде, а PVP–rGO или AuNPs обеспечивают прекрасную проводимость, что сильно повышает электроактивность этого сенсора. По сравнению с другими сенсорами, разработанный нами сенсор демонстрирует очень хорошее электрохимическое поведение: область линейности электродной функции от 1.00 × 10–12 до 5.00 × 10–9 моль/л, наименьшая определяемая концентрация 1.00 × 10–12 моль/л, а также коэффициент корреляции (R) равный 0.9985. Сенсор был испробован на примере определения сальбутамола в образцах свинины с процентом обратного извлечения от 94.0 до 107.0%. Предложен вероятный механизм реакции окисления сальбутамола. Хорошие рабочие характеристики сенсора ZIF-8/AuNPs/PVP–rGO/GCE позволяют сделать вывод о том, что он перспективен для определения сальбутамола в образцах свинины.
Список литературы
Crescenzi, C., Bayoudh, S., Cormack, P.A.G., Klein, T., and Ensing, K., Determination of clenbuterol in bovine liver by combining matrix solid-phase dispersion and molecularly imprinted solid–phase extraction followed by liquid chromatography/electrospray ion trap multiple-stage mass spectrometry, Anal. Chem., 2001, vol. 73, pp. 2171–2177. Doi: https://doi.org/10.1021/ac0014360
Martinez-Navarro, J.F., Food poisoning related to consumption of illicit β–agonist in liver, Lancet, 1990, vol. 336, pp. 1311–1311. Doi: https://doi.org/org/10.1016/0140-6736(90)92990-Y
Jin, O.Y., Duan, J.L., Baeyens, W.R.G., and Delanghe, J.R., A simple method for the study of salbutamol pharmacokinetics by ion chromatography with direct conductivity detection, Talanta, 2005, vol. 65, pp. 1–6. Doi: https://doi.org/10.1016/j.talanta.2004.01.026
Taylor, D.M., Joffe, P., Taylor, S.E., Jones, A., Cheek, J.A., Craig, S.S., Graudins, A., Dhir, R., Krieser, D., and Babl, F.E., Off-label and unlicenced medicine administration to paediatric emergency department patients, Emerg. Med. Australas., 2015, vol. 27, pp. 440–446. Doi: https://doi.org/10.1111/1742-6723.12431
Cui, Z.T., Cai, Y.Y., Wu, D., Yu, H.Q., Li, Y., Mao, K.X., Wang, H., Fan, H.X., Wei, Q., and Du, B., An ultrasensitive electrochemical immunosensor for the detection of salbutamol based on Pd@SBA-15 and ionic liquid, Electrochim. Acta, 2012, vol. 69, pp. 79–85. Doi: https://doi.org/10.1016/j.electacta.2012.02.073
Sairi, M. and Arrigan, D.W.M., Electrochemical detection of ractopamine at arrays of micro-liquid interfaces, Talanta, 2015, vol. 132, pp. 205–214. Doi: https://doi.org/10.1016/j.talanta.2014.08.060
Chen, D., Yang, M., Zheng, N.J., Xie, N., Liu, D.L., Xie, C.F., and Yao, D.S., A novel aptasensor for electrochemical detection of ractopamine, clenbuterol, salbutamol, phenylethanolamine and procaterol, Biosens. Bioelectron., 2016, vol. 80, pp. 525–531. Doi: https://doi.org/10.1016/j.bios.2016.01.025
Shi, L.B., Zhu, X., Liu, T.T., Zhao, H.L., and Lan, M.B., Encapsulating Cu nanoparticles into metal–organic frameworks fornonenzymatic glucose sensing, Sens. Actuators B Chem., 2016, vol. 227, pp. 583–590. Doi: https://doi.org/10.1016/j.snb.2015.12.092
Yao, S., Hu, Y.F., Li, G.K., and Zhang, Y.K., Adsorption behavior of ractopamine on carbon nanoparticle modified electrode and its analytical application, Electrochim. Acta, 2012, vol. 77, pp. 83–88. Doi: https://doi.org/10.1016/j.electacta.2012.05.078
Rychagov, A.Yu., Gubin, S.P., Chuprov, P.N., Kornilov, D.Yu., Karaseva, A.S., Krasnova, E.S., Voronov, V.A., and Tkachev, S.V., Electrochemical reduction and electric conductivity of graphene oxide films, Russ. J. Electrochem., 2017, vol. 53, pp. 721–727. Doi: https://doi.org/10.1134/S1023193517070102
Zhang, Y., Zhang, M.Q., Wei, Q.H., Gao, Y.J., Guo, L.J., Al-Ghanim, K.A., Mahboob, S., and Zhang, X.J., An Easily Fabricated Electrochemical Sensor Based on a Graphene-Modified Glassy Carbon Electrode for Determination of Octopamine and Tyramine, Sensors, 2016, vol. 16, pp. 535–549. Doi: https://doi.org/10.3390/s16040535
Liu, Q., Zhu, X., Huo, Z.H., He, X.L., Liang, Y., and Xu, M.T., Electrochemical detection of dopamine in the presence of ascorbic acid using PVP/graphene modified electrodes, Talanta, 2012, vol. 97, pp. 557–562. Doi: https://doi.org/10.1016/j.talanta.2012.05.013
Mashhadizadeh, M.H., and Talemi, R.P., Multilayer film of thiourea and gold nanoparticles as an effective platform for immobilization of activated non-labeled-DNA and construction of an ultrasensitive electrochemical DNA biosensor, Russ. J. Electrochem., 2016, vol. 52, pp. 154–162. Doi: https://doi.org/10.1134/S1023
Kim, S.H., Nanoporous gold: Preparation and applications to catalysis and sensors, Curr. Appl. Phys., 2018, Doi: https://doi.org/10.1016/j.cap.2018.03.021
Hosseini, H., Ahmar, H., Dehghani, A., Bagheri, A., Fakhari, A.R., and Amini, M.M., Au–SH–SiO2 nanoparticles supported on metal-organic framework (Au–SH–SiO2@Cu–MOF) as a sensor for electrocatalytic oxidation and determination of hydrazine, Electrochimi. Acta, 2013, vol. 88, pp. 301–309. Doi: https://doi.org/10.1016/j.electacta.2012.10.064
Park, K.S., Ni, Z., Côté, A.P., Choi, J.Y., Huang, R., Uribe–Romo, F.J., Chae, H.K., O’Keeffe, M., and Yaghi, O.M., Exceptional chemical and thermal stability of zeolitic imidazolate frameworks, Proc. Nati. Acad. Sci., 2006, vol. 103, pp. 10186–10191. Doi: https://doi.org/10.1073/pnas.0602439103
Stackhouse, C.A. and Ma, S.Q., Azamacrocyclic-based metal organic frameworks: Design strategies and applications, Polyhedron, 2018, vol. 145, pp. 154–165. Doi: https://doi.org/10.1016/j.poly.2018.01.036
Lu, G. and Hupp, J.T., Metal–Organic Frameworks as Sensors: A ZIF-8 Based Fabry–Pérot Device as a Selective Sensor for Chemical Vapors and Gases, J. Amer. Chem. Soc., 2010, vol. 132, pp. 7832–7833. Doi: https://doi.org/10.1021/ja101415b
Samadi-Maybodi, A., Ghasemi, S., and Ghaffari-Rad, H., Ag-doped zeolitic imidazolate framework–8 nanoparticles modified CPE for efficient electrocatalytic reduction of H2O2, Electrochim. Acta, 2015, vol. 163, pp. 280–287. Doi: https://doi.org/10.1016/j.electacta.2015.02.129
Gao, Y.L., Wu, J.X., Zhang, W., Tan, Y.Y., Zhao, J.C., and Tang, B.J., The electrochemical performance of SnO2 quantum dots@zeolitic imidazolate frameworks–8 (ZIF-8) composite material for supercapacitors, Mater. Lett., 2014, vol. 128, pp. 208–211. Doi: https://doi.org/10.1016/j.matlet.2014.04.175
Li, D., Müller, M.B., Gilje, S., Kaner, R.B., and Wallace, G.G., Processable aqueous dispersions of graphene nanosheets, Nat. Nano, 2008, vol. 3, pp. 101–105. Doi: https://doi.org/10.1038/nnano.2007.451
Guo, S.J., Dong, S.J., and Wang, E., Three-dimensional Pt-on-Pd bimetallic nanodendrites supported on graphene nanosheet: facile synthesis and used as an advanced nanoelectrocatalyst for methanol oxidation, ACS Nano, 2010, vol. 4, pp. 547–555. Doi: https://doi.org/10.1021/nn9014483
Tran, U.P.N., Le, K.K.A., and Phan, N.T.S., Expanding applications of metal–organic frameworks: zeolite imidazolate framework ZIF-8 as an efficient heterogeneous catalyst for the knoevenagel reaction, Acs Catal., 2011, vol. 1, pp. 120–127. Doi: https://doi.org/10.1021/cs1000625
Ye, X.L., Gu, Y.G., and Wang, C.M., Fabrication of the Cu2O/polyvinyl pyrrolidone–graphene modified glassy carbon–rotating disk electrode and its application for sensitive detection of herbicide paraquat, Sens. Actuators B Chem., 2012, vol. 173, pp. 530–539. Doi: https://doi.org/10.1016/j.snb.2012.07.047
Nasirpouri, F., Pourmahmoudi, H., Abbasi, F., Littlejohn, S., Chauhan, A.S., and Nogaret, A., Modification of Chemically Exfoliated Graphene to Produce Efficient Piezoresistive Polystyrene–Graphene Composites, J. Electron. Mater., 2015, vol. 44, pp. 3512–3522. Doi: https://doi.org/10.1007/s11664-015-3799-0
Uddin, E.Md., Layek, K.R., Kim, H.N., Hui, D., and Lee, H.J., Preparation and properties of reduced graphene oxide/polyacrylonitrile nanocomposites using polyvinyl phenol, Composites Part B, 2015, vol. 80, pp. 238–245. Doi: https://doi.org/10.1016/j.compositesb.2015.06.009
Zhang, W.J., Li, Y.J., Zhang, X.X., and Li, C.L., Facile synthesis of highly active reduced graphene oxide–CuI catalyst through a simple combustion method for photocatalytic reduction of CO2 to methanol, J. Solid State Chem., 2017, vol. 253, pp. 47–51. Doi: https://doi.org/10.1016/j.jssc.2017.05.022
Jomekian, A., Behbahani, R.M., Mohammadi, T., and Kargari, A., Utilization of Pebax 1657 as structure directing agent in fabrication of ultra-porous ZIF-8, J. Solid State Chem., 2016, vol. 235, pp. 212–216. Doi: https://doi.org/10.1016/j.jssc.2016.01.004
Jayashree, E., Francesca, B., Carlo, L., and Silvia, B., H2S interaction with HKUST-1 and ZIF-8 MOFs: A multitechnique study, Microporous Mesoporous Mater., 2015, vol. 207, pp. 90–94. Doi: https://doi.org/10.1016/j.micromeso.2014.12.034
Liu, J.X., Li, R., Hu, Y.Y., Li, T., Jia, Z.H., Wang, Y.F., Wang, Y.W., Zhang, X.C., and Fan, C.M., Harnessing Ag nanofilm as an electrons transfer mediator for enhanced visible light photocatalytic performance of Ag@AgCl/Ag nanofilm/ZIF-8 photocatalyst, Appl. Catal. B, 2017, vol. 202, pp. 64–71. Doi: https://doi.org/10.1016/j.apcatb.2016.09.015
Lu, W.B., Ning, R., Qin, X.Y., Zhang, Y.W., Chang, G.H., Liu, S., Luo, Y.L., and Sun, X.P., Synthesis of Au nanoparticles decorated graphene oxide nanosheets: Noncovalent functionalization by TWEEN 20 in situ reduction of aqueous chloroaurate ions for hydrazine detection and catalytic reduction of 4-nitrophenol, J. Hazard. Mater., 2011, vol. 197, pp. 320–326. Doi: https://doi.org/10.1016/j.jhazmat.2011.09.092
Gong, J.M., Zhou, T., Song, D.D., and Zhang, L.Z., Monodispersed Au nanoparticles decorated graphene as an enhanced sensing platform for ultrasensitive stripping voltammetric detection of mercury(II), Sens. Actuators B Chem., 2010, vol. 150, pp. 491–497. Doi: https://doi.org/10.1016/j.snb.2010.09.014
Dong, S.Y., Zhang, P.H., Liu, H., Li, N., and Huang, T.L., Direct electrochemistry and electrocatalysis of hemoglobin in composite film based on ionic liquid and NiO microspheres with different morphologies, Biosens. Bioelectron., 2011, vol. 26, pp. 4082–4087. Doi: https://doi.org/10.1016/j.bios.2011.03.039
Laviron, E., Adsorption, autoinhibition and autocatalysis in polarography and in linear potential sweep voltammetry, J. Electroanal. Chem., 1974, vol. 52, pp. 355–393. Doi: https://doi.org/10.1016/S0022-0728(74)80448-1
Karuwan, C., Wisitsoraat, A., Maturos, T., Phokharatkul, D., Sappat, A., Jaruwongrungsee, K., Lomas, T., and Tuantranont, A., Flow injection based microfluidic device with carbon nanotube electrode for rapid salbutamol detection, Talanta, 2009, vol. 79, pp. 995–1000. Doi: https://doi.org/10.1016/j.talanta.2009.02.015
Karuwan, C., Sriprachuabwong, C., Wisitsoraat, A., Phokharatkul, D., Sritongkham, P., and Tuantranont, A., Inkjet-printed graphene-poly(3,4-ethylenedioxythiophene): poly(styrene–sulfonate) modified on screen printed carbon electrode for electrochemical sensing of salbutamol, Sens. Actuators B Chem., 2012, vol. 161, pp. 549–555. Doi: https://doi.org/10.1016/j.snb.2011.10.074
Lin, X.Y., Ni, Y.N., and Kokot, S., A novel electrochemical sensor for the analysis of β-agonists: The poly(acid chrome blue K)/graphene oxide–nafion/glassy carbon electrode, J. Hazard. Mater., 2013, vol. 260, pp. 508–517. Doi: https://doi.org/10.1016/j.jhazmat.2013.06.004
Lin, K.C., Hong, C.P., and Chen, S.M., Simultaneous determination for toxic ractopamine and salbutamol in pork sample using hybrid carbon nanotubes, Sens. Actuators B Chem., 2013, vol. 177, pp. 428–436. Doi: https://doi.org/10.1016/j.snb.2012.11.052
Huang, J.D., Lin, Q., Zhang, X.M., He, X.R., Xing, X.R., Lian, W.J., Zuo, M.M., and Zhang, Q.Q., Electrochemical immunosensor based on polyaniline/poly (acrylic acid) and Au–hybrid graphene nanocomposite for sensitivity enhanced detection of salbutamol, Food Res. Int., 2011, vol. 44, pp. 92–97. Doi: https://doi.org/10.1016/j.foodres.2010.11.006
Alizadeh, T. and Fard, L.A., Synthesis of Cu2+-mediated nano-sized salbutamol-imprinted polymer and its use for indirect recognition of ultra-trace levels of salbutamol, Anal. Chim. Acta, 2013, vol. 769, pp. 100–107. Doi: https://doi.org/10.1016/j.aca.2013.01.032
Дополнительные материалы отсутствуют.