Электрохимия, 2019, T. 55, № 9, стр. 1059-1068
Селективный к алюминию(III) изготовленный методом трафаретной печати датчик на основе метилового красного
Эман Йоссри Фраг a, *, Марва Э. Мохамед a, Яссер Сами a
a Отделение химии, факультет естественных наук, Каирский университет
12613 Гиза, ул. Гамаа, Египет
* E-mail: emanyossri@sci.cu.edu.eg
Поступила в редакцию 09.07.2018
После доработки 12.01.2019
Принята к публикации 12.02.2019
Аннотация
Модифицированный изготовленный методом трафаретной печати электрод (МТПЭ), содержащий метиловый красный (2-[[4-(диметиламино)фенил]диазенил]бензойная кислота), получен для определения ионов алюминия в образцах воды и фармацевтических препаратов (маалокс и эпикогель). МТПЭ проявляет линейный отклик в широком диапазоне концентраций алюминия от 5.0 × 10–6 до 1.0 × 10–2 М при 25°С с наклоном для трехзарядного катиона 20.4 ± 0.5 мВ/декада и пределом обнаружения 5.0 × 10–6 М в диапазоне pH от 3 до 5. Кроме того, механизм химической реакции между метиловым красным и ионами алюминия на поверхности датчика исследовали, используя аналитические методы ИК-спектроскопии, энергодисперсионной рентгеновской спектроскопии (ЭДР) и сканирующей электронной микроскопии (СЭМ). Полученный датчик также проявлял воспроизводимость и устойчивость быстрого отклика в течение 14-недельного периода, причем время отклика составляло приблизительно 5 с. Предложенный потенциометрический метод валидирован согласно рекомендациям IUPAC. Результаты, полученные с помощью предложенного датчика, были сопоставимы с результатами, полученными методом масс-спектрометрии с индуктивно связанной плазмой (МС–ИСП).
ВВЕДЕНИЕ
В ряде исследований внимание сосредоточено на опасности алюминия для человека, хотя соединения алюминия используют в лечении повышенной кислотности желудочного сока и язвы желудка и двенадцатиперстной кишки без каких-либо побочных эффектов. Кроме того, алюминий играет важную роль в заболеваниях, связанных с диализом, болезни Альцгеймера и болезни Паркинсона [1–5]. Таким образом, для определения алюминия используют множество методов. К ним относятся оптическая эмиссионная спектроскопия с индуктивно связанной плазмой (ОЭС-ИСП) [6, 7], эндотермическая атомно-абсорбционная спектрометрия [8–11] и ВЭЖХ [12]. Электрохимические методы, применяемые для оценки концентрации алюминия в разнообразных образцах воды, включают методы квадратно-волновой вольтамперометрии [13], циклической вольтамперометрии [14], дифференциальной импульсной вольтамперометрии [15] и потенциометрии [16–21]. С другой стороны, электроаналитические методы проявляют высокую селективность в измерении электрических величин, включая заряд, потенциал и ток, а также связанные с ними химические параметры. Их широко используют во многих областях, таких как промышленный контроль качества, биохимический анализ и экологический мониторинг. Электроаналитические процедуры регулируют характеристики поверхности исследуемого электрода.
Ионоселективные электроды (ИСЭ) используют для потенциометрической оценки активностей или концентраций ионов в различных формах. ИСЭ имеют многочисленные преимущества, такие как простое изготовление, короткое расходуемое время, применимость к окрашенным и мутным растворам, низкая стоимость, низкий предел обнаружения, относительно хорошая селективность и точность [22]. Кроме того, ИСЭ применяют для определения ионов в широком диапазоне концентраций в воде и других средах [23].
Хотя угольные пастовые электроды широко используют в аналитических процедурах, их промышленное применение ограничено вследствие их относительно большого размера и жидкой природы. Затем были разработаны твердофазные датчики посредством смешивания полимера с частицами графита и растворителя с последующим нанесением на ленточную подложку. Растворитель затем испаряют и получают проводящую пленку с внедренными частицами графита, связанными полимерными молекулами. Сетку заданной толщины (от 20 до 100 мкм) наносят на подложку, обычно представляющую собой изолятор, и угольную краску наносят на сетку таким образом, что краска заполняет отверстия. Всю матрицу датчиков обычно печатают в одной партии. В конструкции изготовленных методом трафаретной печати электродов используют различные конфигурации, содержащие один или несколько слоев. Изготовленные методом трафаретной печати электроды проявляют многочисленные преимущества, такие как простота, механическая устойчивость, высокая воспроизводимость и надежность, низкая стоимость, высокая гибкость и превосходная однородность [24].
Цель настоящей работы заключалась в том, чтобы получить и исследовать простой потенциометрический модифицированный изготовленный методом трафаретной печати электрод (МТПЭ), предназначенный для селективного определения алюминия в образцах воды и фармацевтических препаратов (эпикогель и маалокс).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реагенты и приборы
Сульфат алюминия [Al2(SO4)3 ∙ 16H2O] получен от компании Koch Light. Для получения МТПЭ были использованы 2-[[4-(диметиламино)фенил]диазенил]бензойная кислота (Sanofi labaz laboratories), графитовый порошок (синтетический с размером частиц от 1 до 2 мм, Aldrich), трикрезилфосфат (TCP; Alfa-Aesar), высокомолекулярный поливинилхлорид (PVC, Aldrich), ацетон и циклогексанон (Fluka, Швейцария).
Для измерений потенциала использовали pH/милливольтметр Jenway 3505. В сочетании с рабочими изготовленными датчиками использовали электрод сравнения Ag/AgCl (Metrohm 6.0726.100). Для исследования морфологии поверхности предложенного датчика использовали энергодисперсионный рентгеновский (ЭДР) анализатор (Египетский национальный исследовательский центр) и сканирующий электронный микроскоп (СЭМ) Quanta FEG250 (национальный исследовательский центр). Для регистрации ИК-спектров с преобразованием Фурье (таблетки с KBr) в диапазоне от 4000 до 400 см–1 использовали спектрометр Perkin-Elmer 1650 (Микроаналитический центр, Каирский университет, Египет).
Образцы
Образцы воды получали со станции водоснабжения, расположенной в городе Эмбаба, фильтровали и анализировали, определяя содержание ионов алюминия с помощью изготовленного датчика. В водопроводную воду добавляли ионы алюминия в различных концентрациях.
Эпикогель (8.1 г гидроксида алюминия на 100 мл суспензии) от компании Egyptian International Pharmaceutical Industries Co. (EIPICO).
Маалокс (4.6 г гидроксида алюминия на 100 мл суспензии) от компании Sanofi.
Получение модифицированных изготовленных методом трафаретной печати электродов
Чувствительные к ионам ТПЭ изготавливали согласно ранее опубликованной процедуре [25] с использованием угольной краски, для получения которой смешивали метиловый красный (5–20 мг), TCP (0.90 г) TCP, 8% поливинилхлорид (2.5 г) и угольный порошок (1.5 г). Тщательно перемешанную графитовую краску насыпали на сетку и вдавливали в сетку, используя шестидюймовый резиновый валик Sericol SE–C52 средней твердости, который держали под углом, составляющим приблизительно 60°. Затем резиновым валиком прокатывали трафарет; таким образом, электродные трафареты заполняли краской. После печати осуществляли отверждение в течение 2 ч при 50°C. После завершения процесса печати трафарет очищали, используя товарный ацетон в качестве растворителя, чтобы удалить с трафарета избыток краски. Затем на печатные электроды наносили слой изолятора, оставляя прямоугольную рабочую область, имеющую заданные размеры (5 × 5 мм) и такую же (для электрического контакта) на другой стороне. Изготовленные датчики хранили в закрытых резервуарах в холодильнике при 4°C и использовали без какой-либо предварительной обработки.
Измерение потенциала с использованием МТПЭ
Потенциал содержащих алюминий растворов измеряли, используя МТПЭ в сочетании с электродом сравнения Ag/AgCl и аликвоты по 3 мл растворов с концентрацией ионов алюминия в диапазоне от 1.0 × 10–7 до 1.0 × 10–1 М. Калибровочный график строили по показаниям потенциала в зависимости от pAl. Потенциал МТПЭ измеряется, когда ионы алюминия переходят границу раздела между фазой пасты и фазой водного образца.
Определение алюминия в реальных образцах
Для определения алюминия в фармацевтическом препарате эпикогель или маалокс (1 мл образца) разбавляли до 1000 мл дистиллированной водой. После этого отбирали образец (3 мл) разбавленного раствора, содержащего эпикогель или маалокс, или реальной воды и определяли концентрацию алюминия(III) посредством потенциометрической калибровочной кривой, используя МТПЭ в качестве чувствительного электрода и метод МС–ИСП, причем фармацевтический препарат содержит алюминий в такой высокой концентрации, что метод стандартных добавок оказывается неприемлемым для этой цели, и авторы предпочли метод калибровки. Процедуру повторяли несколько раз, чтобы проверить ее прецизионность и точность, анализируя образец методом МС–ИСП.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Состав и исследование электродов
Содержание ионофора в полученной краске влияет на чувствительность потенциометрических МТПЭ, что было исследовано. Для этой цели изготавливали четыре МТПЭ, содержащие 5, 10, 15 и 20 мг метилового красного, причем содержание углерода, пластификатора и PVC оставалось неизменным. На основании полученных результатов, представленных в табл. 1, содержание 10 мг метилового красного в датчике был выбрано в качестве наилучшего содержания для получения чувствительного к алюминию электрода, который проявляет на графике по уравнению Нернста для трехзарядного иона наклон 20.4 ± 0.5 мВ/декада (приблизительно 59.2/3) в диапазоне концентраций от 5.0 × 10–6 до 1.0 × 10–2 М, рис. 1. Предел обнаружения представляет собой минимальное содержание исследуемого соединения в образце, которое может быть обнаружено, но не должно быть обязательно определено количественно, с приемлемой определенностью. Предел обнаружения электроаналитического метода представляет собой важный фактор, если количественные измерения должны быть проведены при концентрациях, близких к данному пределу. Предел обнаружения, вычисленный по пересечению двух экстраполированных линейных сегментов калибровочного графика, составлял 5.0 × 10–6 М для активности алюминия. Последующее увеличение количества метилового красного не привело к какому-либо усилению отклика датчика в отношении наклона графика Нернста или рабочего диапазона концентраций.
Таблица 1.
Влияние содержания метилового красного на характеристики изготовленного датчика для потенциометрической калибровки по ионам алюминия
| Содержание метилового красного, мг | Линейный диапазон концентраций, М | Наклон ± ± среднеквадратичное отклонение, мВ/декада (n = 5) | Коэффициент корреляции, r2 |
|---|---|---|---|
| 5.0 | 5.0 × 10−6 – 1.0 × 10–2 | 21.2 + 0.06 | 0.9996 |
| 10.0 | 5.0 × 10−6 – 1.0 × 10–2 | 20.4 + 0.5 | 0.9999 |
| 15.0 | 5.0 × 10−6 – 1.0 × 10–2 | 18.1 + 0.4 | 0.9998 |
| 20.0 | 5.0 × 10−6 – 1.0 × 10–2 | 16.9 + 0.06 | 0.9994 |
Рис. 1.
Влияние содержания метилового красного на отклик МТПЭ для потенциометрического определения ионов алюминия.

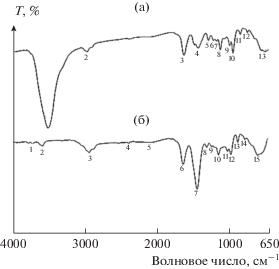
Энергодисперсионный рентгеновский (ЭДР) анализатор и сканирующий электронный микроскоп (СЭМ) представляют собой важные приборы, используемые для исследования морфологии поверхности предложенного датчика. На рис. 2 представлено изображение датчика до и после взаимодействия с ионами алюминия. Микрофотографии показали увеличение площади поверхности графита, которая была заполнена комплексом, образующимся в результате взаимодействия ионофора (метилового красного) с ионами алюминия, которые были экстрагированы пастой с помощью пластификатора (TCP), о чем свидетельствовало процентное содержание алюминия, определенное методом ЭДР после выдерживания датчика в растворе, содержащем алюминий. Эти данные подтвердили ИК-спектры на рис. 3. Свободный лиганд метиловый красный проявляет широкую полосу при 3434 см–1, которой соответствуют валентные колебания ν(OH) карбоксильной группы, интенсивную полосу при 1626 см–1, которой соответствуют валентные колебания ν(C=O) карбоксильной группы, полосу при 1520 см–1, которой соответствуют асимметричные колебания ν(COO–), полосу при 1442 см–1, которой соответствуют симметричные колебания ν(COO–), и полосу при 1303 см–1, которой соответствуют колебания ν(N=N), для датчика перед выдерживанием в растворе, содержащем ионы иона алюминия. После выдерживания датчика в растворе, содержащем ионы иона алюминия, и регистрации ИК-спектров наблюдали спектральные различия. Спектральные полосы, которым соответствуют колебания групп (OH), (C=O), (COO–) и (N=N), были сдвинуты к значениям, составляющим 3432, 1628.6, 1434.7 и 1306.5 см–1, соответственно, что предполагает образование комплекса в результате координации ионофора метилового красного и иона алюминия посредством групп COO– и N=N. В спектре комплекса новые полосы, которые наблюдали при 599 и 550 см–1, соответствуют колебаниям ν(Al–O) и ν(Al–N), как показывает предложенная структура образующегося комплекса [26], рис. 4.
Рис. 2.
Полученные методом СЭМ изображения поверхности датчика МТПЭ (a) до и (б) после взаимодействия с ионами алюминия в концентрации 1.0 × × 10–3 М с анализом методом ЭДР, показывающим массовое процентное содержание различных элементов, присутствующих в МТПЭ.

Эксплуатационные характеристики датчика
Характеристики отклика потенциометрического датчика, чувствительного к алюминию и модифицированного добавлением 10 мг метилового красного в качестве ионофора и TCP в качестве пластификатора, оценивали согласно рекомендациям IUPAC [27].
Отклик и срок службы
Время динамического отклика исследовали для электрода посредством изменения времени, необходимого для достижения устойчивого уровня потенциала (в пределах ±1 мВ). После выдерживания электрода в растворах с различными концентрациями ионов алюминия, которые десятикратно возрастали на последовательных стадиях в диапазоне концентраций от 5.0 × 10–6 до 1.0 × 10–2 М, см. рис. 5 МТПЭ проявлял очень короткое время отклика, составляющее приблизительно 5 с, т.е. короче, чем время отклика в ранее опубликованных работах по исследованию датчиков алюминия [30–34]. Короткое время отклика представляет собой результат наилучшего состава краски, поскольку электрод содержит углеродные частицы, которые заключает в себе очень тонкая пленка пластификатора (TCP), имеющего высокую диэлектрическую проницаемость, причем добавление пластификаторов не только улучшает технологичность пасты, но также увеличивает рабочий диапазон концентраций, устойчивость и срок хранения датчика. Пластификатор представляет собой обязательный компонент электрода и влияет на селективность, предел обнаружения, чувствительность электродов и подвижность электроактивного катиона в пасте. Он также выступает в качестве проводника и способствует экстракции ионов алюминия в пасту, что было подтверждено содержанием ионов алюминия, составляющим 4.82% по данным ЭДР. Быстрое и устойчивое показание потенциала обеспечило тот факт, что для всего процесса калибровки с использованием предложенного датчика оказалось достаточным время, составляющее лишь от 1 до 2 мин.
Предложенный датчик калибровали в различные дни в течение приблизительно 100 сут (на протяжении этого периода электрод использовали в течение 1 ч в сутки без какой-либо предварительной обработки) и не наблюдали при этом какого-либо существенного отклонения наклона, соответствующего трехзарядному иону, времени отклика и рабочего диапазона концентраций. Срок службы МТПЭ был более продолжительным, чем в случае других описанных датчиков, что свидетельствовало о высокой устойчивости и высокой механической прочности предложенного датчика. В течение этого периода были обнаружены незначительные изменения наклона и времени отклика.
Влияние pH
Было исследовано влияние изменения pH изучаемых растворов на отклик потенциала электродов. Значение pH изменяли посредством добавления хлористоводородной кислоты или гидроксида натрия в растворы с концентрацией алюминия от 1.0 × 10–4 до 1.0 × 10–2 М. Для всех значений pH от 2 до 10 измеряли потенциал и затем строили графики зависимости потенциала от pH для двух концентраций алюминия. На рис. 6 представлено, что отклик потенциала датчика сохранял постоянное значение в диапазоне pH от 3.0 до 5.0, и увеличение показаний потенциала при pH < 3.0 может быть обусловлено конкуренцией иона гидроксония, в то время как при pH > > 5.0 среда становится более основной, приводя к уменьшению концентрации свободных ионов алюминия вследствие образования осадка гидроксида алюминия в исследуемом растворе, что задерживает отклик датчика на ионы алюминия, приводя к уменьшению получаемых значений потенциала.
Влияние температуры исследуемого раствора на отклик датчика
Были построены калибровочные графики при различных температурах исследуемого раствора (от 10 до 60°C), чтобы определить изотермический коэффициент (dE/dt) электрода. Потенциалы (E) электрода при различных температурах, полученные из калибровочных графиков как точки пересечения при p[Al3+] = 0, наносили на график зависимости от (t – 25), где t представляет собой температуру (в °C) раствора, содержащего ионы алюминия, и прямолинейный график был получен согласно уравнению Антропова [28]:
Наклон графика дает изотермический коэффициент электрода, который оказался равным 1.3997 × 10–3 В/°C. Это низкое значение изотермического коэффициента электрода показывает высокую термическую устойчивость электрода без какого-либо отклонения от уравнения Нернста в исследуемом температурном диапазоне от 10 до 60°C.
Селективность и помехи
Селективность потенциометрических датчиков представляет собой важный параметр, который влияет на эффективность и применимость датчика. Исследование селективности осуществляли для датчика, который проявлял наилучшие эксплуатационные характеристики, такие как наклон, время отклика, срок службы и рабочий диапазон концентраций. Коэффициенты селективности lgKpot вычисляли с применением метода отдельных растворов (МОР) [29], используя следующее уравнение:
По методу согласованных потенциалов (МСП) [29] коэффициент селективности определяют как соотношение активностей основных ионов (A) и примесных ионов (B), которые дают одинаковое изменение потенциала в сравнительном растворе. Коэффициент селективности определяют по следующему уравнению:
В табл. 2 отрицательные значения коэффициента селективности показывают предпочтение в отношении ионов алюминия по сравнению с примесными ионами. Таким образом, коэффициент селективности показывает, что предложенный датчик способен обнаруживать ионы алюминия в присутствии других примесных ионов в меньшей или несколько большей концентрации, чем концентрация ионов алюминия.
Таблица 2.
Потенциометрические значения коэффициента селективности МТПЭ с применением МОР и МСП
| Примесные ионы | ${\text{lg}}{{K}_{{{\text{pot}}\,{\text{A}}{{{\text{l}}}^{{3 + }}},\,\,{\text{В}}}}}$ | |
|---|---|---|
| МОР | МСП | |
| Zn2+ | –4.00 | –3.5 |
| Ni2+ | –4.25 | –3.6 |
| Cr3+ | –3.90 | –4.2 |
| Mn2+ | –3.95 | –4.4 |
| Co2+ | –2.15 | –3.2 |
| Na+ | –1.20 | –1.5 |
| K+ | –1.85 | –2.1 |
| Cd2+ | –3.15 | –2.3 |
Межсуточная и внутрисуточная точность и прецизионность
Воспроизводимость и повторяемость предложенного датчика оценивали, измеряя отклик потенциала для трех различных концентраций алюминия в различных реальных образцах воды в течение 5 сут (межсуточная точность) и в течение 1 сут для подтверждения повторяемости (внутрисуточная точность), см. табл. 3. Значения степени обнаружения (%), среднеквадратического отклонения и относительного среднеквадратического отклонения (%) также подтверждают высокую точность предложенного датчика.
Таблица 3.
Внутрисуточная и межсуточная точность определения алюминия с помощью МТПЭ в чистых образцах (стандартные растворы) и образцах воды с добавками
| Стандарт-ные растворы, мг мл–1 | Найдено, мг мл–1 | Степень обнаружения, % | Среднеквадратичное отклонение | Относительное среднеквадратическое отклонение, % | ||||
|---|---|---|---|---|---|---|---|---|
| внутри-суточная точность | меж-суточная точность | внутри-суточная точность | меж-суточная точность | внутри-суточная точность | меж-суточная точность | внутри-суточная точность | меж-суточная точность | |
| Чистые образцы | ||||||||
| 0.6300 | 0.6300 | 0.6210 | 100 | 98.6 | 0.0200 | 0.03000 | 3.1 | 4.7 |
| 0.0063 | 0.00623 | 0.00626 | 98.8 | 99.3 | 0.0003 | 0.00024 | 3.8 | 4.1 |
| 0.00315 | 0.00313 | 0.00312 | 99.4 | 99.00 | 0.0001 | 0.00014 | 3.3 | 4.8 |
| Образцы воды с добавками | ||||||||
| 0.6300 | 0.6100 | 0.6230 | 96.8 | 98.4 | 0.0280 | 0.0310 | 4.5 | 4.9 |
| 0.063 | 0.0624 | 0.0613 | 98.4 | 96.8 | 0.0029 | 0.0030 | 4.6 | 4.8 |
| 0.0063 | 0.0061 | 0.0062 | 96.8 | 98.4 | 0.0003 | 0.00029 | 4.9 | 4.6 |
Аналитические приложения
Для исследования возможности применения селективного по отношению к алюминию МТПЭ для реальных образцов предложенный датчик использовали для определения концентрация ионов алюминия в воде и фармацевтических препаратах (маалокс, эпикогель). Как видно из табл. 4, полученные результаты в случае предложенного датчика аналогичны полученным результатам анализа тех же образцов методом МС–ИСП, что демонстрирует применимость селективного по отношению к алюминию электрода для анализа образцов воды и фармацевтических образцов без какого-либо взаимодействия с матрицей.
Таблица 4.
Определение ионов алюминия в образцах воды и фармацевтических препаратов с использованием предложенного датчика и описанного метода
| Образцы | Взято, мг мл–1 | Найдено с помощью МТПЭ, мг мл–1 | Найдено методом МС–ИСП, мг мл–1 | Степень обнаружения, % |
|---|---|---|---|---|
| Образец реальной воды | – | 0.26 × 10–3 | 0.27 × 10–3 | – |
| Образец воды с добавками | 6.3 × 10–5 | 6.12 × 10–5 | 6.0 × 10–5 | – |
| Эпикогель | 0.16146 | 0.1591 | – | 98.57 |
| Маалокс | 0.1200 | 0.116 | – | 96.60 |
Сравнительные исследования определения ионов алюминия
Данные, приведенные в табл. 5, представляют собой сравнение предложенного электрода МТПЭ и ранее разработанных электродов, селективных по отношению к алюминию, в отношении линейного диапазона, наклона, предела обнаружения, времени отклика и pH. Следует отметить, что по сроку службы, времени отклика, наклону и линейному диапазону МТПЭ значительно превосходит ранее описанные электроды, селективные по отношению к алюминию.
Таблица 5.
Сравнение предложенного потенциометрического метода и ранее опубликованных методов
| Тип электрода [ссылка] | Модификатор | Наклон, мВ/декада | Диапазон концентраций, М | Диапазон pH | Время отклика, с | Срок службы, недель | Предел обнаружения, М | Недостатки |
|---|---|---|---|---|---|---|---|---|
| Мембрана PVC [30] | NDTH | 19.6 ± 0.4 | 1.0 × 10–6–1.0 × 10–1 | 2.9–5.0 | 10 | 12 | 6.3 × 10−7 | Требуется получение NDTH. PVC не выдерживает механическое напряжение |
| Мембрана PVC [31] | 12C4 | 19.0 ± 0.18 | 1.0 × 10–6–1.0 × 10–1 | 2.9–5.0 | 15 | 10 | 5.5 × 10−7 | PVC не выдерживает механическое
напряжение Продолжительное время отклика |
| Мембрана PVC [32] | SSDA | 15.6 | 1.0 × 10–5–1.5 × 10–1 | 3.5–4.5 | – | >12 | 5.1 × 10−6 | Требуется получение SSDA PVC не выдерживает механическое напряжение Узкий диапазон pH Низкое значение наклона |
| Мембрана PVC [33] | 5PHAZSAL-NPHN | 19.3 ± 0.8 | 5.0 × 10–6–1.0 × 10–2 | 2.9–5.0 | 10 | 10 | 2.5 × 10−6 | Требуется получение ионофора PVC не выдерживает механическое напряжение Продолжительное время отклика |
| CPE [34] | AMC | 21.3 ± 0.18 | 7.0 × 10–6–1.0 × 10–2 | 3.0–5.0 | 6 | – | 6.0 × 10−6 | Требуется предварительная обработка CPE Отсутствует срок службы |
| МТПЭ данная работа | Метиловый красный | 20.4 ± 0.5 | 5.0 × 10–6–1.0 × 10–2 | 3.0–5.0 | 5 | 14 | 5.0 × 10−6 |
Примечание. NDTH: 6-(4-нитрофенил)-2-фенил-4-(тиофен-2-ил)-3,5-диаза-бицикло[3,1,0]гекс-2-ен.
12C4: 12-краун-4.
SSDA: основание Шиффа, бис(5-сульфонатсалицилальдегид)2,3-диаминобензол.
5PHAZOSAL-NPHN: бис(5-фенилазосалицилальдегид)2,3-нафталиндиамин.
AMC: азитромицин.
C15H15N3O2: 2-[[4-(диметиламино)фенил]диазенил]бензойная кислота.
Из табл. 5 очевидно, что все ранее разработанные методы относятся к определению алюминия с использованием ионоселективных электродов с мембраной PVC, в то время как предложенный датчик обладает многочисленными преимуществами, такими как малый размер, большая удельная поверхность, необязательность предварительной обработки, сокращенное время отклика, увеличенный срок службы, устойчивость к механическому напряжению, отсутствие внутреннего раствора, простота переноски и хранения и отсутствие необходимости подготовки используемого ионофора.
ВЫВОДЫ
Новый изготовленный методом трафаретной печати электрод исследован для определения ионов алюминия в реальных образцах воды и фармацевтических препаратов. Применение нового МТПЭ на основе метилового красного для определения алюминия обеспечивает наилучшие характеристики отклика и поведение согласно уравнению Нернста в широком диапазоне концентраций от 5.0 × 10–6 до 1.0 × 10–2 М и быстрый отклик в течение 5 с. Датчик хорошо работает в при pH от 3.0 до 5.0. Следовательно, предложенный датчик превосходит существующие датчики в отношении времени отклика и срок службы и при этом является сопоставимым в отношении других параметров, таких как наклон, диапазон pH и диапазон концентраций, как показывает табл. 5.
Список литературы
Campbell, A., The potential role of aluminum in Alzheimer’s disease, Nephrol Dial Transplant, 2002, vol. 17, p. 17–20.
Kawahara, M., Muramoto, K., Kobayashi, K., Mori, H., and Kuroda, Y., Aluminum promotes the aggregation of Alzheimer’s amyloid beta-protein in vitro, Biochem. Biophys. Res. Commun., 1994, vol. 198, p. 531.
Paik, S.R., Lee, J.H., Kim, D.H., Chang, C.S., and Kim, J., Aluminum-induced structural alterations of the precursor of the non-A beta component of Alzheimer’s disease amyloid, Arch. Biochem. Biophys., 1997, vol. 344, p. 325.
Lin, J.L., Kou, M.T., and Leu, M.L., Effect of Long-Term Low-Dose Aluminum-Containing Agents on Hemoglobin Synthesis in Patients with Chronic Renal Insufficiency, Nephron, 1996, vol. 74, p. 33.
Good, P.F., Olanow, C.W., and Perl, D.P., Neuromelanin-containing neurons of the substantia nigra accumulate iron and aluminum in Parkinson’s disease: a LAMMA study, Brain Res., 1992, vol. 593, p. 343.
Malik, J., Frankova, A., Drabek, O., Szakova, J., Ash, C., and Kokoska, L., Aluminum and other elements in selected herbal tea plant species and their infusions, Food Chem., 2013, vol. 139, p. 728.
Scancar, J., Stibilj, V., and Milacic, R., Determination of aluminum in Slovenian foodstuffs and its leachability from aluminum cookware, Food Chem., 2004, vol. 85, p. 151.
López C. Cabrera, F.F., Lorenzo, M.L., and López, M.C., Aluminum content of drinking waters, fruit juices and soft drinks: contribution to dietary intake, Sci. Total Environ., 2002, vol. 292, p. 205.
Jalbani, N., Kazi, T.G., Jamali, M.K., Arainm, B.M., Afridi, H.I., and Baloch, A., Evaluation of aluminum contents in different bakery foods by electrothermal atomic absorption spectrometer, J. Food Comp. and Anal., 2007, vol. 20, p. 226.
Bamjiand, N.M.S. and Kaladhar, M., Risk of increased aluminum burden in the Indian population contribution from aluminum cookware, Food Chem., 2000, vol. 70, p. 57.
Arvand, M. and Asadollahzade, S.A., Ion selective electrode for aluminum determination in pharmaceutical substances, tea leaves and water samples, Talanta, 2008, vol. 75, p. 1046.
Soleimani, M. and Afshar, M.G., Octaethylporphyrin as an ionophore for aluminum potentiometric sensor based on carbon paste electrode, Russ. J. Elektrokhim., 2014, vol. 50, p. 554. [Солемани, М., Афшар, М.Г. Октаэтилпорфирин – ионофор для потенциометрического сенсора на алюминий на основе угольно-пастового электрода. Электрохимия. 2014. Т. 50. С. 618.]
Kumar, R.H., Rani, S., and Malik, A., Development of a rapid and sensitive method for the determination of aluminum by reverse phase high performance liquid chromatography using a f luorescence detector, J. Chromatogr. Sci., 2014, vol. 53, p. 800.
Beltagiand, A.M. and Ghoneim, M.M., Simultaneous determination of trace aluminum(III), copper(II) and cadmium(II) in water samples by square wave adsorptive cathodic stripping voltammetry in the presence of oxine, J. Appl. Electrochem., 2009, vol. 39, p. 627.
Mersal, G.A.M. and Arida, H.A., New carbon paste modified micro electrode based on haematoxylin for determination of aluminum in underground water, Int. J. Electrochem. Sci., 2011, vol. 6, p. 1116.
Liu, J., Bi, S., Yang, L., Gu, X., Ma, P., Gan, N., Wang, X., Longa, X., and Zhanga, F., Speciation analysis of aluminum(III) in natural waters and biological fluids by complexing with various catechols followed by differential pulse voltammetry detection, Anal., 2002, vol. 12, p. 1657.
Tajik, S., Taherand, M.A., and Sheikhshoaie, I., Potentiometric determination of trace amounts of aluminum utilizing polyvinyl chloride membrane and coated platinum sensors based on E-N'-(2-hydroxy-3-methoxy-benzylidene) benzohydrazide, J. AOAC Int., 2013, vol. 96, p.1204.
Bera, R.K., Sahoo, S.K., Mittal, S.K., and Kumar, A.S.K., An imidazol based novel potentiomet-ric PVC membrane sensor for aluminum(III) determination, Int. J. Electrochem. Sci., 2010, vol. 5, p. 29.
Li, Y., Chai, Y., Yuan, R., Liang, W., Zhang, L., and Ye, G., Aluminum(III) selective electrode based on a newly synthesized glyoxal-bis-thiosemicarbazone Schiff base, J. A. Chem., 2008, vol. 63, p. 1090.
Evsevleeva, L., Bykova, L., and Badenikov, V., Aluminum selective electrode, J. A. Chem., 2005, vol. 60, no. 9, p. 866. [Евсевлеева, Л., Быкова, Л., Бадейников, В. Алюминий-селективный электрод. Журн. аналит. химии. 2005. Т. 60. № 9. С. 976.]
Abd El-Ghany, N.A., Frag, E.Y., and Abd El Fattah, M., Fabrication of chemically modified carbon paste electrode based on functionalized biopolymer for potentiometric determination of Al(III) ion in real water and pharmaceutical samples, J. Iranian Chem. Soc., 2018, vol. 15, p. 1987.
Bratovčić, A., Odobašić, A., and Ćatić, S., The advantages of the use of ion selective potentiometry in relation to UV/Vis spectroscopy, Agriculturae Conspectus Scientificus, 2009, vol. 3, p. 139.
Nour El Dein, F.A., Mohamed, G.G., Frag, E.Y.Z., and Mohamed, M.E., Modified screen printed and carbon paste ion selective electrodes for potentiometric determination of naphazoline hydrochloride in pure and pharmaceutical preparations, Int. J. Electrochem. Sci., 2012, vol. 7, p. 10266.
Frag, E.Y., Mohamed, M.E., and Fahim, E.M., Application of carbon sensors for potentiometric determination of copper(II) in water and biological fluids of Wilson disease patients. Studying the surface reaction using SEM, EDX, IR and DFT Biosensors and Bioelectronics, 2018, vol. 118, p. 122; Frag, E.Y., Omar, M.M., and Mohamed, H.A. Electrochemical characterization of vanadium(V) sensors modified with 2,4-dinitrophenyl hydrazine. Studying the reaction mechanism using SEM and IR, J. Electroanal. Chem., 2017, vol. 784, p. 124; Frag, E.Y., Aglan, R.F., and Mohamed, H.A., Lanthanum(III) potentiometric sensors based on ethyl benzoyl acetate, Arabian J. Chem., in press 2016.
Frag, E.Y.Z., Mohamed, G.G., and El-Sayed, W.G., Potentiometric determination of antihistaminic diphenhydramine hydrochloride in pharmaceutical preparations and biological fluids using screen-printed electrode, Bioelectrochemistry, 2011, vol. 82, p. 79; Frag, E.Y.Z., Mohamed, G.G., Nour El-Dien, F.A., and Mohamed, M.E., Construction and performance characterization of screen printed and carbon paste ion selective electrodes for potentiometric determination of naphazoline hydrochloride in pharmaceutical preparations, Analyst, 2011, vol. 136, p. 332; Nour El-Dien, F.A., Mohamed, G.G., Frag, E.Y.Z., and Mohamed, M.E., Modified Screen Printed and Carbon Paste Ion Selective Electrodes for Potentiometric Determination of Naphazoline Hydrochloride in Pure and Pharmaceutical Preparations, Int. J. Electrochem.Sci., 2012, vol. 7, p. 10266.
Jarad, A.J., Synthesis and Characterization of New Azo Dye Complexes with Selected Metal Ions, J. Al Nahrain Univer., 2012, vol. 15, no. 4, p. 74.
Recommendations for nomenclature of ion-selective electrodes, Pure & App. Chem., 1976, vol. 48, p. 127.
Антропов, Л.И. Теоретическая электрохимия. М.: Мир, 1972.
Umezawa, Y., Umezawa, K., and Sato., H., Selectivity coefficients for ion-selective electrodes: Recommended methods for reporting KA, Bpot values, Pure & Appl. Chern., 1995, vol. 67, no. 3, p. 507.
Arvand, M. and Asadollahzadeh, S.A., Ion selective electrode for aluminum determination in pharmaceutical substances,tea leaves and water samples, Talanta, 2008, vol. 75, p. 1046.
Pourfarkhani, M.E., Rounaghi, G.H., and Arbab Zavar, M.H., Construction of a New Aluminum(III) Cation Selective Electrode Based on 12-Crown-4 as an Ionophore, J. Braz. Chem. Soc., 2015, vol. 26, no. 5, p. 963.
Abbaspour, A., Esmaeilbeig, A.R., Jarrahpour, A.A., Khajeh, B., and Kia, R., Aluminum(III)-selective electrode based on a newly synthesized tetradentate Schiff base, Talanta, 2002, vol. 58, p. 397.
Yao, H., Wang, S., Ma, X., Ren, L., and Yan, F., A Novel Aluminum(III)-selective PVC Membrane Electrode Based on a Schiff Base Complex of bis(5-sulphonate salicylaldehyde) 2,3-diaminobenzene, Int. J. Electrochem. Sci, 2014, vol. 9, p. 2158.
Mohamed, M.E., Modified Carbon Paste Electrode for Potentiometric Determination of Aluminum Ion in Spiked Real Water Sample, Russ. Elektrokhimiya, 2016, vol. 52, no. 8, p. 843. [Мохаммед, М.Э. Модифицированный электрод из угольной пасты для потенциометрического определения иона алюминия, добавленного в образцы природной воды. Электрохимия. 2016. Т. 52. № 8. С. 843.]
Дополнительные материалы отсутствуют.