Электрохимия, 2020, T. 56, № 3, стр. 246-255
КОМПЬЮТЕРНОЕ МОДЕЛИРОВАНИЕ СТРУКТУРЫ И МЕХАНИЗМОВ ФУНКЦИОНИРОВАНИЯ АКТИВНОГО СЛОЯ КАТОДА ЛИТИЙ-КИСЛОРОДНОГО АККУМУЛЯТОРА
Ю. Г. Чирков а, *, В. И. Ростокин b, **, В. Н. Андреев а, ***, В. А. Богдановская а, ****
b Национальный исследовательский ядерный университет (МИФИ)
115409 Москва, Каширское шоссе, 31, Россия
а Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119071 Москва, Ленинский просп., 31, корп. 4, Россия
* E-mail: olga.nedelina@gmail.com
** E-mail: viktor.rostockin@yandex.ru
*** E-mail: vandr@phyche.ac.ru
**** E-mail: bogd@elchem.ac.ru
Поступила в редакцию 21.03.2019
После доработки 26.06.2019
Принята к публикации 29.07.2019
Аннотация
В настоящее время возник большой интерес к созданию литий-кислородного (воздушного) аккумулятора (ЛКА), удельная энергия которого будет, как считается, примерно на порядок превышать характеристики ставших уже традиционными литий-ионных аккумуляторов. Активный слой (АС) катода, этого главного узла ЛКА, представляет собой слой материала, имеющего сложную структуру пор. В нем при разряде в результате ряда электрохимических и химических превращений происходит накопление конечного продукта – пероксида лития, который затем используется при заряжении ЛКА. Пока этот источник тока обладает еще многими недостатками. В настоящей статье с помощью компьютерного моделирование исследуется, как особенности структуры АС катода влияют на величины габаритных характеристик ЛКА при заряжении и разряде. Выявлена совокупность причин, препятствующих возможности улучшить габаритные характеристики ЛКА. Показано, что эти трудности носят органический характер и в рамках принятой ныне практики конструирования АС катода ЛКА не могут быть преодолены. Поэтому необходим поиск принципиально новых подходов к изготовлению АС катода.
ВВЕДЕНИЕ (ПОСТАНОВКА ЗАДАЧИ ИССЛЕДОВАНИЯ)
Использование литий-кислородных аккумуляторов (ЛКА), чрезвычайно мощных устройств хранения энергии (теоретическая оценка – 5200 Вт ч/кг), может привести к значительному прогрессу в совершенствовании портативной электроники, гибридных средств передвижения и возобновляемых источников энергии [1–3]. В таких источниках тока успешное функционирование активного слоя (АС) катода играет ключевую роль, как при заряжении, так и в процессе разряда ЛКА. В настоящее время Li–O2 батареи пока еще находятся на начальной стадии своего совершенствования. Крайне мала величина плотности тока (десятые доли мА/см2), что создает большие препятствие для коммерческих приложений. При разряде оказывается невысокой емкость катода, невелика и плотность энергии ЛКА. При заряжении значительное увеличение потенциала вызывает деструкцию материалов, из которых изготовлен катод. Процессы заряжения и разряда занимают много времени.
Характерной особенностью процесса разряда ЛКА с неводным электролитом является закупорка пор положительного электрода нерастворимым в электролите и неэлектропроводным веществом – пероксидом лития Li2O2 [4, 5], который является конечным продуктом реакции при восстановлении кислорода [6, 7]:
(1)
$\begin{gathered} {{{\text{О}}}_{2}} + {\text{}} \to {\text{О}}_{2}^{ - },\,\,\,\,{\text{О}}_{2}^{ - } + {\text{ L}}{{{\text{i}}}^{ + }} \to {\text{Li}}{{{\text{O}}}_{2}}, \\ 2{\text{Li}}{{{\text{O}}}_{2}} \to {\text{L}}{{{\text{i}}}_{2}}{{{\text{O}}}_{2}} + {{{\text{O}}}_{2}}. \\ \end{gathered} $Пероксид лития может быть окислен при наложении анодного тока. При заряжении ЛКА на аноде идет процесс регенерации кислорода:
(2)
${\text{L}}{{{\text{i}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{2}}}} \to 2{\text{L}}{{{\text{i}}}^{ + }} + {{{\text{O}}}_{2}} + 2{\text{e}}.$Существует большая литература, посвященная выбору материалов и структур АС катодов ЛКА. Значительные усилия экспериментаторов и теоретиков затрачены на поиски оптимальной структуры катода. Подробный анализ этих работ можно найти, к примеру, в обзорах [8, 9] и в публикации [10]. Цель настоящей статьи – поиски причин, отчего в настоящее время габаритные характеристики катодов ЛКА все еще обладают рядом вышеперечисленных недостатков.
ОСОБЕННОСТИ ПОРИСТОЙ СТРУКТУРЫ АКТИВНОГО СЛОЯ КАТОДА
Исследователями, конструирующими новые типы положительного электрода ЛКА, было перепробовано огромное число композиций самых различных материалов. Эти электрокатализаторы для Li–O2 системы с неводным электролитом могут быть условно классифицированы на три группы: 1. пористые высокодисперсные углеродные материалы, включая сажу, функционализированный углерод, наноструктурированный углерод (нанотрубки, волокна, графены); 2. простые и сложные оксиды переходных не платиновых металлов; 3. благородные металлы, их оксиды и сплавы. В результате многочисленных экспериментальных и теоретических исследований постепенно стало складываться общее качественное представление о том, какой в идеале должна быть оптимальная архитектура пористой структуры АС катода ЛКА. А если выражаться точнее, какие надо предъявлять требования к пористости, к удельным поверхностям различных сегментов пор (микропоры, мезопоры, макропоры) и к общей удельной поверхности всех пор катода.
Экспериментальные исследования показали, что пористость катода, размер его общей удельной поверхности оказывают существенное влияние на величину емкости катода при разряде. Одновременно с экспериментальными работами велось и компьютерное моделирование пористой структуры катода и хода совершающихся в нем процессов. Особый интерес тут представляют теоретические работы [10, 11]. В них развивается новый многоуровневый (multiscale) подход к модельным исследованиям, при котором на характеристики катода при разряде оказывают влияние уже не отдельные группы пор, но вся совокупность микроструктуры пористого пространства АС катода. В [11] прямо указывается, что для выбранной в статье модели катода надо стремиться к увеличению общей пористости. Общая удельная поверхность пор должна составлять величину 3.5–4.5 × 106 см–1. В распределении пор по размерам должны присутствовать два пика групп пор с размерами 7–8 нм для мелких пор и 33–110 нм для пор крупных. Рекомендации подобного же рода высказывались также и в работе [12].
Как свидетельствует соотношение (1), процесс образования пероксида лития в процессе разряда ЛКА требует создания в АС катода двух каналов. Подачи в активный слой (в нем все поры заполнены электролитом) по возможности на большую глубину молекул кислорода, поступающих из газодиффузионного слоя (ГДС), и потоков ионов лития, идущих из межэлектродного пространства ЛКА. При этом перечень требований, позволяющих полагать АС катода ЛКА удачным для проведения в нем процесса разряда, можно при принятых ныне попытках конструирования структуры АС катода ЛКА представить в следующем виде.
Требование 1. Наличие в катоде макропор с радиусами в сотни нм. Они практически не “зарастают” нерастворимым и не электропроводным в электролите пероксидом лития. В работе [13] в модели монопористого АС катода было показано, как быстро с ростом радиусов отдельных пор катода возрастает время окончания разряда, обусловленная “зарастанием” устья этих пор. Ввиду этого макропоры, если их сравнивать с микропорами и мезопорами, могут стать “газовым” каналом для подачи кислорода вглубь АС катода. Таким образом, можно, в принципе, заставить работать уже сравнительно толстые пористые АС катода.
Требование 2. В то же время в катоде необходимо присутствие кроме макропор также мезопор. Они, обладая высокой удельной поверхностью, необходимой для протекания первой стадии процесса (1), одновременно в отличие от микропор имеют значительные собственные объемы, необходимые для запасания в них значительного количества образующегося в мезопорах АС катода пероксида лития. Кроме того, мезопоры в совокупности служат каналом для подачи в АС катода ионов лития.
Требование 3. Чтобы быть эффективным поставщиком молекул кислорода в АС катода, каждая макропора должна быть, это очевидно, в контакте с соседними макропорами. Должен быть создан кластер из макропор, каждая из которых способна получать кислород от соседа и передавать его дальше. Для этого концентрация макропор в АС катода должна быть достаточно большой. Если же в АС катода макропор мало, и преобладают мезопоры, то они, “обволакивая” редкие макропоры, прерывают движение молекул кислорода по цепочкам макропор вглубь пористой структуры. И кислород оказывается неспособным проникнуть в АС катода на большую глубину. Таким образом, должен быть сформирован с точки зрения теории перколяции [14] перколяционный кластер, способный обеспечивать путем диффузии в макропорах, заполненных электролитом, транспорт кислорода к мезопорам. Перколяционный кластер из макропор дальше будем называть “кислородным кластером”.
Требование 4. Образование пероксида лития совершается в заполненных электролитом мезопорах. Они получают необходимый им кислород из макропор там, где мезопоры встречаются (пересекаются) с макропорами. Расчеты показывают, что образование пероксида лития наиболее быстро идет в области пересечения этих двух типов пор. Именно здесь, в устьях мезопор, концентрация кислорода наиболее велика, поэтому тут процесс образования пероксида лития идет наиболее активно. Вход в мезопору постепенно и достаточно быстро “зарастает” пероксидом лития. При полном «зарастании» устья мезопоры процесс образования в ней пероксида лития полностью прекращается.
Крайне важно подчеркнуть, что “зарастание” устьев мезопор ограничивает не только поступление кислорода из макропор в мезопоры, но также и поступление ионов лития в мезопоры из находящегося в макропорах электролита. Поэтому можно с достаточно большой степенью достоверности полагать, что в основном ионы лития поступают в мезопоры не из макропор, а из перколяционного кластера заполненных электролитом мезопор, которые питаются в свою очередь ионами лития, поступающими из межэлектродного пространства ЛКА.
Таким образом, очевидна необходимость существования в АС катода двух перколяционных кластеров пор. “Кислородного кластера” (кластер из макропор, получающий кислород из ГДС) и “ионного кластера” (кластер, состоящий только из мезопор, осуществляющий поставку ионов лития из межэлектродного пространства ЛКА).
КОМПЬЮТЕРНОЕ МОДЕЛИРОВАНИЕ АКТИВНОГО СЛОЯ КАТОДА
Рассмотрим теперь процесс генерации пероксида лития в АС катода ЛКА более подробно. Займемся компьютерным моделированием. Разобьем объем АС катода на мелкие равновеликие кубики двух типов. Один тип кубиков будет представлять собой макропоры, заполненные электролитом с растворенным в них кислородом. Материалом для другого типа кубиков станет углеродная монопористая масса (мезопоры с фиксированным радиусом пор). Так возникает выбранная нами модель бипористой (макропоры и мезопоры) структуры АС катода, она представлена на рис. 1. В модельном кубе серые (макропоры) и черные (углеродный материал с мезопорами) кубики перемешаны случайным образом.
Рис. 1.
Модельный куб бипористого АС катода ЛКА. Серые кубики – крупные не “зарастающие” пероксидом лития макропоры, поставляющие кислород, черные кубики заполнены углеродной массой с мелкими порами (мезопорами), в них образуется пероксид лития и происходит транспорт ионов лития.
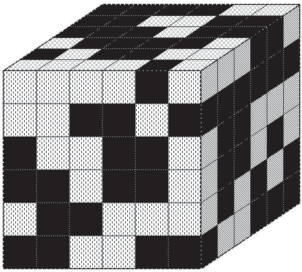
Охарактеризуем условия, при которых в АС катода способны возникнуть необходимые для нормального функционирования АС катода при проведении разряда два перколяционных кластера, с макропорами (кислородный кластер) и мезопорами (ионный кластер). Введем параметр ω, долю в модельном кубе черных (углеродных) кубиков. При ω = 0 модельный куб состоит только из серых кубиков, при ω = 1 – только из черных кубиков.
Согласно теории перколяции [15], можно рассчитать величину порога перколяции ω* – тот критический момент, когда в системе возникает перколяционный кластер из черных углеродных кубиков с мезопорами. Вот это предназначенное для расчета порога перколяции ионного кластера уравнение:
(3)
$2\left( {d - 1} \right){{\gamma }^{2}}{{\omega }^{3}} + \left( {2d - 3} \right)\gamma \omega - 1 = 0,$Решив его, в качестве единственного действительного решения для величины порога перколяции ω* получим значение:
(5)
$\omega * = {{\left[ {{{{\left( {1 + {{2}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}} \right)}}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}} + {{{\left( {1 - {{2}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}} \right)}}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} \right]} \mathord{\left/ {\vphantom {{\left[ {{{{\left( {1 + {{2}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}} \right)}}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}} + {{{\left( {1 - {{2}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}} \right)}}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} \right]} 2}} \right. \kern-0em} 2} = 0.298.$Таким образом, в модельном кубе черный (или ионный) перколяционный кластер образуется, если концентрация черных кубиков становится примерно равной 30%. Если это условие не выполнено, то в области 0 ≤ ω ≤ 0.3 серым кубикам с макропорами в модельном кубе удается блокировать связи между черными кубиками.
Сделаем теперь два существенных замечания. Во-первых, как было показано в [16], чтобы реализовать полноценный перколяционный кластер, к примеру, из черных кубиков с мезопорами, требуется несколько увеличить их концентрацию ω. Поднять ее от величины 0.3 (условие (5)) до концентрации порядка 0.35. Поэтому дальше будем полагать, что фактически перколяционный ионный (черный) кластер возникает при ω = 0.35.
Во-вторых, из соображений симметрии очевидно, что при ω > 0.65 в АС катода перестает существовать и полноценный перколяционный кислородный кластер из серых кубиков. И тогда нарушается подача кислорода из газодиффузионного слоя в АС катода.
Теперь можно сформулировать условия для полноценного функционирования АС катода при разряде ЛКА. Следует искать область значений параметра ω, где имеет место необходимая для полноценного осуществления в АС катода процесса разряда ЛКА реализация сразу двух перколяционных кластеров (ионного и кислородного) одновременно. Это условие выполняется только в интервале 0.35 < ω < 0.65. Так в исследуемой нами модели структуры АС слоя катода для параметра ω обозначаются три реперные точки: 0.35, 0.50 и 0.65.
РЕЗУЛЬТАТЫ КОМПЬЮТЕРНЫХ РАСЧЕТОВ
Уже простой взгляд на рис. 2а–2в показывает, насколько в них разнятся условия для проведения процесса разряда в АС катода ЛКА. При трех выбранных нами реперных концентрациях: при долях концентрации углеродных кубиков ω = 0.35, 0.50 и 0.65.
Рис. 2.
Сечение модельного куба размером 40 × 40 × 40 плоскостью, параллельной его фронтальной и тыльной поверхностям. (а) Углеродные кубики (ионный кластер) помечены черным цветом, кубики-макропоры (кислородный кластер) помечены серым цветом, концентрация черных кубиков ω = 0.35, доля кубиков-макропор – 0.65. (б) Углеродные кубики помечены черным цветом, кубики-макропоры помечены серым цветом, концентрация черных кубиков ω = 0.50, доля кубиков-макропор – 0.50. (в) Углеродные кубики помечены черным цветом, кубики-макропоры помечены серым цветом, концентрация черных кубиков ω = 0.65, доля кубиков-макропор – 0.35. Белым цветом помечены кубики, которые не входят ни в один из двух перколяционных кластеров.

Для успешного проведения процесса разряда важно иметь в катоде как можно большее число встреч-контактов макропор, поставляющих кислород (серые кубики на рис. 2а–2в), с фактически полностью, как это отмечалось выше, поставляющими ионы лития углеродными кубиками (черные кубики на рис. 2а–2в). Тут следует подчеркнуть, что при этом серые и черные контактирующие кубики должны обязательно входить в состав соответственно кислородного и ионного кластеров.
Количественные данные здесь таковы (они представлены в табл. 1). Компьютер перебирает все входящие в ионный кластер углеродные кубики и определяет, сколько контактов у каждого из них имеется с входящими в состав кислородного кластера кубиками-пустотами (эти межфазные контакты в табл. 1 обозначены как n).
Таблица 1.
Число входящих в перколяционный ионный кластер углеродных кубиков, имеющих с входящими в перколяционный кислородный кластер кубиков-макропор n межфазных контактов для трех реперных концентраций углеродных зерен в модельном кубе размером 40 × 40 × 40
| Число контактов n | |||||
|---|---|---|---|---|---|
| Доля черных кубиков ω | 1 | 2 | 3 | 4 | 5 |
| 0.35 | 575 | 2099 | 4149 | 4718 | 2404 |
| 0.50 | 4278 | 7992 | 9028 | 5888 | 1939 |
| 0.65 | 11 262 | 8524 | 4373 | 1497 | 255 |
Полезно также численные данные табл. 1 представить в виде семейства трех кривых – они показаны на рис. 3. Видно, что при увеличении в модельном кубе (рис. 1) доли углеродных кубиков ω происходит смещение максимума кривых на рис. 3 справа налево. Физически ясно, что при ω = 0.65, когда количество черных кубиков превалирует над числом кубиков-макропор, вероятность межфазоных контактов с n = 1 должна быть, очевидно, гораздо выше максимальных контактов с n = 5 (см. данные нижней строки в табл. 1).
Рис. 3.
Модельный куб размером 40 × 40 × 40. Связь числа углеродных кубиков nk с количеством межфазных контактов n с кислородным кластером. Доля углеродных кубиков в модельном кубе: 0.35 – 1; 0.50 – 2; 0.65 – 3.

Теперь решим, каким может быть в модельном кубе (рис. 1) суммарное число N встреч черных и серых кубиков. Ответ на этот вопрос дают данные рис. 4. Он демонстрирует очевидные истины. То, что максимум числа межфазных контактов N должен наблюдаться при ω = 0.50, и что относительно этой точки N, ω – кривая должна проявлять признаки симметрии. А абсолютные значения для N таковы: примерно 81 000 при ω = 0.50 и примерно по 48 000 для значений ω = 0.35 и ω = 0.65.
Рис. 4.
Зависимость полного числа межфазных контактов N в модельном кубе размером 40 × 40 × 40 АС катода с двумя типами пор от доли углеродных зерен ω.

Итак, казалось бы, предпочтительными для проведения разряда в ЛКА являются катоды с ω = = 0.50, в которых объемные концентрации двух компонентов равны. Но не будем спешить с окончательными выводами.
Разобьем теперь углеродные кубики (они помечены на рис. 2а–2в черным цветом) на два класса: те, которые со всех 6-ти сторон-граней окружены черными же кубиками и всеми остальными черными кубиками, которые не обладают этим свойством. Будем считать, что первые кубики – это кубики типа 1, все другие – кубики типа 2.
В табл. 2 для трех реперных значений доли углеродных кубиков в АС катода ω проведен подсчет кубиков типа 1 и типа 2. Очевидно, что в проводимость ионного кластера львиную долю должны вносить именно кубики типа 1. Поэтому даже без расчетов ясно, что приведенная удельная проводимость ионного кластера при переходе от рис. 2а к рис. 2в должна значительно возрастать.
Таблица 2.
Число “изолированных” (тип 1) и имеющих межфазные контакты (тип 2) входящих в перколяционный ионный кластер углеродных кубиков для трех концентраций углеродных кубиков в АС катода ω
| Куб = 40 × 40 × 40 = 64 000 | ||
|---|---|---|
| ω | N (тип 1) | N (тип 2) |
| 0.35 | 58 | 13 945 |
| 0.50 | 1163 | 29 125 |
| 0.65 | 14 681 | 25 911 |
Нами проведены также расчеты эффективной приведенной удельной проводимости для ионных кластеров, представленных на рис. 2а–2в. Их результаты представлены в табл. 3.
Таблица 3.
Зависимость эффективной приведенной удельной проводимости ионного кластера Σ от концентрации углеродных кубиков ω. Проводимость исходного углеродного кубика σ1 = 1, приведенная проводимость кубика после проведения разряда σ2
| σ1 | ω | σ2 | Σ |
|---|---|---|---|
| 1 | 0.35 | 1 | 0.0058 |
| 0.75 | 0.0044 | ||
| 0.5 | 0.0029 | ||
| 0.25 | 0.0011 | ||
| 0.1 | 0.00056 | ||
| 0.001 | 0.0000055 | ||
| 0.50 | 1 | 0.1266 | |
| 0.75 | 0.0694 | ||
| 0.5 | 0.0508 | ||
| 0.25 | 0.0241 | ||
| 0.1 | 0.0091 | ||
| 0.001 | 0.00008 | ||
| 0.65 | 1 | 0.2942 | |
| 0.75 | 0.2319 | ||
| 0.5 | 0.1643 | ||
| 0.25 | 0.0901 | ||
| 0.1 | 0.0431 | ||
| 0.001 | 0.0036 |
Будем различать в модельном кубе (рис. 1) приведенную удельную ионную проводимость углеродных кубиков, если в их порах не содержится пероксида лития, тут σ1 = 1 (первый столбец в табл. 3), от проводимости углеродных кубиков, содержащих в своих порах пероксид лития (данные третьего столбца в табл. 3), здесь σ2 < σ1.
Нам точно неизвестно, как после окончания очередного процесса разряда, выглядит точное распределение пероксида лития по углеродным кубикам в ионном кластере, ибо процесс образования пероксида лития может охватывать сразу несколько кубиков и также может зависеть от числа контактов углеродного кубика с кубиками-макропорами. Поэтому естественно предположить самое простое, это мы и будем дальше делать, что основная масса пероксида лития может быть более или менее равномерно распределена в углеродных кубиках.
Тогда возникает задача о расчете эффективной приведенной удельной ионной проводимости Σ в зависимости от величины ω (второй столбец в табл. 3) и от значения параметра σ2 уже в трехкомпонентной системе кубиков (третий столбец в табл. 3). В модельном кубе все кубики-макропоры при этом будут иметь нулевую приведенную удельную проводимость, ибо мы фактически исключили (об этом говорилось выше) поступление ионов лития из макропор в мезопоры. А углеродные кубики типа 1 будут иметь проводимость σ1 = 1, углеродные кубики типа 2 – проводимость σ2. Результаты расчетов эффективной удельной проводимости ионного кластера представлены и на рис. 5.
Рис. 5.
Зависимость эффективной приведенной удельной проводимости ионного кластера Σ от величины параметра σ2; доля углеродных зерен ω: 0.35 – 1; 0.50 – 2; 0.65 – 3.

Несколько пояснений о методике расчетов эффективной удельной проводимости ионного кластера Σ в трехкомпонентном модельном кубе. Вначале, как это делалось выше, определяется доля серых кубиков, входящих в состав кислородного кластера. В нем все серые кубики имеют нулевую проводимость. Затем подсчитываются доли черных кубиков, входящих в ионный кластер типа 1 с проводимостью σ1 и доля кубиков типа 2 с проводимостью σ2. Все эти кубики перемешаны случайным образом. Методика и особенности проведенных расчетов величины Σ (ω, σ1 или σ2) изложены в приложении.
Данные табл. 2, 3 и рис. 5 свидетельствуют о том, что характер перколяционного ионного кластера (пропорции долей в нем черных зерен типа 1 и типа 2) должен оказывать решающее влияние на величину удельной емкости С, Кл/см2 катода, при разряде. Рост концентрации черных зерен типа 2 в АС катода ЛКА (эффект “засорения” мезопор пероксидом лития) резко снижает величину эффективной приведенной проводимости Σ, что при заданной постоянной плотности тока приводит и к значительному увеличению потенциала при заряжении ЛКА.
Далее становится очевидным (данные 4-го столбца в табл. 3), что активный слой катода фактически не способен функционировать не только при доле углеродных зерен ω = 0.35, но даже и при ω = = 0.5, когда число контактов N кубиков кислородного и ионного кластеров достигает максимума (данные рис. 4). Функционирование АС катода идет более или менее нормально лишь в области, лежащей в интервале 0.50 < ω < 0.65. Но даже здесь на получение высоких габаритных характеристик катода при проведении разрядов ЛКА рассчитывать не приходится по ряду следующих причин.
Во-первых, коэффициент диффузии кислорода в апротонных растворителях очень мал, порядка 10–6–10–5 см2/с. К тому же проникновение кислорода в АС катода идет по макропорам перколяционного кислородного кластера. Ввиду этого, как показывают численные оценки, величина эффективного коэффициента диффузии оказывается еще примерно на порядок ниже, до возможной величины 10–7 см2/с.
Во-вторых, процесс образования пероксида лития в АС катода совершается в той области значений параметра ω, в которой число контактов N частиц кислородного и ионного кластеров уже значительно снижено, см. данные рис. 4.
В-третьих, становится очевидным, что, скажем, при естественном стремлении увеличить параметр ω от 0.65 до 0.5, в этом случае будет возрастать N, число контактов зерен двух типов, наблюдается значительное ослабление функционирования поставляющего ионы кластера (данные табл. 3) из-за возможности образования в углеродных кубиках пероксида лития. Это приводит к тому, что эффективная приведенная удельная проводимость АС катода Σ в обсуждаемой нами области концентраций ω может снижаться, достигая лишь десятых долей и менее (данные рис. 5).
Ввиду всего только что сказанного ясно, что в этих условиях величина удельной емкости катода при разряде не может быть большой, а потенциал при заряжении становится непомерно высоким.
Отметим еще, что снижение емкости катода, о которой мы говорим, сродни тому, что обычно экспериментально наблюдается при увеличении толщины АС катода. К примеру, в работе [17] было показано, что при увеличении толщины активного слоя катода в ряду 19.7, 65.5, 219.2 мкм регистрируемая емкость образовала убывающую последовательность значений – 2550, 1580, 350 мА ч/г.
Объяснение подобного рода фактов достаточно простое. Область, где реально происходит образование Li2O2, довольно узка, она примыкает к плоскости, отделяющей область, откуда поступает кислород (ГДС), от АС катода. При одной и той же заданной плотности тока с ростом толщины АС катода доставка ионов лития к этому тонкому слою, где совершается образование пероксида лития, естественно, все более и более затрудняется. Ионам лития приходится двигаться теперь не только в межэлектродном пространстве, но частично дополнительно также и по мелким порам АС катода (по мезопорам), к тому же частично “засоренным” нерастворимым в электролите Li2O2. Это и приводит в итоге к снижению поступления ионов лития в той области АС катода, в которой в основном и происходит образование Li2O2.
Обычно принято считать при проведении теоретических расчетов габаритных характеристик ЛКА при разряде, что концентрация ионов лития в порах достаточно велика. И что определяющей процесс разряда катода величиной является лишь концентрация кислорода, поток которого обеспечивает на стенках пор образование супероксида аниона ${\text{О}}_{2}^{ - }$ (см. формулу (1)). Слов нет, этот процесс крайне важен, но если поступление ионов лития снижается, то не может не возникнуть больших затруднений со второй стадией процесса (1) – реакцией ${\text{О}}_{2}^{ - }$ + Li+ → LiO2. И дальше с последующим образованием пероксида лития 2LiO2 → Li2O2 + O2. Поэтому-то с ростом толщины АС катода, когда поступление ионов лития к области, где совершается процесс образования пероксида лития, начинает слабеть, и наблюдается уменьшение емкости катода.
Ввиду всего только что сказанного становится понятным, что наблюдать то же снижение емкости катода при разряде можно не только при увеличении толщины АС катода, но даже при одной и той же фиксированной толщине АС катода, если намеренно начать постепенно уменьшать эффективную приведенную удельную проводимость ионов лития. Таким образом, следует констатировать, что образование в мезопорах АС катода ЛКА пероксида лития ухудшает не только поступление молекул кислорода в мезопоры из кислородного кластера, но одновременно и поступление ионов лития из ионного кластера. Все это вместе не может не сказаться отрицательно на величинах габаритных характеристик ЛКА при процессах разряда и заряжения.
ЗАКЛЮЧЕНИЕ
В структуре АС катода ЛКА имеет смысл выделить пять основополагающих элементов. Это макропоры, которые в силу своего значительного размера практически не “зарастают” нерастворимым в электролите пероксидом лития. Это мезопоры, в которых совершается сложный процесс образования пероксида лития. Это те локусы структуры АС, где кислород из макропор поступает в мезопоры. А также в АС катода ЛКА должны существовать два перколяционных кластера – “кислородный кластер”, состоящий из макропор, и “ионный кластер”, фактически сложенный в основном из мезопор.
Роль кислородного кластера – гарантировать непрерывную подачу молекул кислорода из ГДС в мезопоры, роль ионного кластера – обеспечивать также непрерывную поставку в мезопоры ионов лития из межэлектродного пространства ЛКА. Для успешной работы катода необходимо совместное слаженное функционирование этих двух перколяционных кластеров. Кислородный кластер определяет величину эффективного коэффициента диффузии молекул кислорода в АС катода, ионный кластер обязан создать приемлемую величину эффективной проводимости электролита в АС катода.
Путем подбора типа апротонного растворителя с растворенными в нем солями лития, можно добиться некоторого улучшения величин параметров процессов разряда и заряжения. Увеличения растворимости кислорода в электролите и коэффициента диффузии кислорода, а также проводимости ионов лития в электролите. Однако этим путем все же трудно надеяться получить значительно более высокие габаритные характеристики ЛКА.
Казалось бы, большего успеха тут можно добиться, одновременно улучшая характеристики двух перколяционных кластеров – кислородного и ионного. Ведь тем самым можно существенно увеличить потоки кислорода и ионов лития в АС катода, а также значительно развить суммарное число контактов макропор с мезопорами, где в основном и идет наработка пероксида лития.
Проведенное в данной статье компьютерное моделирование структуры и механизма функционирования АС катода ЛКА убедительно показало, что принципиально невозможно одновременно стремиться к улучшению характеристик сразу двух перколяционных кластеров. Совершенствуя кислородный кластер, мы одновременно ухудшаем характеристики кластера ионного, и наоборот, улучшая ионный кластер, затрудняем процесс подачи молекул кислорода в катод.
Причина в том, что объем АС катода конечен и на 100% заполнен структурными элементами двух типов: макропорами и материалом, в котором имеются мезопоры. И если мы, допустим, увеличим концентрацию макропор, то характеристики кислородного кластера могут улучшиться, но при этом автоматически уменьшится доля объема АС катода, приходящаяся на материал с мезопорами. И, естественно, характеристики ионного кластера при этом станут гораздо хуже.
При принятых ныне попытках конструирования оптимальной структуры АС катода ЛКА из компонентов той или иной природы (создание всех вышеперечисленных пяти основополагающих элементов в АС катода ЛКА) надеяться на значительное улучшение характеристик катода ЛКА при его разряде и последующем заряжении, видимо, не приходится. При этом стоит еще раз подчеркнуть принципиальный момент – трудности оптимизации структуры АС носят не внешний, привнесенный извне, а сугубо органичный, присущий самой пористой структуре АС катода ЛКА характер и в рамках принятой ныне практики формирования пористой структуры АС катода не могут быть преодолены.
Чтобы устранить многие присущие пока недостатки (они были перечислены в первом разделе этой статьи) в работе катода при разряде и последующем заряжении ЛКА, на наш взгляд, необходимо вести поиск таких новых пористых структур АС катода, в которых каналы подачи кислорода и ионов лития были бы взаимно независимы. Только в этом случае можно одновременно порознь совершенствовать условия функционирования сразу двух каналов и добиваться улучшения габаритных характеристик ЛКА.
И последнее, что стоит отметить особо. При теоретическом описании хода процессов, совершающихся при разряде ЛКА, обычно во внимание принимается лишь расход поступающих в мезопоры из макропор молекул кислорода. И при этом молчаливо предполагается, что концентрация ионов лития в мезопорах всегда достаточна для полноценного осуществления процесса восстановления кислорода. В данном же исследовании показано обратное. Оказывается, именно подача ионов лития по ионному кластеру в АС катода играет при проведении процесса разряда, да и при последующем процессе заряжения, решающую роль. Этот процесс также не дает возможности получать высокие характеристики ЛКА.
Список литературы
Christensen, J., A critical review of Li/air batteries / Jake Christensen, J. Electrochem. Soc., 2012, vol. 159(2), p. R1.
Luntz, Alan, C., Nonaqueous Li-air batteries: a status report / A.C. Luntz, B.D. McCloskey // Chemical Reviews, 2014. vol. 114(23). p. 11721.
Nobuyki, Imanishi, The Lithium Air Battery: Fundamentals / N. Imanishi, [etc] // Springer, Berlin, 2014.
Tran, C., Yang, X.-Q., and Qu, D., Investigation of the gas-diffusion-electrode used as lithium/air cathode in non-aqueous electrolyte and the importance of carbon material porosity, J. Power Sources, 2010, vol. 195(7), p. 2057.
Yang, X.-h., He, P., and Xia, Y.-y., Preparation of mesocellular carbon foam and its application for Lithium/Air Battery, Electrochemistry Communications, 2009, vol. 11(6), p. 1127.
Laoire, C.O., Mukerjee, S., Abraham, K.M., Plichta E.J., and Hendrickson, M.A., Elucidating the mechanism of oxygen reduction for lithium-air battery applications, J. Physical Chemistry C, 2009, vol. 113(46), p. 20127.
Laoire, C.O., Influence of nonaqueous solvents on the electrochemistry of oxygen in the rechargeable lithium-air, J. Physical Chemistry C, 2010, vol. 114(19), p. 9178.
Ma, Z., Yuan, X., Li, L., Ma, Z-F., Wilkinson, D.P., Zhang L., and Zhang J., A review of cathode materials and structures for rechargeable lithium-air batteries, Energy Environ. Sci., 2015, vol. 8, p. 2144.
Тарасевич, М.Р., Андреев, В.Н., Корчагин, О.В., Трипачев, О.В. Литий-кислородные (воздушные) источники тока (современное состояние и перспективы). Физикохимия поверхности и защита материалов. 2017. Т. 53. № 1. С. 3.
Bao, J., Hu, W., Bhattacharya, P., Stewart, M., Zhang, J.-G., and Pan, W., Discharge performance of Li–O2 batteries using a multiscale modeling approach, J. Physical Chemistry C., 2015, vol. 119(27), p. 14851.
Pan, W., Yang, X., Bao, J., and Wang, M., Optimizing discharge capacity of Li–O2 Batteries dy design of air-electrode porous structure: Multifidelity modeling and optimization, J. Electrochemical Society, 2017, vol. 164(11), p. E3499.
Богдановская, В.А., Андреев, В.Н., Чирков, Ю.Г., Ростокин, В.И., Емец, В.В., Корчагин, О.В., Трипачев, О.В. Влияние структуры положительного электрода на процесс разряда литий-кислородного (воздушного) источника тока. Теория монопористого катода. Физикохимия поверхности и защита материалов. 2018. № 6. С. 549.
Чирков, Ю.Г., Андреев, В.Н., Ростокин, В.И., Богдановская, В.А. Разряд литий-кислородного источника тока: теория монопористого катода, роль константы процесса расхода кислорода. Альтернативная энергетика и экология. 2018. № 4–6. С. 95.
Тарасевич, Ю.Ю. Перколяция: теория, приложения, алгоритмы. М.: Эдиториал УРСС. 2011. 112 с.
Чирков, Ю.Г. Теория пористых электродов: перколяция, расчет линий перколяции. Электрохимия. 1999. Т. 35. С. 1449. [Chirkov, Yu.G., Russ. J. Electrochem., 1999, vol. 35, p. 1281.]
Чирков, Ю.Г., Ростокин, В.И., Скундин, А.М. Компьютерное моделирование работы положительного электрода литий-ионного аккумулятора: модель равновеликих зерен, перколяционные расчеты. Электрохимия. 2011. Т. 47(1). С. 77. [Chirkov, Yu.G., Rostokin, V.I., and Skundin, A.M., Russ. J. Electrochem., 2011, vol. 47, p. 71.]
Zhang, G.Q., Zheng, J.P., Liang, R., Zhang, C., Wang, B., Hendrickson M., and Plichta, E. J., Lithium–Air Batteries Using SWNT/CNF Buckypapers as Air Electrodes, J. Electrochem. Soc., 2010, vol. 157, p. A953.
Kirkpatrick, S., Percolation and Conduction, Rev. Mod. Phys., 1973, vol. 45, p. 574.
Stauffer, D., Scaling theory of percolation clusters, Phys. Reports, 1979, vol. 54, p. 1.
Дополнительные материалы отсутствуют.


