Электрохимия, 2020, T. 56, № 6, стр. 511-519
Импрегнация кислородного электрода Pt|YSZ микроколичествами оксида празеодима
А. И. Коврова a, *, В. П. Горелов a, Д. А. Осинкин a
a Институт высокотемпературной электрохимии УрО РАН
620137 Екатеринбург, ул. Академическая, 20, Россия
* E-mail: kovrova@ihte.uran.ru
Поступила в редакцию 24.01.2019
После доработки 24.07.2019
Принята к публикации 08.10.2019
Аннотация
Методом импеданса в атмосфере воздуха в интервале температур 500–700°С на ячейках Pt|YSZ|Pt изучено поведение поляризационной проводимости пористых платиновых электродов, импрегнированных микроколичествами оксида празеодима PrOx (от 0.1 до 1 × 10–4 мг/см2) путем пропитки спиртовыми растворами нитрата празеодима. После пропитки образцы прокаливали при 850°С в режиме медленного нагрева (50°С/ч), при котором на поверхности электролита образуется нанопленка оксида празеодима. Обнаружено, что введение PrOx даже в количестве 10–4 мг/см2 существенно увеличивает поляризационную проводимость электрода. Проведен анализ спектров электрохимического импеданса методом распределения времен релаксации (метод DRT), который выявил смену скорость-определяющей стадии электродного процесса в диапазоне концентраций оксида празеодима 1 × 10–3–3.3 × 10–3 мг/см2. Исследованные электроды обсуждены с точки зрения островковой модели плотных оксидных PrOx-электродов, в которых платина играет роль коллектора.
ВВЕДЕНИЕ
В области разработок твердооксидных топливных элементов (ТОТЭ) отчетливо выражен тренд на снижение рабочих температур до 700–500°С. Снижение температуры позволит применять недорогие конструкционные материалы, увеличить срок службы вследствие снижения деградационных процессов, упростить конструкцию. Для достижения этой цели кроме применения пленочных твердых электролитов требуются высокоэффективные электроды. В этом направлении перспективными являются методы увеличения электрохимической активности электродов путем пропитки (инфильтрации, импрегнации) пористого субстрата термически нестойкими солями соответствующих элементов с последующей термообработкой, что приводит к образованию наноструктурированных электродов с развитой трехфазной границей [1–6]. В этом отношении соединения на основе празеодима представляют несомненный интерес и они достаточно давно исследуются как импрегнирующие добавки для повышения производительности ТОТЭ. При этом в ряде работ [7–9] было экспериментально показано, что импрегнация катода ТОТЭ позволяет в несколько раз снизить интерфейсное сопротивление топливного элемента. Однако физико-химические механизмы такого улучшения транспортных характеристик интерфейса до сих пор не имеют однозначной интерпретации.
Ранее, при изучении пористых платиновых электродов в ячейке Pt|YSZ|Pt (где YSZ – твердый электролит состава ZrO2 + 10 мол. % Y2O3), пропитанных малыми количествами нитрата празеодима (концентрация PrOx ∼ 0.1 мг/см2) с последующей прокалкой при 850°С, нами было обнаружено [10, 11], что в случае образования порошковой формы PrOx импрегнация слабо влияет на поляризационные характеристики электрода. В случае же образования пленки PrOx при тех же его концентрациях наблюдалось резкое увеличение поляризационной проводимости на несколько порядков величины, которая при повторных пропитках не менялась. Нами была предложена концепция работы такого электрода, суть которой состоит в том, что наличие на поверхности электролита нанопленки со смешанной ионно-электронной проводимостью приводит к расширению зоны электродной реакции на всю площадь электролита. В этом случае реализуется модель плотного оксидного электрода со смешанной ионно-электронной проводимостью. Электродная реакция протекает на поверхности пленки, т.е. на двухфазной границе, а пористая платина играет роль токового коллектора [11, 12].
Модель плотного оксидного электрода была подтверждена исследованиями пористого платинового электрода Pt|YSZ, импрегнированного пленками различных оксидов (СеО2 – х, PrОх, TbОх и Ce2Tb4О11 – х), обладающих электронно-ионной проводимостью. Исследование показало: поляризационная проводимость ση таких электродов коррелирует с амбиполярной проводимостью пленок [12].
Однако остался открытым вопрос, как будет изменяться поляризационная проводимость электрода Pt|YSZ при уменьшении количества импрегнированных оксидов вплоть до величин, при которых пленка должна становиться атомарной. Изучение этого вопроса важно для более глубокого понимания процессов, происходящих в электродных системах с импрегнированной оксидной пленкой.
Цель работы: изучить влияние микроколичеств оксида празеодима (от 0.1 до 1 × 10–4 мг/см2), импрегнированного в электроды ячейки Pt|YSZ|Pt в режиме образования пленки, на поляризационную проводимость электродов в атмосфере воздуха.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Тонкие пластинки электролита YSZ толщиной 0.5 мм, диаметром 8 мм и плотностью выше 95% были вырезаны из мембран для топливных элементов, как и в предыдущих работах [10–12]. Мембраны были изготовлены методом горячего литья под давлением [13].
Электроды из платины наносили методом окрашивания, используя крупнодисперсный порошок чистой платины. Грубодисперсный порошок применяли для того, чтобы поляризационное сопротивление электрода было большим и влияние оксида празеодима проявлялось бы более заметно. Электроды наносили на обе стороны пластинок YSZ и припекали на воздухе при температуре 1100°С (1 ч). Нанесение и припекание электродов проводили дважды, удельная масса нанесенной платины составила около 15 мг/см2. Такие электроды можно рассматривать как модельные с малой протяженностью трехфазной границы.
Импрегнирование электродов производили, вводя в них капельно известный объем спиртовых титрованных растворов нитрата празеодима. Для пропитки использовали набор растворов различной концентрации. Концентрация исходного раствора составляла около 1.5 мас. % (в пересчете на PrOх), далее раствор разбавляли в 3, 10, 30, 100 и 1000 раз. Соответственно, количество вводимого оксида празеодима уменьшалось пропорционально разбавлению. Содержание основного катиона в прекурсоре было не ниже 99.9%. Термообработка образцов проводилась в режиме медленного нагрева (50°С/ч) на воздухе до 500°С, затем со скоростью 200°С/ч до температуры 850°С (выдержка 1 ч). В этом режиме образуется пленка PrOх, как было установлено ранее в экспериментах по нанесению пленок на чистую подложку YSZ без электрода [10, 11, 14].
Растровая электронная микроскопия (РЭМ) выполнена на микроскопе JSM 5900LV (Япония).
Импеданс-спектроскопические измерения выполнены с использованием импедансметра PARSTAT 2273 (США) в области частот 0.1 Гц–1 МГц при амплитуде сигнала 30 мВ. Измерения проводили в окислительной (воздух) атмосфере в интервале температур 700–500°C. Спектры электрохимического импеданса симметричных ячеек были обработаны при помощи расчета функции распределения времен релаксации (метод DRT) в программном пакете, разработанном авторами [15] на основе метода регуляризации Тихонова [16].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Аттестация образцов
По данным РЭМ, платиновый электрод представлял собой спекшийся конгломерат преимущественно плоских частиц неправильной формы размером от 10 до 60 мкм, между которыми видна свободная поверхность YSZ-электролита (рис. 1). Плоская форма частиц образовалась из-за растирания Pt-порошка в ступке со спиртом. Средняя толщина электрода около 100 мкм. Если учесть, что концентрация платины на поверхности электролита составляет около 15 мг/см2, то пористость электрода равна ≈90%. Состав электролита по данным микрорентгеновского спектрального анализа: Zr (87.5 ат. %); Y (10.5 ± 0.5 ат. %); Hf (1.0 ат. %); Al (1.0 ат. %).
Спектры импеданса ячеек Pt|YSZ|Pt
Спектры импеданса симметричных ячеек Pt|YSZ|Pt с импрегнированными электродами имели вид асимметричных полукругов (рис. 2). Аналогичные спектры импеданса при 600°С на воздухе приведены в работе [17] для пленочного электрода Pr0.1Ce0.9O2 – δ толщиной около 260 нм, нанесенного на электролит YSZ, и пленок PrOx.
Рис. 2.
Импеданс-спектры ячеек Pt|YSZ|Pt (воздух, 600°С) при различных содержаниях PrOx в электродах (мг/см2): 1 – без PrOx; 2 – 1 × 10–4; 3 – 1 × 10–3; 4 – 3.3 × 10–3; 5 – 1 × 10–2; 6 – 3.3 × 10–2: 7 – 0.1. Для электрода без оксида празеодима видна только высокочастотная часть годографа.

Отрезок на действительной оси, заключенный внутри полуокружности, рассматривался как поляризационное сопротивление Rη, которое уменьшалось с увеличением концентрации оксида празеодима.
Отрезки от начала координат до пересечения с левой частью полуокружности на спектре соответствуют омическому сопротивлению YSZ-электролита. Величины этих сопротивлений различаются для разных образцов (рис. 2, врезка), хотя геометрические размеры ячеек были одинаковы (по данным четырехзондового метода сопротивление данного электролита при 600°С должно быть около 25 Ом). Наибольшее омическое сопротивление наблюдалось для образца без оксида празеодима. Введение оксида празеодима резко снижает это сопротивление, но величины этих сопротивлений с количеством PrOх не коррелируют. Вероятно, в этом разбросе проявляется эффект растекания тока, обусловленный неравномерным распределением грубодисперсного платинового порошка на поверхности электролита, что изменяет реальное l/s образца. Сопротивления электролита YSZ малы по сравнению с поляризационным сопротивлением электродов, и этот разброс не оказывает существенного влияния на измеряемое Rη.
Поляризационная проводимость Pt-электрода
Температурные зависимости поляризационной проводимости ση = 1/Rη исследованных платиновых электродов в координатах Аррениуса могут быть аппроксимированы прямыми линиями (рис. 3). Поляризационная проводимость ση платинового электрода без оксида празеодима самая низкая (рис. 3, прямая 1) и имеет энергию активации Eη = 1.66 ± 0.02 эВ, что хорошо согласуется с величиной 1.7 эВ, приведенной в [18] для Pt|YSZ-электрода.
Рис. 3.
Температурные зависимости поляризационной проводимости платинового электрода ячейки Pt|YSZ|Pt в зависимости от содержания PrOx (мг/см2): 1 – без PrOx; 2 – 1 × 10–4; 3 – 1 × 10–3; 4 – 3.3 × 10–3; 5 – 1 × 10–2; 6 – 3.3 × 10–2: 7 – 0.1.
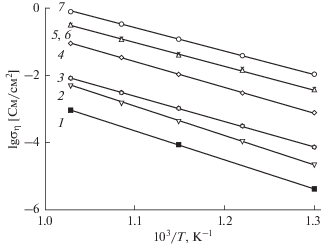
Как говорилось выше, введение в платиновый электрод PrOх в количестве 0.1 мг/см2 не оказывает существенного влияния на поляризационную проводимость, если пленка оксида празеодима на поверхности электролита не образуется. Но поляризационная проводимость резко увеличивается на несколько порядков при том же количестве PrOх, если пленка образуется [11]. Настоящее исследование показало, что введение в электрод даже в 1000 раз меньшего количества PrOх (1 × 10–4 мг/см2) в режиме образования пленки приводит к существенному возрастанию поляризационной проводимости ση (рис. 3, прямая 2). Дальнейшее увеличение PrOх в электроде от 0.001 до 0.1 мг/см2 (рис. 3, прямые 3–7) ведет к дальнейшему пропорциональному увеличению поляризационной проводимости (рис. 4). При этом энергия активации Eη ≈ 1.5 эВ сохраняется практически неизменной.
Рис. 4.
Зависимость поляризационной проводимости Pt-электрода ячейки Pt|YSZ|Pt от содержания PrOx (мг/см2) при 600°C в атмосфере воздуха при естественной влажности.

Величина поляризационной проводимости ση при концентрации PrOх 0.1 мг/см2 является максимальной, и две дополнительные импрегнации в количестве 0.1 мг/см2 каждая не меняют характеристики электрода [11]. Из этого факта следуют два вывода: 1) импрегнация электрода оксидом празеодима в количестве 0.1 мг/см2 приводит к образованию пленки, которая полностью покрывает всю свободную поверхность YSZ, поэтому последующие пропитки не меняют ситуацию; 2) так как увеличение толщины пленки PrOx не влияет на характеристики электрода, это означает, что основная электродная реакция идет на поверхности пленки. В работе [19] методом импеданса в интервале температур 550–700°С изучены катоды в виде пленок PrOx, изготовленные магнетронным напылением на монокристаллическом твердом электролите 10YSZ, и авторы считают лимитирующей стадией электродного процесса реакцию перехода заряда на поверхности пленки PrOx.
Оценить толщины нанопленок оксида празеодима методом РЭМ проблематично, в частности вследствие их эпитаксиального осаждения на поверхности твердого электролита (YSZ и PrOx имеют одинаковые структуры типа флюорита). Но нас интересует число слоев оксида празеодима на электролите YSZ, а для этого эффективные толщины пленок можно грубо оценить, зная, что при содержании PrOx, равном 0.1 мг/см2, вся поверхность электролита покрыта пленкой. Так как поверхность YSZ смачивается раствором нитрата празеодима под электродом, то с учетом данных [14] по получению пленки PrOx методом окунания (deep-coating), толщина пленки на поверхности YSZ при данной концентрации раствора не может быть меньше 40 нм. Другими словами, если YSZ смочен таким раствором, то пленка на нем не может быть меньше этой толщины. Это нижняя граница толщины пленки. Верхнюю границу 140 нм получим в предположении, что в электроде весь PrOx осел на поверхности электролита (при плотности PrOx, равной 6.8 г/см3). Даже свежепрокаленная металлическая платина очень плохо смачивается спиртовым раствором, но можно считать, что не менее половины оксида празеодима осядет на ней, тогда эффективная толщина пленки PrOx будет около 70 нм. Подчеркнем, что это именно эффективная толщина, так как поверхность электролита отнюдь не атомно-гладкая.
Параметр кубической решетки типа флюорита для пленки PrOx равен приблизительно 0.548 нм (совпадает с параметром керамики) [14], следовательно, расстояние между слоями ионов празеодима ≈0.274 нм и количество слоев для пленки толщиной 70 нм будет около 250. При разбавлении импрегнирующего раствора число атомных слоев пленки PrOx будет уменьшаться в соответствующее число раз, а при разбавлении в 1000 раз на поверхности электролита не сможет образоваться даже одного атомного слоя PrOx.
Анализ спектров импеданса методом функций DRT
Результаты анализа спектров электрохимического импеданса методом распределения времен релаксации (метод DRT) в виде нормированных на единицу функций DRT показали наличие одного максимально выраженного пика в области 1–6 Гц (рис. 5). Поэтому можно однозначно заключить, что стадия перехода заряда не является скорость-определяющей в электродной реакции электровосстановления кислорода в Pt|YSZ-системе, и это хорошо коррелирует с общими представлениями о природе электродных процессов в данных системах в атмосфере воздуха [20, 21].
Рис. 5.
Нормированные на единицу, частотные зависимости функции распределения времен релаксации при различных содержаниях PrOx в электродах (мг/см2): 1 – без PrOx; 2 – 1 × 10–4; 3 – 1 × 10–3; 4 – 3.3 ×10–3; 5 – 1 × 10–2; 6 – 3.3 × 10–2: 7 – 0.1.
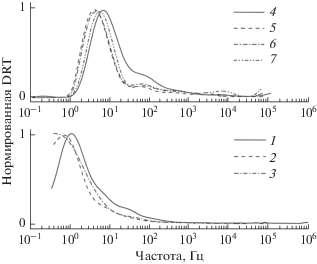
При введении даже самых малых концентраций оксида празеодима (1 × 10–4 и 1 × 10–3 мг/см2) омическое сопротивление ячейки заметно уменьшается (врезка на рис. 2, зависимости 1–3) с одновременным увеличением поляризационной проводимости электрода (рис. 3). При этом не наблюдается существенного изменения вида функции DRT (рис. 5), что говорит о неизменности природы скорость-определяющей стадии электровосстановления кислорода в этом интервале добавок PrOx.
Однако дальнейшее увеличение концентрации оксида празеодима до 3.3 × 10–3 мг/см2 ведет к резкому изменению вида функции DRT: наблюдается скачкообразное смещение главного пика на DRT кривой с 1 до ≈6 Гц, что говорит о резком изменении природы скорость-определяющей стадии электровосстановления кислорода. Последующее увеличение содержания оксида празеодима до 0.1 мг/см2 не изменяет существенно вида функции DRT (рис. 5).
Обсуждение результатов
Электролит YSZ обладает некоторой долей дырочной проводимости в окислительных условиях, поэтому на его поверхности возможно протекание электрохимической реакции электровосстановления кислорода с участием дырок, что впервые было показано Глумовым [22]. Лимитирующей стадией в этом случае является диффузия дырок в электролите, т.е. стадия перехода заряда не ограничивает электродный процесс, что хорошо коррелирует с нашими данными. Из-за крайне малой концентрации дырок в YSZ-электролите подобный механизм реакции проявляется только в случае модельных электродов с неразвитой трехфазной границей, как это реализуется в нашей работе. Совпадение энергий активации поляризационной проводимости электрода Pt|YSZ в нашей работе (1.66 ± 0.02 эВ) с энергией активации обмена кислорода YSZ-электролита с кислородом газовой фазы, измеренной методом изотопного обмена (1.67 эВ) [23], является дополнительным подтверждением гипотезы протекания электрохимической реакции на поверхности YSZ-электролита. Тогда можно предположить, что именно этот процесс регистрируется на спектре импеданса при низких частотах и как низкочастотный пик на DRT-кривой (рис. 5, кривая 1). На DRT-кривой присутствует также отклик от релаксационного процесса в области 40 Гц. Исходя из общих соображений, можно предположить, что данный процесс соответствует адсорбции кислорода.
Так как электрохимические характеристики электрода Pt|YSZ изменяются только при уменьшении содержания PrOx ниже 0.1 мг/см2, то можно сделать вывод, что при этом происходят изменения в структуре пленки.
Вначале рассмотрим модель электрода в предположении, что пленка оксида празеодима покрывает всю поверхность электролита, но при уменьшении содержания PrOx ниже 0.1 мг/см2 делается тоньше, и вследствие этого затрудняется диффузия электронных носителей вдоль пленки. Однако это предположение противоречит эксперименту, так как экстраполяция на реальную ось частей спектра, кажущихся линейными, идет в отрицательные значения, указывая на то, что это не импеданс Warburg или Gerischer. Отсюда следует, что при концентрации PrOx ниже 0.1 мг/см2 пленка оксида празеодима не делается тоньше, а покрывает не всю поверхность электролита. А так как основная электродная реакция протекает на поверхности пленки, это ведет к понижению поляризационной проводимости, пропорциональному уменьшению ее площади. Это согласуется с экспериментальными данными по пропорциональной зависимости ση от концентрации PrOx (рис. 4) при сохранении величины энергии активации.
Причина, по которой пленка занимает только часть поверхности электролита при уменьшении концентрации PrOх ниже 0.1 мг/см2, обусловлена процессом кристаллизации нитрата празеодима из импрегнированного спиртового раствора. Процесс этот довольно очевиден. Ясно, что для кристаллизации нужны центры, такими центрами являются частицы платины, и в первую очередь кристаллизация при испарении спирта из раствора будет происходить вокруг частиц платины. Закристаллизовавшийся нитрат празеодима Pr(NO3)3 ⋅ 6H2O при 73°С расплавится в кристаллизационной воде [11] и за счет смачивания растечется по электролиту на некоторое расстояние вокруг частиц платины. При дальнейшем медленном нагреве нитрат разложится, образовав вокруг платиновых частиц островки пленки PrOх. Площадь этих островков будет увеличиваться с увеличением концентрации PrOх, пока они не сомкнутся. Конечно, кристаллизация будет происходить и на других центрах, кроме платины, но если эти другие островки изолированы от платины, которая играет роль коллектора тока, то на электродный процесс они влиять не будут. На основе результатов DRT-анализа (сохранение вида функции DRT) можно считать, что предлагаемая островковая модель выполняется в диапазоне концентраций PrOх от 0.1 до 3.3 × 10–3 мг/см2.
Что касается электродов с концентрациями оксида празеодима ниже 3.3 × 10–3 мг/см2 (1 × 10–4 и 1 × 10–3 мг/см2), формально имеющих 0.25 и 2.5 атомных слоев PrOх, то совершенно очевидно, что при термической обработке такие малые количества PrOх растворяются в электролите YSZ, не создавая на его поверхности пленку. (Растворение можно видеть на простых опытах. Нагрев белой пластинки YSZ, cмоченной раствором нитрата празеодима и прокаленной при 850°С, приводит к образованию неудаляемого коричневого пятна на пластинке. Удалить его можно только шлифовкой.) Поэтому эти электроды имеют такие же функции DRT, как и электрод без оксида празеодима, что указывает на неизменность скорость-определяющих стадий электродного процесса при введении малых добавок PrOx.
Но вид DRT скачком меняется при введении большего количестве PrOx до 3.3 × 10–3 мг/см2 (рис. 5). Это означает, что появились и заработали другие скорость-определяющие стадии. И мы это связываем с появлением островков пленки. По достаточно очевидной логике – что пленка должна появиться с увеличением концентрации празеодима.
Можно считать, что при появлении пленки PrOx лимитирующая стадия диффузии дырок в YSZ-электролите меняется на диффузию ионов кислорода в пленке PrOx.
ЗАКЛЮЧЕНИЕ
Проведено импрегнирование электродов ячейки Pt|YSZ|Pt микроколичествами PrOх (от 1 × × 10–4 до 0.1 мг/см2) c помощью спиртовых растворов нитрата празеодима в режиме, при котором на электролите YSZ (ZrO2 + 10 моль. % Y2O3) образуется пленка оксида празеодима. Методом электрохимического импеданса (воздух, 500–700°С) измерена поляризационная проводимость импрегнированных электродов, которая возрастает пропорционально содержанию PrOх.
В соответствии с предложенной моделью, импрегнация электрода возрастающими концентрациями нитрата празеодима предполагает следующие последовательные этапы этого процесса: 1) катионы празеодима покрывают только часть поверхности электролита; 2) катионы празеодима покрывают всю поверхность электролита; 3) катионы празеодима покрывают всю поверхность электролита, но появляются островки пленки PrOх вокруг частиц платины; 4) островки пленки PrOх растут и сливаются в единую пленку; 5) при последующих импрегнациях толщина пленки PrOх возрастает.
Так как диффузионный импеданс Варбурга на спектрах импеданса не наблюдается, предложена островковая модель пленочного электрода, в соответствии с которой электродный процесс лимитируется не толщиной пленки PrOх, а тем, что пленка занимает только часть поверхности электролита. Это обусловлено кристаллизацией нитрата празеодима на частицах платины с последующим образованием островков пленок вокруг них.
Как показал анализ спектров импеданса методом распределения времен релаксации (метод функций DRT), островковая модель выполняется в интервале концентраций PrOх от 0.1 до 3.3 × × 10–3 мг/см2. Вид функций DRT для этих электродов резко отличается от функций DRT для электродов с более низкими концентрациями оксида празеодима, при которых оксид празеодима растворяется в электролите YSZ, не образуя пленки. Отличие обусловлено сменой скорость-определяющих стадий электродного процесса: процесс диффузии дырок в YSZ-электролите меняется на диффузию ионов кислорода в пленке PrOx.
Список литературы
Chen, M., Liu, T., and Lin, Z., Theory for the conductivity of nanoparticle-infiltrated SOFC electrode, ECS Transactions, 2013, vol. 57, p. 2763.
Bertei, A., Pharoah, J.G., Gawel, D.A.W., and Nicolella, C., A particle-based model for effective properties in infiltrated solid oxide fuel cell electrodes, J. Electrochem. Soc., 2014, vol. 161, p. 1243.
Ramos, T., Veltze, S., Sudireddy, B.R., Jordensen, P.S., Theil Kuhn L., and Holtappels, P., Effect of Ru/CGO versus Ni/CGO co-Infiltration on the performance and stability of STN-based SOFCs, Fuel Cells, 2014, vol. 14, p. 1062.
Dan, Tang, Han, Min-Fang, and Zheng, Zi-Wei, Fabrication and performance of La0.6Sr0.4Co0.2Fe0.8O3 – δ infiltrated-yttria-stabilized zirconia cathode on anode-supported solid oxide fuel cell, J. Fuel Cell Science and Technology, 2015, vol. 12, p. 011001.
Kishimoto, M., Lomberg, M., Ruiz-Trejo, E., and Brandon, N.P., Enhanced triple-phase boundary density in infiltrated electrodes for solid oxide fuel cells demonstrated by high-resolution tomography, J. Power Sources, 2014, vol. 266, p. 291.
Ярославцев, И.Ю., Бронин, Д.И., Вдовин, Г.К., Исупова, Л.А. Оксидные катоды для электрохимических устройств, изготовленные с применением наноструктурированного композиционного материала. Электрохимия. 2012. Т. 48, С. 1084. [Yaroslavtsev, I.Yu., Bronin, D.I., Vdovin, G.K., and Isupova, L.A., Oxide cathodes for electrochemical devices made with the use of a nanostructured composition material, Russ. J. Electrochem., 2012, vol. 48, p. 981.]
Hong, W., Liu, Y., Wang, J., and Wang, E., LNF SOFC cathodes with active layer using Pr6O11 or Pr-doped CeO2, J. Power Sources, 2013, vol. 241, p. 768.
Ding, X., Zhu, W., Hua, G., Li, J., and Wu, Zh., Enhanced oxygen reduction activity on surface-decorated perovskite La0.6Ni0.4FeO3 cathode for solid oxide fuel, Electrochim. Acta, 2015, vol. 163, p. 204.
Chiba, R., Taguchi, H., Komatsu, T., Orui H., Nozawa, K., and Arai H., High temperature properties of Ce1 –xPrx O2 – δ as an active layer material for SOFC cathodes, Solid State Ionics, 2011, vol. 197, p. 42.
Вшивкова, А.И., Горелов, В.П. Способ изготовления электродов электрохимических устройств с твердым электролитом. Пат. 2543071 (Россия). 2015 [Vshivkova, A.I., and Gorelov, V.P., The method of manufacture of electrodes of electrochemical devices with solid electrolyte, The Patent 2543071 (Russia), 2015.]
Вшивкова, А.И., Горелов, В.П. Активация кислородной реакции пленкой оксида празеодима на платиновом электроде в контакте с электролитом YSZ. Электрохимия. 2016. Т. 52. С. 549. [Vshivkova, A.I. and Gorelov, V.P., Activation of oxygen reaction by praseodymium oxide film on platinum electrode in contact with YSZ electrolyte, Russ. J. Electrochem., 2016, vol. 52, p. 488.]
Коврова, А.И., Горелов, В.П. Пленки некоторых оксидов редкоземельных элементов в качестве активаторов платинового электрода на электролите ZrO2 + 10 мол. % Y2O3. Электрохимия, 2017, Т. 53. С. 592. [Kovrova, A.I. and Gorelov, V.P., Films of Certain Oxides of Rare-Earth Elements as the Activators of Platinum Electrode on ZrO2 + 10 mol % Y2O3 Electrolyte, Russ. J. Electrochem., 2017, vol. 5, p. 592.]
Рутман, Д.С., Торопов, Ю.С., Плинер, С.Ю., Неуймин, А.Д., Полежаев, Ю.М. Высокоогнеупорные материалы из диоксида циркония. М.: Металлургия, 1985, 137 с. [Rutman, D.S., Toropov, Yu.S., Pliner, S.Yu., Neuimin, A.D., and Polezhaev Yu.M., High-refractory materials from zirconia. M.: Metallurgy, 1985, 137 p.]
Вшивкова, А.И., Горелов, В.П., Кузьмин, А.В., Плаксин, С.В., Панкратов, А.А., Ярославцева, Т.В. Синтез и физико-химические свойства пленок и керамики оксида празеодима. Неорган. материалы. 2015. Т. 51. С. 1260. [Vshivkova, A.I., Gorelov, V.P., Kuzmin, A.V., Plaksin, S.V., Pankratov, A.A., and Yaroslavtseva, T.V., Preparation and physicochemical properties of praseodymium oxide films and ceramics, Inorganic Materials, 2015. vol. 51, p. 1168.]
Гаврилюк, А.Л., Осинкин, Д.А., Бронин, Д.И. О применении метода регуляризации Тихонова для вычисления функции распределения времен релаксации в импедансной спектроскопии, Электрохимия. 2017. Т. 53. С. 651. [Gavrilyuk, A.L., Osinkin, D.A., and Bronin, D.I., The use of Tikhonov regularization method for calculating the distribution Function of relaxation times in impedance spectroscopy, Russ. J. Electrochem, 2017, vol. 53, p. 575.]
Tikhonov, A.N. and Arsenin, V.Y., Solution of ill-posed problems, Amer. Math. Soc., 1979, vol. 1, p. 521.
Kim, J.J., Bishop, S.R., Chen, D., and Tuller, H.L., Defect chemistry of Pr doped ceria thin films investigated by in situ optical and impedance measurement, Chem. Mater., 2017, vol. 29, p. 1999.
Чеботин, В.Н., Перфильев, М.В. Электрохимия твердых электролитов. М.: Химия, 1978, 252 с.
Okada, S., Miyoshi, Sh., and Yamaguchi, Sh., Rate Determining Step in ORR of PrOx-Based Film Cathodes, ECS Transactions, 2015, vol. 68, p. 987.
Mizusaki, J., Amano, K., Yamauchi, S., and Fueki, K., Electrode reaction at Pt, O2 (g)/stabilized zirconia interfaces. Part I: Theoretical consideration of reaction model, Solid State Ionics, 1987, vol. 22, p. 313.
Mizusaki, J., Amano, K., Yamauchi, S., and Fueki, K., Electrode reaction at Pt, O2 (g)/stabilized zirconia interfaces. Part II: Electrochemical measurements and analysis, Solid State Ionics, 1987, vol. 22, p. 323.
Глумов, М.В. Исследование поляризации пористого платинового электрода в твердоэлектролитной ячейке в атмосфере кислорода. Электрохимия. 1986. Т. 22. № 2. С. 235.
Kurumchin, E.Kh., Isotope exchange studies of electrochemical systems with solid oxide electrolytes, Ionics, 1998, vol. 4, p. 390.
Дополнительные материалы отсутствуют.



