Электрохимия, 2020, T. 56, № 9, стр. 844-853
Гидротермальный синтез WO3 для электрохимического окисления парацетамола: микроструктурированный датчик парацетамола
Бхагьяшри Б. Камбл a, Анита К. Таваде b, Правин Камбл b, Мукеш Н. Падави b, Киран Кумар К. Шарма b, Балу Д. Аджалкар a, Шиваджи Н. Тайаде c, *
a Колледж Шиврадж Гадхинглай, Университет Шиваджи
416004 Махараштра, Колхапур, Индия
b Школа нанонауки и биотехнологии, Университет Шиваджи
416004 Махараштра, Колхапур, Индия
c Химический факультет Университета Шиваджи
416004 Махараштра, Колхапур, Индия
* E-mail: snt_chem@unishivaji.ac.in
Поступила в редакцию 29.12.2018
После доработки 19.07.2019
Принята к публикации 08.10.2019
Аннотация
Оксид вольфрама (WO3) в форме микроблоков получали гидротермальным способом. Подготовленный материал характеризовали полевой эмиссионной сканирующей электронной микроскопией (FE-SEM), рентгеновской дифракцией (XRD), инфракрасной (ИК) спектроскопией. Полученный материал был использован в качестве модификатора для стеклоуглеродного электрода простым методом капельного литья для исследования электрохимических характеристик парацетамола методами циклической вольтамперометрии и дифференциальной импульсной вольтамперометрии. Этот датчик показывает высокую каталитическую активность по окислению парацетамола. Пределы обнаружения (LOD) и предел количественного определения (LOQ) были определены как 7.17 × 10–4 и 2.39 × 10–3 М с линейным диапазоном от 0.75 × 10–4 до 6.75 × 10–3 М. Предлагаемый датчик был успешно использован для определения содержания парацетамола в образцах мочи человека.
ВВЕДЕНИЕ
Парацетамол (N-ацетил-п-аминофенол) широко используется в качестве обезболивающего и жаропонижающего препарата [1]. Он эффективно лечит бактериальные и вирусные лихорадки по всему миру. Он имеет большое значение благодаря своим свойствам не только как эффективный анальгетик, но и биологически безопасный для лечения болей, связанных с головной болью, артритом, болью в спине, зубной болью и послеоперационной болью [2, 3]. Ограниченная доза парацетамола имеет меньше побочных эффектов, однако более высокая доза может вызвать почечную недостаточность, которая приводит к печеночной недостаточности [4, 5] из-за образования 4-аминофенола в результате гидролитической деградации парацетамола [7‒9]. Чрезмерная доза парацетамола у детей может вызвать увеличение риноконъюнктивита, астмы и экземы [6]. Поэтому важно разработать простой и эффективный аналитический метод для обнаружения парацетамола в образце лекарства. Исследователь разработал различные аналитические методы, такие как жидкостная хроматография [10], капиллярный электрофорез [11], проточная инъекция [12], спектрофотометрия [13, 15], хемилюминесценция [14]. Однако эти инструментальные методы дороги и требуют много времени для анализа. Электрохимические методы [16–20] очень чувствительны, быстры и доступны по низкой цене. Таким образом, методы электрохимического обнаружения привлекли внимание исследователей по сравнению с другими аналитическими методами [21]. Электрохимический анализ зависит от электронной разности энергии между электродом и анализируемыми веществами. Модификация поверхности электрода наноматериалами или материалами микроструктуры усиливает эффективный процесс переноса заряда [22], который подходит для разработки электрохимических датчиков. Модифицированный электрод исследуется для обнаружения биомолекул (глюкоза, мочевая кислота, дофамин), экологических и фармацевтических образцов [23]. Этот анализ предоставляет информацию о химическом поведении образцов с точки зрения реакций окисления и восстановления. В последние годы проводящие тонкие пленки были разработаны для модификации электрода для повышения скорости, чувствительности и селективности различных лекарств и биосенсирования [24, 25]. В последнее десятилетие WO3 изучали на предмет его многочисленных применений, таких как электрохромный эффект [26], применение топливных элементов [27], солнечных элементов [28], фоторазложение [29] и обнаружение биомолекул [30]. Синтез тонкой пленки WO3 проводят различными способами, такими как золь–гель-метод [31], метод электроосаждения [32], метод химического осаждения в ванне [33] и гидротермальный метод [34, 35]. Синтез микроструктуры/наноструктуры WO3 гидротермальным методом является одним из наиболее универсальных методов. Синтез также может быть достигнут без использования каких-либо укупорочных средств, и, что наиболее важно, это одностадийный метод. По сравнению с материалами электродов с модификаторами, такими как Au, Ag и Pd, которые используются для электроокисления парацетамола [45], WO3 является предпочтительным, поскольку он очень стабилен и экономически эффективен.
В настоящей работе структурированные микроблоки WO3 синтезированы гидротермальным способом и использованы для модификации стеклоуглеродного электрода (GCE) до GCE/WO3. Модифицированный электрод использовали в качестве рабочего электрода для определения PA в 0.2 М фосфатно-солевом буфере (PBS), рН 8.3. Новый электрод обладает хорошей чувствительностью, стабильностью и воспроизводимостью в отношении определения парацетамола (PA) с помощью циклической вольтамперометрии (CV) и дифференциальной импульсной вольтамперометрии (DPV).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Приборы
Электрохимические измерения: циклическая вольтамперометрия и дифференциальная импульсная вольтамперометрия проводились с использованием электрохимической рабочей станции модели PGSTAT-302 N (Metrohm, AUTOLAB-302N) с обычной трехэлектродной системой. Немодифицированный стеклоуглеродный электрод и модифицированный WO3 стеклоуглеродный электрод (GCE/WO3) использовали в качестве рабочих электродов, платиновую проволоку в качестве противоэлектрода и хлоридсеребряный электрод (Ag/AgCl в насыщенном KCl) в качестве электрода сравнения. GCE тщательно полировали порошком оксида алюминия (2.5 мкм) и обрабатывали ультразвуком в течение одной минуты в этаноле. Противоэлектрод очищали концентрированной HNO3 и промывали трижды дистиллированной водой перед каждым электрохимическим экспериментом.
Реагенты
Вольфрамат натрия (Na2WO4 · 2H2O) получен от Loba Chemie, этанол (абсолютный), соляная кислота (HCl), оксалат аммония [(NH4)2C2O4] (Thomas Baker), парацетамол (500 мг) получен от Cipla, дигидрофосфат калия (KH2PO4) и гидрофосфат калия (K2HPO4) получены от sd fine-Chem Ltd., все реагенты были аналитического качества и использовались без дальнейшей очистки.
Гидротермальный синтез микроблочной структуры тонкой пленки WO3
WO3 в форме блоков синтезировали гидротермальным методом [35] с небольшими модификациями. 0.231 г дигидрата вольфрамата натрия растворяли в 30 мл трижды дистиллированной (TD) воды при постоянном перемешивании при комнатной температуре. Значение pH раствора регулировали путем добавления HCl (pH 2). Оксалат аммония (0.2 г) добавляли к приготовленному раствору при постоянном перемешивании с последующим добавлением 40 мл TD воды. 20 мл приготовленного раствора переносили в автоклав из нержавеющей стали с тефлоновым покрытием на 50 мл. Чистые стеклянные подложки были погружены вертикально в вышеуказанный раствор и плотно закрыты. Гидротермальный синтез проводили в муфельной печи при температуре реакции 1800°С в течение 16 ч. После завершения реакции автоклаву давали остыть до комнатной температуры. Осажденные тонкие пленки WO3 на стеклянной подложке промывали TD водой, этанолом и сушили при 600°C. Высушенные пленки WO3 отжигали при 5500°С в течение одного часа в муфельной печи.
Механизм роста WO3
Схема 1 . Вероятный механизм реакции образования микроблоков WO3.
Пределы обнаружения (LOD) и пределы количественного определения (LOQ) были рассчитаны соответственно с использованием уравнений (1) и (2) [38, 39]
где S представляет собой стандартное отклонение пикового тока, M представляет собой наклон калибровочной кривой.ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Получение и исследование электрода GCE/WO3
Чистый немодифицированный стеклоуглеродный электрод был модифицирован WO3 (1 мг мл–1) простым методом капельного литья. WO3 диспергируют путем интенсивной обработки ультразвуком в этаноле в течение 30 мин. 100 мкл диспергированного WO3 осаждают (1 мг мл–1) методом капельного литья на чистый полированный GCE. Это неоднократно делалось, пока поверхность GC не была покрыта полностью. Модифицированный электрод промывают TD водой для удаления слабо адсорбированных частиц и покрывают ионопроницаемым полимером Nafion TM для обеспечения адсорбционной стойкости осажденного WO3. Площадь активной поверхности электрода определяли методом циклической вольтамперометрии с использованием ферроцена в качестве стандартной окислительно-восстановительной пары при скорости сканирования 70 мВ с–1, как показано на рис. 1. Используя доступную литературу, значение коэффициента диффузии 0.16 × 10–6 см2 с–1 [36], площадь активной поверхности электрода была найдена равной 0.23 см2 [ipa = 2.53 × 10–6 A]. Площадь активной поверхности модифицированного электрода примерно в 3 раза превышает геометрическую площадь (0.0707 см2 по размерам GCE) GCE. Это говорит о том, что на модифицированном электроде GCE/WO3 присутствует тонкая пленка WO3, что приводит к увеличению активной площади поверхности электрода. Было установлено, что коэффициент шероховатости поверхности модифицированного электрода составляет 3.25.
Исследование полученного WO3
Кристалличность и структурные параметры синтезированного микроблока WO3 исследовали с использованием XRD (Thermo ARLSCINTAG X’TRA с CuKα-излучением, L ≈ 0.154056 нм). Рентгеновская дифрактограмма была получена в диапазоне 2θ от 10° до 70° с шагом 0.02° при скорости сканирования 2.4 мин–1. На рис. 2 показана рентгеновская дифрактограмма дифракции WO3, дифракционные пики наблюдались при 2θ = = 24.24°, 25.46°, 35.17°, соответствующих плоскостям (200) (020) (220) моноклинной структуры WO3 (данные карты JCPDS № 85-0950) [35]. На рис. 3 представлен ИК-фурье-спектр гидротермально синтезированных частиц WO3 при 180°С. Колебания триоксида вольфрама(VI) были обнаружены в области 467–1733 см–1. Полосы около 1733 см–1, соответствуют деформационным колебаниям ОН-групп (OHO, OH), ИК-пик при 467 см–1 относится к деформационным колебаниям WO, в то время как деформационным колебаниям W–OH соответствует пик при 1083 см–1, валентным колебаниям WO соответствует пик при 1424 см–1 [37]. Морфологию материала WO3 исследовали с помощью FESEM (аналитический сканирующий электронный микроскоп JEOL JSM-6360A). На рис. 4 показано формирование поверхности трехмерной кирпичной морфологии тонких пленок WO3, выращенных при 180°С в течение 16 ч. Связки пластинок превращаются в трехмерные кубоидные блоки, подобные структурам, в результате процесса созревания Оствальда [35]. Зарождение и рост наночастиц происходят на зародышевом слое в соответствии с законом созревания Оствальда. Следовательно, более крупные зародыши на поверхности посевного слоя дополнительно растут, образуя морфологию, похожую на блок.
Воспроизводимость и стабильность
Воспроизводимость сигнала модифицированного электрода была проверена с использованием 0.1 мМ PA в 0.2 М PBS (фосфатно-солевой буферный раствор) (рН 8.3), для последовательных 10 циклов почти одинаковый ток пика окисления контролировали с помощью вольтамперометрии при 50 мВ с–1 и получали относительное значение. Стандартное отклонение (RSD) составляло 2%. Стабильность модифицированного электрода проверяли путем измерения вольтамперограмм в течение 30 сут. Обнаружено, что ток пика окисления уменьшается на 6% от своего исходного значения. Эти наблюдения указывают на воспроизводимость и стабильный характер модифицированного электрода.
Вольтамперометрическое исследование PA на модифицированном электроде
Электрохимическое окислительно-восстановительное поведение 2.25 мМ PA в PBS при pH 8.3 было исследовано с использованием метода циклической вольтамперометрии при чистом GCE и GCE/WO3 (рис. 5a и 5б). На рис. 5а представлена CV PA на немодифицированном GCE без какой-либо фарадеевской активности, а на рис. 5б показана CV PA в GCE, модифицированном WO3, которая содержит пик окисления парацетамола при 0.48 В и пик восстановления при 0.032 В. Обнаружено, что окислительно-восстановительное поведение PA на поверхности модифицированного электрода является квазиобратимым, что видно из разделения пиков прямого и обратного сканирования вольтамперограммы. Резкое появление пиков окисления и восстановления PA с WO3 указывает на электрокаталитический эффект модифицированного электрода по сравнению с чистым GCE. Острые окислительные сигналы PA с модифицированным электродом указывают на хорошую чувствительность WO3 к PA.
Влияние концентрации PA на циклическую вольтамперограмму
Влияние концентрации PA наблюдалось в 0.2 М PBS (pH 8.3) на поверхности модифицированного электрода GCE/WO3 с использованием CV и DPV, как показано на рис. 6 и 7 соответственно. Рисунок 6 иллюстрирует линейное увеличение анодного пикового тока с увеличением концентрации PA. CV показывает сдвиг на 40 мВ в потенциале пика окисления, связанный с самой низкой и самой высокой концентрацией PA. Это меньшее смещение потенциала пика окисления объясняется возможным переносом электронов без осаждения окисленных продуктов PA. На рис. 6 показан пик тока восстановления PA при 0.032 В. Положение этого пика не меняется при увеличении концентрации PA [22], исключая возможность использования механизма ECE, в котором ток катодного пика уменьшается с увеличением числа сканирований. Изменение концентрации PA (от 0.0325 до 6.75 мМ) в зависимости от анодного пикового тока (рис. 6) показывает превосходную линейную корреляцию с уравнением регрессии i (A) = 0.01c + 2.31 × 10–5 (R2 = 0.99) (значение STYEX = 2.57 × 10–6, функция EXCEL STYEX вычисляет стандартную ошибку для линии наилучшего соответствия, используя набор значений x и y).
Рис. 6.
Циклические вольтамперограммы, полученные на модифицированном GCE/WO3 при разных концентрациях РА в PBS pH 8.3 при скорости сканирования 50 мВ с–1. Вставка на рис. 6 показывает линейное изменение тока пика окисления в зависимости от концентрации.
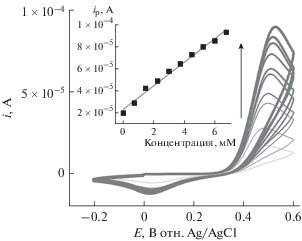
Рис. 7.
DPV на GCE/WO3 при разных концентрациях PA в 0.2 М PBS (pH 8.3) при 50 мВ с–1. Вставка на рис. 7 показывает линейное изменение тока пика окисления в зависимости от концентрации ПА.

Аналогичным образом, влияние концентрации PA было исследовано методом дифференциальной импульсной вольтамперометрии. Рисунок 7 иллюстрирует, что анодный пиковый ток увеличивается с увеличением концентрации PA. На вставках рис. 7 показано линейное изменение тока анодного пика в зависимости от концентрации PA с линейной регрессией ia (A) = 0.0017c + + 1.78 × 10–6 (R2 = 0.99).
Из CV и DPV пределы обнаружения составляют 7.17 × 10–4 и 5.29 × 10–4 М, и пределы количественного определения составляют 2.39 × 10–3 и 1.76 × 10–3 М.
LOD и линейный диапазон PA для различных электродных систем сравнивали с изготовленным электродом GCE/WO3, и они представлены в табл. 1. Как видно из табл. 1, микроблоки модификатора WO3 показывают более широкий линейный диапазон по сравнению с остальными модификаторами, использованными в табл. 1. Чувствительность электрода сравнима с данными литературы.
Таблица 1.
Сравнительные характеристики модифицированного электрода, используемого в определении PA
| Электрод | Метод | LOD, M | Линейный диапазон, мкМ | Чувствительность, A л моль–1 см–2 | Литература |
|---|---|---|---|---|---|
| SWCNT/CCE | DPV | 0.12 × 10–6 | 0.2–100 | – | [40] |
| MWCNT/GCE | DPV | 0.6 × 10–6 | 3–300 | – | [41] |
| Графен/GCE | SWV | 0.05 × 10–6 | 0.1–20 | – | [42] |
| CILE | DPV | 0.3 × 10–6 | 1–1000 | – | [43] |
| Электрод BDD | DPV | 0.49 × 10–6 | 0.5–83 | – | [44] |
| Электрод Au | PAD | – | – | – | [45] |
| BSPCE | – | 1.3 × 10–8 | – | 0.295 | [46] |
| SPCE/CB-ERGO | – | 1.5 × 10–6 | – | 0.311 | [47] |
| GCE/WO3 | CV | 7.17 × 10–4 | 75–6750 | 0.2769 | Настоящая работа |
| GCE/WO3 | DPV | 5.29 × 10–4 | 75–6750 | 0.0435 | Настоящая работа |
Сокращения: CPE – угольный пастовый электрод, CILE – углерод-ионный жидкий электрод, CCE – угольно-керамический электрод, DPV – дифференциальная импульсная вольтамперометрия, SWCNT – одностенная углеродная нанотрубка, MWCNT – многостенные углеродные нанотрубки, SWV – прямоугольная вольтамперометрия, PAD – импульсное амперометрическое обнаружение, BDD – алмаз, легированный бором, SPCE – углеродный электрод с трафаретной печатью, BSPCE – углеродный электрод с трафаретной печатью (немодифицированный).
В табл. 1 показано 100-кратное увеличение значений LOD при сравнении GCE/WO3 с литературным значением [40–45], что указывает на плохую реакцию на PA. Так как углеродистые материалы с одномерной или двумерной морфологией обладают потенциальной способностью к переносу заряда, а наличие большой площади поверхности делает их заметным кандидатом для зондирования PA. Однако для изготовления датчиков на основе углерода требуется путь синтеза, очистка и интенсивный уход. В этой статье впервые мы сообщаем о зондировании PA гидротермально синтезированными микрочастицами WO3. Несмотря на низкую чувствительность, эти микрочастицы показывают каталитическую реакцию на PA. Оптимизация морфологии поверхности в зависимости от времени синтеза может открыть двери для недорогого датчика PA на основе WO3.
Влияние pH
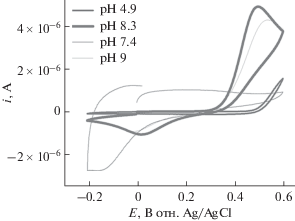
Вольтамперометрический отклик 0.75 мМ PA в 0.2 М PBS был изучен при увеличении рН от 4.9 до 9.0 на рабочем электроде GCE/WO3, чтобы исследовать влияние рН на окисление PA. Этот анализ проводится для изучения роли участия протонов в окислительно-восстановительном механизме окисления парацетамола и для прогнозирования условий каталитического окисления PA, происходящих в протонной эффективной или дефицитной среде. Никакой фарадеевской активности не наблюдалось для рН 4.9 и 7.4, тогда как при рН 8.3 и 9.0 PA проявлял анодный и катодный пиковый ток. Это указывает на то, что роль протонов в окислении PA незначительна. Однако при рН 8.3 наблюдалось увеличение анодного и катодного пикового тока, а также отрицательный сдвиг в потенциале пика окисления и положительный сдвиг в потенциале восстановления пика по сравнению с рН 9.0. Это смещение пикового потенциала с ростом рН объясняется трудностью окисления PA. Поэтому рН 8.3 был оптимальным для дальнейших электрохимических исследований PA. Окислительно-восстановительная активность PA в основном pH на поверхности GCE/WO3 объясняется незначительным взаимодействием водородных связей с раствором электролита, поэтому адсорбция PA на поверхности WO3 становится энергетически более благоприятной, что приводит к каталитическому окислению PA на поверхности GCE/WO3 [48].
Влияние скорости сканирования
Влияние скорости сканирования на ток пика окисления PA (0.75 мМ) изучали в диапазоне скорости сканирования от 10 до 100 мВ с–1 в 0.2 М PBS (pH 8.3) на электроде GCE/WO3 с использованием метода CV. Как на рис. 9 при увеличении скорости сканирования анодный и катодный пиковый ток также увеличивается, однако потенциал анодного пика смещается в положительную сторону, а потенциал катодного пика в отрицательную сторону. Вставка на рис. 9 показывает хорошую линейность с квадратным корнем частоты сканирования по сравнению с анодным и катодным пиковым током с коэффициентами корреляции (R2) 0.9973 и 0.9982 соответственно [49]. Линейная зависимость между пиковыми токами и скоростью сканирования приписывается диффузионно-контролируемому электродному процессу PA. Уравнения линейной регрессии представляли собой:
Оценка кажущегося коэффициента диффузии PA
Был оценен кажущийся коэффициент диффузии 0.75 мМ PA в 0.2 М PBS (рН 8.3) на GCE, модифицированном WO3. Значение Dapp рассчитывали по модифицированному уравнению Рэндлса–Шевчика для квазиобратимой реакции [22]
(3)
${{i}_{{\text{p}}}} = \left( {2.99 \times {{{10}}^{5}}} \right){{n}^{{{3 \mathord{\left/ {\vphantom {3 2}} \right. \kern-0em} 2}}}}{{\left( {\alpha n} \right)}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}A{{c}_{0}}{{D}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}{{v}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}.$Исследование воздействия биомолекул
Хроноамперометрическое исследование (представленное на рис. 10) проводили для изучения воздействия биомолекул, таких как аскорбиновая кислота (AA), мочевая кислота (UA) и дофамин (DA). Зависимость тока от времени исследовали при 0.48 В (при потенциале окисления парацетамола) относительно Ag/AgCl в течение 240 с. Эксперимент начинали с 1.5 мМ парацетамола в фосфатном буферном растворе (рН 8.3), а затем с интервалом 50, 100 и 150 с добавляли AA (35 мкМ), UA (35 мкМ) и DA (40 мкМ) соответственно. Зависимость тока от времени не показывает изменений при добавлении этих биомолекул. Наконец, через 180 с добавляли 1.5 мМ парацетамола, что приводило к повышению профиля зависимости тока от времени, указывая на то, что WO3 проявляет чувствительность только к PA и не является чувствительным по отношению к AA, UA и DA.
Определение PA в образце мочи человека
Исследование чувствительности к окислению PA проводили на поверхности электрода GCE/WO3 в 0.2 М PBS (pH 8.3) на образцах трех добровольцев. Результаты исследования представлены в табл. 2. Анализ проводили путем добавления 150 мкМ PA в каждый образец соответственно. Вольтамперограмма показывает четкий сигнал окисления PA с чувствительностью, близкой к 100%, свидетельствуя, что электрод GCE/WO3 может работать как хороший датчик для PA.
ВЫВОДЫ
В настоящей работе в качестве датчика для определения PA использовали электрод GCE, модифицированный микроблоками WO3. Разработанный датчик проявляет высокую каталитическую активность и чувствительность к PA. Датчик был успешно использован для оценки PA в образце мочи человека. Благодаря высокой стабильности и воспроизводимости GCE/WO3, он имеет потенциал для будущего развития датчиков.
Список литературы
Martindale, The Extra Pharmacopoeia, 29th Ed., The Pharmaceutical Press, London (1989), 32.
Jia, L., Zhang, X. Li, Q., and Wang, S., Determination of Acetaminophenone by square wave voltammetry at a gold electrode modified by 4-amino2-mercaptopyrimidine self-assembled monolayers, J. Analyt. Chem., 2007, vol. 62, p. 266.
Kachoosangi, R.T., Wildgoose, G.G., and Compton, R.G., Sensitive adsorptive stripping voltammetric determination of paracetamol at multiwalled carbon nanotube modified basal plane pyrolytic graphite electrode, Analyt. Chim. Acta, 2008, vol. 618, p. 54.
Cramer, D.W., Harlow, B.L., Titus-Ernstoff, L., Bohlke, K., Welch, W.R., and Greenberg, E.R., Over-the-counter analgesics and risk of ovarian cancer, The Lancet, 1998, vol. 351, p. 104.
Rowden, A.K., Norvell, J., Eldridge, D.L., and Kirk, M.A., Acetaminophen poisoning, Clinics in Laboratory Medicine, 2006, vol. 26, p. 49.
Sullivan, J.E. and Farrar, H.C., Fever and antipyretic use in children, Pediatrics, 2011, vol. 127, p. 580.
Jeevagan, A.J. and John, S.A., Electrochemical determination of caffeine in the presence of paracetamol using a self-assembled monolayer of non-peripheral amine substituted copper (II) phthalocyanine, Electrochim. Acta, 2012, vol.77, p. 137.
Li, L., Lu, Y., Ding, Y., Cheng, Y., Xu, W., and Zhang, F., Determination of paracetamol based on its quenching effect on the photoluminescence of CdTe fluorescence probes, J. Fluoresc., 2012, vol. 22, p. 591.
Shiroma, L.Y., Santhiago, M., Gobbi, A.L., and Kubota, L.T., Separation and electrochemical detection of paracetamol and 4-aminophenol in a paper-based microfluidic device, Anal. Chim. Acta, 2012, vol. 725, p. 44.
Sirajuddin, Khaskheli, A.R., Shah, A., Bhanger, M.I., Niaz, A., and Mahesar, S., Simpler spectrophotometric assay of paracetamol in tablets and urine samples, Spectrochim. Acta A, Mol. Biomol. Spectrosc., 2007, vol. 68, p. 747.
Capella-Peiró, M.-E., Bose, D., Rubert, M.F., and Esteve-Romero, J., Optimization of a capillary zone electrophoresis method by using a central composite factorial design for the determination of codeine and paracetamol in pharmaceuticals, J. Chromatography B, 2006,vol. 839, p. 95.
Knochen, M., Giglio, J., and Reis, B.F., Flow-injection spectrophotometric determination of paracetamol in tablets and oral solutions, J. Pharmaceut. and Biomed. Analysis, 2003, vol. 33, p. 191.
Yousefinejad, S. and Hemmateenejad, B., Simultaneous spectrophotometric determination of paracetamol and para-aminophenol in pharmaceutical dosage forms using two novel multivariate standard addition methods based on net analyte signal and rank annihilation factor analysis, Drug Testing Anal., 2012, vol. 4, p. 507.
Franeta, J.T., Agbaba, D., Eric, S., Pavkov, S., Aleksic, M., and Vladimirov, S., Il Farmaco HPLC assay of acetylsalicylic acid, paracetamol, caffeine and phenobarbital in tablets, Farmaco, 2002, vol. 57, p. 709.
Moreira, A.B., Oliveira, H.P.M., Atvars, T.D.Z., Dias, I.L.T., Neto, G.O., Zagatto, E.A.G., and Kubota, L.T., Direct determination of paracetamol in powdered pharmaceutical samples by fluorescence spectroscopy, Anal. Chim. Acta, 2005, vol. 539, p. 257.
Saraswathyamm, B., Grzybowsk, I., Orlewsk, C., Radecki, J., Dehaen, W., Kumar, K.G., and Radecka, H., Electroactive dipyrromethene-Cu(II) monolayes deposited onto Au electrode for voltammetric determination of paracetamol, Electroanalysis, 2008, vol. 20, p. 2317.
Baranowska, I. and Koper, M., The preliminary studies of electrochemical behavior of paracetamol and its metabolites on glassy carabon electrode by voltammetric method, Electroanalysis, 2009, vol. 21, p. 1194.
L, B.C., Medeiros, R.A., Rocha-Filho, R.C., Mazo, L.H., and Fatibello-Filho, O., Simultaneous voltammetric determination of paracetamol and caffeine in pharmaceutical formulations using a boron-doped diamond electrode, Talanta, 2009, vol. 78, p. 748.
Hou, X., Shen, G., Meng, L., Zhu, L., and Guo, M., Multi-walled carbon nanotubes modified glass carbon electrode and its electrocatalytic activity towards oxidation of paracetamol, Russ. J. Electrochem., 2011, vol. 47, p. 1262. [Ху, Х., Шен, Г., Мэн, Л., Чжу, Л., Гуо, М. Многослойные углеродные нанотрубки модифицированного стеклоуглеродного электрода и его электрокаталитическая активность в отношении окисления парацетамола, Электрохимия. 2011. Т. 47. С. 1262.]
Tayade, S., Patil, K., Sharma, G., Patil, P., Mane, R., Mahulikar, P., and Sharma K.K., Electrochemical investigations of Thymine and Thymidine in 1-butyl-3-methylimidazolium tetrafluoroborate ionic liquids at room temperature, Chem. Papers, 2019, vol. 73, p. 2275.
Dalmasso, P.R., Pedano, M.L., and Rivas, G.A., Electrochemical determination of ascorbic acid and paracetamol in pharmaceutical formulations using a glassy carbon electrode modified with multi-wall carbon nanotubes dispersed in polyhistidine, Sens. Actuators B, 2012, vol. 173, p. 732.
Bard A.J. and Faulkner, L.R., Electrochemical Methods: Fundamentals and Applications, John Wiley, New York, 2001.
Kamble, B., Naikwade, M., Garadkar, K.M., Mane, R., Sharma, K., Ajalkar, B., and Tayade, S.N., Ionic liquid assisted synthesis of chromium oxide (Cr2O3) nanoparticles and their application in glucose sensing, J. Mater. Sci.: Materials in Electronics, 2019, vol. 30, p. 13984.
Zhou, H., Chen, J., Huang, T., Chen, D., Wu, Y., Zheng, F., Yu, H., and Li, S., Uniformly distributed and in situ iron–nitrogen co-doped porous carbon derived from pork liver for rapid and simultaneous detection of dopamine, uric acid, and paracetamol in human blood serum, N. J. Chem., 2017, vol. 41, p. 2081.
Y. Veera Manohara Reddy, Sravani, Bathinapatla, Fernandes, Diana M., Ch. Madhuri L. Sarm, Subramanyam, and Madhavi, G., Facile one pot synthesis of bimetallic Pd–Ag/reduced graphene oxide nanocomposite as an electrochemical sensor for sensitive detection of antihypotensive drug, Colloids and Surfaces A, 2018, vol. 546, p. 293.
Velevska, Julijan, Stojanov, Nace, Pecovska-Gjorgjevich, Margareta, and Najdoski, Metodija, Electrochromism in tungsten oxide thin films prepared by chemical bath deposition, J. Electrochem. Sci. Eng., 2017, vol. 7, p. 27.
Danga, Dai, Zhao, Bote, Chen, Dongchang, deGlee, Ben M., Qu, Chong, Daia, Shuge, Zeng, Xiaoyuan, Liu, Jing, Lu, Yunfeng, Liao, Shijun, and Liu, Meilin, A bi-functional WO3-based anode enables both energy storage and conversion in an intermediate-temperature fuel cell, Energy Storage Materials, 2018, vol. 12, p. 79.
Simchi, H., McCandless, B.E., Meng, T., and Shafarman, W.N., Structural, optical, and surface properties of WO3 thin films for solar cells, J. Alloys and Compounds, 2014, vol. 617, p. 609.
Hunge, Y.M., Mahadik, M.A., Moholkar, A.V., and Bhosale, C.H., Photoelectrocatalytic degradation of phthalic acid using spray deposited stratified WO3/ZnO thin films under sunlight illumination, Appl. Surface Sci., 2017, vol. 420, p. 764.
Anitha, A.C., Lavanya, N., Asokan, K., and Sekar, C., WO3 nanoparticles based direct electrochemical dopamine sensor in the presence of ascorbic acid, Electrochim. Acta, 2015, vol. 167, p. 294.
Breedon, Michael, Spizzirri, Paul, Taylor, Matthew, du Plessis, Johan, McCulloch, Dougal, Zhu, Jianmin, Yu, Leshu, Hu, Zheng, Rix, Colin, Wlodarski, Wojtek, and Kalantar-zadeh, Kourosh, Synthesis of Nanostructured Tungsten Oxide Thin Films: A Simple, Controllable, Inexpensive, Aqueous Sol–Gel Method, Crystal Growth Design Article, 2010, vol. 10, P. 430.
Poongodi, S., Suresh Kumar, P., Masud, Yoshitake, Mangalaraj, D., Ponpandiana, N., Viswanathan, C., and Ramakrishna, Seeram, Synthesis of Hierarchical WO3 nanostructured thin films with enhanced electrochromic performance for switchable smart windows, RSC Adv., 2015, vol. 5, p. 96416.
Ifeanyichukwu, Amaechi, Assumpta, Nwanya, Paul u. Asogwa, Rose u. Osuji, Malik Maaza, and Fabian i. Ezema, Hall Coefficient Determination and Electrical Properties of Chemical Bath-Deposited n-WO3 Thin Films, J. Elecctronic Materials, 2015, vol. 44, p. 1110.
Rashad, M.M. and Shalam, A.E., Hydrothermal synthesis of hierachical WO3 nanostructures for dye sensitized solar cell, Appl. Phys. A, 2014, vol. 116, p. 781.
Mathuri, S., Margoni, Mudaliar Mahesh, Ramamurthi, K., Ramesh Babu, R., and Ganesh, V., Hydrothermal assisted growth of vertically aligned platelet like structures of WO3 films on transparent conducting FTO substrate for electrochromic performance, Appl. Surface Sci., 2018, vol. 449, p. 77.
Alaa A.A. Aljabali, J. Elaine Barclay, Jule N. Butt, George P., Lomonossoffa and David J. Evans, Redox-active ferrocene-modified Cowpea mosaic virus nanoparticles, Dalton Trans., 2010, vol. 39, p. 7569.
Díaz-Reyes, J., Dorantes-García, V., Pérez-Benítez, A., and Balderas-López, A., Obtaining of films of tungsten trioxide (WO3) by resistive heating of a tungsten filament, Superficies y Vacío, June 2008, vol. 21, p. 12.
Reddaiah, K., Madhusudana Reddy, T., and Raghu, P., Electrochemical investigation of L dopa and simultaneous resolution in the presence of uric acid and ascorbic acid at a poly (methyl orange) film coated electrode: A voltammetric study, J. Electroanal. Chem., 2012, vol. 682, p. 164.
Madhusudana Reddy, T., Sreedhar M., and Reddy, S.J., Voltammetric behavior of Cefixime and Cefpodoxime Proxetil and determination in pharmaceutical formulations and urine, J. Pharm. Biomed. Anal., 2003, vol. 31, p. 811.
Habibi, B., Jahanbakhshi, M., and Pournaghi-Azar, M.H., Simultaneous determination of acetaminophen and dopamine using SWCNT modified carbon–ceramic electrode by differential pulse voltammetry, Electrochim. Acta, 2011, vol. 56, p. 2888.
Alothman, Z.A., Bukhari, N., Wabaidur, S.M., and Haider, S., Simultaneous electrochemical determination of dopamine and acetaminophen using multiwall carbon nanotubes modified glassy carbon electrode, Sens. Actuators B, 2010, vol. 146, p. 314.
Kang, X., Wang, J., Wu, H., Liu, J., Aksay, I.A., and Lin, Y., A graphene-based electrochemical sensor for sensitive detection of paracetamol, Talanta, 2010, vol. 8, p. 754.
ShangGuan, X., Zhang, H., and Zheng, J., Electrochemical behavior and differential pulse voltammetric determination of paracetamol at a carbon ionic liquid electrode, Anal. Bioanal. Chem., 2008, vol. 391, p. 1049.
Lourenc, B.C., Medeiros, R.A., Rocha-Filho, R.C., Mazo, L.H., and Fatibello-Filho, O., Simultaneous voltammetric determination of paracetamol and caffeine in pharmaceutical formulations using a boron-doped diamond electrode, Talanta, 2009, vol. 78, p. 748.
Koprowski, L., Kirchmann, E., and Welch, L.E., The electrochemical oxidation of penicillins on gold electrodes, Electroanalysis, 1993, vol. 5, p. 473.
Karikalan, N., Karthik, R., Chen, S.-M., Velmurugan, M., and Karuppiah, C., Electrochemical properties of the acetaminophen on the screen printed carbon electrode towards the high performance practical sensor applications, J. Colloid Interface Sci., 2016, vol. 483, p. 109.
Ibáñez-Redín, G., Wilson, D., Gonçalves, D., and Oliveira Jr., O.N., J. Colloid and Interface Sci., 2018, vol. 515, p. 101.
Bernal, Valentina, Erto, Alessandro, Giraldo, Liliana, and Moreno-Piraján, Juan Carlos, Effect of Solution pH on the Adsorption of Paracetamol on Chemically Modified Activated Carbons, Molecules, 2017, vol. 22, p. 1032.
Raoof, B., Ojani, R., and Mohammadpour, Z., Electrocatalytic Oxidation and Voltammetric Determination of Hydrazine by 1,1-Ferrocenedicarboxylic Acid at Glassy Carbon Electrode, Int. J. Electrochem. Sci., 2010, vol. 5, p. 177.
Narayana, P. V., Madhusudana Reddy, T., Gopala, P., and Naidu, G.R., Electrochemical sensing of paracetamol and its simultaneous resolution in the presence of dopamine and folic acid at a multi-walled carbon nanotubes/poly(glycine) composite modified electrode, Anal. Methods, 2014, vol. 6, p. 9459.
Дополнительные материалы отсутствуют.