Электрохимия, 2021, T. 57, № 5, стр. 276-282
Влияние термической обработки на физические свойства LiCoO2 стехиометрического состава
Р. И. Корнейков a, В. В. Ефремов a, *, В. И. Иваненко a, К. А. Кесарев a
a Институт химии и технологии редких элементов и минерального сырья им. И.В. Тананаева –
обособленное подразделение Федерального государственного бюджетного учреждения науки
Федерального исследовательского центра “Кольский научный центр Российской академии наук”
184209 Апатиты, Академгородок, 26а, Россия
* E-mail: v.efremov@ksc.ru
Поступила в редакцию 18.03.2020
После доработки 23.10.2020
Принята к публикации 02.11.2020
Аннотация
Методом золь–гель-синтеза был получен кобальтат лития (LiCoO2) стехиометрического состава. Установлены физические параметры (размер частиц, удельная площадь и удельная статическая электропроводность) исследуемых образцов и влияние на них температуры прокалки. Определено, что в электропроводность вносят свой вклад три механизма проводимости: частотно-независимый σ0, ионный транспорт объема образца σsv, ионный транспорт на границе электрод/ионный проводник σdl. Определены оптимальные режимы термической обработки, позволяющие сохранить высокоразвитую удельную поверхность LiCoO2.
ВВЕДЕНИЕ
Из многообразия автономных источников тока выделяются литий-ионные аккумуляторы. Они нашли широкое применение как в устройствах массового потребления, так и в военной технике, медицине [1, 2]. Наибольшее распространение в качестве материала, из которого изготавливается катод в литий-ионных источниках питания, получил кобальтат лития (LiCoO2) стехиометрического состава [3–9]. Батарея, созданная на основе LiCoO2, обладает существенными преимуществами: высокой энергетической плотностью, низким саморазрядом, высоким током работы, жизненным циклом и т.д. [10–17]. При этом не прекращаются исследования по поиску как новых материалов, способных улучшить характеристики литий-ионных аккумуляторов, так и способов модификации уже использующихся материалов при производстве батарей. Наиболее распространенным способом синтеза LiCoO2 является твердофазный метод. Смесь оксида кобальта с карбонатом (гидроксидом) лития спекают долгое время при 600–900°С. Подобный способ синтеза LiCoO2 является энергетически затратным [18]. Перспективным методом получения LiCoO2, устраняющим недостатки твердофазного синтеза, является золь–гель-технология. Данный технологический процесс не требует использования высоких температур и сокращает время тепловой обработки. Однако этот способ предполагает применение дорогостоящих сильных окислителей [19, 20]. В связи с этим, цель работы заключалась в поиске более эффективного способа синтеза монофазного наноразмерного кобальтата лития (соотношение Li+ : Co3+ = 1) с использованием золь–гель-технологии без применения дорогостоящих окислителей и исследование влияния условий синтеза на физические свойства.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
На начальном этапе синтеза осуществляли перевод Co2+ в Co3+ в среде гидроксида лития (Li : Co = 10 : 1) путем насыщения суспензии кислородом из воздуха.
Процесс проводили при температуре 90°С, непрерывном репульпировании и барботировании. В данных условиях образуется высокогидратированный гидроксид кобальта. В результате термообработки происходила частичная потеря воды, что способствовало формированию прекурсора оксогидроксида кобальта [21]. Далее замещали ионы водорода ОН–-групп CoOOH на ионы Li+. После чего осуществляли упаривание, прокаливание (при 500°С) и отмывку от маточного электролита. В итоге был получен монофазный кобальтат лития стехиометрического состава, что подтверждается данными рентгенофазового анализа (рис. 1). Рентгенофазовый анализ синтезированного LiCoO2 осуществляли на дифрактометре ДРОН-2 с CuKα-излучением и графитовым монохроматором. Скорость съемки составляла 2 град/мин. Фазы идентифицировали, используя базу данных JCPDS.
Кроме того, был проведен химический анализ полученного продукта (мас. %): Li2O – 15.24, Co2O3 – 84.72, который также подтвердил полученный нами результат. Химический анализ осуществляли, используя масс-спектрометрическую систему с индуктивно-связанной плазмой с динамической реакционной системой “ELAN 9000 DRC-e”, а также плазменный эмиссионный спектрометр ICPS-9000.
В результате нами была разработана принципиальная технологическая схема получения монофазного LiCoO2 стехиометрического состава, приведенная на рис. 2.
Для изучения микроструктуры частиц синтезированных порошков LiCoO2 использовали сканирующий электронный микроскоп SEM LEO-420 и программу ScanMaster, предназначенную для математической обработки полученных изображений и проведения измерений. Программа позволяет на изображении выделять отдельные объекты, определять их характеристики и выполнять статистическую обработку совокупности выделенных объектов по выбранным критериям. В качестве критерия нами выбрана длина объекта – максимальное из значений длин 18 проекций на прямую ориентации объекта. Удельную поверхность синтезированных материалов определяли с помощью измерителя удельной поверхности FlowSorb II 2300. Для дальнейших исследований из синтезированных порошков изготавливали таблетки с помощью гидравлического пресса при давлении 1 т/см2 и спекали при 800°С в течение 1 ч.
Электрофизические свойства исследовали импедансметром Solartron-1260 в диапазоне частот 0.1–107 Гц. Электроды на плоской поверхности образца создавались путем магнетронного напыления тонкого слоя платины, после чего образец с нанесенными электродами можно рассматривать как плоский конденсатор.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Результаты структурного исследования, полученного с помощью электронного микроскопа, показали, что размер частиц LiCoO2 неоднороден и связан с температурой прокалки порошков, при этом ярко выражена агломерация частиц (рис. 3). Кобальтат лития, прокаленный при 500°С в течение 1.5 ч, обладает меньшим средним размером зерна и, соответственно, имеет более развитую удельную поверхность в отличие от образца, подвергшегося термической обработке при 800°С.
Значительное уменьшение удельной поверхности является результатом увеличения среднего размера кристаллитов вследствие процессов перекристаллизации частиц LiCoO2, происходящих при более высокой температуре. В табл. 1 сведены данные физических характеристик образцов, прокаленных при разных температурах.
Таблица 1.
Физические характеристики образцов кобальтата лития
| № образца | Термообработка, °С | Характеристика LiСоO2 | |
|---|---|---|---|
| удельная поверхность, м2/г | средний размер частиц, нм | ||
| 1 | 500 | 22.09 | 100 |
| 2 | 800 | 1.97 | 602 |
Далее нами исследовалась дисперсия комплексного импеданса кобальтата лития. Метод импеданс-спектроскопии основан на регистрации частотных зависимостей импеданса электрохимической ячейки с последующей их интерпретацией с использованием метода эквивалентных электрических схем. Если спектр достаточно сложен, то нередко его можно удовлетворительно описать несколькими схемами с различным набором параметров, что является недостатком данного метода. Таким образом, выбор электрической схемы замещения для моделирования спектров импеданса является наиболее важным моментом в интерпретации результатов.
На рис. 4 и 5 представлены годографы импеданса LiСоO2, прокаленного при 500°С (рис. 4) и 800°С (рис. 5), с удельными значениями составляющих импеданса по осям Ом см2, рассчитанными с учетом внешней поверхности частиц. Из сравнения рис. 4 и 5 видно, что комплексные Z ''Z '-диаграммы импеданса качественно подобны. На них обнаруживаются два релаксационных процесса Дебаевского типа в виде дуг полуокружностей: высокочастотный и низкочастотный. При этом дуги плохо разрешены в силу близости времен релаксаций.
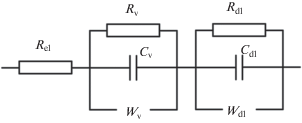
В высокочастотной области спектра годографы импеданса представляют собой искаженную полуокружность с центром, лежащим ниже оси абсцисс (рис. 4, 5), которая создается параллельным RC-соединением. Искаженная полуокружность может моделироваться различными схемами замещения [22–24], мы же выбрали схему, представленную на рис. 6, как в наибольшей степени отвечающую физической картине процессов и удовлетворительно моделирующую экспериментальные годографы. Подобная схема замещения использовалась для описания спектра импеданса литиевого электрода в работах [25, 26]. Выбор схемы с импедансом Варбурга представляется вполне обоснованным применительно к рассматриваемым спектрам, так как начальный участок высокочастотной области в небольшом интервале линеен, а угол наклона прямой близок к 45°, что характерно для диффузии.
В низкочастотной области спектра годографы импеданса также представляют собой искаженные дуги. Диффузия лития частично или полностью маскируется иными процессами, в том числе накоплением заряда или утечкой заряда через блокирующую границу электрода, что выражается отклонением низкочастотной прямой от 45° или ее переходом в дугу большой полуокружности. Преобладание того или иного процесса отражается в конструкции эквивалентной схемы замещения параллельным подключением к W сопротивления утечки R или емкости образца C (рис. 6).
Таким образом, мы полагаем, что высокочастотная дуга характеризует процессы, происходящие в объеме исследуемых образцов, а низкочастотная связана с процессами, протекающими в приэлектродной области. Поскольку процесс ионной миграции протекает достаточно медленно, он доминирует в импедансе при низких частотах. Кроме того, из рис. 4 видно, что часть полуокружности, относящаяся к высокочастотному релаксационному процессу, выходит не из нуля, что свидетельствует о наличии в образце частотно-независимой проводимости (наиболее вероятно, что данными носителями являются свободные электроны). Исходя из теории электрических цепей зависимость Z*(ω) достоверно аппроксимирует эквивалентная схема, представленная на рис. 6.
Параметры результатов обработки диаграмм импедансов с помощью эквивалентных схем замещения приведены в табл. 2.
Таблица 2.
Параметры эквивалентной схемы замещения, полученные моделированием спектров импеданса LiСоO2
| Rel, Ом см2 | Rv, Ом см2 | Rdl, Ом см2 | Cv, Ф см–2 | Cdl, Ф см–2 | Wv, Ом см2/c1/2 | Wdl, Ом см2/c1/2 | |
|---|---|---|---|---|---|---|---|
| 500 | 2980 | 4 × 104 | 5.7 × 104 | 2.4 × 10–13 | 3 × 10–10 | 5.2 × 107 | 8.4 × 106 |
| 800 | 5069 | 3.7 × 106 | 6.5 × 107 | 1 × 10–12 | 9.5 × 10–12 | 4.9 × 108 | 2.8 × 108 |
Для подтверждения предположения о том, что низкочастотный релаксационный процесс связан с образованием двойного электрического слоя, была исследована дисперсия реальной части диэлектрической проницаемости (рис. 7). Значительная дисперсия диэлектрической проницаемости при наличии ионной проводимости в гетерогенных системах обычно обусловлена миграционной поляризацией по механизму Максвелла–Вагнера. Носители заряда накапливаются на границах компонента и дают вклад в поляризацию, т.е. приводят к увеличению диэлектрической проницаемости материалов. В керамических материалах такой вклад пропорционален объему границ электрод–композит [27].
Рис. 7.
Дисперсия реальной части диэлектрической проницаемости при комнатной температуре: 1 – температура прокалки 500°С, 2 – температура прокалки 800°С.

Действительно, как видно из рис. 6, в области низких частот значения реальной части диэлектрической проницаемости достигают высоких значений (~104–105 в зависимости от температуры прокалки), следовательно, предположение об образовании двойного электрического слоя подтверждается.
Сравнивая значения, приведенные в табл. 2, видно, что собственная удельная ионная проводимость σv LiСоO2, прокаленного при 500°С, существенно выше (на два порядка) в сравнении с LiСоO2, прокаленным при 800°С. Таким образом можно сделать вывод, что повышение температуры прокалки оказывает существенное влияние на собственную ионную проводимость LiСоO2 вследствие процессов перекристаллизации и увеличения среднего размера зерна.
ЗАКЛЮЧЕНИЕ
Нами была разработана технологическая схема, согласно который был синтезирован LiСоO2 стехиометрического состава. Разработанная нами методика синтеза на основе золь–гель-технологии позволила отказаться от применения дорогостоящих окислителей и высокотемпературной прокалки. Были определены оптимальные режимы синтеза для получения наноразмерного LiСоO2 стехиометрического состава, обладающего оптимальными физическими характеристиками. Методом импеданс-спектроскопии были проведены электрофизические исследования LiСоO2. Обнаружено, что три механизма проводимости вносят свой вклад в электропроводность: частотно-независимый (электронная) σel, собственная ионная проводимость σv и ионный транспорт на границе электрод/ионный проводник σdl. Определены параметры эквивалентной схемы замещения, полученные моделированием спектров импеданса LiСоO2. Установлено, что повышение температуры прокаливания исходного образца уменьшает величину собственной ионной проводимости кобальтата лития.
Список литературы
Ярославцев, А.Б., Кулова, Т.Л., Скундин, А.М. Электродные наноматериалы для литий-ионных аккумуляторов. Успехи химии. 2015. Т. 84. С. 826. [Yaroslavtsev, A.B., Kulova, T.L., and Skundin, A.M., Electrode nanomaterials for lithium-ion batteries, Russ. Chem. Rev., 2015, vol. 84, p. 826.] https://doi.org/10.1070/RCR4497
Abe, T. and Koyama, T., Thermodynamic modeling of the LiCoO2–CoO2 pseudo-binary system, Calphad: Comp. Coupl. Phase Diag. Thermochem., 2011, vol. 35, p. 209. https://doi.org/10.1016/j.calphad.2011.02.006
Deng, Y., Kang, T., Ma, Z., Tan, X., Song, X., Wang, Z., Pang, P., Shu, D., Zuo, X., and Nan, J., Safety influences of the Al and Ti elements modified LiCoO2 materials on LiCoO2/graphite batteries under the abusive conditions, Electrochim. Acta, 2019, vol. 295, p. 703. https://doi.org/10.1016/j.electacta.2018.11.010
Chao, D., Wang, L., Shen, W., and Guo, S., Effects of the lateral sizes and basal plane structure of graphene on the electrochemical properties of LiCoO2, J. Alloys Compd., 2019, vol. 785, p. 557. https://doi.org/10.1016/j.jallcom.2019.01.126
Bezza, I., Luais, E., Ghamouss, F., Zaghriou, M., Tran-van, F., and Sakai, J., LiCoO2 with double porous structure obtained by electrospray deposition and its evaluation as an electrode for lithium-ion batte, J. Alloys Compd., 2019, vol. 805, p. 19. https://doi.org/10.1016/j.jallcom.2019.07.062
Yoon, M., Lee, S., Lee, D., Kim, J., and Moon, J., All-solid-state thin film battery based on well-aligned slanted LiCoO2 nanowires fabricated by glancing angle deposition, Appl. Surf. Sci., 2017, vol. 412, p. 537. https://doi.org/10.1016/j.apsusc.2017.03.268
Yasuharaa, S., Yasuia, S., Teranishib, T., Yoshikawa, Y., Taniyama, T., and Itoh, M., The effects of BaTiO3 nanodots density support on epitaxial LiCoO2 thin-film for high-speed rechargeability, Electrochem. Commun., 2019, vol. 109, p. 106604. https://doi.org/10.1016/j.elecom.2019.106604
Silva, S.P., Sita, L.E., Santos, C.S., and Scarminio, J., Effects on the phases and crystalline structures of LiCoO2 cathode under thermal treatments up to 400°C, J. Alloys Compd., 2019, vol. 810, p.151933. https://doi.org/10.1016/j.jallcom.2019.151933
Meng, Q., Zhang, Y., and Dong, P., A combined process for cobalt recovering and cathode material regeneration from spent LiCoO2 batteries: Process optimization and kinetics aspects, Waste Manage. (Oxford), 2018, vol. 71, p. 372. https://doi.org/10.1016/j.wasman.2017.10.030
Xu, N., Zhoua, H., Liao, Y., Li, G., Xu, M., and Li, W., A facile strategy to improve the cycle stability of 4.45 V LiCoO2 cathode in gel electrolyte system via succinonitrile additive under elevated temperature, Solid State Ionics, 2019, vol. 341, p. 115049. https://doi.org/10.1016/j.ssi.2019.115049
Santosa, C.S., Alvesa, J.C., Silva, S.P., Sita, L.E., Silva, P.R.-C., Almeida, L.C., and Scarminio, J., A closed-loop process to recover Li and Co compounds and to resynthesize LiCoO2 from spent mobile phone batteries, J. Hazard. Mater., 2019, vol. 362, p. 458. https://doi.org/10.1016/j.jhazmat.2018.09.039
Chao, D., Wang, L., Shen, W., and Guo, S., Effects of the lateral sizes and basal plane structure of graphene on the electrochemical properties of LiCoO2, J. Alloys Compd., 2019, vol. 785, p. 557. https://doi.org/10.1016/j.jallcom.2019.01.126
HakanYudar, H., Pat, S., Özen, S., Mohammadigharehbagh, R., Musaoglu, C., Korkmaz, S., and Pat, Z., Microstructural, surface and electrochemical properties of the nano layered LiCoO2 thin film cathode for Li ion battery, Vacuum, 2018, vol. 152, p. 248. https://doi.org/10.1016/j.vacuum.2018.03.043
Wang, F., Jiang, Y., Lin, S., Wang, W., Hu, C., Wei, Y., Mao, B., and Liang, C., High-voltage performance of LiCoO2 cathode studied by single particle microelectrodes influence of surface modification with TiO2, Electrochim. Acta, 2019, vol. 295, p. 1017. https://doi.org/10.1016/j.electacta.2018.09.050
Niemöller, A., Jakesa, P., Eichela, R.-A., and Granwehra, J., In operando EPR investigation of redox mechanisms in LiCoO2, Chem. Phys. Lett., 2019, vol. 716, p. 231. https://doi.org/10.1016/j.cplett.2018.12.022
Hu, S., Wang, C., Zhou, L. Zeng, X., Shao, L., Zhou, J., Zhou, C., Huang, C., Xi, X., and Yang, L., Hydrothermal-assisted synthesis of surface aluminum-doped LiCoO2 nanobricks for high-rate lithium-ion batteries, Ceram. Int., 2018, vol. 44, p. 14995. https://doi.org/10.1016/j.ceramint.2018.05.128
Lim, J., Choi, A., Kim, H., Doo, S.W., Park, Y., and Lee, K.T., In situ electrochemical surface modification for high-voltage LiCoO2 in lithium ion batteries, J. Power Sources, 2019, vol. 426, p. 162. https://doi.org/10.1016/j.jpowsour.2019.04.011
Махонина, Е.В., Первов, В.С., Дубасова, В.С. Оксидные материалы положительного электрода литий-ионных аккумуляторов. Успехи химии. 2004. Т. 73. С. 1075. [Makhonina, E.V., Pervov, V.S., and Dubasova, V.S., Oxide materials as positive electrodes of lithium-ion batteries, Russ. Chem. Rev., 2004, vol. 73, р. 991.] http://doi.org/10.1070/RC2004v073n10ABEH000896.
Porthaul, H., Le Cras, F., and Franger, S., Synthesis of LiCoO2 thin films by sol/gel process, J. Power Sources, 2010, vol. 195, p. 6262. https://doi.org/10.1016/j.jpowsour.2010.04.058
Zhu, C., Yang, C., Yang, W.-D., Hsieh, C.-Y., Ysai, H.-M., and Chen, Y.-S., High performances of ultrafine and layered LiCoO2 powders for lithium batteries by a novel sol-gel process, J. Alloys Compd., 2010, vol. 496, p. 703https://doi.org/10.1016/j.jallcom.2010.02.178
Третьяков, Ю.Д., Мартыненко, Л.И. Григорьев, А.Н., Цивадзе, А.Ю. Неорганическая химия, М.: Химия, Т. I, 2001. С. 378. [Tretyakov, Yu.D., Martynenko, L.I., Grigoriev, A. N., and Tsivadze, A. Yu., Inorganic chemistry (in Russian), Moscow: Chemistry, vol. I, 2001, p. 378–442.]
Levi, M.D. and Aurbach, D., Impedance of a Single Intercalation Particle and of Non-Homogeneous, Multilayered Porous Composite Electrodes for Li-ion Batteries, J. Phys. Chem., 2004, vol. 108, p. 11693. https://doi.org/10.1021/jp0486402
Umeda, M., Dokko, K., Fujita, Y., Mohamedi, M., Uchida, I., and Selman, J.R., Electrochemical impedance study of Li-ion insertion into mesocarbon microbead single particle electrode: Part I. Graphitized carbon, Electrochim. Acta, 2001, vol. 47, p. 885. https://doi.org/10.1016/S0013-4686(01)00799-X
Wang, C., Appleby, A.J., and Little, F.E., Electrochemical impedance study of initial lithium ion intercalation into graphite powders, Electrochim. Acta, 2001, vol. 46, p. 1793. https://doi.org/10.1016/S0013-4686(00)00782-9
Ivanishchev, A.V., Gridina, N.A., Rybakov, K.S., Ivanishcheva, I.A., and Dixit, A., Structural and electrochemical investigation of lithium ions insertion processes in polyanionic compounds of lithium and transition metals, J. Electroanal. Chem., 2020, vol, 860, p. 113894. https://doi.org/10.1016/j.jelechem.2020.113894
Чуриков, А.В., Иванищев, А.В., Иванищева, И.А., Гамаюнова, И.М., Запсис, К.В., Сычева, В.О. Процессы внедрения лития в тонкопленочные литий-оловянные и литий-углеродные электроды. Исследование методом импедансной спектроскопии. Электрохим. энергетика. 2007. № 4(7). С. 169.
Baryshnikov, S., Stukova, E., and Koroleva, E., Dielectric properties of the ferroelectric composite (NaNO2)0.9/(BaTiO3)0.1, Composites Part B, 2014, vol. 66, p. 190. https://doi.org/10.1016/j.compositesb.2014.05.005
Дополнительные материалы отсутствуют.