Электрохимия, 2021, T. 57, № 9, стр. 538-548
Электропроводность стекол системы MgO–V2O5–P2O5
А. А. Расковалов a, *, Н. С. Саетова b, М. И. Власов a, Б. Д. Антонов a
a Институт высокотемпературной электрохимии УрО РАН
Екатеринбург, Россия
b Вятский государственный университет
Киров, Россия
* E-mail: other@e1.ru
Поступила в редакцию 30.11.2020
После доработки 09.03.2021
Принята к публикации 12.03.2021
Аннотация
В работе методом закаливания расплава получены стекла состава xMgO–yP2O5– (100 – x – y)V2O5 с x = 1–5 и y = 5, 10 и 15 мол. %. Аморфное состояние полученных образцов подтверждено методом рентгенофазового анализа. Плотности стекол определены пикнометрическим способом. Введение 1 мол. % оксида магния в состав стекла приводит к резкому снижению плотности, дальнейшее увеличение концентрации оксида магния сопровождается постепенным ростом плотности. Электропроводность стекол измерена двумя методиками: на постоянном токе и с помощью импедансной спектроскопии. Сопоставление результатов измерений позволило сделать вывод об электронной природе проводимости. Температурная зависимость электропроводности стекол линейна в координатах Аррениуса. Для составов с y = 10 и 15 мол. % зависимость электропроводности от содержания оксида магния (x) проходит через максимум при x, равном 1 мол. %. Для построения модели стекла была использована процедура самосборки при помощи метода молекулярной динамики с непостоянным полем сил. Анализ полученных конфигураций показал наличие небольшого максимума концентрации 4-координированного окружения ванадия по ванадию при 1 мол. % содержании MgO в разрезе xMgO–10P2O5–(90 – x)V2O5, что можно рассматривать как одно из объяснений максимума электропроводности.
ВВЕДЕНИЕ
Среди аморфных материалов, обладающих электрической проводимостью, наибольшее распространение получили материалы, в которых в качестве стеклообразующего оксида выступает оксид фосфора. В первую очередь, это обусловлено высокой стеклообразующей способностью оксида фосфора в сочетании как c щелочными оксидами [1–3], так и оксидами металлов с переменной валентностью [4–6]. Наиболее перспективными, с точки зрения электрохимических применений, считаются стекла бинарной системы P2O5–V2O5, благодаря возможности введения оксида ванадия вплоть до 95 мол. %, что позволяет достичь высоких значений проводимости, обусловленной электронным переносом между разновалентными ионами ванадия [6, 7]. Наибольшее распространение получили работы, направленные на получение смешанных проводников за счет введения в состав стекла оксида лития и дальнейшее улучшение свойств полученных стекол путем направленной кристаллизации [8–11]. В то же время почти не уделялось внимания изучению влияния на электропроводность таких стекол добавок других щелочных (M2O) или щелочноземельных оксидов (MO). Большинство работ по данному направлению направлено на изучение свойств стекол бинарных систем с общей формулой xV2O5–(100 – x)MO. Так, в работе [12] исследованы свойства стекол (V2O5)x (SrO)1 –x (0.5 ≤ x ≤ 0.8), электропроводность которых закономерно увеличивалась с ростом доли оксида ванадия. Аналогичная зависимость проводимость от содержания V2O5 наблюдается и в случае систем xBaO–(100 – x)V2O5 и xCaO–(100 – x)V2O5 (x = 30–50 мол. %) [13, 14]. В более широком диапазоне концентраций оксидов щелочноземельных металлов изучены свойства стекол xBaO–(100 – x)V2O5 и xSrO–(100 – x)V2O5 [15]; в диапазоне содержания MO 20–30 мол. % проводимости стекол, содержащих оксиды бария и стронция сопоставимы, однако при дальнейшем увеличении доли MO электропроводность барийсодержащих составов выше. В целом, тенденция уменьшения проводимости по мере роста концентрации MO сохраняется, как и в случае ранее упомянутых систем. Влияние щелочноземельных оксидов (MgO, CaO, SrO, BaO) на свойства стекол xV2O5–(1 – x)RO (x = 50–90 мол. %) изучено в работе [16]. Установлено, что при значении x > 70 мол. % тип щелочноземельного катиона оказывает слабое влияние на электропроводность, и проводимости всех изученных составов сопоставимы. Показано, что MgO-содержащие стекла обладают самой высокой проводимостью среди изученных систем, которая, тем не менее, ниже, чем у традиционных бинарных стекол типа V2O5–P2O5 и V2O5–TeO2. Электропроводность системы уменьшается по мере роста концентрации MgO, что связано с уменьшением числа катионов ванадия в системе. Зависимость электропроводности от типа катиона MO была изучена также для стекол 80V2O5–20MO (MO = Mg, Ca, Sr, Ba) [17] и установлено, что проводимость незначительно снижается в ряду Ba → Sr → Ca → Mg, но ее значения сопоставимы для всех составов, что согласуется с данными работы [16]. В [18] было изучение влияние концентрации MgO на свойства стекол бинарной системы V2– xMgxO5 – δ (x от 0.05 до 0.30) [12], где отмечено уменьшение электропроводности с ростом содержания MgO. Авторы связывают такое поведение с возникновением затруднений в перескоке V4+/V5+ из-за встраивания катионов Mg2+ между ванадий-кислородными структурными единицами.
Также можно выделить ряд работ, в которых изучены тройные системы, содержащие оксиды ванадия и щелочноземельного элемента, а также традиционный стеклообразующий оксид (B2O3 или V2O5). Так, в [19] установлено, что стекла состава xV2O5·40CaO(60 – x)P2O5 (10 ≤ x ≤ 30) являются проводниками p-типа при x = 10 и 15 мол. % и проводниками n-типа при x = 25 и 30 мол. %, а состав с x = 20 мол. % является “переходным” между двумя типами проводимости. Электропроводность стекол системы 60V2O5–40B2O3–(40 – x)BaO (x = 0–40 мол. %) снижается по мере увеличения х [20], что согласуется с результатами работы [16], где показано, что во всех случаях проводимость MO-содержащих составов ниже по сравнению с бинарными системами.
Согласно приведенному обзору, основное внимание уделено изучению свойств бинарных систем V2O5–MO, причем содержание оксидов щелочноземельных элементов во всех случаях не ниже 10 мол. %. Работы же по изучению свойств тройных систем немногочисленны, а максимальная концентрация V2O5 в рассмотренных системах не превышает 60 мол. %. Целью данной работы является рассмотрение влияния небольшой (1–5 мол. %) добавки оксида элемента с постоянной валентностью на электропроводность стекол, обусловленную электронным переносом между катионами с разной валентностью, на примере системы xMgO–yP2O5–(100 – x – y)V2O5. Кроме того, предпринята попытка объяснить наблюдаемое поведение зависимости электропроводности от содержания MgO с помощью анализа простых геометрических зависимостей, таких как среднее координационное число пары V–V. Компьютерные модели структуры стекол, необходимые для такого анализа, были получены методом молекулярной динамики с непостоянным полем сил [21] путем самосборки из расплава, как в нашей предыдущей работе [22]. Подобный анализ позволяет понять, реализуется ли в системе сокращение расстояний V–V и возникают ли более связанные пути переноса электронов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
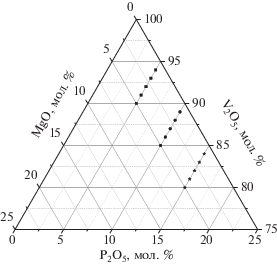
Стекла состава xMgO–yP2O5–(100 – x – y)V2O5 с x = 1–5 и y = 5, 10 и 15 мол. % (рис. 1) получены традиционным методом закаливания расплава. В качестве шихты для получения расплава использовали смесь оксида магния (MgO, “х. ч.”), дигидрофосфата аммония (NH4H2PO4, “х. ч.”) и оксида ванадия (V2O5, “х. ч.”) в соответствующих стехиометрических соотношениях. Полученную смесь помещали в платиновый тигель и выдерживали в печи LOIP LF-5/13-G2 в атмосфере воздуха при температуре 900°C в течение 1 ч, после чего расплав закаливали между двумя стальными пластинами. Стоит отметить, что после закаливания расплава наблюдалось образование тонкой пленки кристаллической фазы в месте соприкосновения расплава с металлической пластиной. Эта пленка удалялась шлифованием поверхности образца.
Аморфность материалов после синтеза была подтверждена методом порошкового рентгенофазового анализа (РФА) на дифрактометре D/Max 2200 (Rigaku, Япония) с CuKα-излучением в диапазоне углов 2θ от 15° до 55°. Определение элементного состава исследуемых материалов проводили методом атомно-эмиссионной спектроскопии (АЭС) с индуктивно-связанной плазмой на спектрометре Optima 4300 DV (Perkin Elmer, США). Общая погрешность определения концентрации элементов не превышала 3 отн. %. Равномерность распределения элементов в объеме стекла была оценена методами растровой электронной микроскопии (РЭМ) и рентгеноспектрального микроанализа (РСМА). Исследования проводились на сломах стекол на микроскопе MIRA 3LMU (TESCAN, Чехия) с системой рентгеновского энергодисперсионного микроанализа INCA Energy 350 X-max 80 (Oxford Instruments, Великобритания). Исследования методами РФА и РЭМ выполнены при комнатной температуре.
Плотности стекол определены методом жидкостной пикнометрии. Измерения были проведены в стандартных пикнометрах объемом 10 мл в среде изопропилового спирта при комнатной температуре. Масса образцов для измерений составляла ~0.2 г. Плотности стекол безмагниевых составов были определены нами ранее [6]. Структура стекол исследовалась методом спектроскопии комбинационного рассеяния света (КРС) на рамановском микроскопе-спектрометре U 1000 (Renishaw, Англия). Спектры КРС регистрировались при комнатной температуре с предварительно отполированной поверхности стекол в диапазоне 4000–50 см–1 со спектральным разрешением 1 см–1 при возбуждении лазерным излучением с длиной волны 532 нм (мощность 5 мВт).
Для определения сопротивления образцов использовались импедансная спектроскопия (ИС) и импульсный гальваностатический метод. Для проведения измерений на предварительно подготовленную поверхность методом электровакуумного напыления наносили тонкий слой платины, используя напылитель Q150T ES (Quorum technologies, Великобритания). Измерения проводились в интервале температур от комнатной до 145°C с использованием потенциостата-гальваностата ZIVE MP2 (WonATech, Южная Корея).
ДЕТАЛИ МОДЕЛИРОВАНИЯ
С помощью численных методов исследован разрез стекол xMgO–10P2O5–(90 – x)V2O5. Построение компьютерной модели стекол выполнено процедурой самосборки [22] с помощью метода молекулярной динамики с непостоянным полем сил [21]. Расчеты проведены в компьютерной программе azTotMD (http://aztotmd.ru) [23], версией для графических процессоров, написанной с использованием технологии CUDA. Для вычислений использовали персональный компьютер с видеокартой GeForce RTX 2080 Ti с тактовой частотой 1650 МГц.
Стартовые конфигурации для процедуры самосборки представляли собой случайно расположенные ионы V5+, P5+, O2– и Mg2+. Процедура выполнена в каноническом (NVT) ансамбле с применением кубических периодических границ. Температура моделирования поддерживалась равной 398 K с помощью термостата Нозе–Гувера. Размеры бокса были определены согласно полученным данным по плотности стекол. Количество частиц каждой системы и ее размеры приведены в табл. 1. Параметры для потенциалов взаимодействия взяты из работ [6, 22], а также из [24] – для пары Mg…O. Чтобы жестко задать длины двойных связей, внутримолекулярные потенциалы V=O и P=O задали в виде гармонического потенциала с константой жесткости 100 эВ/Å2 и равновесным расстоянием 1.62 и 1.42 Å для ванадия и фосфора соответственно.
Таблица 1.
Размеры моделируемых систем: nV5+, nP5+, nMg2+ и nO2– – количества соответствующих ионов в моделируемой системе, Ntot – общее число частиц, a – длина ребра бокса
| x | nV5+ | nP5+ | nMg2+ | nO2– | Ntot | a, Å |
|---|---|---|---|---|---|---|
| 0 | 900 | 100 | 0 | 2500 | 3500 | 36.8 |
| 1 | 890 | 100 | 5 | 2480 | 3475 | 37.8 |
| 2 | 880 | 100 | 10 | 2460 | 3450 | 37.9 |
| 3 | 870 | 100 | 15 | 2440 | 3425 | 38.0 |
| 4 | 860 | 100 | 20 | 2420 | 3400 | 38.4 |
| 5 | 850 | 100 | 25 | 2400 | 3375 | 37.2 |
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Аттестация образцов
Согласно данным РФА (рис. 2), изученные в данной работе составы являются полностью аморфными без каких-либо кристаллических включений. Для удобства на рисунке приведены дифрактограммы “крайних” составов каждого разреза. Для этих же составов в табл. 2 представлены результаты АЭС, согласно которым не наблюдается значительных отклонений от заданной стехиометрии в реальных составах изученных стекол.
Таблица 2.
Результаты атомно-эмиссионной спектроскопии (АЭС) стекол системы xMgO–yP2O5–(100 – x – y)V2O5
| Обозначение состава | Состав, мол. % | P2O5 | V2O5 | MgO |
|---|---|---|---|---|
| 5P2O5–1MgO | Заданный | 5 | 94 | 1 |
| АЭС | 5.66 | 93.41 | 0.93 | |
| 5P2O5–5MgO | Заданный | 5 | 90 | 5 |
| АЭС | 6.17 | 89.49 | 4.34 | |
| 10P2O5–1MgO | Заданный | 10 | 89 | 1 |
| АЭС | 11.89 | 87.06 | 1.05 | |
| 10P2O5–5MgO | Заданный | 10 | 85 | 5 |
| АЭС | 11.08 | 84.85 | 4.06 | |
| 15P2O5–1MgO | Заданный | 15 | 84 | 1 |
| АЭС | 16.84 | 82.26 | 0.90 | |
| 15P2O5–5MgO | Заданный | 15 | 80 | 5 |
| АЭС | 16.87 | 79.02 | 4.11 |
Чтобы установить, происходит ли в системе ликвация и, как следствие, образование неоднородных по составу областей, поверхность слома образцов была исследована методами растровой электронной микроскопии и рентгеноспектрального микроанализа. По результатам РСМА (рис. 3) видно, что распределение элементов в исследованных стеклах однородно, фазового расслоения не наблюдается.
Плотность и структурные особенности стекол
Результаты измерения плотности стекол и их пересчет в мольный объем приведены в табл. 3. При допировании стекол системы yP2O5–(100 –y)V2O5 оксидом магния плотность сначала падает относительно исходного состава, а затем монотонно возрастает, по мере роста содержания оксида магния. Согласно литературным данным [25], при одновременном замещении оксидом натрия и фосфора оксидом магния в системе (50 – x/2)Na2O–xMgO–(50 – x/2)P2O5 наблюдается уменьшение молярного объема и рост плотности, связанные с уплотнением сетки стекла. В системе 30ZnO–xMgO–(70 – x)P2O5 [26] плотность стекол уменьшается по мере замещения оксида фосфора оксидом магния. В стеклах бинарной системы V2– xMgxO5 – δ [12] также наблюдается уменьшение плотности с увеличением содержания MgO. В то же время в системе xMgO–(100 – x)V2O5 (x = 10–40 мол. %) [27] плотность стекол по мере увеличения концентрации MgO колеблется около значения 2.9 г/см3, что близко к нашим значениям.
Таблица 3.
Плотности (ρ) и мольный объем (Vm) исследованных стекол, в сравнении с безмагниевыми составами [6]
| Система | 5P2O5–(95 – x)V2O5–xMgO | 10P2O5–(90 – x)V2O5–xMgO | 15P2O5–(85 – x)V2O5–xMgO | |||
|---|---|---|---|---|---|---|
| X | ρ, г/см3 | Vm, см3/моль | ρ, г/см3 | Vm, см3/моль | ρ, г/см3 | Vm, см3/моль |
| 0 | 3.015 ± 0.002 [6] | 59.65 ± 0.02 [6] | 2.950 ± 0.002 [6] | 60.31 ± 0.02 [6] | 2.943 ± 0.001 [6] | 59.76 ± 0.01 [6] |
| 1 | 2.7 ± 0.1 | 65 ± 3 | 2.7 ± 0.1 | 65 ± 3 | 2.6 ± 0.1 | 67 ± 3 |
| 2 | 2.9 ± 0.2 | 61 ± 3 | 2.7 ± 0.1 | 66 ± 3 | 2.8 ± 0.1 | 62 ± 3 |
| 3 | 2.8 ± 0.2 | 62 ± 5 | 2.6 ± 0.2 | 66 ± 4 | 2.9 ± 0.2 | 58 ± 3 |
| 4 | 3.0 ± 0.2 | 58 ± 3 | 2.5 ± 0.1 | 68 ± 3 | 3.2 ± 0.1 | 54 ± 2 |
| 5 | 3.0 ± 0.1 | 58 ± 2 | 2.8 ± 0.2 | 62 ± 4 | 3.2 ± 0.2 | 52 ± 3 |
Влияние введения оксида магния на строение стекол системы P2O5–V2O5 было изучено с помощью спектроскопии комбинационного рассеяния света. Полученные спектры приведены на рис. 4. Видно, что во всех рассмотренных системах введение магния не оказывает значительного влияния на структуру стекол, можно отметить лишь слабые сдвиги и перераспределения интенсивностей пиков. Позиции пиков и их соотнесение с литературными данными [28–36] приведены в табл. 4. Согласно этим данным, значительная часть наблюдаемых пиков принадлежит колебаниям ванадий-кислородных связей, что вызвано высоким содержанием V2O5 во всех исследованных стеклах. Пик при 145 см–1 указывает на формирование слоистого ванадий-кислородного каркаса, подобного структуре кристаллического V2O5 [37].
Рис. 4.
Спектры комбинационного рассеяния света стекол системы xMgO–yP2O5–(100 – x – y)V2O5 с y, мол. %: 5 (a), 10 (б) и 15 (в).

Рис. 5.
Типичные годографы импеданса стекол системы xMgO–yP2O5–(100 – x – y)V2O5 для стекла состава 1MgO·5P2O5·94V2O5 при разных температурах (а) и для стекол разных составов при температуре 30°C (б).

Таблица 4.
Расшифровка пиков, наблюдаемых на спектрах комбинационного рассеяния света
| Положение пика, см–1 | Тип колебания | Ссылка на источник |
|---|---|---|
| 145 | Межслоевые связи V–O, соединяющие вершины ванадий-кислородных бипирамид | [28] |
| 284–286 | Деформационные колебания связей O–P–O Деформационные колебания связей V–O и P–O |
[29, 30] |
| 404–407 | Деформационные колебания связей O–P–O | [29] |
| 524–530 | Деформационные колебания связей O–P и групп PO4 | [29, 31, 32] |
| 707–709 | Симметричные валентные колебания связей P–O–P | [33] |
| 930 | Колебания связей V–O–V и O–V–O в группах VO4 | [29, 31, 34, 35] |
| 989–992 | Колебания связей V=O в тетрагональных пирамидах VO5 | [33] |
| 1015–1020 | Колебания связей V=O и групп PO3 | [32, 34, 36] |
Интересно отметить, что во всех рассмотренных разрезах увеличение содержания оксида магния сопровождается смещением пика при 404 см–1, соответствующего деформационным колебаниям связей O–P–O, в сторону больших волновых чисел. Это может быть связано с тем, что ионы магния, встраиваясь в сетку стекла, разрывают связи и увеличивают степень деполимеризации сетки. В разрезе 15P2O5–(85 – x)V2O5–xMgO введение даже 1 мол. % оксида магния приводит к исчезновению пика при 930 см–1, соответствующего колебаниям связей в ванадий-кислородных тетраэдрах VO4 и сдвигу его в сторону больших волновых чисел. Это может указывать на изменение доминирующего типа структурных групп в ванадий-кислородной сетке: замещение ванадий-кислородных тетраэдров VO4 тетрагональными пирамидами VO5.
Транспортные свойства
Электрическое сопротивление стекол было измерено двумя способами, методом электрохимического импеданса и на постоянном токе с блокирующими (по Mg2+) электродами. Измерения на постоянном токе были проведены, чтобы исключить возможный вклад магний-ионной проводимости. Типичные годографы импеданса приведены на рис. 5. За величину сопротивления принималась точка пересечения годографа импеданса с осью реальных сопротивлений. Величины электропроводности были рассчитаны из сопротивлений с учетом геометрических размеров образцов. На рис. 6 приведены температурные зависимости электропроводности в координатах Аррениуса, рассчитанные из данных, полученных различными методами. Результаты, полученные разными методами, совпадают в пределах погрешности, что подтверждает предположение об исключительно электронном характере проводимости в исследуемых стеклах. Также стоит отметить, что температурные зависимости, представленные на рис. 6, являются типичными для всех составов системы xMgO–yP2O5–(100 – x – y)V2O5. Они являются линейными в координатах Аррениуса, что указывает на активационный характер проводимости. Из температурных зависимостей проводимости в координатах Аррениуса были рассчитаны значения энергии активации электропроводности (табл. 5).
Рис. 6.
Температурные зависимости электропроводности стекол системы xMgO–yP2O5–(100 – x – y)V2O5 в координатах Аррениуса, полученные на постоянном токе (полые значки) и с помощью импедансной спектроскопии (закрашенные значки).

Таблица 5.
Энергия активации проводимости исследованных стекол, кДж/моль
| x, мол. % | 5P2O5–(95 – x)V2O5–xMgO | 10P2O5–(90 – x)V2O5–xMgO | 15P2O5–(85 – x)V2O5–xMgO |
|---|---|---|---|
| 0 | 36.0 ± 1.8 | 38.0 ± 0.4 | 35.2 ± 2.1 |
| 1 | 33.5 ± 0.5 | 37.6 ± 0.6 | 37.1 ± 0.5 |
| 2 | 36.8 ± 0.1 | 38.7 ± 0.4 | 39.6 ± 0.4 |
| 3 | 34.2 ± 0.5 | 38.6 ± 1.5 | 39.9 ± 0.4 |
| 4 | 38.6 ± 0.4 | 36.9 ± 0.6 | 39.9 ± 0.5 |
| 5 | 38.9 ± 0.7 | 36.6 ± 0.8 | 40.0 ± 0.4 |
Поскольку величины проводимости всех составов довольно близки между собой и изменяются в пределах одного порядка величины, для наглядности изменения проводимости в зависимости от состава и температуры на рис. 7 приведены изотермы проводимости стекол системы xMgO–yP2O5–(100 – x – y)V2O5 при температурах 50, 100 и 145°C. При допировании составов с наименьшим содержанием фосфора (y = 5 мол. %) электропроводность Mg-содержащих стекол в пределах погрешности не превышает проводимость безмагниевого состава (рис. 7а). Для остальных разрезов с постоянным содержанием фосфора (y = 10 и 15 мол. %) наблюдается скачок электропроводности при переходе от недопированного к допированному составу (рис. 7б, 7в). Для всех исследованных разрезов характерно дальнейшее снижение электропроводности с ростом содержания магния, что объясняется уменьшением концентрации ванадия, обеспечивающего электронный перенос в системе. Наиболее заметное увеличение проводимости наблюдается в системе с 10 мол. % оксида фосфора, поэтому для этой системы было проведено численное моделирование, пример полученной конфигурации стекол приведен на рис. 8. Поскольку именно пара ионов V–V отвечает за электронный перенос, для всех моделируемых систем было найдено распределение координационных чисел для этой пары на расстоянии до 3.2 Å и соответствующее распределению среднее координационное число, результаты представлены на рис. 9. Как видно из рисунка, с ростом содержания оксида магния вероятность найти атом ванадия рядом с другим атомом уменьшается, это проявляется и в увеличении доли координационного числа 0 и в уменьшении долей других координаций. Среднее координационное число, соответственно, также падает. Однако, для состава с 1 мол. % MgO наблюдается некоторое увеличение 4-координированного окружения ванадия по ванадию, что, возможно, объясняет увеличение проводимости, за счет более разветвленных путей переноса электронов. В целом же, геометрические соображения не очень убедительно объясняют увеличение электропроводности, и, вероятно, рост ее обусловлен стабилизацией степени окисления V4+, содержание которой в ванадатных системах обычно определяет проводимость [38]. Заметим, что данные по координационным числам V–V в литературе отсутствуют, поскольку относятся ко второй координационной сфере. Координационные числа во второй координационной сфере можно получить, полностью расшифровав структуру вещества, но экспериментально это возможно только для кристаллических тел. С помощью проведенного численного моделирования мы оценили те структурные особенности, которые сложно или даже невозможно установить экспериментально.
Рис. 7.
Изотермы электропроводности стекол системы xMgO–yP2O5–(100 – x – y)V2O5 с содержанием P2O5, мол. %: 5 (a), 10 (б) и 15 (в), в полулогарифмических координатах.

ЗАКЛЮЧЕНИЕ
В ходе работы было изучено влияние введения небольших количеств катионов с постоянной степенью окисления на свойства и строение стекол системы xMgO–yP2O5–(100 – x – y)V2O5 с y = = 5, 10 и 15 мол. %. Исследования методом жидкостной пикнометрии показали, что во всех изученных разрезах плотность стекол уменьшается при введении 1 мол. % MgO. Согласно данным КРС, сетка стекла состоит из ванадатных структурных групп и представляет собой слоистый ванадий-кислородный каркас. Комбинацией постоянно-токовых измерений и метода электрохимического импеданса показано, что электропроводность данных стеклообразных систем обусловлена исключительно переносом электронов. Электропроводность разрезов с y = 10 и 15 мол. % увеличивается при добавлении 1 мол. % MgO. Методом молекулярной динамики показано, что это увеличение сложно объяснить геометрическими факторами. Вероятнее всего, причина роста проводимости заключается в увеличении концентрации четырехвалентного ванадия.
Список литературы
Sokolov, I.A., Tarlakov, Y.P., Ustinov N.Y., and Pronkin, A.A., Structure and electric properties of lithium phosphate glasses, Russ. J. Appl. Chem., 2005, vol. 78, p. 741.
Money, B.K. and Hariharan, K., Lithium ion conduction in lithium metaphosphate based systems, Appl. Phys. A Mater. Sci. Process., 2007, vol. 88, p. 647.
Pakhomov, G.B. and Neverov, S.L., Glasses and supercooled melts in the Li2O–P2O5 system, Solid State Ionics, 1999, vol. 119, p. 235.
Moustafa, Y.M., El-Egili, K., Doweidar, H., and Abbas, I., Structure and electric conduction of Fe2O3–P2O5 glasses, Phys. B: Condensed Matter, 2004, vol. 353, p. 82.
Šantić, A., Moguš-Milanković, A., Furić, K., Bermanec, V., Kim, C.W., and Day, D.E., Structural properties of Cr2O3–Fe2O3–P2O5 glasses, Part I, J. Non-Cryst. Solids, 2007, vol. 353, p. 1070.
Saiko, I.A., Saetova, N.S., Raskovalov, A.A., Il’ina, E.A., Molchanova, N.G., and Kadyrova, N.I., Hopping conductivity in V2O5–P2O5 glasses: experiment and non-constant force field molecular dynamics, Solid State Ionics, 2020, vol. 345, Art. No. 115180.
Pietrzak, T.K., Pawliszak, Ł., Michalski, P.P., Wasiucionek, M., and Garbarczyk, J.E., Highly conductive 90V2O5·10P2O5 nanocrystalline cathode materials for lithium-ion batteries, Procedia Engineering, 2013, vol. 251, p. 78.
Garbarczyk, J.E., Jozwiak, P., Wasiucionek, M., and Nowinski, J.L., Enhancement of electrical conductivity in lithium vanadate glasses by nanocrystallization, Solid State Ionics, 2004, vol. 175, p. 691.
Garbarczyk, J.E., Jozwiak, P., Wasiucionek, M., and Nowinski, J.L., Effect of nanocrystallization on the electronic conductivity of vanadate–phosphate glasses, Solid State Ionics, 2006, vol. 177, p. 2585.
Garbarczyk, J.E., Jozwiak, P., Wasiucionek, M., and Nowinski, J.L., Nanocrystallization as a method of improvement of electrical properties and thermal stability of V2O5-rich glasses, J. Power Sources, 2007, vol. 173, p. 743.
Pietrzak, T.K., Wasiucionek, M., Nowinski, J.L., and Garbarczyk, J.E., Isothermal nanocrystallization of vanadate–phosphate glasses, Solid State Ionics, 2013, vol. 251, p. 78.
Khattak, G.D., Mekki, A., and Siddiqui, M.N., Compositional dependence of DC electrical conductivity of SrO-vanadate glasses, Solid State Ionics, 2012, vol. 211, p. 5.
Al-Hajry, A., Al-Shahrani, A., and El-Desoky, M.M., Structural and other physical properties of barium vanadate glasses, Mater. Chem. Phys, 2006, vol. 95, p. 300.
Tashtoush, N., Qudah, A.M., and El-Desoky, M.M., Compositional dependence of the electrical conductivity of calcium vanadate glassy semiconductors, J. Phys. Chem. Solids, 2007, vol. 68, p. 1926.
Oh, S., Kang, M., Chung, S., Kim, H., Moon, H., and Oh, H., Electrical Properties in Semiconducting SrO–V2O5 and BaO–V2O5 Glasses, J. Korean Phys. Soc., 1997, vol. 31, p. 664.
Sen, S. and Ghosh, A., Polaronic transport properties of some vanadate glasses: Effect of alkali-earth oxide modifiers, Phys. Rev. B., 1999, vol. 60, p. 15143.
Ghosh, A., Sural, M., and Sen, S.J., Phys.: Condens. Matter., 1998, vol. 10, p. 7567.
Khan, S. and Singh, K., Effect of MgO on structural, thermal and conducting properties of V2 –xMgxO5 – δ (x = 0.05–0.30) systems, Cer. Int., 2019, vol. 45, p. 695.
Sharma, B.I. and Srinivasan, A., Electrical properties of V2O5–CaO–P2O5 glasses exhibiting majority charge carrier reversal, J. Mater. Sci., 2005, vol. 40, p. 5125.
El-Desoky, M.M., DC conductivity and hopping mechanism in V2O5–B2O3–BaO glasses, Phys. Stat. Sol. (a), 2003, vol. 195, p. 422.
Raskovalov, A.A., Non-Constant Force Field Molecular Dynamics, in An Introduction to Molecular Dynamics, Kemp M.S., Ed, New York: Nova Science Publishers, Inc., 2019, p. 143.
Саетова, Н.С., Расковалов, А.А., Ильина, Е.А., Антонов, Б.Д., Гржегоржевский, К.В. Структура и электропроводность стекол 30Na2O–xV2O5–(70 – x)B2O3: эксперимент и молекулярная динамика с элементами самосборки. Журн. неорг. химии. 2021. Т. 66. С.325. [Saetova, N.S., Raskovalov, A.A., Il’ina, E.A., Antonov, B.D., and Grzhegorzhevskiy, K.V., Structure and conductivity of 30Na2O–xV2O5–(70 – x)B2O3 glasses: experiment and molecular dynamics with elements of self-assembly, Russ. J. Inorg. Chem., 2021, vol. 66, p. 313.]
Raskovalov, A.A. and azTotMD: Software for non-constant force field molecular dynamics, SoftwareX, 2019, vol. 10, Art. no. 100233.
Pedone, A., Malavasi, G., and Menziani, M.C., Computational insight into the effect of CaO/MgO substitution on the structural properties of phospho-silicate bioactive glasses, J. Phys. Chem. C, 2009, vol. 113, p. 15723.
Omrani, R.O., Kaoutar, A., Jazouli, A.El, Krimi, S., Khattech, I., Jemal, M., Videau, J.-J., and Couzi, M., Structural and thermochemical properties of sodium magnesium phosphate glasses, J. Alloys and Compounds, 2015, vol. 632, p. 766.
Khor, S.F., Talib, Z.A., Daud, W.M., Sidek, H.A.A., and Ng, B.H., Effects of MgO on dielectric properties and electrical conductivity of ternary zinc magnesium phosphate glasses, J. Non-Cryst. Solids, 2009, vol. 355, p. 2533.
Sen, S. and Ghosh, A., Structure and other physical properties of magnesium vanadate glasses, J. Non-Cryst. Solids, 1999, vol. 258, p. 29.
Attos, O., Massot, M., Balkanski, M., Haro-Poniatowski, E., and Asomoza, M., Structure of borovandate glasses studied by Raman spectroscopy, J. Non-Cryst. Solids, 1997, vol. 210, p. 163.
Yadav, A.K. and Singh, P., A Review on structure of glasses by Raman spectroscopy, RSC Advances, 2015, vol. 83, p. 67583.
Bhargava, R.N. and Condrate, R.A., The vibrational spectra of VPO5 crystal phases and related glasses, Appl. Spectroscopy, 1977, vol. 31, p. 230.
Magdas, D.A., Vedeanu, N.S., and Toloman, D., Study on the effect of vanadium oxide in calcium phosphate glasses by Raman, IR and UV–vis spectroscopy, J. Non-Cryst. Solids, 2015, vol. 428, p. 151.
Hejda, P., Holubová, J., Černošek, Z., and Černošková, E., The structure and properties of vanadium zinc phosphate glasses, J. Non-Cryst. Solids, 2017, vol. 462, p. 65.
Chrissanthopoulos, A., Pouchan, C., and Papatheodorou, G.N., Structural investigation of vanadium-sodium metaphosphate glasses, Z. Naturforsch, 2001, Bd 56a, S. 773.
Kerkouri, N., Haddad, M., Et-tabirou, M., Chahine, A., and Laanab, L., FTIR, Raman, EPR and optical absorption spectral studies on V2O5-doped cadmium phosphate glasses, Physica B, 2011, vol. 406, p. 3142.
Lewandowska, R., Krasowski, K., Bacewicz, R., and Garbarczyk, J.E., Studies of silver–vanadate superionic glasses using Raman spectroscopy, Solid State Ionics, 1999, vol. 119, p. 229.
Laorodphan, N., Pooddee, P., Kidkhunthod, P., Kunthadee, P., Tapala, W., and Puntharod, R., Boron and pentavalent vanadium local environments in binary vanadium borate glasses, J. Non-Cryst. Solids, 2016, vol. 453, p. 118.
Lee, S.-H., Cheong, H.M., Seong, M.J., Liua, P., Tracy, C.E., Mascarenhas, A., Pitts, J.R., and Deb, S.K., Raman spectroscopic studies of amorphous vanadium oxide thin films, Solid State Ionics, 2003, vol. 165, p. 111.
Saetova, N.S., Raskovalov, A.A., Antonov, B.D., Yaroslavtseva, T.V., Reznitskikh, O.G., Zabolotskaya, E.V., Kadyrova, N.I., and Telyatnikova, A.A., Conductivity and spectroscopic studies of Li2O–V2O5–B2O3 glasses, Ionics, 2018, vol. 24, p. 1929.
Дополнительные материалы отсутствуют.