Электрохимия, 2022, T. 58, № 2, стр. 66-75
Структура и транспортные характеристики монокристаллических и керамических твердых электролитов ZrO2–Y2O3
Е. Е. Ломонова a, Д. А. Агарков b, c, М. А. Борик a, Г. М. Кораблёва b, А. В. Кулебякин a, И. Е. Курицына b, М. Н. Маякова a, Ф. О. Милович a, d, В. А. Мызина a, Н. Ю. Табачкова a, d, *, Е. И. Чернов e
a Институт общей физики им. А.М. Прохорова РАН
Москва, Россия
b Институт физики твердого тела РАН
Черноголовка, Россия
c Федеральное государственное автономное образовательное учреждение высшего образования
“Московский физико-технический институт (национальный исследовательский университет)”
Долгопрудный, Россия
d Национальный исследовательский технологический университет “МИСиС”
Москва, Россия
e Научно-производственное предприятие “ЭКОН”
Обнинск, Россия
* E-mail: ntabachkova@gmail.com
Поступила в редакцию 20.11.2020
После доработки 21.08.2021
Принята к публикации 31.08.2021
- EDN: RZOMTK
- DOI: 10.31857/S0424857022020074
Аннотация
Методом направленной кристаллизации расплава выращены монокристаллы твердых растворов (ZrO2)1– x(Y2O3)x (x = 0.08–0.12). Исследовано влияние концентрации стабилизирующего оксида Y2O3 на транспортные характеристики монокристаллических твердых растворов на основе ZrO2. Показано, что в исследуемом диапазоне составов, максимальной электропроводностью обладают кристаллы (ZrO2)0.91(Y2O3)0.09. Кристаллы данного состава измельчали и полученный порошок использовали в качестве исходного материала для изготовления керамических образцов методом шликерного литья на движущуюся подложку. Размер зерен керамических образцов составлял 10 – 30 мкм, а плотность – 5.86 г/см2. Проведен сравнительный анализ структуры и электрофизических свойств керамических и монокристаллических образцов твердых электролитов (ZrO2)0.91(Y2O3)0.09. Показано, что используемый метод получения керамических образцов не приводит к изменению фазового состава и кристаллической структуры керамики. Значения ионной проводимости монокристаллов и керамики из плавленого материала в области температур 973–1173 К были близки и составляли при температуре 1173 К 0.076 и 0.065 См/см соответственно.
ВВЕДЕНИЕ
Материалы на основе диоксида циркония являются твердыми электролитами и широко используются в датчиках кислорода в разных средах, в кислородных насосах и в твердооксидных топливных элементах [1–6]. К этим материалам предъявляются требования высокой ионной проводимости и стабильности характеристик при рабочих температурах в сочетании с химической инертностью как в окислительной, так и в восстановительной атмосфере. Технология производства этих материалов должна обеспечивать возможность получения механически прочных и плотных мембран с малой толщиной и большой площадью, а также изделий сложной формы. Как правило, в таких устройствах используются поликристаллические материалы. Для керамической технологии практически нет ограничений для изготовления изделий разной формы и размеров. Однако хорошо известно, что величина электропроводности керамических твердых электролитов на основе диоксида циркония может сильно различаться в зависимости от метода их изготовления [7–24]. Причинами этого могут быть различия в микроструктуре материала, содержании примесей и термической предыстории материала, связанной с процессом его получения.
Зависимость электропроводности от микроструктуры обусловлена разницей свойств объема зерна и межзеренного пространства – межзеренных границ [7–14, 18–45 ] и их соотношением в структуре материала. Кроме того, в материале могут присутствовать поры и легирующие добавки, способствующие лучшему спеканию. В [16] показано увеличение электрической проводимости с уменьшенным размером зерна для Zr0.84Ca0.16O1.84 при температурах ниже 800°C. Однако переход к наноразмерной зеренной структуре твердых электролитов на основе ZrO2 не всегда приводит к однозначному увеличению проводимости. Так, в образцах ZrO2–Y2O3 с размером зерен ~40 нм повышения проводимости по сравнению с микрокристаллическими образцами аналогичного состава не наблюдалось [44]. Исследования электропроводности микро- и наноструктурированной керамики ZrO2–Y2O3 показали, что электропроводность границ зерен на 2–3 порядка меньше, чем электропроводность объема кристаллического зерна [24–33, 38–40]. Соответственно, энергия активации электропроводности границ раздела составляла ~1.0–1.2 эВ, и была выше, чем значения 0.84–0.93 эВ, характерные для проводимости зерен [39, 40, 43].
Наличие примесей в исходных материалах также влияет на транспортные характеристики твердых электролитов. Например, примесь оксида кремния значительно уменьшает межзеренную проводимость диоксида циркония [24, 38, 40–43]. Добавление всего 0.2 мас. % кремнезема приводило к уменьшению зернограничной проводимости ZrO2–Y2O3 в 15 раз [43]. Введение небольшого количества Al2O3 увеличивает межзеренную проводимость ZrO2–Y2O3, однако может снижать объемную проводимость зерна [45].
Высокое удельное сопротивление границ зерен в керамике с низким содержанием примесей объясняют существованием пространственного заряда, уменьшением концентрации кислородных вакансий и дефектов на границах зерен [4, 24, 39, 40, 46–50].
При достаточно высоких температурах сопротивление границ зерен незначительно отличается от объемного сопротивления зерна, однако в низкотемпературной области эта разница становится значительной. Поэтому влияние границ зерен на ионную проводимость электролита особенно важно для низкотемпературных применений.
Таким образом, на электропроводность границ зерен может оказывать влияние наличие посторонних примесей, разница в концентрациях введенных примесей в зерне и межзеренных областях, сегрегация второй фазы, наличие пространственного заряда, наличие микротрещин, а также комбинация всех этих факторов.
Материалы на основе диоксида циркония могут быть получены также методом кристаллизации расплава в холодном тигле [17, 51, 52]. Электропроводность монокристаллов в отличие от керамики зависит только от исходного состава и условий кристаллизации. Достоинствами метода является высокая технологичность, быстрый синтез твердых растворов в расплаве из исходных оксидов и наличие оборудования, позволяющего в одном технологическом цикле получать до нескольких сот килограмм монокристаллов в течение 24 ч. На стенках и дне водоохлаждаемого разрезного трубчатого медного контейнера при плавлении образуется гарниссажный поликристаллических слой, который предупреждает контакт расплава с трубками и имеет тот же состав, что и состав расплава. Поэтому зарождение монокристаллов является гетерогенным и многоцентровым. Конструкция холодного контейнера не предусматривает каких-либо специальных приспособлений, ограничивающих число растущих кристаллов, подобных тем, которые используют в горячих тиглях. В результате процесса кристаллизации получается слиток, состоящий из столбчатых монокристаллов, количество и размеры которых зависят от многих параметров (состава исходного расплава, режимов наплавления, кристаллизации и т.д.). Высокие температуры плавления ~3000°С способствуют очистке расплава от легко летучих примесей, а наличие гарниссажного слоя способствует высокой чистоте расплава, который не загрязняется материалом “тигля”. Кроме того, при направленной кристаллизации происходит очистка кристаллов от ряда примесей, таких как оксиды кремния, алюминия, титана, вольфрама, молибдена и т.д., которые оттесняются в верхнюю часть расплава [17, 51, 52]. Однако применение монокристаллических материалов в качестве твердых электролитов в электрохимических устройствах ограничено сложными формами датчиков и большими размерами электролитических мембран. Хотя технически это решаемая задача, но существенным ограничением в настоящее время является достаточно дорогая механическая обработка монокристаллов.
Цель настоящей работы – определить влияние концентрации стабилизирующего оксида Y2O3 на транспортные характеристики монокристаллических твердых растворов на основе ZrO2. Другими целями являлось получить керамические твердые электролиты, используя в качестве исходного материала порошок, приготовленный из плавленого материала, и провести сравнительный анализ структуры и электрофизических свойств монокристаллических и керамических образцов твердых электролитов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез монокристаллов твердого раствора (ZrO2)1 –x(Y2O3)x (x = 0.08–0.12) был проведен методом направленной кристаллизации расплава в холодном контейнере. В качестве исходного сырья использовали оксиды марки “ос. ч.” с содержанием основного вещества не менее 99.96 вес. %. Исходные оксиды циркония и иттрия механически перемешивали, загружали в водоохлаждаемый трубчатый контейнер и плавили с помощью прямого высокочастотного нагрева. Частота генератора составляла 5.28 МГц, мощность – 60 кВт. Для стартового плавления использовали металлический цирконий. В результате кристаллизации расплава в холодном контейнере получали слиток, состоящий из отдельных монокристаллов.
Часть кристаллов измельчали и полученный порошок использовали в качестве исходного материала для изготовления керамических образцов. Измельчение проводили в барабане, футерованном стабилизированным диоксидом циркония, с мелющими телами из того же материала. Для изготовления керамики использовали порошок с размером частиц менее 40 мкм и с удельной поверхностью около 8000 см2/г. Керамические образцы получали методом шликерного литья тонкой пленки на движущуюся подложку на оригинальной установке, изготовленной на предприятии “ЭКОН”. Из полученной пленки вырезали заготовки заданных размеров. Полученные заготовки отжигали при температуре 1680°С в течение 2 ч на воздухе.
Фазовый анализ керамики и монокристаллов осуществляли методом рентгеновской дифрактометрии на дифрактометре Bruker D8 на СuKα-излучении, а также методом спектроскопии комбинационного рассеяния света (КРС), используя в качестве источника возбуждения лазер с длиной волны 633 нм. Плотность определяли методом гидростатического взвешивания на приборе для гидростатического взвешивания фирмы “Сарториус”. Исследования микроструктуры образцов проводили на сканирующем электронном микроскопе JEOL 5910 LV с энергодисперсионной приставкой INCA Energy.
Измерения проводимости монокристаллических и керамических образцов проводили в температурном интервале 300‒900°С с использованием анализатора частотных характеристик Solartron SI 1260 в частотном интервале 1 Гц‒5 МГц с амплитудой переменнотокового сигнала 24 мВ. Для измерений были использованы пластины площадью 7 × 7 мм2 и толщиной 0.5 мм. Для формирования токовых контактов на противоположные стороны кристаллов наносили платиновую пасту, которую вжигали при температуре 950°С в течение часа на воздухе. Обработку импедансных спектров осуществляли с помощью программы ZView (ver. 2.8). Удельную проводимость кристаллов рассчитывали из данных, полученных при обработке импедансных спектров, с учетом геометрических размеров образцов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Методом направленной кристаллизации в холодном контейнере были выращены монокристаллы ZrO2, стабилизированные 8, 9, 10, 11 и 12 мол. % Y2O3, обозначенные далее по тексту как 8YSZ, 9YSZ, 10YSZ, 11YSZ и 12YSZ соответственно. Все кристаллы были прозрачными и имели столбчатую форму, характерную для кристаллов диоксида циркония, полученных данным методом.
Фазовый состав кристаллов приведен в табл. 1. Для оценки фазовой устойчивости кристаллов к механическим воздействиям анализ фазового состава проводили на кристаллах и на порошках, приготовленных из кристаллов.
Таблица 1.
Фазовый состав и параметры кристаллической структуры кристаллов ZrO2–Y2O3
| Образец | Фазовый состав* | Пространственная группа симметрии | Параметры решетки, Å | |
|---|---|---|---|---|
| кристаллы | порошки | |||
| 8YSZ | с | c t |
Fm3m P42/nmc |
а = 5.138 ± 0.001 а = 3.633 ± 0.002 c = 5.143 ± 0.002 |
| 9YSZ | с | с | Fm3m | а = 5.141 ± 0.001 |
| 10YSZ | с | с | Fm3m | а = 5.144 ± 0.001 |
| 11YSZ | с | с | Fm3m | а = 5.147 ± 0.001 |
| 12YSZ | с | с | Fm3m | а = 5.149 ± 0.001 |
Все исследуемые монокристаллы твердых растворов ZrO2–Y2O3 имели кубическую структуру типа флюорита. Исследование фазового состава порошков, приготовленных из кристаллов, показало, что фазовый состав твердых растворов после истирания кристаллов не меняется, за исключением образца кристалла 8YSZ. Порошок, приготовленный из кристаллов 8YSZ, содержал смесь кубической и тетрагональной модификаций ZrO2. Таким образом, легирование ZrO2 8 мол. % Y2O3 позволяет стабилизировать в твердом растворе высокотемпературную кубическую фазу, однако кубическая модификация в данных кристаллах является нестабильной и при механическом воздействии может испытывать кубическо-тетрагональный фазовый переход.
Анализ фазового состава кристаллов проводили также методом комбинационного рассеяния света. На рис. 1 приведены спектры КРС кристаллов.
В спектрах КРС кристаллов 11YSZ и 12YSZ присутствуют только линии, характерные для кубической фазы. В спектрах КРС кристаллов 8YSZ, 9YSZ и 10YSZ, кроме линий кубической фазы, присутствует линия ~480 см–1, являющаяся характерной для тетрагональной t″-фазы [53–57]. Эта фаза имеет степень тетрагональности с/√2а = 1, но принадлежит пространственной группе симметрии P42/nmc из-за смещения ионов кислорода в анионной подрешетке [54]. Таким образом, кристаллы 8YSZ, 9YSZ и 10YSZ являются псевдокубическими и имеют структуру t″-фазы.
На рис. 2 приведены температурные зависимости удельной электропроводности кристаллов ZrO2–Y2O3 и зависимость электропроводности твердых растворов от концентрации Y2O3 при 1173 K.
Рис. 2.
Температурная зависимость удельной электропроводности (а) кристаллов 8YSZ (1), 9YSZ (2), 10YSZ (3), 11YSZ (4) и 12YSZ (5) и зависимость электропроводности твердых растворов от концентрации Y2O3 при 1173 K (б).
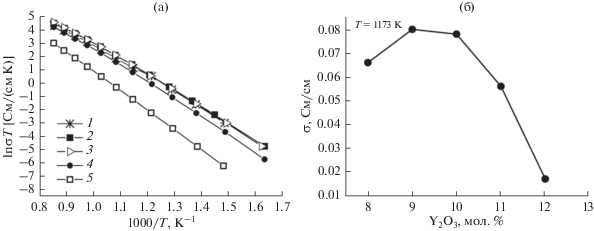
Из исследуемого диапазона составов наибольшей проводимостью во всем температурном интервале обладали кристаллы 9YSZ. Как следует из данных, приведенных на рис. 2б, при увеличении концентрации Y2O3 удельная электропроводность меняется немонотонно. При увеличении концентрации Y2O3 от 8 до 9 мол. % электропроводность увеличивается, и для кристаллов 9YSZ наблюдается слабовыраженный максимум проводимости. При увеличении концентрации Y2O3 до 10 мол. % значения проводимости изменяются незначительно. Но при дальнейшем увеличении концентрации Y2O3 проводимость твердых растворов уменьшается.
В качестве исходного материала для изготовления керамических образцов, из исследуемого диапазона составов были выбраны кристаллы, содержащие 9 мол. % Y2O3, поскольку они имели максимальную проводимость.
На рис. 3 приведено изображение микроструктуры керамического образца 9YSZ, полученного методом шликерного литья на движущуюся подложку.
Керамические образцы 9YSZ имели плотность ~5.86 г/см2, величина которой составляла 98% от плотности беспористых монокристаллов того же состава (~5.98 г/см2). Размеры зерен в полученных образцах варьировались от 10 до 30 мкм. Методом энергодисперсионного анализа в объеме и по границам зерен было обнаружено наличие оксида алюминия. На рис. 4 приведено изображение отдельных зерен в образце 9YSZ и спектры энергодисперсионного анализа в объеме и на границе зерна. Если в объеме зерен концентрация Al2O3 не превышала 0.5 мол. %, то по границам зерен концентрация Al2O3 была существенно выше и в отдельных участках достигала 3 мол. %.
Рис. 4.
Изображение отдельных зерен в керамическом образце 9YSZ и спектры энергодисперсионного анализа в объеме и на границе зерен.

Вероятно, наличие оксида алюминия в керамических образцах связано с термообработкой заготовок после шликерного литья, которая проводилась в закрытых тиглях из оксида алюминия.
Исследование влияния оксида алюминия на транспортные характеристики керамического твердого электролита было проведено в работах [58–62]. Показано, что, как правило, Al2O3 скапливается на границах зерен, поскольку растворимость Al2O3 в ZrO2 очень низкая.
По данным фазового анализа, получение керамических образцов 9YSZ из кристаллов не привело к изменению фазового состава. На рис. 5 приведены спектры КРС моно- и поликристаллического образцов 9YSZ. Для керамических образцов спектр КРС близок к спектру КРС монокристалла аналогичного состава. В спектре присутствует линия ~480 см–1, характерная для псевдокубической структуры t″-фазы. По данным рентгеновской дифрактометрии, параметр решетки керамического образца 9YSZ меньше, чем параметр решетки монокристалла. Это может быть связано с вхождением оксида алюминия в твердый раствор ZrO2–Y2O3.
Для определения объемной, зернограничной и общей проводимости образцов использовали данные, полученные при обработке импедансных спектров. Величину объемного сопротивления кристаллов (Rb) рассчитывали в рамках модели эквивалентной электрической цепи: (Rb– CPEb)(Relectrode– – CPEelectrode) при низких температурах 300–450°С, а для поликристаллов величину объемного сопротивления рассчитывали в рамках модели эквивалентной электрической цепи: (Rb– ‒ CPEb)(Rgb– CPEgb)(Relectrode – CPEelectrode) и LRb(Relectrode – CPEelectrode) в интервале высоких температур 450–900°С для кристаллов и поликристаллов, где Relectrode – сопротивление границы электрод/электролит, CPEelectrode – элемент постоянной фазы, характеризующий процессы на электродном интерфейсе, Rgb – сопротивление границ зерен, CPEgb – элемент постоянной фазы, характеризующий процессы на границах зерен, L – индуктивность токоподводов.
На рис. 6 приведены типичные спектры импеданса, полученные при температуре 691 K для монокристаллического и керамического образца 9YSZ.
Рис. 6.
Спектры импеданса для монокристаллического (1) и керамического (2) образца кристалла 9YSZ при температуре 691 K.
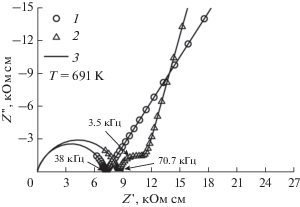
Спектры импеданса для керамических образцов состоят из хорошо разделенных трех частей при низких температурах: первый высокочастотный полукруг представляет объемное сопротивление керамики диоксида циркония, второй полукруг в интервале промежуточных частот связан с эффектом сопротивления внутренних границ зерен, а дуга в низкочастотной области описывает поляризационное сопротивление электродов. В спектрах импеданса монокристалла можно видеть только две области: полукруг в высокочастотной части спектра, который описывает объемное сопротивление кристалла, и дуга в низкочастотной области, характеризующая поляризационное сопротивление электродов.
Объемная проводимость (σb) была определена по формуле (1), а полная проводимость (σtotal) керамических образцов была рассчитана с учетом общего сопротивления, равного сумме объемного и зернограничного сопротивлений [10]:
где L – толщина образца, А – его площадь.Расчет величины зернограничной проводимости (σgb) для керамики проведен с использованием следующего уравнения [10]:
(2)
${{\sigma }_{{{\text{gb}}}}} = \frac{{{{C}_{{\text{b}}}}}}{{{{C}_{{{\text{gb}}}}}}}\frac{L}{{{{R}_{{{\text{gb}}}}}A}},$На рис. 7 в аррениусовских координатах приведены температурные зависимости удельной объемной проводимости монокристаллического и керамического образцов, а также температурные зависимости удельной объемной, зернограничной и общей проводимости керамического образца.
Рис. 7.
Температурные зависимости удельной объемной проводимости монокристаллического (1) и керамического (2) образцов (а). Температурные зависимости удельной объемной (1), общей (2) и зернограничной (3) проводимости керамического образца 9YSZ (б).
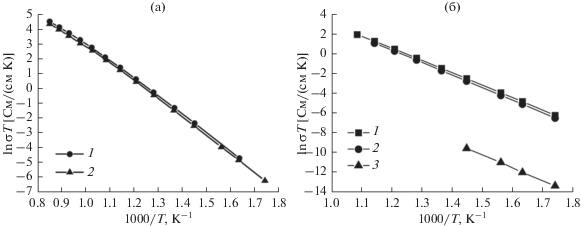
Для исследованных керамических образцов проводимость зерна была намного выше (в ~103 раз), чем проводимость границ зерен при температурах измерения от 575 до 690 К, что согласуется с разницей проводимости зерен и границ зерен для керамики 8YSZ, приведенной в [10].
Данные разных исследований [10, 23, 24, 39, 40] показывают, что удельное сопротивление границ зерен часто на несколько порядков выше, чем объемное сопротивление. Границы зерен ZrO2 проявляют блокирующий эффект в отношении ионного транспорт через них. Перенос носителей заряда через границы зерен происходит только через межзеренные контакты, свойства которых определяются слоем пространственного заряда. Этот блокирующий эффект является “внутренним” по своей природе и заметен только в материалах высокой чистоты. В работе [40] была предложена модель дефектной структуры границы зерен для легированного ZrO2, в которой имеет место обеднение кислородных вакансий и обогащение легирующей примесью в слое пространственного заряда. Было показано для материалов на основе ZrO2 с высокой степенью чистоты удельное сопротивление границы зерна на два-три порядка выше, чем сопротивление объема зерна за счет блокирующего эффекта пространственного заряда, который обеднен кислородными вакансиями. Энергия активации для удельного сопротивления границы зерна определяется свойствами слоя пространственного заряда. Эффект блокирования более выражен при низких температурах.
В керамических образцах 9YSZ за счет увеличения сопротивления границ зерен снижается общая проводимость материала. Общая проводимость керамики в диапазоне температур 600–700 К (1 × 10–5–1 × 10–4 См/см) в 1.5 раза ниже, чем проводимость монокристаллов (1.5 × 10–5–1.4 × × 10–4 См/см). При увеличении температуры разница в значениях удельной проводимости кристаллов и керамики из плавленого материала уменьшается из-за снижения влияния границ зерен на величину проводимости материалов [24]. Следует отметить близость значений ионной проводимости монокристаллов и керамики из плавленого материала в области температур 973–1173 К. Так при температуре 1173 К удельная электропроводность монокристалла составляет 0.086 См/см, а для керамики она слегка ниже 0.065 См/см. Снижение объемной проводимости зерна по сравнению с монокристаллами может быть вызвано вхождением в состав твердого раствора небольшого количества оксида алюминия. Как отмечено в работе [53], вхождение оксида алюминия всегда снижает удельную электропроводность твердых растворов на основе диоксида циркония. Это связано с увеличением числа комплексов трехвалентных катионов Al3+ с кислородными вакансиями и уменьшением концентрации свободных кислородных вакансий, являющихся носителями заряда для ионной проводимости. Образование дефектных комплексов при добавлении Al2O3 отвечает за увеличение энергии активации для объемной удельной электропроводности. Так энергия активации электропроводности в области температур 973–1173 К для кристаллов и керамики была практически одинаковой и составляла 0.87 эВ, а в области температур 600–750 К энергия активации электропроводности для монокристалла составляла 1.07 эВ, а для зернограничной проводимости 1.24 эВ.
ЗАКЛЮЧЕНИЕ
Методом направленной кристаллизации расплава выращены монокристаллы твердых растворов (ZrO2)1 –x(Y2O3)x (x = 0.08–0.12). Исследовано влияние концентрации стабилизирующего оксида Y2O3 на фазовый состав и транспортные характеристики монокристаллических твердых растворов на основе ZrO2. Показано, что в исследованном диапазоне составов, при концентрации стабилизирующего оксида Y2O3 ≤ 10 мол. % кристаллы имеют псевдокубическую структуру t''‑фазы. При концентрации Y2O3 > 10 мол. % кристаллы обладали кубической флюоритовой структурой. По данным рентгеновской дифрактометрии, фазовый состав кристалла (ZrO2)0.92(Y2O3)0.08 неустойчив, и при механическом воздействии в данных материалах наблюдали образование тетрагональной фазы.
Показано, что максимальной электропроводностью обладали кристаллы (ZrO2)0.91(Y2O3)0.09. Кристаллы данного состава измельчали и полученный порошок использовали в качестве исходного материала для изготовления керамических образцов методом шликерного литья на движущуюся подложку. Плотность полученных керамических образцов (ZrO2)0.91(Y2O3)0.09 составляла 98% от плотности монокристаллов. Размеры зерен в полученных образцах варьировались от 10 до 30 мкм. Методом энергодисперсионного анализа было обнаружено наличие оксида алюминия в объеме и по границам зерен.
Проведен сравнительный анализ структуры и электрофизических свойств керамических и монокристаллических образцов твердых электролитов (ZrO2)0.91(Y2O3)0.09. Показано, что используемый метод получения керамических образцов не приводит к изменению фазового состава и кристаллической структуры керамики. Значения ионной проводимости монокристаллов и керамики из плавленого материала в области температур 973–1173 К были близки и составляли при температуре 1173 К 0.076 и 0.065 См/см соответственно.
Список литературы
Goodenough, J.B., Oxide-ion electrolytes, Annu. Rev. Mater. Res., 2003, vol. 33, p. 91.
Kharton, V.V., Marques, F.M.B., and Atkinson, A., Transport properties of solid oxide electrolyte ceramics: A brief review, Solid State Ionics, 2004, vol. 174, p. 135.
Kilner, J.A. and Steele, B.C.H., Nonstoichiometric Oxides, N.Y.: Academic Press, 1981. p. 233.
Yamamoto, O., Solid oxide fuel cells: fundamental aspects and prospects, Electrochim. Acta, 2000, vol. 45, nos. 15–16, p. 2423.
Wachsman, E.D. and Lee, K.T., Lowering the temperature of solid oxide fuel cells, Science, 2011, vol. 334, p. 935.
Han, F., Mücke, R., Gestel, T.V., Leonide, A., Menzler, N.H., Buchkremer, H.P., and Stöver, D., Novel high-performance solid oxide fuel cells with bulk ionic conductance dominated thin-film electrolytes, J. Power Sources, 2012, vol. 218, p. 157.
Omar, S., Belda, A., Escardino, A., and Bonanos, N., Ionic conductivity ageing investigation of 1Ce10ScSZ in different partial pressures of oxygen, Solid State Ionics, 2010, vol. 184, p. 2.
Jasper, A., Kilner, J.A., and McComb, D.W., TEM and impedance spectroscopy of doped ceria electrolytes, Solid State Ionics, 2008, vol. 179, nos. 21–26, p. 904.
Jais, A.A., Ali, S.A.M., Anwar, M., Somalu, M.R., Muchtar, A., Isahak, W.N.R.W., Tan, C.Y., Singh, R., and Brandon, N.P., Enhanced ionic conductivity of scandia-ceria-stabilized-zirconia (10Sc1CeSZ) electrolyte synthesized by the microwave-assisted glycine nitrate process, Ceram. International, 2017, vol. 43, no. 11, p. 8119.
Zhang, J., Lenser, C., Menzler, N.H., and Guillon, O., Comparison of solid oxide fuel cell (SOFC) electrolyte materials for operation at 500°C, Solid State Ionics, 2020, vol. 344, p. 115138.
Yeh, T.-H., Hsu, W.-C., and Chou, C.-C., Mechanical and electrical properties of ZrO2 (3Y) doped with RENbO4 (RE = Yb, Er, Y, Dy, YNd, Sm, Nd), J. Phys. IV France, 2005, vol. 128, p. 213.
Kumar, A., Jaiswa, A., Sanbui, M., and Omar, S., Oxygen-ion conduction in scandia-stabilized zirconia-ceria solid electrolyte (xSc2O3–1CeO2–(99 – x)ZrO2, 5 ≤ x ≤ 11), J. Amer. Ceram. Soc., 2016, vol. 100, p. 659.
Lee, D.-S., Kim, W.S., Choi, S.H., Kim, J., Lee, H.-W., and Lee, J.-H., Characterization of ZrO2 co-doped with Sc2O3 and CeO2 electrolyte for the application of intermediate temperature SOFCs, Solid State Ionics, 2005, vol. 176, no. 1–2, p. 33.
Chen, X.J., Khor, K.A., Chan, S.H., and Yu, L.G., Influence of microstructure on the ionic conductivity of yttria-stabilized zirconia electrolyte, Materials Science and Engineering: A, 20002, vol. 335, no. 1–2, p. 246.
Abbas, H.A., Argirusis, C., Kilo, M., Wiemhöfer, H.-D., Hammad, F.F., and Hanafi, Z.M., Preparation and conductivity of ternary scandia-stabilised zirconia, Solid State Ionics, 2011, vol. 184, no. 1, p. 6.
Tien, T.Y., Grain boundary conductivity of Zr0.84Ca0.16O1.84 ceramics, J. Appl. Phys., 1964, vol. 35, p. 122.
Osiko, V.V., Borik, M.A., and Lomonova, E.E., Handbook of Crystal Growth, Berlin: Springer, 2010. p. 433.
Spirin, A., Ivanov, V., Nikonov, A., Lipilin, A., Paranin, S., Khrustov, V., and Spirina, A., Scandia-stabilized zirconia doped with yttria: synthesis, properties, and ageing behavior, Solid State Ionics, 2012, vol. 225, p. 448.
Omar, S., Najib, W.B., Chen, W., and Bonanos, N., Electrical conductivity of 10 mol % Sc2O3–1 mol % M2O3–ZrO2 ceramics, J. Amer. Ceram. Soc., 2012, vol. 95, no. 6, p. 1965.
Rocha, R.A., Muccillo, E.N.S., Dessemonda, L., and Djurado, E., Thermal ageing of nanostructured tetragonal zirconia ceramics: characterization of interfaces, J. Europ. Ceram. Soc., 2010, vol. 30, p. 227.
Araki, W., Koshikawa, T., Yamaji, A., and Adachi, T., Degradation mechanism of scandia-stabilised zirconia electrolytes: discussion based on annealing effects on mechanical strength, ionic conductivity, and Raman spectrum, Solid State Ionics, 2009, vol. 180, nos. 28–31, p. 1484.
Hirano, M., Watanabe, S., Kato, E., Mizutani, Y., Kawai, M., and Nakamura, Y., High electrical conductivity and high fracture strength of Sc2O3-doped zirconia ceramics with submicrometer grains, J. Amer. Ceram. Soc., 1999, vol. 82, no. 10, p. 2861.
Irvine, J.T.S., Sinclair, D.C., and West, A.R., Electroceramics: Characterization by impedance spectroscopy, Adv. Mater., 1990, vol. 2, no. 3, p. 132.
Hui, S.R., Roller, J., Yick, S., Zhang, X., Decés-Petit, C., Xie, Y., Maric, R., and Ghosh, D., A brief review of the ionic conductivity enhancement for selected oxide electrolytes, J. Power Sources, 2007, vol. 172, no. 2, p. 493.
Kilo, M., Taylor, M.A., Argirusis, C., Borchardt, G., Lesage, B., Weber, S., Scherrer, S., Scherrer, H., Schroeder, M., and Martin, M., Cation self-diffusion of 44Ca, 88Y and 96Zr in single crystalline calcia- and yttria-doped zirconia, J. Appl. Phys., 2003, vol. 94, no. 12, p. 7547.
Chevalier, J., Gremillard, L., Virkar, A.V., and Clarke, D.R., The tetragonal-monoclinic transformation in zirconia: lessons learned and future trends, J. Amer. Ceram. Soc., 2009, vol. 92, no. 9, p. 1901.
Aktas, B., Tekeli, S., and Kucuktuvek, M., Electrical conductivity of Er2O3-doped c-ZrO2 ceramics, J. Mater. Engineering and Performance, 2014, vol. 23, no. 1, p. 349.
Cheikh, A., Madani, A., Touati, A., Boussetta, H., and Monty, C., Ionic conductivity of zirconia based ceramics from single crystals to nanostructured polycrystals, J. Europ. Ceram. Soc., 2001, vol. 21, nos. 10–11, p. 1837.
Aoki, M., Chiang, Y.-M., Kosacki, I., Lee, L.J.-R., Tuller, H., and Liu, Y., Solute segregation and grain-boundary impedance in high-purity stabilized zirconia, J. Amer. Ceram. Soc., 1996, vol. 79, no. 5, p. 1169.
Shukla, S., Seal, S., Vij, R., and Bandyopadhyay, S., Reduced activation energy for grain growth in nanocrystalline yttria-stabilized zirconia, Nano Letters, 2003, vol. 3, no. 3, p. 397.
Mondal, P., Klein, A., Jaegermann, W., and Hahn, H., Enhanced specific grain boundary conductivity in nanocrystalline Y2O3-stabilized zirconia, Solid State Ionics, 1999, vol. 118, no. 3–4, p. 331.
Choen, K.-W., Chen, J., and Xu, R., Metal–organic vapor deposition of YSZ electrolyte layers for solid oxide fuel cell applications, Thin Solid Films, 1997, vol. 304, nos. 1–2, p. 106.
Liaw, B.Y. and Weppner, W., Low temperature limiting-current oxygen sensors based on tetragonal zirconia polycrystals, J. Electrochem. Soc., 1991, vol. 138, no. 8, p. 2478.
Brett, D.J.L., Atkinson, A., Brandon, N.P., and Skinner, S.J., Intermediate temperature solid oxide fuel cells, Chem. Soc. Rev., 2008, vol. 37, p. 1568.
Badwal, S.P.S. and Drennan, J., The effect of thermal history on the grain boundary resistivity of Y-TZP materials, Solid State Ionics, 1988, vol. 28–30, p. 1451.
Ye, F., Mori, T., Ou, D.R., Takahashi, M., Zou, J., and Drennan, J., Ionic conductivities and microstructures of ytterbium-doped ceria, J. Electrochem. Soc., 20007, vol. 154, no. 2, p. B180.
Gerhardt, R. and Nowick, A.S., Grain boundary effect in ceria doped with trivalent cations: I, Electrical measurements, J. Amer. Ceram. Soc., 1986, vol. 69, no. 9, p. 641.
Wang, D.Y. and Nowick, A.S., The “grain-boundary effect” in doped ceria solid electrolytes, J. Solid State Chem., 1980, vol. 35, no. 3, p. 325.
Guo, X. and Waser, R., Electrical properties of the grain boundaries of oxygen ion conductors: Acceptor-doped zirconia and ceria, Prog. Mater. Sci., 2006, vol. 51, p. 151.
Guo, X. and Maier, J., Grain boundary blocking effect in zirconia: a Schottky barrier analysis, J. Electrochem. Soc., 2001, vol. 148, no. 3, p. E121.
Tuller, H.L., Ionic conduction in nanocrystalline materials, Solid State Ionics, 2000, vol. 131, nos. 1–2, p. 143.
Heitjans, P. and Indris, S., Diffusion and ionic conduction in nanocrystalline ceramics, J. Phys: Condens. Matter, 2013, vol. 15, no. 30, p. R1257.
Badwal, S.P.S., Grain boundary resistivity in zirconia-based materials: effect of sintering temperatures and impurities, Solid State Ionics, 1995, vol. 76, nos. 1–2, p. 67.
Mondal, P. and Hahn, H., Investigation of the complex conductivity of nanocrystalline Y2O3-stabilized zirconia, Ber. Bunsenges. Phys. Chem., 1997, vol. 101, no. 11, p. 1765.
Lee, J.-H., Mori, T., Li, J.-G., Ikegami, T., Komatsu, M., and Haneda, H., Improvement of grain-boundary conductivity of 8 mol % yttria-stabilized zirconia by precursor scavenging of siliceous phase, J. Electrochem. Soc., 2000, vol. 147, no. 7, p. 2822.
Maier, J., Space charge regions in solid two phase systems and their conduction contribution – II contact equilibrium at the interface of two ionic conductors and the related conductivity effect, Ber. Bunsenges. Phys. Chem., 1985, vol. 89, no. 4, p. 355.
Guo, X., Sigle, W., Fleig, J., and Maier, J., Role of space charge in the grain boundary blocking effect in doped zirconia, Solid State Ionics, 2002, vols. 154–155, p. 555.
Liu, T., Zhang, X., Wang, X., Yu, J., and Li, L., A review of zirconia-based solid electrolytes, Ionics, 2016, vol. 22, p. 2249.
Röwer, R., Knöner, G., Reimann, K., Schaefer, H.-E., and Södervall, U., Oxygen diffusion in YSZ single crystals at relatively low temperatures, Phys. Stat. Sol. B, 2003, vol. 239, no. 2, p. R1.
Badwal, S.P.S. and Rajendran, S., Effect of micro- and nano-structures on the properties of ionic coductors, Solid State Ionics, 1994, vols. 70–71, p. 83.
Lomonova, E.E. and Osiko, V.V., Growth of Zirconia Crystal by Skull-Mellting Technique, in Crystal Growth Technology, Scheel, H.J. and Fukuda, T., Eds., N.Y.: John Wiley & Sons, 2003. p. 461–486.
Kuz’minov, Yu.S., Lomonova, E.E., and Osiko, V.V., Cubic zirconia and skull melting, Cambridge: Cambr. Internat. Sci. Publ. Ltd., 2009. 346 p.
Yashima, M., Sasaki, S., Kakihana, M., Yamaguchi, Y., Arashi, H., and Yoshimura, M., Oxygen-induced structural change of the tetragonal phase around the tetragonal-cubic phase boundary in ZrO2–YO1.5 solid solutions, Acta Crystallogr. B Struct. Sci., 1994, vol. B50, p. 663.
Yashima, M., Ohtake, K., Kakihana, M., Arashi, H., and Yoshimura, M., Determination of tetragonal-cubic phase boundary of Zr1 –xRxO2 –x/2 (R = Nd, Sm, Y, Er and Yb) by Raman scattering, J. Phys. Chem. Solids, 1996, vol. 57, no. 1, p. 17.
Hemberger, Y., Wichtner, N., Berthold, C., and Nickel, K.G., Quantification of yttria in stabilized zirconia by Raman spectroscopy, Int. J. Appl. Ceram. Technol., 2016, vol. 13, no. 1, p. 116.
Borik, M.A., Bredikhin, S.I., Bublik, V.T., Kulebyakin, A.V., Kuritsyna, I.E., Lomonova, E.E., Milovich, P.O., Myzina, V.A., Osiko, V.V., Ryabochkina, P.A., and Tabachkova, N.Y., Structure and conductivity of yttria and scandia-doped zirconia crystals grown by skull melting, J. Amer. Ceram. Soc., 2017, vol. 100, no. 12, p. 5536.
Agarkov, D.A., Borik, M.A., Bredikhin, S.I., Burmistrov, I.N., Eliseeva, G.M., Kolotygin, V.A., Kulebyakin, A.V., Kuritsyna, I.E., Lomonova, E.E., Milovich, F.O., Myzina, V.A., Ryabochkina, P.A., Tabach-kova, N.Yu., and Volkova, T.V., Structure and transport properties of zirconia crystals co-doped by scandia, ceria and yttria, J. Materiomics, 2019, vol. 5, no. 2, p. 273.
Guo, X., Roles of alumina in zirconia for functional applications, J. Amer. Ceram. Soc., 2003, vol. 86, no. 11, p. 1867.
Miyayama, M., Yanagida, H., and Asada, A., Effects of Al2O3 additions on resistivity and microstructure of yttria-stabilized zirconia, J. Amer. Ceram. Soc. Bull., 1986, vol. 65, no. 4, p. 74.
Navarro, L.M., Recio, P., Jurado, J.R., and Duran, P., Preparation and properties evaluation of zirconia-based/Al2O3 composites as electrolytes for solid oxide fuel cell systems, Part III, Mechanical and electrical characterization, J. Mater. Sci., 1995, vol. 30, p. 1949.
Feighery, J. and Irvine, J.T.S., Effect of alumina additions upon electrical properties of 8 mol % yttria-stabilized zirconia, Solid State Ionics, 1999, vol. 121, p. 209.
Ross, I.M., Rainforth, W.M., McComb, D.W., Scott, A.J., and Brydson, R., The role of trace additions of alumina to yttria–tetragonal zirconia polycrystals (Y-TZP), Scr. Mater., 2001, vol. 45, no. 6, p. 653.
Дополнительные материалы отсутствуют.





