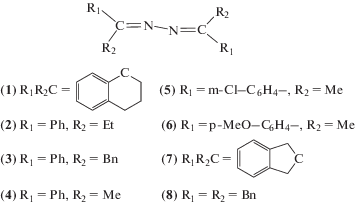
Электрохимия, 2022, T. 58, № 4, стр. 160-167
Изучение электрохимического восстановления азинов методом циклической вольтамперометрии
Н. В. Золотарева a, *, М. Д. Гришин a, Ю. С. Панова a, В. В. Сущев a, А. Н. Корнев a
a ФГБУН Институт металлоорганической химии им. Г.А. Разуваева РАН
603950 Нижний Новгород, ул. Тропинина, 49, Россия
* E-mail: natkamel@yandex.ru
Поступила в редакцию 09.07.2021
После доработки 16.09.2021
Принята к публикации 21.09.2021
- EDN: ADFQQD
- DOI: 10.31857/S0424857022040144
Аннотация
Исследовано электрохимическое восстановление серии азинов с помощью циклической вольтамперометрии. Восстановление азинов 1-тетралона, пропиофенона, фенилбензилкетона, ацетофенона, м-хлорацетофенона, п-метоксиацетофенона протекает в две стадии: с обратимым образованием анион-радикала на первой стадии и необратимым образованием дианиона на второй, скорость-определяющей стадии. Азины 2-инданона и дибензилкетона имеют единственный пик восстановления до дианиона (необратимый). Для всех вышеуказанных азинов определены: коэффициенты диффузии, коэффициенты переноса, константы скорости переноса электрона, критерии обратимости Матсуды–Аябе.
ВВЕДЕНИЕ
Азины (диимины) представляют собой 2,3-диазааналоги 1,3-бутадиена и вызывают повышенный интерес, обусловленный разнообразием практических приложений [1]. Они используются при создании нелинейно-оптических материалов [2], светодиодов, фотоэлементов и фотоэмиттеров [3], обладают противоопухолевой активностью [4]. В координационной химии азины являются потенциальными дииминовыми лигандами [5], используются в реакциях образования связей, полимеризации и синтезе гетероциклических соединений [6, 7]. Наш интерес к азинам вызван их использованием в качестве прекурсоров для синтеза диазадифосфапенталенов (ДДП), − ароматических гетероциклов нового класса − обладающих одновременно и свойствами стабилизированных фосфиниденов [8, 9].
Структурные и электронные свойства азинов являются критическими для выбора условий получения ДДП и определяют их реакционную способность. Одним из вариантов синтеза ДДП было металлирование диизопропиламидом лития (с последующим фосфорилированием). В случае алифатических азинов стадия металлирования имела место, в то время как ароматические азины давали смесь нецелевых продуктов. В сложившейся ситуации, наша задача заключалась в характеристике электрохимического поведения азинов и определения их кинетических параметров. Существует серия работ по измерению энергии граничных орбиталей для альдазинов и кетазинов с помощью циклической вольтамперометрии (ЦВА) [10, 11]. Однако это касается ограниченного числа азинов, кинетические параметры электровосстановления которых не были определены. В нашей работе впервые представлены расчеты коэффициента диффузии, коэффициента переноса и константы скорости переноса электрона для лимитирующей стадии восстановления серии азинов на основе 1-тетралона, пропиофенона, фенилбензилкетона, ацетофенона, м-хлорацетофенона, п‑метоксиацетофенона, 2-инданона, дибензилкетона в апротонной среде с помощью метода ЦВА. Исходя из полученных данных, определен характер их восстановления с использованием критерия Матсуды и Аябе.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все исследуемые азины 1-тетралона, пропиофенона, фенилбензилкетона, ацетофенона, м‑хлорацетофенона, п-метоксиацетофенона, 2-инданона, дибензилкетона, циклогексанона, диэтилкетона были получены и очищены в соответствии с литературными методиками, проанализированы методами ИК- и ЯМР-спектроскопии, хромато-масс-спектрометрии [12]. Диметилформамид (≥99.8%, безводный, “VWR Chemicals”) использовался без предварительной очистки, хранился в ампулах под сухим аргоном. В качестве электролита использовался гексафторфосфат тетрабутиламмония TBAPF6 (≥99.0%, для электрохимических измерений, “Sigma-Aldrich”).
Все измерения были выполнены в стандартной трехэлектродной ячейке с помощью одноканального потенциостата-гальваностата CS300 (Corrtest, Китай) в среде аргона. В качестве рабочего электрода использовался стеклоуглеродный дисковый электрод с диаметром 1 мм, вспомогательный электрод – платиновая проволока (диаметр 0.5 мм), электрод сравнения – неводный Ag/Ag+ в ацетонитриле (0.1 М AgNO3 + 0.1 М TBAPF6). Компенсация потери омического напряжения проводилась методом положительной обратной связи, а численное значение сопротивления определялось методом прерывания электрохимической цепи [13]. Для этих измерений был приготовлен 5 мM раствор ферроцена (≥98%, “Sigma-Aldrich”) в ДМФА в присутствии 0.1 М TBAPF6.
Численное значение площади рабочего электрода определялось методом ЦВА. Для этих измерений был приготовлен 2 мМ раствор ферроцена (≥98%, “Sigma-Aldrich”) в ацетонитриле (≥99.8%, для ВЭЖХ, “Криохром”) в присутствии 0.1 М TBAPF6. По заранее известному коэффициенту диффузии для данной системы D = 2.6 × 10–7 см2/с [14], согласно уравнению Рэндлса–Шевчика для обратимых процессов, было определено значение площади рабочего электрода. Оно составило 0.008 cм2 (отклонение ±10%).
Для измерений были приготовлены 5 мМ растворы азинов при добавлении фонового электролита TBAPF6 (0.1 М) в ДМФА. Все манипуляции проводились под аргоном. Перемешивание выполнялось перед каждым запуском измерений, чтобы обновить поверхность электродов.
Методика эксперимента включала в себя проведение ЦВА при разных скоростях сканирования (50, 75, 100, 125, 150, 175, 200 мВ/c) в диапазоне от –0.8 до –3.5 В (относительно неводного Ag/Ag+ электрода сравнения). На основе расчетов и внешнего вида полученных вольтамперограмм делался вывод о характере электрохимического процесса. Уравнение Лавирона, Гохштейна, кривые Тафеля (v = 5 мВ/с) были использованы для определения кинетических параметров лимитирующей стадии электрохимического восстановления азинов. Определение коэффициента диффузии для необратимых процессов проводили с использованием соответствующего уравнения Рэндлса–Шевчика. На основе полученных значений был рассчитан критерий обратимости Λ и определен характер процесса.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В ходе выполнения работы были исследованы восстановительные превращения серии азинов: 1-тетралона (1), пропиофенона (2), фенилбензилкетона (3), ацетофенона (4), м-хлорацетофенона (5), п-метоксиацетофенона (6), 2-инданона (7), дибензилкетона (8) с помощью метода ЦВА. В работе также изучались алифатические азины: циклогексанона и диэтилкетона, однако на зарегистрированных вольтамперограммах отсутствовали сигналы в заданном интервале потенциалов.
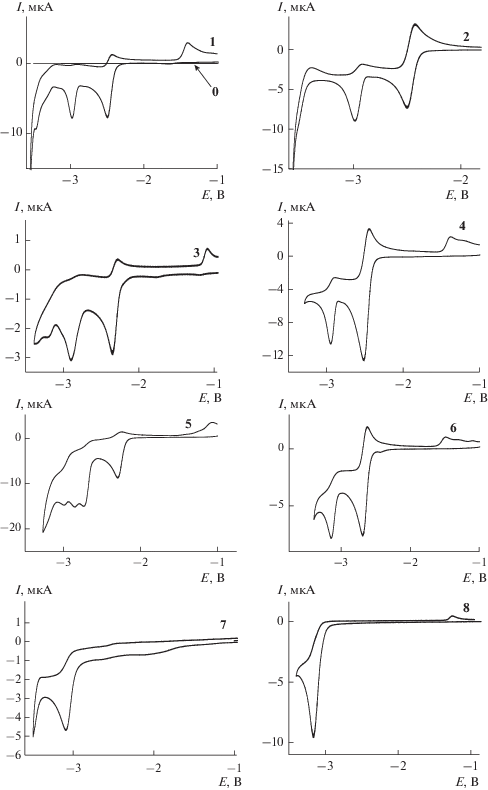
Получены серии кривых ЦВА для каждого из азинов в диапазоне потенциалов от –0.8 до –3.5 В (относительно неводного Ag/Ag+-электрода сравнения) при изменении скорости сканирования от 50 до 200 мВ/с. На рис. 1 представлены кривые ЦВА растворов фонового электролита 0 и азинов 1–8.
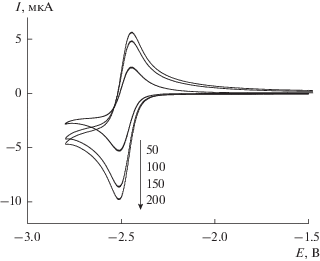
Установлено, что механизм восстановления азинов 1–6 имеет схожий характер. На кривых ЦВА наблюдается последовательное протекание двух стадий переноса электрона. Первый пик восстановления азинов соответствует обратимому одноэлектронному переносу (ΔEп ≈ 65–70 мВ, Iк/Iа ≈ 1) (табл. 1). Значение его потенциала пика не зависит от скорости сканирования (рис. 2).
Таблица 1.
Электрохимические данные восстановления азинов 1–8 в 0.1 М TBAPF6/ДМФА (относительно Ag/Ag+), v = 100 мВ/с
| Азин | E1/2 (0'/–), В | Iк/Iа | Eп (–/2–), В | Eп (0/2–), В | Eп (иное), В |
|---|---|---|---|---|---|
| 1 | –2.487 | 1.11 | –2.968 | – | – |
| 2 | –2.479 | 1.061 | –2.974 | – | – |
| 3 | –2.347 | 0.954 | –2.895 | – | – |
| 4 | –2.472 | 0.928 | –2.948 | – | – |
| 5 | –2.263 | 1.022 | –2.736 | – | –2.854 |
| –2.991 | |||||
| 6 | –2.654 | 0.98 | –3.144 | – | – |
| 7 | – | – | – | –3.093 | – |
| 8 | – | – | – | –3.165 | – |
Второй катодный пик соответствует необратимому переходу и смещается в катодную область при увеличении скорости сканирования (рис. 3). Следует отметить, что значения потенциалов пиков восстановления для п-MeO-замещенного азина 6 смещены в катодную область, а для м-Cl-замещенного 5 – в анодную относительно незамещенного азина 4, что определяется донорным и акцепторным характером заместителей. Наличие двух дополнительных пиков восстановления у азина 5 связано с восстановлением C–Cl-связи в ароматическом кольце.
Рис. 3.
Смещение значения потенциалов пика восстановления для азинов 3 (слева) и 8 (справа) при v = 50~200 мВ/с.
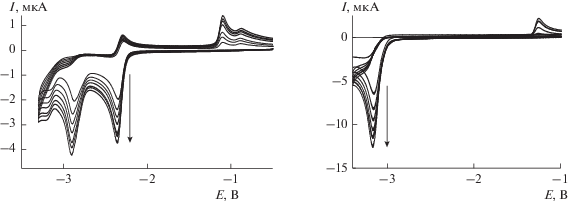
В свою очередь, для азинов 7 и 8 характерно наличие одного пика восстановления в области –3 В, соответствующего необратимому процессу (табл. 1). При увеличении скорости сканирования происходит сдвиг пиковых значений потенциалов в катодную область (рис. 3). Наличие на кривых ЦВА одного пика восстановления, очевидно, связано с тем, что двухэлектронное восстановление протекает одновременно на двух независимых центрах. Это происходит из-за нарушения системы сопряжения атомов в 7 и 8.
В некоторых случаях на кривых ЦВА наблюдается волна восстановления на фоне разряда электролитического фона. А также для многих азинов регистрируется пик окисления в районе –1 В, сопряженный с пиком образования дианиона. Предположительно, это связано с окислением остаточного количества дианиона.
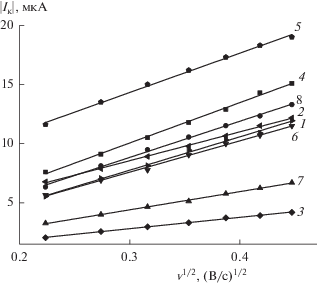
Для всей серии азинов 1–8 была определена линейная зависимость величины пикового тока Iк от квадратного корня скорости сканирования v1/2 (рис. 4). Установлено, что процесс контролируется диффузией. Из графика определен тангенс угла наклона прямой и произведен расчет коэффициента диффузии согласно уравнению (1) Рэндлса–Шевчика для необратимых процессов [15]:
(1)
$\left| {{{I}_{{\text{к}}}}} \right| = 0.496\sqrt {\alpha n{\kern 1pt} '} \,nFcA\sqrt {\frac{{FvD}}{{RT}}} ,$Таблица 2.
Кинетические параметры восстановления исследуемых азинов 1–8
| Азин | αn | α | n | E0′, В | D × 106, см2/с | k0, см/c | Λ (50 мВ/с )– Λ (200 мВ/с) | Характер процесса восстановления |
|---|---|---|---|---|---|---|---|---|
| 1 | 1.538 | 0.754 | 2.04 | –2.85 | 1.58 | 8.99 × 10–5 | 5.1 × 10–2–2.6 × 10–2 | * |
| 2 | 1.771 | 0.858 | 2.064 | –2.84 | 1.54 | 2.55 × 10–5 | 1.5·× 10–2–0.7 × 10–2 | * |
| 3 | 1.317 | 0.721 | 1.825 | –2.64 | 0.20 | 2.59 × 10–7 | 4.15 × 10–4–2.08 × 10–4 | ** |
| 4 | 2.232 | 0.977 | 2.284 | –2.84 | 2.00 | 3.43 × 10–7 | 1.74 × 10–4–0.87 × 10–4 | *** |
| 5 | 1.759 | 0.811 | 2.158 | –2.59 | 4.31 | 3.99 × 10–4 | 1.38 × 10–1–6.9 × 10–2 | * |
| 6 | 1.136 | 0.637 | 1.783 | –3.01 | 1.74 | 4.67 × 10–7 | 2.54 × 10–4–1.27 × 10–4 | ** |
| 7 | 1.874 | 0.738 | 2.539 | –2.93 | 0.51 | 1.54 × 10–6 | 1.55 × 10–3–7.73 × 10–4 | * |
| 8 | 1.77 | 0.715 | 2.475 | –2.92 | 2.21 | 8 × 10–8 | 3.86 × 10–5–1.93 × 10–5 | ** |
Расчет кинетических параметров необратимых процессов (гетерогенная константа скорости переноса электрона k0 и коэффициент переноса α) происходил согласно полученным экспериментальным данным: потенциалам пика восстановления и пиковым катодным токам. Произведение αn и количество электронов n, участвующих в восстановлении, определили, используя уравнение Лавирона для необратимых систем (уравнение (2)) [16]:
(2)
${{E}_{{{\text{пк}}}}} = {{E}^{{0'}}} + \left( {\frac{{RT}}{{\alpha nF}}} \right)\ln \left( {\frac{{RT{{k}^{0}}}}{{\alpha nF}}} \right) - \left( {\frac{{RT}}{{\alpha nF}}} \right)\ln \left( v \right),$Для вычисления количества электронов, участвующих в процессе, был рассчитан коэффициент переноса α с помощью соотношения между значением потенциала пика Eп и потенциала полупика Eп/2 [17]:
(3)
$\left| {{{E}_{{\text{п}}}} - {{E}_{{{{\text{п}} \mathord{\left/ {\vphantom {{\text{п}} 2}} \right. \kern-0em} 2}}}}} \right| = \frac{{47.7}}{\alpha }\,\,{\text{мВ}}.$Среднее вычисленное значение коэффициента переноса α оставляет 0.754 для азина 1 при скоростях сканирования от 50 до 200 мВ/с. Таким образом, количество электронов n, участвующих в восстановлении азинов до дианиона, равно 2.
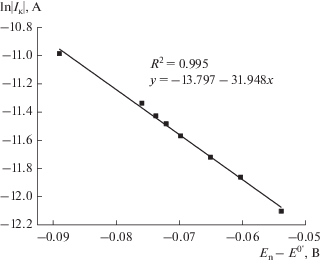
Для оценки константы скорости переноса электрона k0 мы воспользовались методикой Гохштейна, устанавливающей зависимость пикового тока от потенциала в точке максимума для идеально необратимых процессов (уравнение (4)) [18]:
(4)
$\left| {{{I}_{{\text{к}}}}} \right| = 0.227nFA{{c}_{0}}{{k}^{0}}\exp \left[ {\left( { - \alpha n{\kern 1pt} '\frac{F}{{RT}}} \right)\left( {{{E}_{{\text{п}}}} - {{E}^{{0'}}}} \right)} \right].$Логарифмическая форма уравнения позволяет оценить k0, построив линейную зависимость в координатах “ln|Iк|–Еп – E0′” и определив величину отрезка, отсекаемого от оси ординат (рис. 6):
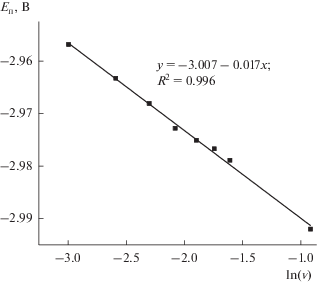
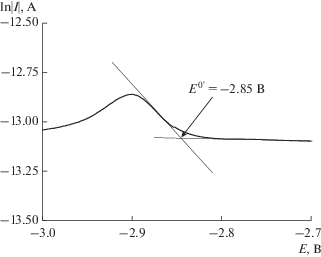
Величина формального потенциала рассчитывалась с помощью кривых Тафеля в координатах “ln|I|–E”. Определялась абсцисса точки, в которой сходятся катодная и анодная ветви (рис. 7). Полученное значение должно соответствовать равновесному потенциалу Eр [17], численно приравненному к формальному потенциалу E0′ [19].
Вычисленные значения констант скорости гетерогенного процесса имеют порядок от 10–4 до 10–8 cм/с. Этот диапазон свидетельствует о невысокой скорости электрохимического восстановления и о необходимости больших перенапряжений для достижения существенной скорости восстановления.
Для описания характера процесса (обратимый, квазиобратимый, необратимый) Матсудой и Аябе [20, 21] был введен критерий обратимости Λ, физический смысл которого заключается в соотношении между скоростью переноса электрона и массообмена:
Для обратимых систем: Λ > 15.
Для квазиобратимых: 15 > Λ > 10–2(1 + α).
Для необратимых систем: Λ < 10–2(1 + α).
Используя приведенную формулу и вычисленные ранее кинетические параметры, мы получили значения параметра Λ и определили его диапазон для v = 50–200 мВ/с. В табл. 2 указаны его граничные значения, на основании которых был сделан вывод о характере процесса. Во всех случаях стадия переноса электрона протекает существенно медленнее, чем планарная диффузия, что подтверждает квазиобратимый (близкий к необратимому) и необратимый характер восстановления до дианиона всех изученных азинов.
ЗАКЛЮЧЕНИЕ
Электрохимическое восстановление азинов 1‑тетралона, пропиофенона, фенилбензилкетона, ацетофенона, м-хлорацетофенона, п-метоксиацетофенона протекает в 2 стадии. Первая одноэлектронная стадия восстановления является быстрой (ΔEп = 65–70 мВ, Iк/Iа ≈ 1) и сопровождается образованием анион-радикала. Вторая стадия – образование дианиона – является медленной, скоростьопределяющей. Для всех азинов характер этого процесса близок к необратимому. Азины 2-инданона и дибензилкетона имеют единственный пик восстановления, соответствующий переносу двух электронов (необратимый). Азины циклогексанона и диэтилкетона не электроактивны в изученном диапазоне. Полученные данные говорят о том, что лучшими прекурсорами для синтеза ДДП являются алифатические азины, так как ароматические азины не металлируются, а восстанавливаются. Значения коэффициентов диффузии для серии азинов рассчитаны по уравнению Рэндлса–Шевчика для необратимых процессов и варьируются от 0.2 × 10–6 до 4.31 × 10–6 cм2/с. Коэффициенты переноса для всех азинов лежат в диапазоне от 0.5 до 1. Константы скорости гетерогенного переноса электрона, согласно уравнению Гохштейна, имеют порядок от 10–4 до 10–8 cм/с. Это свидетельствует о невысокой скорости данного процесса и о необходимости больших перенапряжений для достижения существенной скорости восстановления. Необратимый и квазиобратимый (близкий к необратимому) характер процесса образования дианиона для серии азинов был подтвержден с помощью критерия Матсуды–Аябе, рассчитанного из полученных кинетических характеристик.
Список литературы
Sek, D., Siwy, M., Bijak, K., Grucela-Zajac, M., Malecki, G., Smolarek, K., Bujak, L., Mackowski, S., and Schab-Balcerzak, E., Comparative Studies of Structural, Thermal, Optical, and Electrochemical Properties of Azines with Different End Groups with Their Azomethine Analogues toward Application in (Opto)Electronics, J. Phys. Chem. A., 2013, vol. 117, no. 40, p. 10320.
Anthamatten, M., Barnes, C. L., and Glaser, R., Stereochemistry and stereoelectronics of azines. A solid-state study of symmetrical, (E, E)-configured, parasubstituted (H, F, Cl, Br, CN) acetophenone azines, J. Org. Chem., 1994, vol. 59, p. 4336.
Tang, W., Xiang, Y., and Tong, A., Salicylaldehyde Azines as Fluorophores of Aggregation-Induced Emission Enhancement Characteristics, J. Org. Chem., 2009, vol. 74, p. 2163.
Khodair, A.I. and Bertrand, P., A new approach to the synthesis of substituted 4-imidazolidinones as potential antiviral and antitumor agents, J. Tetrahedron, 1998, vol. 54, p. 4859.
Kulaksızoglu, S. and Gup, R., A new bis(azine) tetradentate ligand and its transition metal complexes: Synthesis, characterisation, and extraction properties, J. Chem. Papers, 2012, vol. 66, no. 3, p. 194.
Schweizer, E.E., Cao, Z., Rheingold, A.L., and Bruch, M., Reactions of azines. Preparation of 6-(phenylmethylene)-5H-pyrazolo[1,5-d][2,4]benzoxazepines, 5H,7H-pyrazolo[1,5-d][2]benzazepin-6-one, and indeno[2,3-c]pyridine-3,9-diones, J. Org. Chem., 1993, vol. 58, p. 4339.
Ranjbar-Karimia, R. and Loghmani-Khouzani, H., Synthesis of New Azines in Various Reaction Conditions and Investigation of Their Cycloaddition Reaction, J. Iran. Chem. Soc., 2011, vol. 8, p. 223.
Kornev, A.N., Sushev, V.V., Panova, J.S., Lukoya-nova, O.V., Ketkov, S.Y., Baranov, E.V., Fukin, G.K., Lopatin, M.A., Budnikova, Y.G., and Abakumov, G.A., N,N'-Fused Bisphosphole: Heteroaromatic Molecule with Two-Coordinate and Formally Divalent Phosphorus. Synthesis, Electronic Structure, and Chemical Properties, 2014, J. Inorg. Chem., vol. 53, p. 3243.
Kornev, A.N., Panova, Y.S., Sushev, V.V., Daza, D.F.D., Novikov, A.S., Cherkasov, A.V., Fukin, G.K., and Abakumov, G.A., The Nature of P(σ2λ3 ↔ σ2λ1) Dualism: 3a,6a-Diaza-1,4-diphosphapentalene as a Form of Stabilized Singlet Phosphinidene, J. Inorg. Chem., 2019, vol. 58, p. 16144.
Poojary, S., Sunil, D., Kekuda, D., and Sreenivasa, S., Fluorescent aromatic symmetrical azines: Synthesis and appraisal of their photophysical and electrochemical properties, Optical Materials, 2018, vol. 85, p. 1.
Sauro, V.A. and Workentin, M.S., Evaluation of the Extent of Conjugation in Symmetrical and Asymmetrical Aryl-Substituted Acetophenone Azines Using Electrochemical Methods, J. Org. Chem., 2011, vol. 66, p. 831.
Safari, J. and Gandomi-Ravandi, S., Structure, synthesis and application of azines: a historical perspective, J. RSC Adv., 2014, vol. 4, p. 46224.
Gosser, D.K., Cyclic voltammetry: simulation and analysis of reaction mechanisms. Weinheim: VCH, 1993, 152 p.
Wang, Y., Rogers, E.I., and Compton, R.G., The measurement of the diffusion coefficients of ferrocene and ferrocenium and their temperature dependence in acetonitrile using double potential step microdisk electrode chronoamperometry, J. Electroanalyt. Chem., 2010, vol. 648, p. 15.
Nicholson, R.S. and Shain, I., Theory of Stationary Electrode Polarography. Single Scan and Cyclic Methods Applied to Reversible, Irreversible, and Kinetic Systems, Analyt. Chem., 1964, vol. 36, p. 706.
Laviron, E., General expression of the linear potential sweep voltammogram in the case of diffusionless electrochemical systems, J. Electroanalyt. Chem., 1979, vol. 101, p. 19.
Bard, A.J. and Faulkner, L.R., Electrochemical Methods: Fundamentals and Applications, N.Y.: Wiley and Sons, 2001, 856 p.
Гохштейн, А.Я., Гохштейн, Я.П. Кинетическое уравнение необратимых реакций в осциллографической полярографии. Докл. АН СССР. 1960. № 3. С. 601. [Gokhshtein, A.Y. and Gokhshtein, Y.P., Kinetic equation of irreversible reactions in oscillographic polarography, Doklady Akad. Nauk SSSR (in Russian), 1960, no. 3, p. 601.]
Li, D., Batchelor-McAuley, C., and Compton, R.G., Some thoughts about reporting the electrocatalytic performance of nanomaterials, Appl. Materials Today, 2019, vol. 18, no. 100404.
Matsuda, H. and Ayabe, Y., Theoretical Analysis of Polarographic Waves. I. Reduction of Simple Metal Ions, Bull. Chem. Soc. Japan, 1955, vol. 28, p. 422.
Wen, Z., Ya-Lan, L., Kui, L., Zhi-Rong, L., Li-Yong, Y., Lu, W., Yi-Xiao, F., Zhi-Fang, C., and Wei-Qun, S., Electroreduction of Gd3+ on Wand Zn Electrodes in LiCl–KCl Eutectic: A Comparison Study, J. Electrochem. Soc., 2015, vol. 162, p. 53.
Дополнительные материалы отсутствуют.