Журнал физической химии, 2019, T. 93, № 10, стр. 1575-1583
Наноструктурированные NiMo- и NiW-катализаторы окисления тиофена, полученные методом лазерного электродиспергирования
А. А. Брыжин a, И. Г. Тарханова a, *, К. И. Маслаков a, С. А. Николаев a, С. А. Гуревич b, В. М. Кожевин b, Д. А. Явсин b, М. Г. Гантман c, Т. Н. Ростовщикова a
a Московский государственный университет имени М.В. Ломоносова, Химический факультет
Москва, Россия
b Российская академия наук, Физико-технический институт имени А.Ф. Иоффе
Санкт-Петербург, Россия
c Friedrich-Alexander Universität Erlangen-Nürnberg, FAU
Erlangen, Deutschland
* E-mail: itar_msu@mail.ru
Поступила в редакцию 15.03.2019
После доработки 15.03.2019
Принята к публикации 09.04.2019
Аннотация
Новые биметаллические катализаторы на основе наночастиц оксидов Ni и Mo или W, нанесенных на оксид алюминия, получены лазерным электродиспергированием плотно спрессованных бинарных смесей порошков NiMo и NiW. Методами СЭМ, ПЭМ и РФЭС показано, что оба компонента каждой пары равномерно распределены по поверхности носителя в виде наночастиц размером 4–7 нм. Металлы на поверхности катализатора находятся преимущественно в окисленном состоянии. Сравнение каталитической активности NiMo/Al2O3 и NiW/Al2O3 проведено на примерах окисления тиофена и дибензотиофена пероксидом водорода. Высокая конверсия реагентов на таких катализаторах со сверхнизким содержанием металлов (<0.01 мас. %) сохраняется при многократном повторении процесса. Введение в реакционную смесь сульфатированной цвиттер-ионной жидкости приводит к дополнительному повышению эффективности катализаторов.
Традиционные химические методы синтеза биметаллических катализаторов имеют ряд существенных недостатков, связанных с неравномерным заполнением поверхности носителя активными компонентами, широким распределением частиц по размерам и недостаточно высокой воспроизводимостью их свойств из-за сильного влияния условий приготовления на структуру получаемых материалов. Кроме того, в большинстве случаев это многостадийные процессы, требующие использования прекурсоров, стабилизаторов и других химических реагентов, воздействующих на окружающую среду.
Физические методы синтеза, основанные чаще всего на лазерной абляции [1, 2], обеспечивают, как правило, более равномерное распределение активных компонентов на поверхности катализатора, являются одностадийными и экологически более благоприятными. Плазменно-электролитическое оксидирование (ПЭО) также позволяет в одну стадию формировать оксидные покрытия заданного состава, обладающие каталитической активностью в окислительных процессах и повышенной химической и термической устойчивостью [3]. Однако этот метод требует использования растворов электролитов и предполагает высокие содержания активных компонентов в составе катализаторов. Лазерное электродиспергирование (ЛЭД) дает возможность без использования химических прекурсов, восстановительных реагентов и стабилизаторов получать “корочковые” катализаторы, в которых моно- и биметаллические частицы строго фиксированного размера равномерно распределены по внешней поверхности носителя [4–6]. По адсорбционным и каталитическим свойствам низкопроцентные катализаторы ЛЭД отличаются от аналогичных материалов, полученных традиционными методами, такими как пропитка, ионный обмен, металло-паровой синтез, осаждение из коллоидных дисперсий [7, 8]. В частности, катализаторы на основе наночастиц никеля, нанесенных на Al2O3 методом ЛЭД, активны в окислении CO при чрезвычайно низком содержании Ni < 0.01 мас. %, в то время как Ni/Al2O3 катализатор, полученный методом пропитки, практически не активен [9]. Такое различие, скорее всего, связано с тем, что в покрытиях ЛЭД никель присутствует в двух электронных состояниях Ni0 и Ni2+, чего не наблюдали в традиционных катализаторах, содержащих только NiO. По данным СТМ/СТС [10] наночастицы, формируемые ЛЭД, аморфны, неоднородны по составу и включают участки с металлической и нулевой проводимостью, соответствующей оксидам никеля, вероятно, нестехиометрического состава, что может быть причиной их повышенной активности в окислении.
В настоящей работе метод ЛЭД впервые применен для формирования биметаллических покрытий на основе Ni и Mo или W на поверхности оксида алюминия, используя в качестве мишеней плотно спрессованные двухкомпонентные смеси порошков. Ранее биметаллические покрытия получали методом ЛЭД путем последовательного нанесения двух компонентов или из предварительно изготовленного сплава металлов [4, 5]. Целью работы является выяснение особенностей строения и каталитического поведения новых материалов в пероксидном окислении серосодержаших ароматических соединений и окислительном обессеривании углеводородного сырья. Этот выбор обусловлен актуальностью процесса сероочистки в современной нефтехимии, что связано с ужесточением экологических требований, предъявляемых к различным видам топлива, а также увеличением доли объемов добычи сернистой и высокосернистой нефти и газа. Основным способом удаления серы из нефтепродуктов является гидроочистка, однако она не всегда позволяет полностью удалить замещенные ароматические сероорганические соединения. В качестве катализаторов в этом случае используют биметаллические системы Co(Ni)/Mo(W) на оксиде алюминия [11, 12]. Следует отметить, что этот процесс является пожаро- и взрывоопасным, поэтому реализуется только на крупных перерабатывающих предприятиях, где может быть использовано дорогостоящее оборудование, в полной мере обеспечивающее безопасность производства. В качестве альтернативы могут применяться окислительные методы, а также адсорбция и экстракция сероорганических соединений с их последующей переработкой. Зачастую эти методы используют в комплексе, что обеспечивает глубокую сероочистку. Твердыми адсорбентами служат оксидные и углеродные материалы, промотированные переходными металлами (Cu, Ni, Ag, Zn) [13]. Гетерогенными катализаторами окисления являются различные композиции, в частности, индивидуальные и смешанные оксиды и соли, содержащие ионы переходных металлов в высоких cтепенях окисления: производные Mo, W, V, Cr, Nb, Сe, а также бинарные системы, например, NiO–MoO3, CoO–MoO3 на оксидных подложках [14–21]. Из анализа состава таких композиций следует, что многие из них проявляют одновременно свойства и катализаторов и адсорбентов. Кроме того, Ni-содержащие композиции являются одновременно адсорбентами и катализаторами двух процессов – гидрирования и окисления [11, 12, 22, 23]. Такие полифункциональные катализаторы представляют особый интерес, так как могут быть использованы как в гидроочистке, так и в окислительной десульфуризации [23]. В настоящей работе биметаллические катализаторы на основе Ni и Mo или W на поверхности оксида алюминия использованы для пероксидного окисления тиофена и дибензотиофена – типичных представителей серосодержащих органических соединений углеводородного сырья. В качестве стабилизатора металлического покрытия при проведении жидкофазной реакции в углеводородной среде использовали 4-(3'-этилимидазолий)-бутансульфонат – цвиттер-ионное соединение, относящееся к классу ионных жидкостей (ИЖ). Такой подход ранее нами успешно применен в аналогичной реакции с участием катализаторов, полученных методом плазменно-электролитического оксидирования [24].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали γ-Al2O3 двух типов, различающихся размером гранул: АИ-05, удельная поверхность 194 м2/г, объем пор 0.75 см3/г, размер гранул 1.6–1.8 мм и АОК-63-11, марка “В”, удельная поверхность 180 м2/г, объем пор 0.55 см3/г, размер гранул 0.4–1.0 мм. Биметаллические катализаторы NiMo/Al2O3 и NiW/Al2O3 получали осаждением наночастиц на гранулы Al2O3 методом ЛЭД в специальной кювете, как описано в работе [5]. В кювету помещали 2 г носителя. В качестве мишеней использовали смеси порошков Ni/Mo и Ni/W с сотношением компонентов 30/70 мас. %, приготовленные холодным прессованием. Размер зерен порошков Ni, Mo и W составлял 3–8 мкм, производитель ABCR Dr. Braunagel GmbH. Содержание металлов в катализаторе определяли на основании калибровочных зависимостей скорости роста осажденных пленок, полученных предварительно с использованием кварцевого измерителя толщины пленок Sycon Instruments SCT-2000A.
Характеристики приготовленных катализаторов приведены в табл. 1. Образец 3-ИЖ получали выдерживанием нескольких гранул образца 3 и 4‑(3'-этилимидазолий)-бутансульфоната (массовое соотношение 1 : 1) в водном растворе и последующей сушкой при комнатной температуре.
Таблица 1.
Характеристики катализаторов
| № | Катализатор/Носитель | r, мм | τ, мин | m, мг | C × 103, мас. % | [Ni]/[M], ат. % (расчет) |
|---|---|---|---|---|---|---|
| 1 | Ni/Mo/АИ-05 | 1.6–1.8 | 12.0 | 0.077 | 3.9 | 0.71 |
| 2 | Ni/W/АИ-05 | 1.6–1.8 | 24.0 | 0.146 | 7.3 | 1.33 |
| 3 | Ni/W/АОК-63-11 | 0.4–1.0 | 18.0 | 0.11 | 5.5 | 1.33 |
Соединение 4-(3'-этилимидазолий)-бутансульфонат получали по стандартной методике, приведенной в работе [25].
Микрофотографии образцов получали методами сканирующей и просвечивающей электронной микроскопии (СЭМ и ПЭМ) на приборах JEOL JSM 6000 NeoScope и JEOL JEM 2100F/UHR с разрешающей способностью 0.1 нм, соответственно. Перед ПЭМ исследованиями несколько гранул образца помещали в спирт и обрабатывали ультразвуком 300 с аналогично [5]. Каплю суспензии с образцом помещали на медную сетку ПЭМ, сушили 1 ч и проводили исследования. Размер нанесенных фаз оценивали как максимальный линейный размер. Качественный анализ поверхности проводили с помощью энергодисперсионного анализа (ЭДА) на приборе JED-2300 in situ.
Текстурные характеристики образцов до и после катализа определяли методами BEТ, BJH и DFT на приборе Autosorb 1 фирмы Quantachrome, США после предварительного вакуумирования в течение 3 ч при 300°С. Расчет удельной поверхности и полного объема пор проводили по изотермам адсорбции и десорбции азота при 77 K с помощью пакета программ, входящего в комплектацию прибора.
Рентгеновские фотоэлектронные спектры катализатора регистрировали на спектрометре Axis Ultra DLD (Kratos) с использованием монохроматического AlKα-излучения c нейтрализатором. Спектры записывали при энергии пропускания анализатора 160 эВ (обзорный) и 40 эВ (спектры высокого разрешения). Калибровку проводили по компоненте C1s – 285.0 эВ.
Для проведения каталитических испытаний в термостатированный реактор помещали 10 мл модельной смеси (1 мас. % раствор тиофена или дибензотиофена в изооктане), 0.1 г катализатора и окислитель – 0.4 мл 50% раствора пероксида водорода в воде. Содержимое реактора перемешивали при нагревании (60°С), периодически отбирали пробы жидкой фазы для анализа. Количественный анализ органической фазы в реакционной смеси осуществляли методом газожидкостной хроматографии на приборе “Кристалл 4000”, с капиллярной колонкой Zebron ZB‑1 l = 30 м и жидкой фазой 100% диметилполисилоксан, пламенно-ионизационный детектор – ПИД. Содержание тиофена и дибензотиофена определяли в режиме линейного программирования при температурах 90–220°С методом внутреннего стандарта. Показано, что окисление исходных реагентов тиофена и дибензотиофена приводит к образованию серной кислоты и сульфона, соответственно [24]. После стандартных 4‑х часовых тестов жидкую фазу сливали, в реактор помещали новую порцию реагентов и испытания проводили аналогичным образом в течение пяти циклов. В отдельных опытах осуществляли дробное введение раствора H2O2 двумя порциями по 0.2 мл раствора через 2 ч. Для проверки влияния цвиттер-ионной жидкости на эффективность процесса в реакционную смесь добавляли 0.1 г 4‑(3'-этилимидазолий)-бутансульфоната.
Начальную скорость окисления тиофена ro (М/ч) рассчитывали по уменьшению его концентрации за первый час реакции. Величину TOF определяли нормированием убыли тиофена в молях за первый час реакции (∆n(тиофена)/ч) к числу молей Mo или W (n (W или Mo)) в образцах, принимая допущение об участии всех атомов в каталитическом процессе. При расчетах учитывали вклад носителя в конверсию тиофена, определенный в независимых экспериментах.
В испытаниях образцов в процессе очистки дизельного топлива с общим содержанием серы 1080 ppm использовали 20 мл дизельного топлива, 0.8 мл 50% H2O2, 0.04 г катализатора. Реакцию проводили в течение 4 ч при 60°С с однократным или дробным введением пероксида водорода в отсутствие и присутствии 0.1 г 4-(3'-этилимидазолий)-бутансульфоната. Далее реакционный раствор промывали дважды диметилформамидом для удаления продуктов окисления и анализировали на рентгенофлуоресцентном спектрометре ASE-2.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Структура катализаторов
Текстурные характеристики катализаторов после нанесения активных компонентов меняются очень незначительно. Например, для образца 3 расчет средних значений удельной поверхности и полного объема пор по данным BEТ, BJH и DFT дал значения 178 м2/г и 0.53 см3/г, что практически совпадает с характеристиками исходного носителя. Аналогичные значения получены для других образцов. Сохранение текстурных характеристик исходных носителей при синтезе катализаторов типично для метода ЛЭД и связано с тем, что осаждение наночастиц осуществляется только на внешнюю поверхность носителя, не затрагивая поровое пространство [6].
Однако добавление ионной жидкости существенно уменьшает удельную поверхность образца, для образца 3-ИЖ средние значения удельной поверхности и полного объема пор по данным BEТ, BJH и DFT уменьшились до значений 74 м2/г и 0.28 см3/г, причем в модифицированном ионной жидкостью образце сохраняются только более крупные поры диаметром около 10 нм, а мелкие поры диаметром 5 нм исчезают.
Типичные примеры микрофотографий поверхности образца 2 показаны на рис. 1а. Спектр ЭДА серых участков поверхности (не показан) включает линии Al, O, С, Cu, относящиеся к оксиду алюминия и материалу сетки. Спектры ЭДА (рис. 1б) черных частиц содержат линии Ni Kα (7.5 кэВ) и W Mα (1.8 кэВ), что позволяет отнести их к местам локализации Ni и W.
Рис. 1.
ПЭМ /ЭДА-изображение (а – места локализации фаз Ni и W по данным ЭДА отмечены квадратами), примеры интегральных спектров ЭДА (б) для выбранных точек и картирование поверхности образца 2 (в). Снимок поверхности ПЭМ – распределение Al, Ni и W.

Из рис. 1а видно, что эти частицы имеют близкую к сферической форму и размер от 4 до 7 нм. На некоторых участках поверхности наблюдаются скопления таких частиц размером около 50 нм (рис. 1в). Как видно из этого рисунка, оба компонента Ni и W распределены равномерно. Места локализации Ni и W полностью совпадали и на всех других проанализированых участках поверхности образцов. Для примера количественные данные по составу ряда выбранных участков поверхности приведены в табл. 2.
Таблица 2.
Распределение элементов на поверхности образца 2 по данным ЭДА
| Точка* | O, ат. % | Al, ат. % | Ni, ат. % | W, ат. % |
|---|---|---|---|---|
| 1 | 46.2 | 36.1 | 10.4 | 7.3 |
| 2 | 35.7 | 36.2 | 16.8 | 11.2 |
| 3 | 57.4 | 32.6 | 5.4 | 4.6 |
| 4 | 56.3 | 38.5 | 2.3 | 2.9 |
| 5 | 53.0 | 42.9 | 2.0 | 2.1 |
| 6 | 49.5 | 40.5 | 6.1 | 3.9 |
| Среднее, ат. % | 7.2 | 5.3 | ||
| Среднее соотношение (ат. %) Ni/W | 1.35 | |||
* – Точки обозначены на рис. 1а.
Из этих данных следует, что полученное экспериментально среднее соотношение (ат. %) Ni/W 1.35 близко к их соотношению 1.32 в составе исходной мишени.
Как видно из данных, приведенных на рис. 2, на поверхности образца 1 места локализации Ni и Mo также совпадают, однако ввиду более низкого содержания металлов получить количественную оценку их соотношения в катализаторе по данным ЭДА не удалось.
Рис. 2.
Микрофотография ПЭМ образца 1. Интегральный спектр ЭДА с выделенных локаций приведен на вставке.

На рис. 3 приведены СЭМ изображения и результаты ЭДА образца 2. Данные исследования не требуют предварительного диспергирования образцов. Из представленных результатов видно, что оба металла равномерно распределены по поверхности оксида алюминия, а их весовое соотношение 34/66 (атомное соотношение 1.61) достаточно близко к составу исходной мишени.
Таким образом, использование смеси порошков в качестве мишени для приготовления биметаллических катализаторов методом ЛЭД, так же как в случае формирования наночастиц из сплава металлов [5], позволяет получать покрытия с заданным соотношением и равномерным распределением активных компонентов по поверхности носителя.
Поскольку, в силу специфики метода ЛЭД, даже при низких содержаниях металла, создается высокая плотность активных частиц на внешней поверхности носителя, такие образцы удается анализировать методом РФЭС, но только используя целые гранулы катализатора без предварительного измельчения.
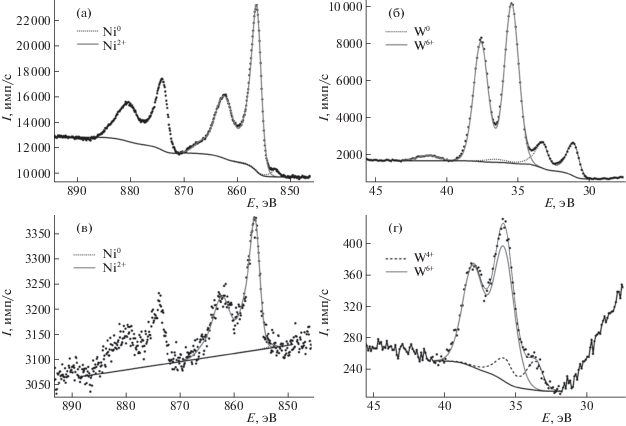
Спектры высокого разрешения линий Al2p во всех образцах оказались одинаковы, они показаны на рис. 4а на примере образца 1 вместе со спектрами линий Ni2p (б). Аналогичный спектр Ni получен для образца 2 на основе никеля и вольфрама на крупном оксиде алюминия.
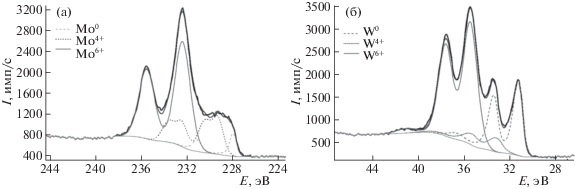
Наблюдаемая энергия связи линии Al2p (74.7–74.9 эВ) во всех спектрах несколько больше типичных значений для оксида алюминия (74.4–74.6 эВ) и значения 74.3 эВ, найденного для монометаллических Ni/Al2O3 катализаторов, также полученных методом ЛЭД [8]. Это может указывать на то, что алюминий частично входит в состав сложных оксидов, скорее всего, с молибденом/или вольфрамом. На рис. 5 приведены РФЭС-спектры высокого разрешения линий Mo и W в образцах 1 и 2.
Спектры линий никеля, молибдена и вольфрама разложены на компоненты, отвечающие различным состояниям этих элементов в образце. Результаты показаны на рис. 4, 5 и приведены в табл. 3, 4. В Ni2p, Mo3d и W4f РФЭС-спектрах (рис. 4, 5 и табл. 3, 4) в основном наблюдается вклад от максимально окисленных форм этих элементов (Ni2+, Mo6+ и W6+). Кроме того, частично сохраняются и металлические состояния Ni0, Mo0 и W0, наблюдаемые энергии связи соответствующих компонент близки к энергиям связям в металлическом никеле (852.7 эВ), молибдене (228.0 эВ) и вольфраме (31.4 эВ) [26]. Что касается спектра Ni2p3/2, то следует отметить два факта. Прежде всего, необычно высокое содержание металлической компоненты с энергией связи 852.8 эВ до 20 и 30% в молибден- и вольфрамсодержащих образцах 1 и 2. Ранее при анализе монометаллических Ni/Al2O3 образцов, также полученных методом ЛЭД, присутствие столь значительного количества Ni0 обнаружили только в многослойных покрытиях с большим содержанием никеля 0.03 мас. % [8, 9]. Кроме того, наблюдаемый спектр окисленной формы никеля Ni+2, так же как для монометаллического образца, существенно отличается от спектра NiO с энергией связи 854.4 эВ и характерен для гидроксида никеля или сложных оксидов, содержащих никель [27].
Таблица 3.
Энергии связи (Е) компонент никеля, молибдена и алюминия в РФЭС-спектрах образца 1, их доли (γ) и соответствующие им типы связей
| Спектр | Е, эВ | γ, % | Тип связи |
|---|---|---|---|
| Ni2p3/2 | 852.8 | 19 | Ni0 |
| 855.9 | 81 | Ni2+ | |
| Mo3d5/2 | 228.0 | 7 | Mo0 |
| 229.4 | 35 | Mo4+ | |
| 232.4 | 58 | Mo6+ | |
| Al 2p | 74.8 | 100 | Al3+ |
Таблица 4.
Энергии связи компонент никеля, вольфрама и алюминия в РФЭС- спектрах образцов NiW/Al2O3 (2, 3, 3-ИЖ), их доли и соответствующие им типы связей
| Спектр | Ni2p3/2 | W4f7/2 | Al2p | ||||
|---|---|---|---|---|---|---|---|
| Е, эВ | 852.5–852.7 | 855.9–856.2 | 31.1–31.3 | 33.2–33.6 | 35.4–35.8 | 74.7 | |
| Тип связи | Ni0 | Ni2+ | W0 | W4+ | W6+ | Al3+ | |
| γ, ат. % | 2 | 28 | 72 | 28 | 12 | 60 | 100 |
| 3 | 2 | 98 | 17 | – | 83 | 100 | |
| 3-ИЖ | – | 100 | – | 22 | 78 | ||
В РФЭС-спектрах молибдена и вольфрама образцов 1 и 2 помимо металлического и максимально окисленного состояний наблюдаются и промежуточные окисленные состояния молибдена и вольфрама. Для полного описания Mo3d и W4f7/2 спектров потребовалось ввести компоненты сложной формы, присутствие которых в основном обусловлено четырехвалентными состояниями Mo4+ и W4+. Подобный спектр сложной формы с энергией связи компоненты Mo3d5/2 равной 229.3 эВ отнесен к оксиду MoO2 [28]. В то же время нельзя исключить присутствия в небольших количествах и других окисленных форм молибдена и вольфрама.
Как видно из рис. 6, спектры Ni2p и W4f7/2 в NiW-образцах 3 (а, б) и 3-ИЖ (в, г) на АОК-63-11 с малым размером гранул отличны от приведенных выше на рис. 4 и 5 спектров. В них значительно ниже доля линий, соответствующих металлическим состояниям Ni0 и W0, и преобладают компоненты, отнесенные к окисленным состояниям Ni2+, W4+ и W6+. Результаты разложения Ni2p и W4f7/2 РФЭС-спектров на компоненты приведены в табл. 4. Более высокая степень окисления металлов на поверхности мелких гранул оксида алюминия может быть связана с большей геометрической площадью поверхности таких гранул и соответственно с меньшей поверхностной плотностью частиц. Подобную закономерность наблюдали ранее для наночастиц никеля на поверхности оксида алюминия [8].
Обработка образца 3 ионной жидкостью (3‑ИЖ) приводит к сильному снижению содержания Ni и W на поверхности, это видно из пониженной интенсивности сигналов (рис. 6). Согласно данным РФЭС по анализу состава поверхности, помимо основных компонентов катализатора Al, Ni, W и О, на поверхности присутствуют C, S и N, причем содержание углерода превышает 60 ат. %, что свидетельствует об адсорбции ионной жидкости на поверхности. Это согласуется с сильным уменьшением удельной поверхности и объема пор образца 3 после обработки ионной жидкостью. В соответствии с видом спектров в образце 3-ИЖ отсутствуют металлические состояния Ni0 и W0. Такие изменения могут быть связаны с окислением наночастиц металлов кислородом воздуха при обработке катализатора водным раствором ИЖ, обладающим высокой полярностью [29].
Каталитическое окисление производных тиофена
Каталитические свойства образцов определяли в модельных реакциях пероксидного окисления тиофена и дибензотиофена, а также десульфировании дизельной фракции, полученной на нефтеперерабатывающем предприятии Ханты-Мансийского АО.
Результаты испытаний катализаторов 1–3 в окислении тиофена приведены в табл. 5. Как видно из таблицы, при однократной загрузке лучшие результаты показывает образец 2. В этом случае и скорость реакции, и величина TOF, и конверсия тиофена за 4 ч максимальны. Два других образца 1 и 3 (Mo- и W-содержащие катализаторы) в этих условиях демонстрируют примерно одинаковую удельную атомную активность (TOF), а также близкие величины конверсии тиофена, поэтому представляло интерес сравнить их свойства при дробной загрузке H2O2. Как видно из таблицы, в этих условиях конверсия тиофена заметно возрастает (с 43 до 56%) на катализаторе 1 и меняется незначительно на катализаторе 3. Указанный эффект связан, по-видимому, с более высокой скоростью разложения H2O2 на Mo-содержащих системах, и дробная загрузка пероксида водорода позволяет уменьшить его расход на эту побочную реакцию [24]. Для W-содержащего катализатора 3, как следует из анализа данных таблицы, этот эффект менее существенен. Следует также отметить исключительно высокое значение TOF для всех трех катализаторов, на несколько порядков превышающее данные для оксидов W и Mo, известные из литературы [30]. Этот расчет достаточно условен, т.к. не учитывали вклад NiO, поскольку, согласно литературе, его активность значительно уступает производным VI группы [23]. Тем не менее, более высокое значение TOF для катализатора 2 может быть связано именно с вкладом NiO, так как его содержание в этом катализаторе выше, чем в катализаторе 3. Однако по нашему мнению, никель на поверхности носителя в данном случае может выступать в качестве центров адсорбции, в то время как окислительными центрами являются производные W и Mo в высоких степенях окисления.
Таблица 5.
Каталитические свойства образцов в окислении тиофена
| Катализатор | 1 | 2 | 3 |
|---|---|---|---|
| ro, М/ч* | 0.018 | 0.023 | 0.009 |
| TOF (1/ч), ∆n(тиофена)/(n (W или Mo) ч) | 4500 | 6800 | 5000 |
| S1, % | 41 | 53 | 43 |
| S2, % | 56 | 49 |
На рис. 7 приведены кинетические кривые конверсии двух субстратов – тиофена и дибензотиофена – в присутствии образцов 3 и 3-ИЖ. Как видно из рисунка, введение ИЖ способствует увеличению конверсии субстратов, что связано с ее участием в адсорбционном процессе [24].
Рис. 7.
Кинетические кривые конверсии субстратов в присутствии катализаторов 3 и 3-ИЖ (60°, 10 мл 1% раствора тиофена (ДБТ), 0.4 мл H2O2 50%, Мкат = = 0.1 г). (1) Тиофен (Кат-р 3-ИЖ), (2) тиофен (Кат-р 3), (3) дибензотиофен (Кат-р 3-ИЖ), (4) дибензотиофен (Кат-р 3).

Однако роль ИЖ состоит также и в стабилизации катализатора, поскольку в ее отсутствие происходит существенное изменение поверхности и частичный смыв металлического покрытия. Особенно этот эффект заметен в случае окисления тиофена, так как одним из продуктов его превращения является серная кислота. Это видно из сравнения фотографий поверхности образцов 3 и 3-ИЖ после их использования в окислении тиофена (рис. 8).
На рис. 9 представлены данные о стабильности катализатора 3-ИЖ в пяти последовательных циклах реакций пероксидного окисления тиофена и дибензотиофена.
Рис. 9.
Конверсия субстратов в присутствии катализатора 3-ИЖ в пяти последовательных циклах (60°, 10 мл 1% раствора тиофена (ДБТ), 0.4 мл H2O2 50%, Мкат = 0.1 г).
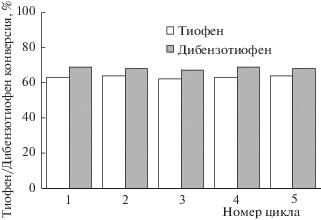
Из анализа рис. 7–9 следует, что введение цвиттер-ионной жидкости способствует дополнительному увеличению конверсии и повышению устойчивости поверхности катализатора к действию реакционной среды, в том числе серной кислоты, образующейся при окислении субстратов.
При окислении серы в дизельном топливе влияние ИЖ оказалось менее существенным: суммарная конверсия S на катализаторе 3 при однократной загрузке H2O2 составила 82% (остаточное содержание S 199 ppm), а на катализаторе 3‑ИЖ 84% (169 ppm). Более действенным оказался прием дробной загрузки H2O2, в результате конверсия S превысила 90%, и после обработки дизельного топлива на катализаторе 3 остаточное содержание S – 92 ppm, на катализаторе 3-ИЖ – 88 ppm.
Таким образом, лазерное электродиспергирование мишеней из спрессованных смесей порошков Ni и Mo или W позволило получить биметаллические наноструктурированные покрытия с заданным соотношением и равномерным распределением компонентов смеси на поверхности гранул оксида алюминия. Компоненты покрытия на поверхности образцов находятся в металлическом и окисленном состояниях в виде наночастиц размером 4–7 нм, степень окисления и доля окисленных состояний металлов определяются поверхностной плотностью частиц. Данные образцы с чрезвычайно низким содержанием активных компонентов меньше 7 × 10-3 мас. % оказались активны в окислении тиофена и дибензотиофена перекисью водорода. Конверсия исходных субстратов на них сопоставима или даже превосходит значения, полученные на известных катализаторах со значительно более высоким содержанием металлов. Высокие значения конверсии сохраняются при многократном использовании катализаторов. Введение в реакционную смесь цвиттер-ионной жидкости способствует дополнительному увеличению конверсии и повышению устойчивости поверхности катализатора к действию реакционной среды, в том числе серной кислоты, образующейся при окислении субстратов. Показана перспективность использования новых высокоактивных и стабильных катализаторов для окислительного обессеривания дизельного топлива.
Работа выполнена с использованием оборудования, приобретенного по Программе развития Московского университета. Формирование структур катализаторов проведено в рамках темы госзадания ФТИ им. А.Ф. Иоффе.
Список литературы
Hong S., Lee H., Yeo J., Hwan Ko S. // Nano Today. 2016. V. 11. P. 547.
Zhang J., Chaker M., Ma D. // J. Coll. Interface Sci. 2017. V. 489. P. 138–149.
Rudnev V.S., Lukiyanchuk I.V., Vasilyeva M.S. et al. // Appl. Surf. Sci. 2017. V. 422. P. 1007.
Lokteva E.S., Peristyy A.A., Kavalerskaya N.E. et al. // Pure and Applied Chem. 2012. V. 84. P. 495.
Golubina E.V., Rostovshchikova T.N., Lokteva E.S. et al. // Ibid. 2018. V. 90. P. 1685.
Rostovshchikova T.N., Lokteva E.S., Golubina E.V., Maslakov K.I., Gurevich S.A., Yavsin D.A., Kozhevin V.M. Advanced Size-Selected Catalysts Prepared by Laser Electrodispersion. Advanced Nanomaterials for Catalysis and Energy: synthesis, characterization and application, Ed. V. Sadykov. Elsevier Inc. 2019. P. 61.
Голубина Е.В., Локтева Е.С., Маслаков К.И. и др. // Российские нанотехнологии. 2017. № 12. № 1–2. С. 16.
Кавалерская Н.Е., Локтева Е.С., Ростовщикова Т.Н. и др. // Кинетика и катализ. 2013. Т. 54. № 5. С. 631.
Ростовщикова Т.Н., Шилина М.И., Голубина Е.В. и др. // Известия РАН. Серия хим. 2015. № 4. С. 812.
Гатин А.К., Гришин М.В., Гуревич С.А. и др. // Там же. 2015. № 10. С. 2337.
Mjalli F.S., Ahmed O.U., Al-Wahaibi T. et al. // Reviews in Chem. Eng. 2014. V. 30. № 4. P. 337.
Srivastava V.C. // RSC Adv. 2012. V. 2. № 3. P. 759.
Prajapati Y.N., Verma N. // Fuel. 2018. V. 216. P. 381.
Abdullah W.N.W., Abu Bakar W.A.W., Ali R. et al. // J. Clean. Prod. 2017. V. 162. P. 1455.
Rakhmanov E.V., Tarakanova A.V., Akopyan A.V. et al. // Pet. Chem. 2014. V. 54. № 1. P. 48.
De Oliveira. L.C.A., Costa N.T., Pliego J.R. et al. // Appl. Catal. B-Environ. 2014. V. 147. P. 43.
Muhammad Y., Shoukat A., Rahman A.U. et al. // Chin. J. Chem. Eng. 2018. V. 26. P. 593.
Waqas A. Sulfur in Petroleum: Petroleum Desulfurization Techniques Applying Nanotechnology to the Desulfurization Process in Petroleum Engineering. IGI Global: Hershey. PA. USA. 2016. P. 1.
Hasan Z., Jeon J., Jhung S.H. // J. Hazard. Mat. 2012. V. 205–206. P. 216.
Polikarpova P., Akopyan A., Shigapova A. et al. // Energy Fuels. 2018. V. 32. № 10. P. 10898–10903.
Abdul-Kadhim W., Deraman M.A., Abdullah S.B. et al. // J. Environ. Chem. Eng. 2017. V. 5. P. 1645.
Wan Nazwanie Wan Abdullah, Wan Azelee Wan Abu Bakar, Rusmidah Ali et al. // J. Clean. Prod. 2017. V. 162. P. 1455.
Ismagilov Z., Yashnik S., Kerzhentsev M. et al. // Catal. Rev. Sci.‑Eng. 2011. V. 53. № 3. P. 199.
Tarkhanova I.G., Bryzhin A.A., Gantman M.G. et al. // Surf. Coat. Techn. 2019. V. 362 . P. 132.
Wu Q., Li W.J., Wang M. et al. // RSC Adv. 2015. V. 5. P. 57968.
Moulder J.F., Stickle W.F., Sobol P.E., Bomben K.D. Handbook of X-ray Photoelectron Spectroscopy. Chigasaki: ULVAC-PHI, Inc., 1995. 261 p.
Mansour A.N. // Surf. Sc. Spectra. 1994. V. 3. № 3. P. 231.
Scanlon D.O., Watson G.W., Payne D.J. et al. // J. Phys. Chem. C. 2010. V. 114. № 10. P. 4636.
Ohno H., Yoshizawa-Fujita M., Kohno Y. et al. // Phys. Chem. Chem. Phys. 2018. V. 20. P. 10978.
Zhang B., Jiang Z., Li J. et al. // J. Catal. 2012. V. 287. P. 5.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии