Журнал физической химии, 2019, T. 93, № 12, стр. 1865-1869
Эффект рассеяния ультрафиолетового излучения деионизованной водой
Д. Л. Тытик a, *, С. А. Бусев a, В. В. Высоцкий a, А. А. Ревина a, О. В. Суворова a, В. И. Кузьмин b, А. Ф. Гадзаов b
a Российская академия наук, Институт физической химии и электрохимии им. А.Н. Фрумкина
119991 Москва, Россия
b Московский технологический университет (МИРЭА)
119454 Москва, Россия
* E-mail: dtytik@yandex.ru
Поступила в редакцию 15.03.2019
После доработки 18.04.2019
Принята к публикации 14.05.2019
Аннотация
Обнаружен эффект возрастания интенсивности рассеяния света в УФ-области во времени образцом деионизованной воды, находящейся на воздухе. Дополнительно изучена зависимость интенсивности рассеяния УФ-излучения деионизованной водой от длины волны. Определена температурная зависимость рассеяния лазерного излучения при λ = 633 нм деионизованной водой.
Вода, по мнению многих исследователей, сложная микрогетерогенная жидкость, обладающая многими уникальными свойствами [1, 2]. В данной работе представлены результаты исследования эффекта рассеяния ультрафиолетового излучения образцами деионизованной воды, взятыми непосредственно из системы очистки без контакта с воздухом (система Milli Q Gradient, время между концом процесса деионизации и началом эксперимента не превышало 5 мин)11. Этот эффект был обнаружен практически случайно при проведении исследований флуоресценции разного рода хемилюминесцентными индикаторами. В одном из таких экспериментов мы наблюдали быстрый рост интенсивности полосы света, на которой происходило возбуждение флуоресценции. Следует заметить, что при флуориметрических измерениях полоса возбуждения обычно исключается из рассмотрения. Обнаруженный эффект воспроизводился в многочисленных экспериментах. На наш взгляд, представляет определенный интерес привести конкретные детали этого исследования.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Первоначально изменение оптических свойств деионизованной воды отслеживали по интенсивности полосы возбуждения в диапазоне длин волн λ = 230–360 нм (флуориметр высокого разрешения F 7000, Hitachi). Спектры флуоресценции регистрировали каждые 5 мин в течение 2.5 ч. В экспериментах использовали деионизованную воду. Время от заполнения водой кварцевой кюветы (длина оптического пути (ДОП) – 10 мм) до размещения ее в кюветном отделении прибора не превышало 5 мин.
На рис. 1а представлена динамика изменения интенсивности полосы рассеянного исходного излучения ксеноновой лампы (длина волны возбуждения 264 нм) в спектрах флуоресценции образца, находившегося на воздухе (условия проведения эксперимента: t = 21°С, P = 755 мм рт. ст.). Видно, что интенсивность полосы возбуждения начинает увеличиваться и примерно за 0.8 ч выходит за границу диапазона регистрации (10000 отн. ед.). Оптическая схема флуориметра F 7000 сконструирована таким образом, что возбуждающий свет от ксеноновой лампы направляется на кювету, а рассеянный свет регистрируется ФЭУ под углом 90°. Очевидно, что рост интенсивности рассеяния излучения во времени свидетельствует о росте концентрации центров рассеяния. Для полноты картины на рис. 1б приведена кинетика изменения интенсивности рассеяния излучения не только для линии возбуждения, но и для ее гармоник 528 и 792 нм.
Рис. 1.
Динамика изменения интенсивности (роста в течение 2.5 ч) рассеяния света образцом деионизованной воды, зарегистрированная при длине волны возбуждения 264 нм (а) и кинетика изменения максимумов интенсивности основной линии возбуждения 264 нм и двух гармоник: 528 и 792 нм (б).
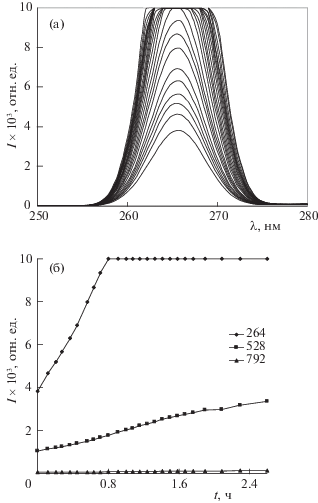
Для оценки величины эффекта рассеяния деионизованной водой света с разной длиной волны проводили оптические эксперименты (флуориметрия) в диапазоне длин волн λ = 230–700 нм (рис. 2). В этом случае эксперимент проводили без доступа воздуха к деионизованной воде (условия проведения эксперимента: t = 23°С, P = 735 мм рт.ст., закрытая кварцевая кювета ДОП – 10 мм). Обратим внимание на локальный минимум (на рис. 2 указан стрелкой) интенсивности рассеяния излучения при длине волны λ = 266 нм. В [3] приведены данные электронной (ультрафиолетовой) спектроскопии о зависимости глубины минимума поглощения излучения гетерогенной системой на длине волны λ ≈ 264 нм от присутствия в ней водородных связей (например, для растворов фенола в воде или в изооктане). Это, по-видимому, и в случае чистой воды указывает на влияние водородных связей на характер ее взаимодействия со светом в окрестности указанной длины волны.
Рис. 2.
Интенсивность рассеяния света деионизованной водой в зависимости от длины волны возбуждения.

Учитывая полученные данные о рассеянии света деионизованной водой при разных длинах волн (рис. 2), естественно было проверить наличие этого эффекта независимым оптическим методом – методом динамического рассеяния света (ДРС) на приборе Malvern ZS. Напомним, что в методе ДРС регистрируется скорость счета фотонов, рассеянных образцом, пропорциональная интенсивности рассеяния света. Эта характеристика используется для расчета корреляционной функции при определении коэффициента диффузии частиц дисперсии. В дальнейшем на основании этого рассчитывается размер частиц дисперсии.
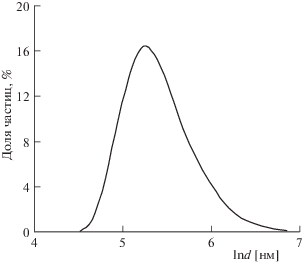
В нашем случае размещение в приборе ДРС акриловой кюветы (ДОП – 10 мм) с деионизованной водой также приводит к регистрации скорости счета фотонов, что указывает на присутствие центров рассеяния света в воде. Однако, интенсивность рассеяния такова, что не удовлетворяет критерию, принятому разработчиками прибора, для корректного применения расчетной методики определения размера “частиц” в воде. В то же время, когда были исследованы образцы деионизованной воды, находившиеся несколько часов на воздухе (закрытый бокс, исключающий осаждение пыли), метод ДРС показал наличие такого же рассеяния света. В частности, в одном из экспериментов средний размер частиц в воде составил dср = 193 ± 25 нм (рис. 3).
Рис. 3.
Распределение размеров “частиц” (нанопузырьков) в деионизованной воде при 25°C в единицах числа частиц (перед экспериментом вода находилась несколько часов на воздухе).
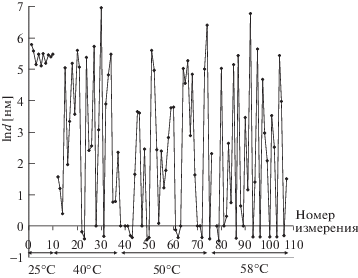
Дополнительно исследовали температурные зависимости рассеяния (термостатирование при 25, 40, 50 и 58°C). Как известно, повышение температуры приводит к уменьшению растворимости газов в воде и, как следствие, может вызывать выделение из нее крупных газовых пузырьков.
На рис. 4 представлены данные о динамике изменения среднего размера частиц в образцах деионизованной воды, предварительно находившихся на воздухе (герметизированный бокс) в течение нескольких часов при t = 25°C и атмосферном давлении (P = 735 мм рт. ст). После этого образцы размещали в приборе ДРС и проводили измерения при соответствующих температурах (средний размер частиц определяли в разные моменты времени усреднением по 15–20 “прогонам”). Обращает на себя внимание значительное колебание среднего размера “частиц”, с одной стороны, для термостатированных при повышенных температурах образцов в течение времени измерения, и небольшая вариация среднего размера “частиц” для образца при комнатной температуре, с другой. Таким образом, повышение температуры приводит к широкому распределению “частиц” по размерам. Кроме того, данные о размере “частиц” в единицах интенсивности указывают на отсутствие крупных “частиц” в образце, находившемся при комнатной температуре. Для образцов же, находившихся при повышенных температурах, в распределениях числа частиц в единицах интенсивности отмечается наличие объектов микронных размеров.
ОБУЖДЕНИЕ РЕЗУЛЬТАТОВ
На основании проведенных экспериментов можно сделать вывод, что мы имеем дело с дисперсией газовых пузырьков в широком диапазоне размеров (от масштаба десятков нанометров до микронных размеров). Иными словами, суть обнаруженного эффекта рассеяния света деионизованной водой состоит в постоянном наличии в ней газовых пузырьков. Отметим, что их распределение по размерам таково, что эффект рассеяния света наиболее проявлен в УФ-области длин волн (рис. 2). Это свидетельствует о том, что их средний размер лежит в диапазоне порядка сотни нанометров.
Проблема пузырьков газов в воде и особенно нанопузырьков чрезвычайно популярна в современной науке о растворах. Начало этому направлению исследований положила, по-видимому, работа [4], в которой продемонстрирована важность процессов, происходящих на границе раздела атмосфера–вода, в частности, формирование слоя газовых пузырьков в приповерхностной области водоемов (море, океан). Отметим важную экспериментальную работу отечественных авторов [5], в которой методом малоуглового рассеяния нейтронов обнаружены микроскопические и, по-видимому, “наноскопические” пузырьки воздуха в воде. В [6] рассмотрены условия формирования стабильных нанопузырьков в объеме воды. В [7] приведена бабстонно-кластерная модель газовой фазы в водных растворах с размером нанопузырьков в диапазоне 30–1000 нм.
Существует достаточно много работ, в которых оцениваются размеры нанопузырьков и их концентрация, например, в [8] отмечается, что преимущественные размеры нанопузырьков в чистой воде находятся в диапазоне 100–200 нм при их концентрации порядка 108–109 1/мл. Следующий момент, который обсуждается в литературе – структура воды на границе раздела газ–жидкость. Для водородных связей молекул воды характерна тетраэдрическая координация, поэтому они, как отмечено в [9], могут сформировать квазикристаллический слой толщиной примерно в три молекулы воды в присутствии стабилизирующего фактора, например, гидрофобной поверхности или газовой фазы. В [9] также приведен и возможный структурный механизм растворения газа, когда молекула газа по системе каналов, образованных на основе полостей (клатраты) [10, 11], проникает в объем воды. Отметим, что при нормальных условиях парциальные давления основных газов в сухой атмосфере составляют примерно: для кислорода – 0.158 атм, азота – 0.598 атм, углекислого газа – 0.03 атм. Кроме того, изменение состава атмосферы, температуры и других параметров влияет на процесс растворения газов в воде. Известно, что растворимость газов в воде быстро уменьшается с увеличением температуры, а, например, при парциальном давлении газа 1 атм и комнатной температуре (t = 20°C) растворимость углекислого газа на порядок превышает растворимость кислорода и азота. Поэтому теоретическая оценка общего количества растворенного газа в 1 л воды требует учета многих физико-химических факторов.
В какой же форме существует в воде растворенный атмосферный газ?
Как было отмечено выше, при атмосферном давлении газ в воде существует в форме газовых нанопузырьков с диапазоном размеров 100–200 нм и концентрацией порядка 109 1/мл. Конечно, какая-то часть молекул газов при комнатной температуре может находиться и в клатратной форме [10, 11], а при повышенных температурах и в форме пузырьков микронных размеров. Следует заметить, что использование термодинамических формул для расчета давления внутри таких нанопузырьков приводит к его громадным значениям. Нам представляется, что, рассматривая процессы молекулярных масштабов, эффективнее использовать модели, учитывающие наличие водородных связей в воде. В частности, для описания процесса растворения газа в воде и формирования нанопузырьков вполне подходит хорошо зарекомендовавшая себя в численных экспериментах модель сетки водородных связей (СВС) в воде [12, 13] и ее расширение – модель упругой сетки водородных связей [14].
В рамках этих моделей может быть сформулирована общая задача о взаимодействии фронта молекул атмосферного газа и упругой сетки водородных связей в объемной воде. При контакте воды с атмосферой каждая молекула газа движется вглубь воды вдоль дефектов СВС. При этом на первой стадии растворения молекула газа, взаимодействуя с молекулами воды, может сформировать газогидрат [10, 11] – своеобразный зародыш нанопузырька. Отметим, что при дальнейшем движении молекул газов внутрь воды в силу сольвофобных эффектов, возникающих при взаимодействии СВС воды с молекулами атмосферных газов, нарастают и силы выталкивания [14]. Таким образом, в процессе растворения газа в воде конкурируют два основных фактора – давление атмосферы на границе газ–жидкость и обратный процесс – выталкивание молекул газа из упругой СВС. Это, по-видимому, приводит к формирующим некоторый оптимум молекулярным процессам, когда избыточное локальное напряжение в упругой СВС может компенсироваться слиянием, например, газогидратных оболочек и последующим формированием более крупных полостей – нанопузырьков. При этом в силу гидрофобного взаимодействия между молекулами газа и молекулами воды внутри пузырька возникает межфазная область [15] (“сферический” слой) по системе сильных водородных связей. Ее “толщина” определяет число сильных водородных связей в межфазной области (связанная вода) и, как следствие, избыточную энергию, необходимую для удержания газа внутри нанопузырька (молекулярный аналог поверхностного натяжения). Энергия сильной водородной связи и возможность супрамолекулярной самоорганизации молекул воды в межфазную область с квазикристаллической структурой [9], по-видимому, определяет достаточно узкие границы размеров нанопузырьков в воде: 100–200 нм. Кроме того, при молекулярном механизме растворения газов в воде происходит динамическая стабилизация СВС, что способствует перераспределению молекул газа и постоянному формированию все новых нанопузырьков. Последнее приводит к “сбрасыванию локальных напряжений”. При изменении внешнего атмосферного давления они уходят из воды и наоборот. Таким образом, вода на открытом воздухе является чрезвычайно “лабильной” системой с постоянно меняющейся “структурой” (состава нанопузырьков) водного раствора.
ЗАКЛЮЧЕНИЕ
По-нашему мнению, общая задача теории водных растворов должна обязательно включать формирование квазиравновесной газовой “нанопузырьковой фазы”. Многие физико-химические свойства водных растворов, по-видимому, определяются постоянным присутствием этой фазы, состояние которой сильно зависит от p–T-условий (и не только) проведения экспериментов. При этом появляется важнейший фактор – внутренняя поверхность нанопузырьков, оценка величины которой при среднем размере нанопузырька 150 нм и их концентрации 4 × 109 1/мл [16] составляет примерно 3000 см2/л (S = πD2 × 4 × × 109 1/мл ≈ 2826 см2/л). Кроме того, межфазная область нанопузырьков, по-видимому, представляет собой связанную (поляризованную) воду, свойства которой и ее влияние на течение физико-химических процессов в водных растворах еще только предстоит исследовать. Такой подход в свою очередь позволит расширить наши представления о зародышеобразовании в водных растворах, разного рода кинетических, электрокинетических явлениях и многом другом.
Авторы выражают признательность М.Н. Родниковой, Г.Г. Маленкову, Ю.И. Наберухину, Н.А. Бульенкову, Е.А. Желиговской, Ю.К. Товбину за обсуждение в разное время отдельных аспектов теории водных растворов.
Авторы выражают благодарность “Центру коллективного пользования физическими методами исследования ИФХЭ РАН” за предоставленную возможность использования в исследованиях приборов: Malvern ZS, флуориметра F 7000.
Работа частично выполнена при финансовой поддержке Российского фонда фундаментальных исследований (код проекта № 19-03-00696).
Список литературы
Эйзенберг Д., Кауцман В. Структура и свойства воды. Л.: Гидрометеоиздат, 1975. 280 с.
Антонченко В.Я., Давыдов А.С., Ильин В.В. Основы физики воды. Киев: Наукова думка, 1991. 672 с.
Кельнер Р., Мерме Ж., Отто М., Видмер Г.М. Аналитическая химия. Проблемы и подходы. Том 2. М.: Мир, 2004. 726 с.
Thorpe A., Stubbs A.R., Hall A.J., Turner R.J. // Nature. 1982. V. 296. P. 636.
Бункин Н.Ф., Виноградова О.И., Куклин А.И. и др. // Письма в ЖЭТФ. 1995. Т. 62. № 8. С. 659.
Oh S.H., Kim J.-M. // Langmuir. 2017. V. 33. P. 3818.
Бункин Н.Ф., Шкирин А.В. // Российская академия наук Труды Института общей физики им. А.М. Прохорова. 2013. Т. 69. С. 3.
Kobayashi H., Maeda S., Kashiwa M., Fujita T. / International Conference on Optical Particle Characterization (OPC 2014). Proc. of SPIE Vol. 9232. P. 92320U-1.
Бульенков Н.А., Желиговская Е.А. // Журн. физ. химии. 2006. Т. 80. № 10. С. 1784.
Дядин Ю.А., Удачин К.А., Бондарюк И.В. Соединения включения. Новосибирск: НГУ, 1988. 101 c.
Белослудов В.П., Дядин Ю.А., Лаврентьев М.Ю. Теоретические модели клатратообразования. Новосибирск: Наука, 1991. 128 с.
Malenkov G.G., Tytik D.L., Zheligovskaya E.A. // J. Mol. Liq. 2003. V. 106/2–3. P. 179.
Волошин В.П., Желиговская Е.А., Маленков Г.Г. и др. // Рос. хим. журн. 2001. т. 45. № 3. с. 31.
Родникова М.Н. / В кн.: Цивадзе А.Ю. (ред.) Структурная самоорганизация в растворах и на границе раздела фаз. М.: ЛКИ, 2008. С. 151.
Товбин Ю.К. Малые системы и основы термодинамики. М.: Физматлит, 2018. 403 с.
Fujita T. / 7th International Symposium of Fine Bubble Technology. Sydney, Australia. 2016. July 25.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии