Журнал физической химии, 2019, T. 93, № 12, стр. 1907-1909
Фазовые диаграммы систем фуллеренол-d–LaCl3–H2O и фуллеренол-d–GdCl3–H2O при 25°С
В. А. Кескинов a, b, *, К. Н. Семенов a, c, Т. С. Гольцов a, Н. А. Чарыков a, d, Н. Е. Подольский c, А. В. Куриленко a, Ж. К. Шаймарданов b, Б. К. Шаймарданова b, Н. А. Куленова b
a Санкт-Петербургский государственный технологический институт (технический университет)
190013 Санкт-Петербург, Россия
b Восточно-Казахстанский государственный технический университет им. Д. Серикбаева
070000 Усть-Каменногорск, Казахстан
c Санкт-Петербургский государственный университет
199034 Санкт-Петербург, Россия
d Санкт-Петербургский государственный электротехнический университет “ЛЭТИ”
197376 Санкт-Петербург, Россия
* E-mail: keskinov@mail.ru
Поступила в редакцию 18.02.2019
После доработки 28.03.2019
Принята к публикации 09.04.2019
Аннотация
Методом насыщения изучены изотермические фазовые диаграммы трехкомпонентных систем фуллеренол-d–LaCl3–H2O и фуллеренол-d–GdCl3–H2O при 25°С. Установлено, что диаграммы растворимости этих систем – простые эвтонические, характеризуются сильным высаливанием хлоридов при добавлении фуллеренола-d и короткими ветвями кристаллизации кристаллогидратов LaCl3 · 7H2O и GdCl3 · 6H2O, на которых наблюдается эффект всаливания.
В продолжение серии работ [1–9], посвященных изучению фазовых равновесий растворимости в системах с участием полигидроксилированного фуллерена (фуллеренола-d): С60(ОН)22–24–неорганическая соль (NaCl, CuCl2, Pr(NO3)3, YCl3, UO2SO4, SmCl3)–H2O. В данной работе исследована растворимость в двух тройных системах: фуллеренол-d–LaCl3–H2O и фуллеренол-d–GdCl3–H2O при 25°С.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реактивы
Использовали оксиды редкоземельных элементов –Ln2O3, Gd2O3 (марки “ч.д.а.”, ТУ 48-4-496-88 и ТУ 48-4-523-89); прочие реактивы для синтеза и комплексонометрического определения LaCl3 и GdCl3 (НСl, CH3COOH, NaOH, C10H14O8N2Na2 · 2H2O (ЭДТА), С31Н28N2Na4O13S (ксиленовый оранжевый), и [трет-(C4H9)4N]OH (гидроксид тетрабутиаммония), С6Н4(СН3)2 (о‑ксилол), CH3OH все марки “ч.д.а.”; фуллерен С60 (производства ЗАО ИЛИП, чистоты 99.5 мас. %, произведенный по ТУ 21 6690 3-58381082). Синтез LaCl3 · 7Н2О и GdCl3 · 6Н2О осуществляли прямой реакцией с НСl c последующей мягкой сушкой продукта. Фуллеренол-d получали с помощью метода прямого межфазного окисления С60 (растворенного в о-ксилоле) NaOH (растворенного в воде) в присутствии межфазного катализатора [трет-(C4H9)4N]OH (см., например, [1, 8]). Полученный продукт нейтрализовали HCl и отмывали от NaCl с помощью CH3OH в аппарате Сокслета В результате получали продукт С60(ОН)22–24 весьма высокой чистоты 99 мас. % с узким распределением по числу привитых гидроксогрупп – С60(ОН)22–24 и практически без примеси ненейтрализованного Na. Фуллеренол-d идентифицировали с помощью элементного анализа, ВЭЖХ, ИК-спектроскопии, масс-спектроскопии, спектрофотометрии в УФ и видимой части света.
Методика изучения растворимости в системах фуллеренол-d–LaCl3–H2O и фуллеренол-d–GdCl3–H2O при 25°С
Насыщенные растворы в тройных системах фуллеренол-d–LaCl3–H2O и фуллеренол-d–GdCl3–H2O готовили методом изотермического насыщения в ампулах в условиях шейкер-термостата (ν = = 2 Гц, ∆T = 25.0 ± 0.1°С, время насыщения t = 8 ч).
Концентрацию фуллеренола-d определяли спектрофотометрически – по оптической плотности в ближней ультрафиолетовой области на длине волны λ = 350 нм (спектрофотометр Shimadzu). Оказалось, что для водных растворов фуллеренола-d закон светопоглощения Бугера–Ламберта–Бера выполняется во всей области концентраций при λ = 350 нм (экстинкция ε350(С60(ОН)22–24) = 16000 см2/г). В то же время коэффициенты экстинкции LaCl3 и GdCl3 при λ = = 350 нм более, чем на 4 порядка меньше: ε350 (LaCl3 и GdCl3) $ \ll $ ε350(С60(ОН)22–24), и светопоглощением хлоридами редкоземельных элементов можно пренебречь. Для пересчета объемных концентраций $С_{{{{{\text{С}}}_{{60}}}{{{({\text{ОН}})}}_{{22--24}}}}}^{{\text{V}}}$ (г/дм3) в весовые концентрации ${{C}_{{{{{\text{С}}}_{{60}}}{{{({\text{ОН}})}}_{{22--24}}}}}}$ (мас. %) (см. табл. 1) пикнометрическим методом определяли плотность насыщенных тройных растворов фуллеренол-d–LaCl3–H2O и фуллеренол-d–GdCl3–H2O при 25°С. Использовали кварцевые термометры с рабочим объемом около 5 см3, ∆ρ = 0.0002 г/см3).
Таблица 1.
Изотермические фазовые диаграммы систем фуллеренол-d–LaCl3–H2O и фуллеренол-d–GdCl3–H2O при 25°С (с1 – концентрация С60(ОН)22–24, с2 – концентрация LaCl3 или GdCl3)
| с1, мас. % | с2, мас. % | Твердая фаза |
|---|---|---|
| фуллеренол-d–LaCl3–H2O | ||
| 0.00 | 5.02 | C60(OH)22–24 · 9H2O |
| 0.18 | 5.00 | – |
| 0.37 | 4.81 | – |
| 0.81 | 4.43 | – |
| 1.09 | 4.1 | – |
| 1.12 | 4.00 | – |
| 1.48 | 2.87 | – |
| 2.06 | 1.30 | – |
| 2.59 | 0.81 | – |
| 7.21 | 0.44 | – |
| 18.51 | 0.042 | – |
| 28.19 | 0.055 | – |
| 37.96 | 0.058 | – |
| 46.10 | 0.060 | – |
| 49.26 | 0.063 | C60(OH)22–24 · 9H2O + LaCl3 · 7H2O |
| 49.17 | 0.056 | LaCl3 · 7H2O |
| 48.88 | 0.041 | – |
| 48.54 | 0.019 | – |
| 48.20 | 0.00 | – |
| фуллеренол-d–GdCl3–H2O | ||
| 0.00 | 5.07 | С60(ОН)22–24 · 9Н2О |
| 0.30 | 3.14 | – |
| 0.55 | 3.02 | – |
| 0.77 | 2.99 | – |
| 1.04 | 2.52 | – |
| 1.73 | 1.41 | – |
| 11.67 | 0.45 | – |
| 31.47 | 0.24 | – |
| 34.49 | 0.23 | – |
| 37.98 | 0.22 | – |
| 39.66 | 0.20 | – |
| 45.11 | 0.19 | – |
| 47.11 | 0.20 | C60(OH)22–24 · 9H2O + GdCl3 · 6H2O |
| 46.97 | 0.16 | GdCl3 · 6H2O |
| 46.82 | 0.11 | – |
| 46.66 | 0.05 | – |
| 46.52 | 0.00 | – |
Для определения концентраций редкоземельных металлов – La3+ и Gd3+ использовали метод комплексонометрического титрования (титрант – Трилон-Б, условия кислотности – ацетатный буферный раствор, индикатор – ксиленовый оранжевый, переход: фиолетовый → желтый).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Данные по растворимости в двух тройных системах фуллеренол-d–LaCl3–H2O и фуллеренол-d–GdCl3–H2O при 25°С представлены в табл. 1 и на рис. 1, 2. Установлено, что обе диаграммы растворимости – простые эвтонические [9], содержат по две ветви кристаллизации – С60(ОН)22–24 · · 9H2O и LaCl3 · 7H2O (рис. 1) и С60(ОН)22–24 · 9H2O и GdCl3 · 6H2O (рис. 2) соответственно. На обеих диаграммах имеется по одной нонвариантной точки – эвтонике [10] (Е на рис. 1, 2)¸ отвечающих насыщению сразу двумя парами кристаллогидратов. Обе диаграммы характеризуются очень сильным высаливанием хлорида редкой земли при добавлении фуллеренола-d и очень короткими ветвями кристаллизации кристаллогидратов LaCl3 · 7H2O и GdCl3 · 6H2O соответственно, на которых наблюдается эффект всаливания.
Рис. 1.
Растворимость в тройной системе фуллеренол-d–LaCl3–Н2О при 25°С (в верхнем правом углу – фрагмент диаграммы, прилегающий к эвтонике – Е).
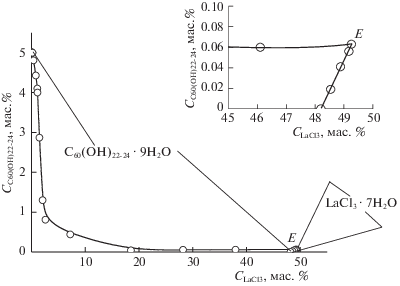
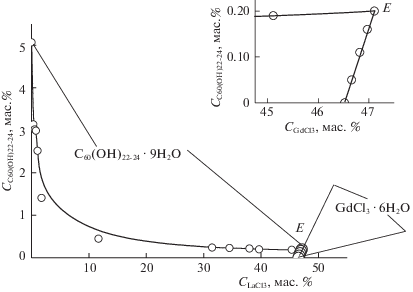
Рис. 2.
Растворимость в тройной системе фуллеренол-d–GdCl3–Н2О при 25°С (в верхнем правом углу – фрагмент диаграммы, прилегающий к эвтонике – Е).
Работа выполнена при поддержке РФФИ (проекты № 18-08-00143 А, № 19-015-00469 А, № 19-016-00003 А).
Список литературы
Semenov K.N., Keskinov V.A., Charykov N.A. et al. // Industrial and Eng. Chem. Res. 2013. V. 52. P. 16095–16100.
Semenov K.N., Charykov N.A., Postnov V.N. et al. // Progress in Solid State Chem. 2016. V. 44. № 2. P. 59.
Семенов К.Н., Чарыков Н.А // Журн. физ. химии. 2012. Т. 86. № 10. С. 1754.
Семенов К.Н., Кантерман И.Г., Чарыков Н.А. и др. // Там же. 2014. Т. 88. № 6. С. 1076.
Семенов К.Н., Кантерман И.Г., Чарыков Н.А., Кескинов В.А // Радиохимия. 2014. Т. 56. № 5. С. 421.
Pestov I.A., Keskinov V.A., Semenov K.N. et al. // Russ. J. Phys. Chem. A. 2015. V. 89. № 6. P. 998.
Юрьев Г.О., Кескинов В.А., Семенов К.Н., Чарыков Н.А. // Журн. физ. химии. 2017. Т. 81. № 5. С. 751.
Semenov K.N., Charykov N.A., Keskinov V.A. // J. Chem. Eng. Data. 2011. V. 56. P. 230.
Semenov K.N., Keskinov V.A., Charykov N.A. et al. // Industrial and Eng. Chem. Res. 2013. V. 52. P. 16095.
Чарыков Н.А., Румянцев А.В., Чарыкова М.В. // Журн. физ. химии. 1998. Т. 72. № 10. С. 1746.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


