Журнал физической химии, 2019, T. 93, № 12, стр. 1910-1912
Размеры и ориентация мицелл тритона Х-100 в водных растворах по данным турбидиметрии
О. А. Федяева a, *, Е. Г. Пошелюжная a
a Омский государственный технический университет
Омск, Россия
* E-mail: kosatine@mail.ru
Поступила в редакцию 19.02.2019
После доработки 19.02.2019
Принята к публикации 12.04.2019
Аннотация
Турбидиметрическим методом определены размеры и ориентация мицелл неионогенного поверхностно-активного вещества Тритон X-100 в водных растворах. Показано, что мицеллы представляют собой вытянутые эллипсоиды, изменяющие свою ориентацию по отношению к падающему свету в зависимости от концентрации раствора.
Тритон X-100 – неиногенное поверхностно активное вещество, которое широко используется в биохимии для солюбилизации белков, липосахаридов и других гидрофобных молекул [1], входит в состав сцинтилляционных жидкостей, используемых при измерениях радиоактивности в водных растворах [2]. Он представляет собой полидисперсный препарат моно-н-(1,1,3,3-тетраметилбутил)фениловый эфир полиэтиленгликоля, содержащий 9–10 оксиэтильных групп в молекуле.
Мицеллы тритона X-100 в водных растворах изучаются достаточно давно [3–17]. Для описания их структуры были предложены две модели частиц – сферические [4–9] и эллипсоидальные [10–17]. Наиболее распространенной в настоящее время является гипотеза о том, что мицеллы данного вещества имеют форму сплющенных эллипсоидов. Авторы [18] при исследовании размера, формы и пространственного расположения молекул тритона X‑100 в агрегированном состоянии установили, что при низких концентрациях его мицеллы являются почти сферическими, а при более высоких концентрациях – эллипсоидальными. О морфологических изменениях мицелл тритона X-100 в водных растворах при добавлении желчных солей сообщается в работе [19]. Трансформацию сферических мицелл в эллипсоидальные авторы объяснили глубоким проникновением молекул желчной кислоты в мицеллы при низком значении pH.
В настоящее время для исследования геометрии структуры макромолекул в растворе используют малоугловое рентгеновское рассеяние [11, 15] и ЯМР-спектроскопию [20]. Эти методы являются универсальными при изучении поверхностно-активных веществ. Полезным дополнением при исследовании их геометрии может стать турбидиметрический метод [21]. Он основан на том, что при прохождении света через коллоидный раствор, в котором отсутствует поглощение, ослабление интенсивности падающего света происходит только за счет его рассеяния дисперсной фазой. При размерах частиц, не превышающих 1/15–1/10 длины световой волны и отношении показателей преломления частиц и дисперсионной среды, равном n1/n2 = 1.15–1.20, величина полного светорассеяния подчиняется уравнению Релея.
Целью данной работы явилось исследование возможности применения турбидиметрического метода для определения размера мицелл тритона X-100 в водных растворах.
Растворы для анализа готовили из коммерческого препарата Triton X-100 фирмы SIGMA-ALDRICH последовательным разбавлением 5.12 × 10–2 моль/л раствора деионизованной водой, полученной на приборе “Водолей”. Значение критической концентрации мицеллообразования (ККМ) определяли кондуктометрическим методом на приборе Мультитест КСЛ. Эта величина при комнатной температуре составила 1.72 × 10‒4 моль/л и согласуется с литературными данными [22]. Cпектры пропускания приготовленных растворов регистрировали на спектрофотометре Specol 1500 с использованием кварцевой кюветы толщиной 1 см. Показатели преломления исходного препарата Triton X-100 и деионизованной воды определяли на рефрактометре ИРФ-454 Б2М. Они оказались равными 1.4886 и 1.3333 соответственно.
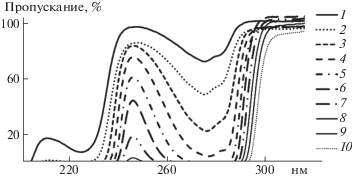
На рис. 1 представлены спектры пропускания водных растворов тритона X-100. Они имеют характерные для феноксильных групп полосы поглощения в области 247–290 нм [22], интенсивность которых изменяется в зависимости от концентрации раствора. При длине волны падающего света, равной 246 нм, поглощение феноксильными группами отсутствует, а интенсивность прошедшего света плавно изменяется с увеличением концентрации раствора. В этих условиях ослабление интенсивности падающего света, вероятнее всего, происходит за счет светорассеяния на мицеллах.
Рис. 1.
Спектры пропускания водных растворов тритона X-100 от его концентрации (моль/л): 1 – 1 × 10–4, 2 – 2 × 10–4, 3 – 4 × 10–4, 4 – 8 × 10–4, 5 – 1.61 × 0–3, 6 – 3.2 × 10–3, 7 – 6.4 × 10–3, 8 – 1.28 × 10–2, 9 – 2.56 × 10–2, 10 – 5.12 × 10–2.
Для проверки данного предположения нами были выполнены расчеты эквивалентных радиусов мицелл тритона X-100 с использованием уравнения Рэлея. Для сферических частиц оно имеет вид:
Размер частиц вычисляли через мутность системы (τ), которая численно равна световой энергии, рассеиваемой 1 см3 раствора во всех направлениях, при интенсивности падающего света, равной единице:
Мутность системы связана с оптической плотностью или пропусканием соотношениями:
где D – оптическая плотность; T – пропускание; L – толщина слоя системы.Объем частицы и ее радиус рассчитывали по формулам:
гдеДля растворов тритона Х-100 из спектров пропускания для λ = 246 нм были рассчитаны значения мутности и построен график зависимости $\frac{\tau }{{{{C}_{V}}}} = f({{C}_{V}})$.
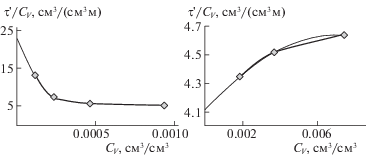
Из графика (рис. 2) видно, что в зависимости от концентрации тритона Х-100 растворы отличаются между собой оптическими свойствами. При этом можно выделить растворы, для которых значение функции $\frac{\tau }{{{{C}_{V}}}} = f({{C}_{V}})$ уменьшается с ростом объемной доли дисперсной фазы, и растворы, для которых эти значения увеличиваются. Для каждого вида растворов графической экстраполяцией величин τ/CV до CV = 0 (рис. 3) были найдены объемы частиц и рассчитаны их радиусы. Для растворов тритона Х-100 с объемной долей дисперсной фазы, равной (1.87–7.47) × 10–3 см3/см3, эквивалентный радиус мицелл составил 6.4 Å, а для растворов с содержанием дисперсной фазы (1.16–9.34) × 10–4 см3/см3 он оказался равным 11.4 Å. Поскольку размеры мицелл и их форма не могут значительно изменяться с разбавлением растворов, полученные результаты можно объяснить эллипсоидальной формой частиц и их различной ориентацией по отношению к падающему свету. При этом эллипсоиды могут принимать вертикальное или горизонтальное сонаправленное со световым потоком положение в зависимости от концентрации раствора поверхностно-активного вещества.
Рис. 3.
Графическая экстраполяция участков кривой $\frac{\tau }{{{{C}_{V}}}} = f({{C}_{V}})$ на ось ординат.
Полученный нами размер полуоси b (11.4 Å) эллипсоидальных мицелл тритона Х-100 согласуются с литературными данными [11, 17]. Эти авторы, предположили, что мицеллы тритона Х-100 имеют форму сплюснутого эллипсоида. Несмотря на то, что рассчитанные ими размеры полуоси b совпали и составляют 10.4 Å, размеры полуоси a у них значительно различаются: 20 Å [17] и 34 Å [11]. Если бы мицеллы имели форму сплюснутых эллипсоидов, вращающихся вокруг малой оси, то они имели бы одинаковый эквивалентный радиус независимо от их ориентации в растворе по отношению к падающему свету. Мицеллы, имеющие форму вытянутых эллипсоидов, при изменении их положения в растворе могут казаться как частицы с различными радиусами.
Таким образом, турбидиметрическим методом мы определили, что мицеллы тритона Х-100 в водных растворах имеют форму вытянутых эллипсоидов вращения с размерами полуосей a = b = = 6.4 Å и с = 11.4 Å. Эллипсоиды изменяют свою ориентацию по отношению к падающему свету в зависимости от концентрации раствора.
Список литературы
Koley D., Bard A.J. // Proceeding of the National Academy of Sciences of the United States of America. 2010. V. 107. № 39. P. 16783.
Беланов С.В., Каширин И.А., Малиновский С.В. и др. Способ идентификации радионуклидов в пробах с использованием жидкостного сцинтилляционного счетчика. Пат. 2132074 РФ, 1999.
Kushner L.M., Hubbard W.D. // J. Phys. Chem. 1954. V. 58. № 12. P. 1163.
Biaselle C.J., Millar D.B. // Biophys. Chem. 1975. V. 3. № 4. P. 355.
Corti M., Degiorgio V. // Opt. Commun. 1975. V. 14. № 3. P. 358.
Dennis E.A., Ribeiro A.A. // ACS Symposium Ser. 1976. № 34. P. 453.
Ribeiro A.A., Dennis E.A. // Biochemistry. 1975. V. 14. № 17. P. 3746.
Ribeiro A.A., Dennis E.A. // J. Phys. Chem. 1976. V. 80. № 16. P. 1746.
Wright A.K. // J. Colloid Interface Sci. 1976. V. 55. № 1. P. 109.
Brown W., Rymden R., Van Stam J., Almgren M., Svensk G. // J. Phys. Chem. 1989. V. 93. № 6. P. 2512.
Robson R.J., Dennis E.A. // Ibid. 1977. V. 81. № 11. P. 1075.
Paradies H.H. // Ibid. 1980. V. 84. № 6. P. 599.
Rao K.S., Goyal P.S., Dasannacharya B.A. et al. // Pramana. 1991. V. 37. P. 311.
Charlton I.D., Doherty A.P. // J. Phys. Chem. B. 2000. V. 104. № 34. P. 8327.
Goyal P.S., Menon S.V.G., Dasannacharya B.A., Thiyagarajan P. // Phys. Rev. E. 1995. V. 51. № 3. P. 2308.
Tanford C., Nozaki Y., Ronde M.F. // J. Phys. Chem. 1977. V. 81. № 16. P. 1555.
Baglione M., Poggi G., Ciolli G. et al. // Materials. 2018. V. 11. № 7 (1144).
Dencova P.S., Van Lokeren L., Verbruggen I., Willem R. // J. Phys. Chem. B. 2008. V. 112. № 35. P. 10935.
Patel V., Bharatiya B., Ray D. et al. // J. Colloid Interface Sci. 2015. V. 441. P. 106.
Mao S.Z., Dy Y.R. // Acta Phys.-Chim. Sin. 2003. V. 19. № 7. P. 675.
Лабораторные работы и задачи по коллоидной химии / Под ред. Ю.Г. Фролова и А.С. Гродского. М.: Химия, 1986. 216 с.
Мицеллообразование и солюбилизация микроэмульсии / Пер. с англ. М.Г. Гольдфельда. Под ред. В.Н. Измайловой. М.: Мир, 1991. 763 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии



