Журнал физической химии, 2019, T. 93, № 3, стр. 476-479
Высокотемпературная теплоемкость и термодинамические свойства Tm2Ge2O7 и TmInGe2O7 в области 350–1000 K
Л. Т. Денисова a, *, Л. А. Иртюго a, Н. В. Белоусова a, В. В. Белецкий a, В. М. Денисов a
a Сибирский федеральный университет, Институт цветных металлов и материаловедения
Красноярск, Россия
* E-mail: antluba@mail.ru
Поступила в редакцию 09.05.2018
Аннотация
Германаты Tm2Ge2O7 и TmInGe2O7 получены твердофазным синтезом из стехиометрических смесей исходных оксидов многоступенчатым обжигом в интервале температур 1273–1473 K. Методом дифференциальной сканирующей калориметрии измерена теплоемкость оксидных соединений. На основании полученных экспериментальных данных рассчитаны температурные зависимости изменения энтальпии, энтропии и приведенной энергии Гиббса.
Уникальные свойства германатов редкоземельных элементов в течение длительного времени привлекают к себе внимание исследователей как компоненты новых материалов [1–6]. В зависимости от природы РЗЭ по типу структур соединения R2Ge2O7 разделяются на четыре структурных подгруппы: La–Pr, Nd–Gd, Tb–Lu, Sc [1]. Германаты с общей формулой A2Ge2O7 и ABGe2O7 (A и B – редкоземельные и трехвалентные элементы, переходные металлы) идентифицируются в двух типах кристаллической структуры тортвейтитоподобной и тортвейтитовой [5]. При этом соединения ABGe2O7 кристаллизуются в четырех разных пространственных группах в зависимости от отношения ионных радиусов rB/rA. К таким материалам относятся Tm2Ge2O7 и TmInGe2O7, которые к настоящему времени являются наименее изученными. В первую очередь это относится к теплофизическим свойствам, которые для этих соединений отсутствуют. Фазовые взаимоотношения в системе Tm2Ge2O7–In2Ge2O7 не построены. В то же время для оптимизации условий твердофазного синтеза и уточнения фазовых равновесий методами термодинамики необходимы сведения об их термодинамических свойствах.
Настоящая работа посвящена экспериментальному определению высокотемпературной теплоемкости Tm2Ge2O7 и TmInGe2O7 в интервале 350–1000 K и расчету, на основании этих данных, их термодинамических функций (изменения энтальпии, энтропии и приведенной энергии Гиббса).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для измерения теплоемкости германаты Tm2Ge2O7 и TmInGe2O7 получены твердофазным методом. Предварительно прокаленные при 1173 K оксиды Tm2O3 (“х.ч.”), In2O3 (“ос.ч.”) и GeO2 (99.999%) тщательно перетирали в агатовой ступке и обжигали на воздухе при 1273 K (40 ч), 1373 K (100 ч) и 1473 K (60 ч). Относительно высокие температуры твердофазного синтеза приводят к частичному испарению GeO2 [2], поэтому синтез проводили в тиглях с крышкой. Кроме того, количество добавляемого сверх стехиометрии GeO2 и время синтеза подбирали экспериментально. Для достижения полноты протекания твердофазного взаимодействия реагентов таблетки через каждые 20 ч перетирали и снова прессовали. Контроль фазового состава синтезированных образцов проводили с использованием рентгенофазового анализа (дифрактометр X’Pert Pro MPD PANalytical, Нидерланды; CoKα-излучение). Регистрацию дифрактограмм выполняли высокоскоростным детектором PIXcel в угловом интервале 2θ = 10–120° с шагом 0.013°. Дифрактограммы синтезированных однофазных образцов приведены на рис. 1. Параметры решеток синтезированных соединений определены подобно [6]. Для Tm2Ge2O7 они в сравнении с данными других авторов приведены в табл. 1. Можно отметить, что наблюдается достаточно хорошее совпадение параметров решетки полученного нами Tm2Ge2O7 с литературными значениями.
Рис. 1.
Экспериментальный (1), расчетный (2) и разностный (3) профили рентгенограмм Tm2Ge2O7 (а) и TmInGe2O7 (б) (штрихи указывают расчетные положения рефлексов).
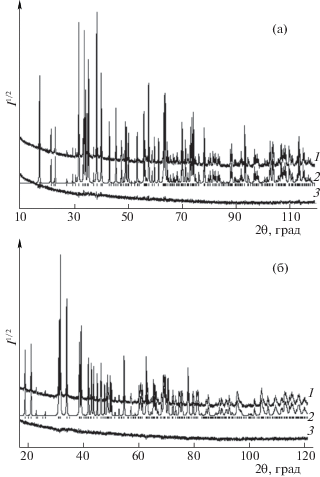
Полученный нами германат TmInGe2O7 имел следующие параметры элементарной ячейки: a = = 6.8060(1) Å, b = 8.8715(2) Å, c = 9.8221(2) Å, β = = 101.90(1)°, V = 580.30(2) Å3, пр. гр. C2/c. Сравнить их с данными других авторов не представлялось возможным вследствие их отсутствия [5].
Высокотемпературная теплоемкость Cp Tm2Ge2O7 и TmInGe2O7 была измерена в области 350–1000 K методом дифференциальной сканирующей калориметрии с помощью термоанализатора STA 449 C Jupiter (NETZSCH, Германия). Измерения проводили в платиновых тиглях с крышкой, при этом использовали специальный держатель TG + DSC 6.226.1–72 + S. Прибор калибровали по температуре и чувствительности при помощи набора солей: RbNO3, KClO4, CsCl, K2Cr2O4, BaCO3 (чистота 99.99%). В качестве эталонного образца использовали синтетический сапфир (Al2O3 чистотой 99.99%) для Cp калибровки (сертификат NETZSCH). Исследуемые материалы перетирали в агатовой ступке и прессовали в таблетки диаметром 6 × 10–3 м на лабораторном прессе ПЛГ-20, после чего подвергали отжигу для исключения процессов спекания. Образцы для измерений предварительно взвешивали на аналитических весах METTLER TOLEDO XP205 Delta Rang с точностью 10–5 г. Масса образцов была близка массе эталона. Внутренний объем печи и весов продувался инертным газом, измерение Cp проводили на воздухе. Скорость нагревания при измерении теплоемкости составляла 10 K/мин. Для каждой серии образцов производили не менее трех измерений. Методика экспериментов описана ранее [8, 9]. Погрешность измерения теплоемкости не превышала 2.8%. Экспериментальные результаты обрабатывали с помощью пакета анализа NETZSCH Proteus Thermal Analysis и лицензионного программного инструмента Systat Sigma Plot 12 (“Systat Software Inc”, США).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
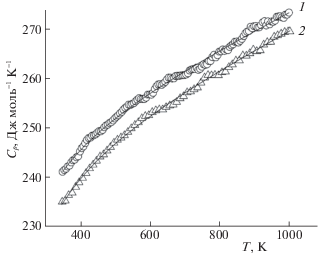
Влияние температуры на теплоемкость Tm2Ge2O7 и TmInGe2O7 показано на рис. 2. Видно, что с ростом температуры значения Cp закономерно увеличиваются, а на зависимостях Cp = f(T) в интервале температур 350–1000 K нет экстремумов. Можно предположить, что это свидетельствует об отсутствии в этой области температур полиморфных превращений у данных германатов. Полученные данные по теплоемкости хорошо описываются уравнением Майера–Келли [10]:
Рис. 2.
Влияние температуры на молярную теплоемкость Tm2Ge2O7 (1), TmInGe2O7 (2). Точки – экспериментальные значения, линия – аппроксимирующая кривая.
для Tm2Ge2O7,
(1)
$\begin{gathered} {{C}_{p}} = (235.1 \pm 0.61) + (35.29 \pm 0.60) \times {{10}^{{ - 3}}}T - \\ - \;(12.98 \pm 0.60) \times {{10}^{5}}{{T}^{{ - 2}}}, \\ \end{gathered} $для TmInGe2O7.
(2)
$\begin{gathered} {{C}_{p}} = (234.8 \pm 0.49) + (36.19 \pm 0.51) \times {{10}^{{ - 3}}}T - \\ - \;(15.91 \pm 0.54) \times {{10}^{5}}{{T}^{{ - 2}}}. \\ \end{gathered} $Коэффициенты корреляции для уравнений (1) и (2) равны 0.9983 и 0.9990 соответственно. Максимальные отклонения экспериментальных точек от сглаживающих кривых составляют 0.53 и 0.43%.
Рассчитанные с помощью этих уравнений величины термодинамических функций Tm2Ge2O7 и TmInGe2O7 приведены в табл. 2. Из нее следует, что значения Cp для этих германатов во всем исследованном интервале температур не превышают классический предел Дюлонга–Пти 3Rs, где R – универсальная газовая постоянная, s – число атомов в формульной единице оксидного соединения.
Таблица 2.
Сглаженные значения молярной теплоемкости и рассчитанные по ним изменения энтальпии H0(T) – H0(350 K), энтропии S0(T) – S0(350 K) и приведенной энергии Гиббса Ф0(Т) = – (ΔG/T) Tm2Ge2O7 и TmInGe2O7
| T, K | Cp, Дж моль–1 K–1 | H0(T) – H0(350 K), кДж моль–1 | S0(T) – S0(350 K), Дж моль–1 K–1 | Ф0(Т) – Ф0(350 K), Дж моль–1 K–1 |
|---|---|---|---|---|
| Tm2Ge2O7 | ||||
| 350 | 240.9 | – | – | – |
| 400 | 245.2 | 12.16 | 32.46 | 2.07 |
| 450 | 248.6 | 24.50 | 61.54 | 7.09 |
| 500 | 251.6 | 37.01 | 87.90 | 13.87 |
| 550 | 254.3 | 49.66 | 112.0 | 21.71 |
| 600 | 256.7 | 62.44 | 134.2 | 30.17 |
| 650 | 259.0 | 75.33 | 154.9 | 38.98 |
| 700 | 261.2 | 88.34 | 174.2 | 47.96 |
| 750 | 263.3 | 101.5 | 192.3 | 56.98 |
| 800 | 265.4 | 114.7 | 209.3 | 65.97 |
| 850 | 267.4 | 128.0 | 225.5 | 74.89 |
| 900 | 269.3 | 141.4 | 240.8 | 83.68 |
| 950 | 271.3 | 154.9 | 255.4 | 92.34 |
| 1000 | 273.2 | 168.5 | 269.4 | 100.8 |
| TmInGe2O7 | ||||
| 350 | 234.5 | – | – | – |
| 400 | 239.3 | 11.85 | 31.64 | 2.02 |
| 450 | 243.2 | 23.92 | 60.06 | 6.91 |
| 500 | 246.5 | 36.16 | 85.86 | 13.54 |
| 550 | 249.4 | 48.56 | 109.5 | 21.21 |
| 600 | 252.1 | 61.10 | 131.3 | 29.48 |
| 650 | 254.5 | 73.77 | 151.6 | 38.10 |
| 700 | 256.9 | 86.55 | 170.5 | 46.89 |
| 750 | 259.1 | 99.45 | 188.3 | 55.73 |
| 800 | 261.3 | 112.5 | 205.1 | 64.55 |
| 850 | 263.3 | 125.6 | 221.0 | 73.29 |
| 900 | 265.4 | 138.8 | 236.1 | 81.92 |
| 950 | 267.4 | 152.1 | 250.5 | 90.42 |
| 1000 | 269.4 | 165.5 | 264.3 | 98.77 |
Сравнить полученные нами значения Cp для Tm2Ge2O7 и TmInGe2O7 с результатами других авторов не представлялось возможным, так как ранее теплоемкость этих соединений не измерялась. В то же время это можно сделать с помощью уравнения Неймана–Коппа [11]
где $c_{{p298}}^{0}(j)$ – удельная теплоемкость сложного оксидного соединения, $c_{{p298}}^{0}(i)$ – удельная теплоемкость i-го простого оксида, mi – мольная доля соответствующего простого оксида. Расчет по уравнению (3) показал, что для Tm2Ge2O7 и TmInGe2O7$c_{p}^{0}$ равны 0.43 и 0.44 Дж K–1 моль–1 соответственно, что несколько выше полученных нами экспериментальных значений 0.40 и 0.42 Дж K–1 моль–1. По данным [12], как положительные, так и отрицательные отклонения от аддитивного правила Неймана–Коппа связаны с изменениями в частотах колебаний атомом в сложном оксидном соединении по сравнению с простыми оксидами. Необходимые значения $c_{p}^{0}$ для расчета по уравнению (3) взяты из литературы: Tm2O3 и GeO2 – [11], In2O3 – [13].Таким образом, определены экспериментальные значения Cp(T) Tm2Ge2O7 и TmInGe2O7 в области 350–1000 K. Рассчитаны температурные зависимости Cp(T), H0(T) – H0(350 K), S0(T) – S0(350 K) и Ф0(Т) – Ф0(350 K) в этом интервале температур.
Работа выполнена при финансовой поддержке работ, выполняемых в рамках Государственного задания Министерства образования и науки Российской Федерации Сибирскому федеральному университету на 2017–2019 годы (проект 4.8083.2017/8.9 “Формирование банка данных термодинамических характеристик сложнооксидных полифункциональных материалов, содержащих редкие и рассеянные элементы”).
Список литературы
Демьянец Л.Н., Лобачев А.Н., Емельченко Г.А. Германаты редкоземельных элементов. М.: Наука, 1980. 152 с.
Becker U.W., Felsche J. // J. Less-Common. Metals. 1987. V. 128. P. 269.
Leskelä M., Ninistö L. // Handbook Phys. Chem. Rare Earth. 1986. V. 8. P. 203.
Juárez-Arellano E.A., Bucio L., Ruvalcaba J.L. et al. // Z. Kristallogr. 2002. V. 217. P. 201.
Juarez-Arellano E.A., Campa-Molina J., Ulloa-Godinez S. et al. // Mater. Res. Soc. Symp. Proc. 2005. V. 848. P. FF 6.15.1.
Денисова Л.Т., Иртюго Л.А., Белецкий В.В. и др. // Физика твердого тела. 2018. Т. 60. № 2. С. 618.
Stadnicka K., Glazer A.M., Koralewski M. et al. // J. Phys.: Condes. Matter. 1990. V. 2. P. 4795.
Денисов В.М., Денисова Л.Т., Иртюго Л.А., Биронт В.С. // Физика твердого тела. 2010. Т. 52. № 7. С. 1274.
Денисова Л.Т., Чумилина Л.Г., Каргин Ю.Ф. и др. // Журн. неорган. химии. 2016. Т. 61. № 11. С. 1515.
Maier C.G., Kelly K.K. // J. Am. Chem. Soc. 1932. V. 54. P. 3243.
Leitner J., Chuchvalec P., Sedmidubský D. et al. // Thermochim. Acta. 2003. V. 395. P. 27.
Резницкий Л.А. Калориметрия твердого тела. М.: МГУ, 1981. 184 с.
Cordfunke E.H.P., Westrum E.F.Jr. // J. Phys. Chem. Solids. 1992. V. 52. P. 361.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


