Журнал физической химии, 2019, T. 93, № 3, стр. 405-413
СОДЕРЖАНИЕ КИСЛОРОДА И ФОРМЫ ЕГО СУЩЕСТВОВАНИЯ В НАНОПОРОШКАХ TaC
А. С. Курлов a, *, Н. Д. Юмашева b, Д. А. Данилов b
a Российская академия наук, Уральское отделение, Институт химии твердого тела
Екатеринбург, Россия
b Уральский федеральный университет имени первого Президента России Б.Н. Ельцина
Екатеринбург, Россия
* E-mail: kurlov@ihim.uran.ru
Поступила в редакцию 16.04.2018
Аннотация
Высокоэнергетическим размолом микрокристаллического порошка TaC получены нанокристаллические порошки со средним размером частиц от 20 до 40 нм. Методами рентгеновской и лазерной дифракции, СЭМ и БЭТ определены фазовый состав, морфология, площадь удельной поверхности и размер частиц нанопорошков. Получена экспериментальная зависимость содержания кислорода в нанопорошках от их площади удельной поверхности. С помощью термодинамического моделирования и фракционного газового анализа установлено, что кислород в нанопорошках TaC находится преимущественно в хемосорбированном состоянии, образуя на поверхности частиц 5–7 монослоев оксидной фазы Ta2O5, независимо от их размера. Показано, что нагрев нанопорошков TaC в отличие от микрокристаллического, может сопровождаться их значительным обезуглероживанием и изменением фазового состава.
Карбид тантала TaC принадлежит семейству тугоплавких соединений [1] и является одним из важнейших компонентов высокотемпературной керамики с высокой твердостью, устойчивостью к окислению, химическому воздействию и термическому удару [2]. Он широко используется в металлургической промышленности в качестве легирующей добавки для упрочнения сталей, а также в качестве ингибитора роста зерен WC при производстве субмикро- и нанокристаллических твердых сплавов WC–Co, которые в настоящее время применяются для производства самого высококачественного бурильного и режущего инструмента [3]. Кроме этого, карбид тантала нашел применение в катализе, в частности, он проявляет каталитическую активность в реакциях гидродеазотирования, дегидрирования и изомеризации, обеспечивает высокую селективность синтеза углеводородов из CO и водорода [4]. Достаточно широкая сфера применения карбида тантала этим не ограничивается, но в большинстве случаев его использования применяются методы порошковой металлургии, которые сопровождаются высокими давлениями и температурами. В связи с этим, стабильность структуры и свойств материалов на основе карбида тантала в процессе эксплуатации зависит не только от технологии их получения, но и во многом определяется качеством и стабильностью исходных порошков TaC, из которых они изготавливаются.
Благодаря постепенному переходу от материалов с микрокристаллической структурой к материалам с нанокристаллической структурой, который, как ожидается, должен сопровождаться заметным улучшением их функциональных свойств [5], на сегодняшний день разработано большое количество способов получения нанокристаллических порошков TaC, среди которых плазмохимический [6] и самораспространяющийся высокотемпературный синтез [7], прекурсорный метод [8], золь–гель-метод с последующим карботермическим восстановлением [9] и др. Однако, одним из наиболее простых и универсальных методов получения карбидных нанопорошков является механический размол, позволяющий получать нанопорошки TaCy с заданным размером частиц и с достаточно узким распределением частиц по размерам [10].
Вместе с переходом на использование нанокристаллических порошков вместо микрокристаллических усугубилась и проблема, связанная с их загрязнением. Чрезвычайно большая площадь границ раздела нанокристаллических порошков обусловливает их высокую химическую активность и делает их очень чувствительными к примесям кислорода, азота и водорода. По этим причинам значительная часть необычных результатов, полученных на различных нанопорошках, особенно в ранний период изучения нанокристаллических веществ – до 1992–1998 года, после тщательной проверки оказалась следствием их загрязнения кислородом, а также другими примесями [11]. На поверхности нанокристаллических порошков карбидов может содержаться адсорбированная вода, а также другие загрязнения, среди которых кислород является наиболее вредной и неизбежной примесью, а его содержание обычно значительно превосходит суммарное содержание всех остальных примесей и определяет общую чистоту порошка [12].
Вследствие хемосорбции кислорода на поверхности карбидных частиц образуются оксиды в разной степени окисления, которые оказывают крайне негативное влияние на их дальнейшее использование [13]. В связи с этим, анализ как общего содержания кислорода, так и различных форм его присутствия в карбидных нанопорошках представляет большой интерес. Появление новых подходов к количественному определению форм существования кислорода, то есть возможность различить его на поверхностный и внутренний [14], позволит организовать рутинный контроль содержания наиболее значимой формы кислорода для стадий подготовки, синтеза, хранения и целевого применения карбидных нанопорошков.
Целью данной работы является определение содержания кислорода и форм его присутствия в нанокристаллических порошках TaC в зависимости от среднего размера частиц.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Нанокристаллические порошки карбида тантала TaC, с разным средним размером частиц от ~20 до ~40 нм, были получены методом высокоэнергетического размола в планетарной шаровой мельнице Retsch PM 200, используя мелющие шары и футеровку размольных стаканов из твердого сплава WC–6 мас. % Co. В качестве исходного был взят микрокристаллический порошок TaC Кировградского завода твердых сплавов (АО “КЗТС”, Россия) со средним размером частиц ~1 мкм (по Фишеру). Средний размер частиц, получаемых нанопорошков, варьировался путем изменения продолжительности размола от 5 до 15 ч, остальные параметры размола были фиксированы: скорость вращения опорного диска размольных стаканов – 500 об./мин; масса порошка, взятого для размола, составляла 10 г; масса мелющих шаров диаметром 3 мм составляла ~100 г; объем размольного стакана – 50 мл; объем изопропилового спирта, добавляемого при размоле, составлял 10 мл. После размола порошки сушили в вакуумном шкафу Binder VDL 23 при остаточном давлении ~103 Па и температуре 358 K.
Содержание общего Ctotal и свободного Cfree углерода в микро- и нанокристаллических порошках TaC определялось путем их сжигания в атмосфере кислорода с помощью анализатора МЕТАВАК CS-30, а затем рассчитывалось содержание в них связанного углерода Cfix = Ctotal – Cfree. Общее содержание кислорода Ototal в этих порошках определялось методом восстановительного плавления в токе аргона на газоанализаторе HORIBA EMGA-620W/С в режиме импульсного нагрева до температуры около 2773 K. Измерения проводились в режиме автоматической загрузки образца. Порошок карбида тантала помещался в оловянную капсулу и при анализе сбрасывался в предварительно дегазированный тигель. Система градуировалась по стандартным образцам стали SS-2-74 и оксида железа JSS-009-3. Для определения форм присутствия кислорода в порошках TaC использовался фракционный газовый анализ в режиме ступенчатого импульсного нагрева, специально подобранного для этих порошков: 623 K – удаление воды и физически адсорбированного кислорода; 2273 K – определение химически связанного поверхностного кислорода; 2773 K – определение остаточного внутреннего кислорода. Измерение проводилось в режиме ручной загрузки. Графитовый тигель заполнялся графитовым порошком и дегазировался, затем вводилась навеска карбида тантала и перемешивалась с графитовым порошком.
Содержание примесных элементов в исследуемых порошках определялось на масс-спектрометре Perkin Elmer SCIEX-ELAN 9000 и энерго-дисперсионным рентгеновским (EDX) анализом на сканирующем электронном микроскопе JEOL JSM 6390 LA с анализатором JED 2300. С помощью этого же микроскопа определялась морфология и размер частиц порошков.
Кристаллическая структура, фазовый состав и параметры решетки микро- и нанокристаллических порошков TaC определялись с помощью рентгеновской дифракции на дифрактометре Shimadzu XRD-7000 с геометрией съемки плоского образца по Бреггу–Брентано в интервале углов 2θ от 10 до 140° с пошаговым сканированием Δ(2θ) = = 0.03° и временем экспозиции 2 с в точке в излучении CuKα1,2. Рентгенограммы анализировались с помощью программного пакета X’Pert HighScore Plus [15]. Для нанокристаллических порошков TaC по уширению дифракционных отражений определялись средний размер DX областей когерентного рассеяния (ОКР), который в первом приближении рассматривался как средний размер частиц порошка, и величина микродеформаций ε без учета их анизотропии, используя методику [16].
Площадь удельной поверхности SBET порошков TaC, до и после размола, измерялась адсорбционным методом Брунауэра–Эммета–Теллера (БЭT) с помощью анализатора площади поверхности и пористости Micromeritics Gemini VII. Перед измерением SBET порошки дегазировались в вакууме ~10 Па при температуре 623 K в течение 1 ч. В приближении одинакового размера и шарообразной формы частиц по измеренной величине SBET определялся средний размер частиц DBET = = 6/(ρXSBET), где ρX – рентгеновская плотность. Рентгеновская плотность ρX рассчитывалась по формуле ρX = nM/NAV, где n = 4 – число формульных единиц TaC, приходящихся на элементарную ячейку с кубической структурой B1; M = = 192.959 г/моль – молярная масса TaC; NA = = 6.022 × 1023 моль–1 – число Авогадро; V = (aB1)3 – объем элементарной ячейки TaC с периодом решетки aB1.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Согласно дифракционным данным исходный порошок карбида тантала TaC-initial является однофазным и имеет кубическую (пр. гр. Fm–3m) структуру типа B1 (рис. 1). Однако, в результате размола исходного порошка в течение разного времени от 5 до 15 ч, наряду с основной кубической фазой TaC, на рентгенограммах нанокристаллических порошков, появляются слабые отражения примесной гексагональной фазы карбида вольфрама WC. Появление примеси WC обусловлено натиранием материала мелющих шаров и футеровки стаканов, изготовленных из твердого сплава WC – 6 мас. % Co. Количественный фазовый анализ показал, что содержание WC в нанопорошках TaC, полученных размолом, возрастает от ~2.5 до ~6.5 мас. % с увеличением продолжительности размола от 5 до 15 ч. Кроме этого, увеличение времени размола tmill сопровождается уширением дифракционных отражений (рис. 1), которое обусловлено малым размером DX областей когерентного рассеяния и наличием микродеформаций ε в нанопорошках. Размер DX во всех изученных нанопорошках TaC приведен в табл. 1. Оценка размера DBET частиц по величине удельной поверхности SBET порошков (табл. 1) в пределах ошибок эксперимента согласуется с размером DX, найденным рентгено-дифракционным методом.
Рис. 1.
Рентгенограммы порошков TaC до и после размола в течение 5, 10 и 15 ч. Пунктирными линиями на рентгенограммах нанопорошков отмечены дифракционные отражения примесного карбида вольфрама WC.
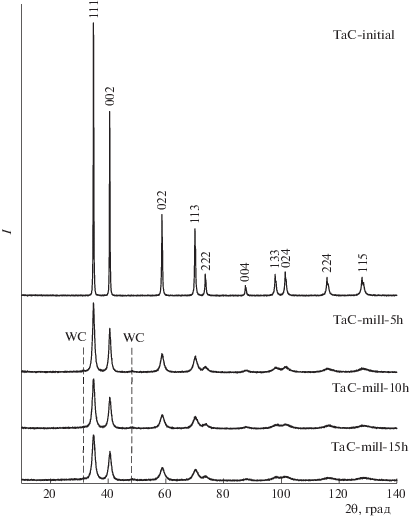
Таблица 1.
Влияние продолжительности размола на химический состав, период кристаллической решетки, плотность, средний размер частиц, величину микродеформаций и площадь удельной поверхности порошков TaC
| Порошок | tmill, ч | [Ctotal ] ± 0.05, мас.% | [Cfree] ± 0.05, мас.% | [Cfix] ± 0.05, мас.% | [Ototal], мас.% | aB1 ± 0.0005, Å | ρX ± 0.01, г/см3 | DX ± 5, нм | ε ± 0.03, % | SBET, м2/г | DBET ± 5, нм |
|---|---|---|---|---|---|---|---|---|---|---|---|
| TaC-initial | 0 | 6.31 | 0.12 | 6.19 | 0.311 ± 0.016 | 4.4552 | 14.49 | – | – | 0.88 ± 0.01 | 471 ± 50 |
| TaC-mill-5h | 5 | 6.31 | 0.26 | 6.05 | 3.06 ± 0.16 | 4.4470 | 14.57 | 42 | 0.80 | 10.8 ± 0.1 | 38 |
| TaC-mill-10h | 10 | 6.38 | 0.37 | 6.01 | 4.63 ± 0.24 | 4.4435 | 14.61 | 28 | 0.93 | 16.4 ± 0.1 | 25 |
| TaC-mill-15h | 15 | 6.40 | 0.49 | 5.91 | 5.61 ± 0.28 | 4.4427 | 14.62 | 23 | 0.97 | 23.2 ± 0.2 | 18 |
По данным сканирующей электронной микроскопии (СЭМ) частицы размолотых порошков TaC намного меньше, чем в исходном порошке (рис. 2). Размол исходного порошка TaC-initial (рис. 2а) в течение 5 ч уже позволяет получить нанопорошок TaC-mill-5h (рис. 2б) с размером частиц менее 100 нм, а более длительный размол в течение 10 и 15 ч позволяет получить нанопорошки TaC-mill-10h и TaC-mill-15h (рис. 2в, г), соответственно, с размером частиц несколько десятков нанометров. Однако в размолотых порошках наночастицы образуют крупные рыхлые агрегаты с размерами от сотен нанометров до нескольких микрометров, что наблюдается не только с помощью СЭМ, но и подтверждается методом лазерной дифракции. Распределения частиц по размеру в нанопорошках TaC, измеренные методом лазерной дифракции, подтвердили сильную агрегацию наночастиц и показали заметно большие средние размеры частиц (в 5–6 раз), чем следует из данных БЭТ и рентгеновской дифракции. Таким образом, в нанопорошках TaC, полученных размолом наблюдается значительная агрегация наночастиц. Избавиться от агрегации не удалось даже при воздействии ультразвука на водную суспензию нанопорошка как до, так и во время измерения методом лазерной дифракции.
Рис. 2.
СЭМ изображения порошков TaC: исходный микрокристаллический порошок TaC-initial (а); нанокристаллические порошки TaC-mill-5h, TaC-mill-10h и TaC-mill-15h (б, в и г), полученные размолом исходного порошка в течение 5, 10 и 15 ч, соответственно.

Увеличение продолжительности размола tmill приводит также к некоторому уменьшению периода решетки в сравнении с исходным порошком (табл. 1), что может быть следствием небольшого изменения состава y карбида тантала TaCy. Небольшое отклонение состава TaCy в результате размола вполне вероятно, поскольку это соединение принадлежит семейству сильно нестехиометрических соединений внедрения и обладает широкой областью гомогенности от TaC0.71 до TaC1.00 [17]. Результаты химического анализа (табл. 1) порошков TaC до и после размола подтверждают это: с увеличением продолжительности размола содержание связанного углерода в порошках TaC уменьшается, а вместе с ним изменяется и состав от TaC1.00 исходного до TaC0.94 после 15-часового размола. Напротив, общее содержание кислорода в порошках TaC увеличивается вместе с увеличением продолжительности размола, что, вероятно, обусловлено, прежде всего, их развитой поверхностью. Площадь удельной поверхности SBET исходного порошка TaC-initial на порядок меньше, чем порошков после размола, а, соответственно, и адсорбирует микрокристаллический порошок намного меньший объем газа, в отличие от нанопорошков, что подтверждается результатами химического анализа (табл. 1).
Найдем соотношение между содержанием адсорбированного газа и площадью удельной поверхности порошка, учитывая только физическую адсорбцию молекул газа на поверхности частиц порошка [18]. Пусть масса порошка равна ms + mg, где ms – масса частиц порошка, а mg – масса газа, адсорбированного на поверхности частиц порошка. Поскольку ms$ \gg $ mg, то массовую долю газа, адсорбированного на поверхности частиц порошка, примем равной ωg = mg/ms.
Допустим, что молекулы газа, в результате адсорбции, образуют на поверхности частиц порошка kg слоев с плотнейшей гексагональной упаковкой (ГПУ), тогда количество молекул адсорбированного газа будет равно
(1)
${{n}_{{\text{g}}}} = {{{{S}_{{{\text{BET}}}}}{{m}_{{\text{s}}}}{{k}_{{\text{g}}}}} \mathord{\left/ {\vphantom {{{{S}_{{{\text{BET}}}}}{{m}_{{\text{s}}}}{{k}_{{\text{g}}}}} {{{\sigma }_{{\text{g}}}}}}} \right. \kern-0em} {{{\sigma }_{{\text{g}}}}}},$С другой стороны, количество молекул адсорбированного газа с молекулярной массой Mg равно ng = mgNA/Mg. Отсюда получаем, что массовая доля газа, адсорбированного на поверхности частиц порошка, равна
(2)
${{\omega }_{{\text{g}}}} = \frac{{{{S}_{{{\text{BET}}}}}{{M}_{{\text{g}}}}{{k}_{{\text{g}}}}}}{{{{\sigma }_{{\text{g}}}}{{N}_{{\text{A}}}}}}.$Поскольку, в карбидных нанопорошках содержание кислорода на порядок перекрывает суммарное содержание всех остальных примесей [12], рассмотрим только адсорбцию кислорода на поверхности частиц порошка TaC. Если предположить, что адсорбированные на поверхности частиц порошка молекулы кислорода образуют ГПУ, то приблизительное значение площади, занимаемой одной молекулой в монослое, можно определить, используя выражение σg = 1.091(Mg/NAρg)2/3 = = 0.141 нм2, в котором ρg = 1.41 г/см3 – плотность кислорода в конденсированном состоянии (сжиженном) [19, 20]. С учетом принятых предположений и допущений выражение (2) можно записать в виде
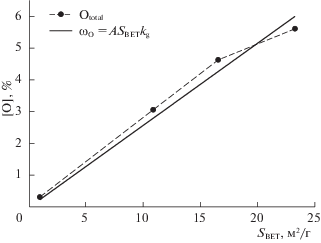
где A = Mg/(σgNA) = 3.763 × 10–4 г/м3.С помощью выражения (3) описана экспериментальная зависимость содержания кислорода в порошках TaC от площади их удельной поверхности (рис. 3). В результате аппроксимации определено среднее количество монослоев kg кислорода, образованных вследствие адсорбции на поверхности карбидных частиц, равное ~7.
Рис. 3.
Содержание кислорода в порошках TaC как функция площади их удельной поверхности SBET. Точками на графике отмечены экспериментальные значения, а сплошной линией их аппроксимация с помощью выражения (3), в котором kg = 6.89.
Выражение (3) подходит для приблизительной оценки общего содержания кислорода в порошках TaC, зная величину их удельной поверхности, но не дает информации о формах его присутствия в этих порошках. В действительности же, кислород в порошках TaC может находиться не только в виде физически адсорбированных молекул на поверхности частиц, но и в виде адсорбированной воды, слабосвязанных с поверхностью углерод-кислородных комплексов, поверхностных оксидов, оксикарбидов и других формах.
Для установления разнообразия форм присутствия кислорода в порошках TaC использовался фракционный газовый анализ (ФГА), который представляет собой модификацию метода высокотемпературной экстракции в токе несущего газа при заданном нагреве образца. Метод анализа основан на различии температурных зависимостей термодинамической прочности оксидов, в которых находится основная часть связанного в образце кислорода [21]. При нагреве образца по заданному режиму происходит взаимодействие присутствующих в нем кислородсодержащих компонентов с графитом тигля и добавляемым графитовым порошком, что приводит к образованию CO или CO2, которые детектируются в потоке инертного газа недисперсионным ИК-детектором. Результатом анализа является эвалограмма, представляющая собой спектр пиков газовыделения CO или CO2, каждый из которых соответствует той или иной форме присутствия кислорода в образце.
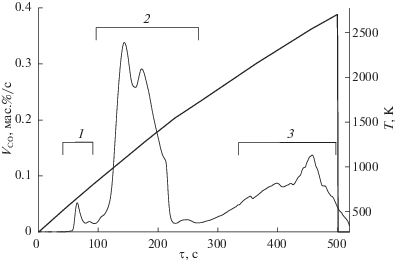
Для микро- и нанокристаллических порошков были получены эвалограммы в режиме линейного нагрева со скоростью ~5 K/с. На всех эвалограммах наблюдаются три группы пиков выделения кислорода в виде CO в интервалах температур: 573–673, 873–1773, 2273–2773 K. В качестве примера, на рис. 4 приведена эвалограмма экстракции кислорода из нанопорошка TaC-mill-15h. Каждая группа наблюдаемых на эвалограммах пиков характеризуется невоспроизводимым профилем, который соответствует определенной форме присутствия кислорода в порошке, что, вероятно, связанно с кинетическими затруднениями при протекании гетерофазных реакций. Чтобы идентифицировать формы присутствия кислорода в порошках TaC, было выполнено термодинамическое моделирование термохимических процессов, протекающих при карботермическом восстановлении образцов во время анализа. Для этих целей использовался программный комплекс HSC Chemistry 6.12, работа которого основана на принципе минимизации изобарно-изотермического потенциала термодинамической системы.
Рис. 4.
Эвалограмма экстракции кислорода в форме CO из нанопорошка TaC-mill-15h при фракционном газовом анализе, полученная в режиме линейного нагрева. На эвалограмме наблюдаются три группы пиков выделения кислорода в виде CO: 1 – 573–673 K, 2 – 873–1773 K, 3 – 2273–2773 K. ${{V}_{{{\text{CO}}}}}$ – скорость выделения СО.
При моделировании предполагалось, что частицы в порошках TaC покрыты кислородсодержащими соединениями, в том числе оксидом тантала Ta2O5. Так как при проведении ФГА в систему вводится еще одна твердая фаза – С (графит), который контактирует с оксидной пленкой на TaC, то при моделировании система была разделена на две подсистемы: С–Ta2O5–Ar (1); TaC–Ta2O5–Ar (2). В качестве исходных данных для каждой подсистемы задавалось следующее количество компонентов: 1 – C – 0.10, Ta2O5 – 0.01 и Ar – 4.5 ммоль; 2 – TaC – 0.18, Ta2O5 – 0.01 и Ar – 4.5 ммоль. Давление в обоих случаях устанавливалось равным 105 Па, а температура изменялась от 300 до 3000 K с шагом 100 К. На основе заданных параметров были получены диаграммы зависимости равновесного состава термодинамических подсистем 1 и 2 от температуры (рис. 5).
Рис. 5.
Диаграммы зависимости равновесного состава термодинамических подсистем от температуры: а – подсистема 1 – С–Ta2O5–Ar с заданными параметрами C – 0.10, Ta2O5 – 0.01 и Ar – 4.5 ммоль; б –подсистема 2 – TaC–Ta2O5–Ar с заданными параметрами TaC – 0.18, Ta2O5 – 0.01 и Ar – 4.5 ммоль. Расчеты выполнены в программном комплексе HSC Chemistry 6.12.
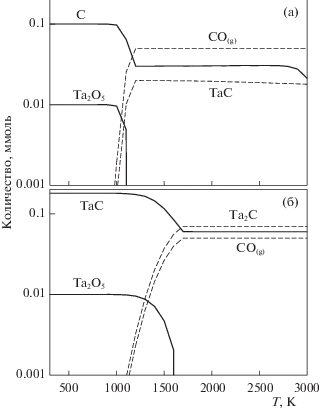
Моделирование показало, что весь рассматриваемый диапазон температур можно условно разделить на три последовательных интервала. При температурах до 900 К Ta2O5 является наиболее термодинамически устойчивым соединением рассматриваемой системы и практически не подвержен восстановлению C, поэтому предварительный нагрев системы до температуры, не превышающей 900 К, можно использовать для удаления адсорбированной воды и физически связанного кислорода. В интервале температур от 900 до 1200 К равновесный состав претерпевает существенные изменения, так как содержащийся в Ta2O5 кислород должен количественно конвертироваться в CO (рис. 5а). Однако, другой твердой равновесной фазой в этих условиях выступает TaC, который образуется на поверхности оксидной пленки и препятствует контакту С с Ta2O5. Согласно результатам термодинамического моделирования подсистемы (2), полная конверсия кислорода в CO завершается при температуре не менее 1700 K (рис. 5б), а снятию кинетических затруднений твердофазной реакции между Ta2O5 и TaC будет способствовать нагрев системы до температуры плавления Ta2O5 (2145 К).
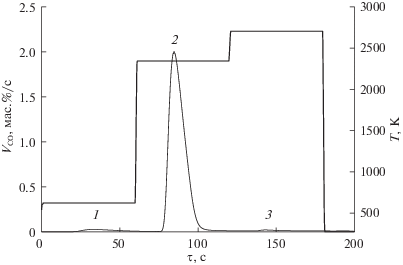
Сопоставляя экспериментальные результаты ФГА, полученные при линейном нагреве (рис. 4), с результатами термодинамического моделирования (рис. 5) был подобран оптимальный режим ступенчатого импульсного нагрева пробы (рис. 6), позволяющий выделить три последовательные стадии газовыделения CO, обусловленные различными формами нахождения кислорода в исследуемых порошках: 1 – обратимо адсорбированных поверхностью соединений, например, воды и физически связанного кислорода, 2 – хемосорбированного на поверхности кислорода, 3 – кислорода внедренного в кристаллы TaC. Кислород, содержащийся в кристаллах TaC, начинает выделяться только при температурах более 2300 К. Импульсный нагрев до температур выше 2800 К в ходе анализа позволяет конвертировать весь кислород в CO и определить его общее содержание, в то время как линейное или ступенчатое увеличение температуры дает информацию о исходном состоянии кислорода в пробе.
Рис. 6.
Эвалограмма экстракции кислорода в форме CO из нанопорошка TaC-mill-5h при фракционном газовом анализе, полученная в режиме ступенчатого импульсного нагрева. На эвалограмме выделены три последовательные стадии газовыделения CO, обусловленные различными формами нахождения кислорода в порошке: 1 – обратимо адсорбированные поверхностью кислород и его соединения (вода, углерод-кислородные комплексы и др.); 2 – хемосорбированный на поверхности кислород (поверхностные оксиды); 3 – кислород, внедренный в кристаллы TaC.
Выполненный в режиме подобранного ступенчатого импульсного нагрева пробы ФГА показал, что практически весь кислород (более 90%), содержащийся в порошках TaC, присутствует в них преимущественно в форме оксида тантала (табл. 2).
Таблица 2.
Анализ содержания кислорода в порошках TaC в режиме ступенчатого импульсного нагрева и оценка потери углерода в них при нагреве
| Порошок | № пика* | [Opart], мас.% | [Ototal], мас.% | [Opart], % | koxide | ΔC, мас.% | [Cresid], мас.% | y** |
|---|---|---|---|---|---|---|---|---|
| TaC-initial | 1 | 0.0069 ± 0.0007 | 0.225 ± 0.011 | 3.1 | ||||
| 2 | 0.210 ± 0.011 | 93.3 | 6.97 | 0.16 | 6.15 | 0.99 | ||
| 3 | 0.0082 ± 0.0008 | 3.6 | ||||||
| TaC-mill-5h | 1 | 0.0116 ± 0.0012 | 2.21 ± 0.11 | 0.5 | ||||
| 2 | 2.19 ± 0.11 | 99.0 | 6.04 | 1.65 | 4.66 | 0.74 | ||
| 3 | 0.0096 ± 0.0010 | 0.5 | ||||||
| TaC-mill-10h | 1 | 0.080 ± 0.008 | 3.61 ± 0.18 | 2.2 | ||||
| 2 | 3.52 ± 0.18 | 97.5 | 6.38 | 2.65 | 3.73 | 0.58 | ||
| 3 | 0.0093 ± 0.0009 | 0.3 | ||||||
| TaC-mill-15h | 1 | 0.084 ± 0.008 | 4.14 ± 0.21 | 2.0 | ||||
| 2 | 4.05 ± 0.21 | 97.8 | 5.21 | 3.04 | 3.36 | 0.52 | ||
| 3 | 0.0060 ± 0.0006 | 0.2 |
* в соответствии с рис. 6 **y = C/Ta в системе Ta-C (т.е. для TaCy)
Оценим степень заполнения поверхности частиц TaC оксидной пленкой Ta2O5. Для кубического (пр. гр. Fm–3m) карбида TaC с периодом решетки aB1 степень заполнения поверхности атомами Ta будет равна nTa = 1/(aB1)2 ≈ 5 × 1018 ат./м2. Таким образом, для образования на поверхности TaC площадью 1 м2 монослоя оксидной фазы Ta2O5 необходимо (5/2)nTaMO/NA кислорода по массе, где MO = 15.999 г/моль – молярная масса O. Зная массовую долю кислорода ωO в составе оксидной фазы Ta2O5 в порошке TaC, можно оценить приблизительное количество монослоев koxide этой оксидной фазы с помощью выражения:
(4)
${{k}_{{{\text{oxide}}}}} = \frac{{2{{\omega }_{{\text{O}}}}{{N}_{{\text{A}}}}}}{{5{{n}_{{{\text{Ta}}}}}{{M}_{{\text{O}}}}{{S}_{{{\text{BET}}}}}}}.$По приблизительной оценке, хемосорбированного в порошках TaC кислорода хватило бы на формирование 5–7 монослоев оксидной фазы Ta2O5 на поверхности карбидных частиц (табл. 2). Причем, как показал ФГА порошков, толщина оксидной пленки, покрывающая поверхность карбидных частиц не зависит от площади удельной поверхности порошков, а значит и от размера самих частиц.
В случае высокотемпературного спекания в вакууме или инертной атмосфере, при нагреве порошков TaC, хемосорбированный кислород будет десорбироваться из них, преимущественно в виде CO и CO2, что будет сопровождаться потерей углерода с поверхности карбидных частиц. Допустим, что при высокотемпературном спекании порошков TaC весь хемосорбированный кислород десорбируется в виде CO, тогда относительная потеря углерода составит ΔC = (MC/MO)ωO, где ωO – массовая доля кислорода в составе оксидной фазы, MС и MO – молярные массы C и O, соответственно. Приблизительная оценка максимально возможной потери углерода из-за десорбции хемосорбированного кислорода показала, что высокотемпературное спекание нанокристаллических порошков TaC, в отличие от микрокристаллического, может сопровождаться их значительным обезуглероживанием, которое в конечном счете приведет к заметному изменению состава y карбида TaCy и, как следствие, фазового состава порошка (табл. 2). Данное предположение подтверждается в экспериментальных работах [22, 23], посвященных влиянию температуры вакуумного отжига на размер частиц и фазовый состав нанопорошков WC и VCy.
Таким образом, установлено, что с уменьшением размера частиц порошков TaC и увеличением их площади удельной поверхности содержание в них общего кислорода линейно возрастает. Большая часть кислорода присутствует в порошках в хемосорбированном состоянии, образуя на поверхности карбидных частиц 5–7 монослоев оксидной фазы Ta2O5, независимо от их размера. В связи с этим, использование нанопорошков TaC вместо микрокристаллических может быть затруднительным, так как нагрев нанопорошков до высоких температур будет сопровождаться их сильным обезуглероживанием и, как следствие, изменением фазового состава.
Список литературы
Стормс Э. Тугоплавкие карбиды. М.: Атомиздат, 1970. 304 с.
Костиков В.И., Варенков А.Н. Сверхвысокотемпературные композиционные материалы. М.: Интермет Инжиниринг, 2003. 560 с.
Панов В.С., Зайцев А.А. // Изв. вузов. Порошк. металлургия и функц. покрытия. 2015. № 2. С. 44.
Kojima I., Miyazaki E., Inoue Y., Yasumori I. // J. Catal. 1982. V. 73. P. 128.
Коч К., Овидько И.А., Сил С., Вепрек С. Конструкционные нанокристаллические материалы. Научные основы и приложения / Пер. с англ. под ред. М.Ю. Гуткина. М.: ФИЗМАТЛИТ, 2012. 448 с.
Исаева Н.В., Благовещенский Ю.В., Благовещенская Н.В. и др. // Изв. вузов. Порошк. металлургия и функц. покрытия. 2013. № 3. С. 7.
Yeh C.L., Liu E.W. // J. Alloys Comp. 2006. V. 415. P. 66.
Lu Y., Ye L., Hana W. et al. // Ceram. Intern. 2015. V. 41. P. 12475.
Симоненко Е.П., Игнатов Н.А., Ежов Ю.С. и др. // Вестн. Самар. гос. аэрокосм. ун-та. 2011. № 1(25). С. 93.
Курлов А.С., Бельков А.М., Выродова Т.Д., Гусев А.И. // Физика твердого тела. 2015. Т. 57. № 1. С. 66.
Гусев А.И. Наноматериалы, наноструктуры, нанотехнологии. М.: ФИЗМАТЛИТ, 2005. 416 с.
Красовский П.В., Благовещенский Ю.В., Григорович К.В. // Неорган. материалы. 2008. Т. 44. № 9. С. 1074.
Gubernat A. // J. Eur. Ceram. Soc. 2013. V. 33. P. 2391.
Шибаев С.С., Шибаева Т.В., Венедиктова И.П., Григорович К.В. // Перспект. материалы. 2010. № 9. С. 295.
X’Pert HighScore Plus Version 2.2e. Software for powder diffraction measurements, phase identification, Rietveld refinements and crystallographic analyses. PANalytical B. V. 2009.
Курлов А.С., Гусев А.И. // Физ. и хим. стекла. 2007. Т. 33. № 3. С. 383.
Гусев А.И. Нестехиометрия, беспорядок, ближний и дальний порядок в твердом теле. М.: Физматлит, 2007. 856 с.
Карнаухов А.П. Адсорбция. Текстура дисперсных и пористых материалов. Новосибирск: Наука. Сиб. предприятие РАН, 1999. 470 с.
Emmet P.H., Brunauer S. // J. Am. Chem. Soc. 1937. V. 59. P. 1553.
McClellan A.L., Harnsberger H.F. // J. Colloid Interface Sci. 1967. V. 23. P. 577.
Григорович К.В. // Аналитика и контроль. 2000. Т. 4. № 3. С. 244.
Курлов А.С. // Журнал физ. химии. 2013. Т. 87. № 4. С. 664.
Курлов А.С., Белькова Т.Д., Бельков А.М., Ремпель А.А. // Неорган. материалы. 2015. Т. 51. № 12. С. 1339.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


