Журнал физической химии, 2019, T. 93, № 4, стр. 529-535
Дегидрирование бициклогексила на катализаторах Ni/окисленный сибунит
А. Н. Каленчук a, b, *, А. В. Леонов a, В. И. Богдан a, b, Л. М. Кустов a, b
a Московский государственный университет имени М.В. Ломоносова, Химический факультет
Москва, Россия
b Российская академия наук, Институт органической химии им. Н.Д. Зелинского
Москва, Россия
* E-mail: akalenchuk@yandex.ru
Поступила в редакцию 14.07.2018
Аннотация
Исследовано дегидрирование бициклогексила на однокомпонентных Ni-нанесенных катализаторах на окисленном сибуните с содержанием 3, 10 и 20 мас. % Ni. Изучено влияние небольших добавок Pt к Ni-катализаторам на их активность в отношении выделения водорода. Показано, что присутствие никеля в окисленном состоянии способствует электронному переносу с платины, что понижает дегидрирующие свойства двухкомпонентных (Ni–Pt)-катализаторов. Установлено, что образование оболочки из двух металлов на поверхности существенно замедляет процесс метанирования углеродного носителя.
В настоящее время водород считается одной из основных альтернатив углеводородному топливу (бензин и дизельное топливо) для экологически чистого транспорта. Дегидрирование циклоалканов, таких как циклогексан, декалин или бициклогексил с высоким содержанием водорода (>7 мас. %) способно обеспечить хорошую возможность для хранения и подачи на топливный элемент химически чистого водорода без примесей СОх-газов [1–6]. Основной задачей является разработка каталитических систем, сочетающих в себе высокую активность с высокой селективностью по конечному продукту. Наиболее эффективными в реакциях дегидрирования циклоалканов являются Pt- и Ni-содержащие катализаторы [7, 8]. Pt-катализаторы обычно активнее в дегидрировании нафтеновых молекул, но никель намного дешевле. В некоторых случаях содержание дорогого благородного металла может быть снижено посредством введения второго металла, присутствие которого приводит к синергетическому эффекту и смещению химического равновесия в сторону образования конечных продуктов [9–11]. В частности, было обнаружено повышение скорости выделения водорода при дегидрировании циклогексана на двухкомпонентном катализаторе Ni–Pt/C при добавлении 0.5 мас. % Pt в катализатор 20Ni/С по сравнению с соответствующими однокомпонентными катализаторами [9]. При этом, несмотря на повышение активности, селективность в отношении побочного процесса образования метана составила 0.3%, что довольно много для обратимых систем хранения водорода. В [12] эффективность катализатора Pt/С (Сибунит) в отношении выделения водорода при дегидрировании бициклогексила повышали гидрофилизацией поверхности.
В настоящей работе изучали дегидрирование бициклогексила на однокомпонентных катализаторах Ni/С (Сибунит, Сиб) с содержанием Ni 3, 10 и 20 мас. % в сравнении с двухкомпонентными катализаторами Ni–Pt/C с добавками Pt 0.1 и 0.5 мас. % и соответствующими однокомпонентными катализаторами Pt/C. Отдельные образцы катализаторов характеризовались с помощью методов РФА, РФЭС, ТПВ, электронной микроскопии (ПЭМ) и хемосорбции СО.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Однокомпонентные катализаторы Ni/Сибох с содержанием Ni – 3 мас. %, 10 мас. % и 20 мас. % готовили пропиткой по влагоемкости углеродного носителя водным раствором Ni(NO2)3 · 6H2O. В качестве носителя использовали окисленный действием азотной кислоты сибунит Сибох [12] с удельной поверхностью 240 м2/г и средним размером пор 4 нм. После нанесения катализаторы вначале сушили на воздухе при комнатной температуре в течение 24 часов, а затем прокаливали в токе N2 (99.9%, 50 мл/мин) при 500°C в течение 2 ч. Перед реакцией Ni-катализаторы активировали в токе Н2 (99.99%, 50 мл/мин) при 500°C в течение 2 ч.
Однокомпонентные катализаторы Pt/Сибох с содержанием Pt – 3 мас. %, 0.5 мас. %, 0.3 мас. % и 0.1 мас. % готовили пропиткой по влагоемкости окисленного сибунита водным раствором H2PtCl6 · · 6H2O. Затем сушили на воздухе при комнатной температуре в течение 24 ч, после чего прокаливали в токе N2 (99.9%, 50 мл мин) при 350°C в течение 2 ч. Перед реакцией Pt-катализаторы активировали в токе Н2 (99.99%, 30 мл/мин) при 350°C в течение 2 ч. Для сравнения по той же методике были подготовлены катализаторы 0.5 мас. % Pt/Сиб и 0.1 мас. % Pt/Сиб на неокисленном сибуните.
Двухкомпонентные (Ni–Pt)-катализаторы готовили двумя способами. В катализаторах 0.1Pt/3Ni/Сибох, 0.1Pt/10Ni/Сибох и 0.5Pt/3Ni/Сибох, платину наносили из водных растворов H2PtCl6 · 6H2O на прокаленные однокомпонентные катализаторы 3 мас. %Ni/Сибох и 10 мас. %Ni/Сибох, соответственно. Катализаторы сушили на воздухе при комнатной температуре в течение 24 ч, а затем прокаливали в токе N2 (99.9%, 50 мл мин) при 350oC (катализаторы с содержанием платины 0.1 мас. %) и при 150°С (катализатор с содержанием платины 0.5 мас. %) в течение 2 часов. Катализаторы (0.1Pt–3Ni)/Сибох и (0.1Pt–10Ni)/Сибох готовили совместной пропиткой смесью рассчитанных количеств водных растворов H2PtCl6 ⋅ 6H2O и Ni(NO3)2 · 6H2O. После нанесения данной смеси растворов катализаторы вначале сушили на воздухе при комнатной температуре в течение 24 ч, а затем прокаливали в токе N2 (99.9%, 50 мл/мин) при 150°C в течение 2 ч. Перед реакцией все двухкомпонентные (Ni–Pt)-катализаторы активировали в токе Н2 (99.99%, 30 мл/мин) при 500°C в течение 2 ч.
Размер частиц и дисперсность Pt определяли с помощью микроанализатора ASAP 2020 (США) методом необратимой хемосорбции CO при температуре 35°С [13]. Состав поверхности и тип поверхностных функциональных групп определяли с помощью рентгеновской фотоэлектронной спектроскопии (РФЭС) на приборе Kratos Axis Ultra DLD (Великобритания) с монохроматическим AlKα-излучением (1486.6 эВ, 150 В) [14]. Микроструктуру образцов катализаторов изучали методом просвечивающей электронной микроскопии (ПЭM) на электронном микроскопе Hitachi HT7700. Съемку изображений вели в режиме светлого поля при ускоряющем напряжении 100 кВ [15].
Кривые термопрограммируемого восстановления (ТПВ) используемых катализаторов регистрировали на лабораторной установке, состоящей из системы подготовки газов, реактора с трубчатой печью и детектора по теплопроводности. Перед проведением ТПВ катализаторы предварительно подвергали термообработке в инертной атмосфере для разложения остаточных солей металлов. Для этого образцы нагревали в токе азота 30 мл/мин до 400°С со скоростью 10 К/мин, а затем медленно (3 К/мин) охлаждали до комнатной температуры. Затем образцы восстанавливали в токе смеси газов 5% H2/Ar со скоростью 23 мл/мин. Скорость линейного нагрева детектора составляла 12 К/мин.
Фазовый состав образцов и размер первичных кристаллов нанесенных частиц металла определяли методом РФА на приборе DRON-3 в Ni-фильтрованном CuKα-излучении (λ = 0.1542 нм) в режиме пошагового сканирования (с шагом 0.02°) в интервале 2θ = 10°–60°. Идентификацию фазового состава осуществляли соотнесением позиции и интенсивности линий на рентгенограмме с данными ICDD (Международного центра данных по дифракции рентгеновского излучения).
Дегидрирование бициклогексила на Ni- и Ni–Pt-катализаторах проводили в проточном реакторе [6, 12]. Реакцию на всех катализаторах вели в течение 4 ч при температуре 320°С, атмосферном давлении и соотношении катализатор/субстрат – 1.85 г/6 мл ч–1. Продукты реакции анализировали на хроматографе Кристалюкс-4000М (Россия) с использованием капиллярной колонки ZB-5 (“Zebron”, CША) на пламенно-ионизационном детекторе хромато-масс-спектрометра FOCUS DSQ II (“Thermo Fisher Scientific”, США) с капиллярной колонкой TR-5ms. Анализ выполняли в программируемом режиме температуры 70–220°C при скорости нагрева 6 К/мин. Чистоту выделяемого водорода определяли методом газовой хроматографии с детектором по теплопроводности на насыпной колонке Porаpak Q.
Конверсию (X) бициклогексила рассчитывали, как отношение изменения количества бициклогексила до и после реакции к исходному количеству бициклогексила. Селективность (S) по бифенилу определяли, как отношение количества получаемого бифенила к общему количеству продуктов реакции. Активность катализаторов (TOF, ммоль (H2)/гМе мин) в отношении выделения водорода рассчитывали, как отношение молей водорода, выделившегося за весь период дегидрирования бициклогексила, к количеству (г) Pt и разделенному на время проведения реакции.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Для всех используемых в работе катализаторов в качестве продуктов реакции идентифицировали циклогексилбензол (C12H16), бифенил (C12H10) и водород. Других продуктов реакции на однокомпонентных Pt-катализаторах обнаружено не было.
Вначале сравнивали активность однокомпонентных Pt-катализаторов в отношении выделения водорода при снижении содержания платины. Экспериментальные данные, полученные на катализаторах на окисленном и неокисленном углеродном носителе, приведены в табл. 1. Сравнение показывает, что с понижением содержания платины в используемых однокомпонентных Pt-катализаторах конверсия дегидрирования бициклогексила также снижается. Однако, с точки зрения выделения водорода эффективность катализаторов, наоборот, возрастает. Конверсия и селективность по конечному бифенилу, а также TOF выше для катализаторов на окисленном сибуните по сравнению с катализаторами на неокисленном носителе, что подтверждает установленную ранее зависимость [12].
Таблица 1.
Конверсия и селективность Pt/С (сибунит) катализаторов в реакции дегидрирования бициклогексила (Т = 320°С, Р = 1 атм)
| № | Катализатор | Конверсия Х, % (±5%) | Селективность S, % | TOF, ммоль (H2)/гМе мин | |
|---|---|---|---|---|---|
| С12Н16 | С12Н10 | ||||
| 1 | 3.0Pt/Сибох | 84 | 29 | 71 | 47 |
| 2 | 0.5Pt/Сиб | 63 | 39 | 61 | 184 |
| 3 | 0.5Pt/Сибох | 73 | 16 | 84 | 238 |
| 4 | 0.3Pt/Сибох | 64 | 21 | 79 | 359 |
| 5 | 0.1Pt/Сиб | 26 | 42 | 58 | 855 |
| 6 | 0.1Pt/Сибох | 55 | 32 | 68 | 1012 |
В табл. 2 приведены экспериментальные данные по дегидрированию бициклогексила на однокомпонентных Ni-содержащих катализаторах. Сравнение показывает, что бициклогексил практически не дегидрируется на однокомпонентном катализаторе 3 мас. % Ni/Сибох. Повышение содержания никеля до 10 мас. % приводит к росту конверсии до 25%, а селективности – до уровня Pt-катализаторов с низким содержанием платины на неокисленном носителе (табл. 1). При повышении содержания никеля до 20 мас. % конверсия дегидрирования бициклогексила на катализаторе 20 мас. % Ni/Сибох заметно снижается. При этом видно, что активность однокомпонентных Ni-катализаторов по величине конверсии и селективности по бифенилу заметно уступает активности используемых Pt-катализаторов с гораздо меньшим содержанием активного металла. Наряду с низкой конверсией высокое содержание металла в однокомпонентных Ni-катализаторах заметно понижает эффективность (TOF) в отношении выделения водорода. На Ni-катализаторах с содержанием никеля 10 и 20 мас. % были обнаружены следовые концентрации продуктов крекинга.
Таблица 2.
Конверсия и селективность Ni/С (Сибох) катализаторов в реакции дегидрирования бициклогексила (Т = 320°С, Р = 1 атм)
| № | Катализатор | Х, % (±5%) | S, % | TOF, ммоль (H2)/гМе мин | |
|---|---|---|---|---|---|
| С12Н16 | С12Н10 | ||||
| 1 | 3 Ni/Сибох | 4 | 65 | 35 | 27 |
| 2 | 10 Ni/Сибох | 25 | 27 | 73 | 10 |
| 3 | 20 Ni/Сибох | 13 | 37 | 63 | 5 |
При нанесении платины поверх однокомпонентных Ni-катализаторов наблюдается значительное ухудшение каталитических свойств двухкомпонентных Ni–Pt-катализаторов при дегидрировании бициклогексила по сравнению с соответствующими однокомпонентными Pt-катализаторами (табл. 3). При совместном нанесении никеля и платины ситуация улучшается. В данных катализаторах небольшие добавки Pt приводят к росту конверсии и TOF по сравнению с однокомпонентными Ni-катализаторами, но по-прежнему уступают показателям соответствующих однокомпонентных Pt-катализаторов на окисленном сибуните. Превышение конверсии и селективности по бифенилу достигается на двухкомпонентном (0.1Pt–10Ni)/Сибох катализаторе только по отношению к однокомпонентому катализатору 0.1 мас. %Pt/Сиб на неокисленном сибуните. Содержание продуктов крекинга на двухкомпонентных Ni–Pt-катализаторах снизилось по сравнению однокомпонентными Ni-катализаторами.
Таблица 3.
Конверсия и селективность Pt–Ni/С (Сибох) катализаторов в реакции дегидрирования бициклогексила (Т = 320°С, Р = 1 атм)
| № | Катализатор | Х, % (±5%) | S, % | TOF, ммоль (H2)/гМе мин | |
|---|---|---|---|---|---|
| С12Н16 | С12Н10 | ||||
| 1 | 0.1Pt/3Ni/Сибох | 9 | 27 | 73 | 34 |
| 2 | 0.1Pt/10Ni/Сибох | 15 | 37 | 63 | 10 |
| 3 | (0.1Pt–3Ni)/Сибох | 23 | 54 | 46 | 28 |
| 4 | (0.1Pt–10Ni)/Сибох | 40 | 38 | 62 | 10 |
| 5 | 0.5Pt/3Ni/Сибох | 31 | 47 | 53 | 26 |
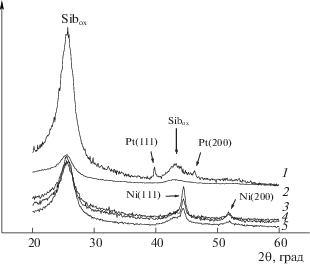
На рис. 1 приведены дифрактограммы однокомпонентных Pt- и Ni-катализаторов. Сравнение показывает, что между дифрактограммами однокомпонентных Ni-катализаторов (табл. 2) нет принципиальных отличий. Соотношение дифракционных пиков коррелирует с содержанием никеля в катализаторах 3%Ni/Сибох, 10%Ni/Сибох и 20%Ni/Сибох. Наиболее интенсивная линия (111) Ni соответствует 2Ɵ = 44.505° (JCPDS 87-712, type Cu), а вторая по интенсивности линия (200) – 2Ɵ = 54.505°. Период решетки по данным линиям составляет а111 ~ 0.3528 нм и а200 ~ 0.3528 нм, что отвечает табличному значению металлического никеля (аNi = 0.3528 нм). Из-за низкой концентрации платины в однокомпонентных Pt-катализаторах (табл. 1) дифракционные пики Pt накладываются на фоновую линию носителя Сибох, что затрудняет оценку параметра решетки платины. Однако, оценка периода решетки Pt (а = = 0.3923 ± 0.0002 нм) по дифрактограмме катализатора сравнения 3%Pt/Сибох, приготовленного по аналогичной методике, полностью соответствует табличному значению для металлической платины (аPt = 0.3923 нм) (JCPDS 87-646, type Cu). Дифрактограммы двухкомпонентных Ni–Pt-катализаторов (табл. 3) не имеют принципиальных отличий от дифрактограмм соответствующих однокомпонентных Ni-катализаторов, что свидетельствует об отсутствии влияния добавок Pt на период решетки никеля.
Рис. 1.
Дифрактограммы катализаторов 3% Pt/Сибох (1), 0.1%Pt/Сибох (2), 3%Ni/Сибох (3), 10%Ni/Сибох (4) и 20%Ni/Сибох (5).
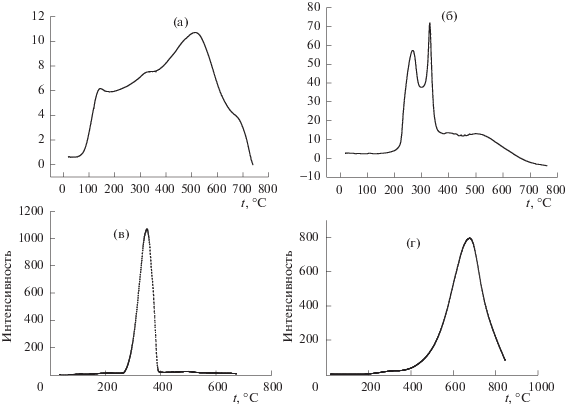
На рис. 2 приведены кривые термопрограммируемого восстановления (ТПВ) для катализаторов 3Ni/Сибох (а) и 0.5Pt/3Ni/Сибох (б) в сравнении с чистым оксидом никеля (NiO) (в) и углеродным носителем Сибох (г). На кривой ТПВ катализатора 3Ni/Сибох в отличие от чистого NiO наблюдается три пика поглощения водорода. Первый пик в диапазоне температур от 130 до 170°C, по-видимому, относится к процессу восстановления NiOOH до оксида никеля (NiO), протекающему по реакции:
Второй пик в диапазоне температур 350–400°C связан с процессом восстановления оксида никеля до металла. И наконец, третий пик связан с процессом гидрогенизации углеродного носителя. Смещение третьего пика в сторону более низких температур по сравнению с чистым носителем, по-видимому, связано с образованием металлической оболочки на поверхности носителя или каталитическим эффектом металла на процесс гидрогенизации углеродного носителя. Присутствие Pt изменяет характер кривой ТПВ двухкомпонентного катализатора 0.5Pt/3Ni/Сибох, по сравнению с катализатором 3Ni/Сибох без платины (рис. 3б). Первый из двух пиков в интервале температур 250–350°C, видимо, соответствует процессу восстановления платины до металла, а второй, как, в однокомпонентном Ni-катализаторе, – образованию оксида никеля. При этом заметно уменьшается интенсивность пика в интервале 450–500°С, что, видимо, связано с подавлением процесса метанирования носителя, вызванным совместным влиянием двух металлов.
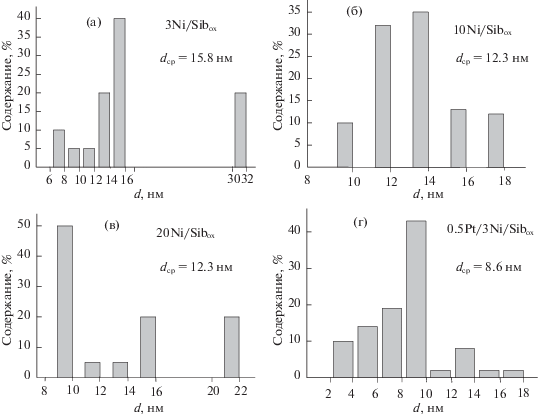
Рис. 3.
Распределение по размерам частиц в катализаторах 3Ni/Сибох (a), 10Ni/Сибох (б), 20Ni/Сибох (в) и 0.5Pt/3Ni/Сибох (г).
Состав и зарядовое состояние металлов на поверхности Pt- и (Ni-Pt)-катализаторов определяли с помощью РФЭС-спектроскопии. Для всех исследованных образцов катализаторов спектры углерода C1s РФЭС идентичны и присутствуют в виде двух линий, характерных для sp2-углерода (более 80%) и sp3-углерода, что свидетельствует о нарушении упорядоченности структуры окисленного сибунита. В Pt4f РФЭС спектрах однокомпонентных Pt-катализаторов более 96% платины находится в состоянии Pt0. В двухкомпонентном катализаторе 0.5Pt/3Ni/Сибох платина находится в трех состояниях: Pt0 (30%), Pt2+ (44%) и Pt4+ (26%). В соответствии со спектрами Ni2p РФЭС никель на поверхности данного катализатора, в основном, присутствует в окисленной форме Ni2+ и только около 2% находится в металлическом состоянии Ni0, что соответствует данным ТПВ анализа.
По данным хемосорбции СО дисперсность и размер частиц кластеров платины в катализаторе 0.5%Pt/Сибох составляет 63% и 1.8 нм, а в двухкомпонентном катализаторе 0.5Pt/3Ni/Sibox – 76% и 1.4 нм соответственно. При снижении содержания платины в катализаторе 0.1%Pt/3Ni/Sibox дисперсность уменьшается до 24%, а размер частиц увеличивается до 4.7 нм. В наиболее активном однокомпонентном Ni-катализаторе 10%Ni/Сибох дисперсность и размер частиц кластеров никеля составляют 7% и 13.8 нм соответственно. Определение дисперсности по хемосорбции СО оказалось завышено, а размер частиц Ni в катализаторе 3%Ni/Сибох занижен из-за легкости образования тетракарбонила никеля Ni(CO)4.
На рис. 3 приведены гистограммы распределения частиц по размерам в однокомпонентных катализаторах 3%Ni/Сибох (а), 10%Ni/Сибох (б), 20%Ni/Sibox (в) и двухкомпонентном катализаторе 0.5Pt/3Ni/Сибох (г), полученных на основе ПЭМ-микрофотографий.
Сравнение гистограмм однокомпонентных Ni-катализаторов показывает, что в катализаторах с содержанием никеля 3 и 20 мас. % наряду с небольшими кластерами присутствуют крупные кластеры. Наличие большего числа кластеров небольшого размера приводит к повышению конверсии с использованием катализатора 20Ni/Сибох. В катализаторе 10Ni/Сибох распределение по размерам частиц кластеров Ni более равномерное, что способствует наибольшей его активности среди трех однокомпонентных Ni-катализаторов. Средний размер частиц в двухкомпонентном катализаторе 0.5Pt/3Ni/Сибох (г) составляет около 9 нм, что больше по сравнению с данными хемосорбции СО для кластеров платины и, видимо, связано с вкладом никеля. Наличие большего количества платины приводит к повышению конверсии, но понижает ТОF данного катализатора. Большое различие в размерах кластеров активных компонентов является вероятной причиной существенного различия в активности Pt- и Ni-катализаторов в реакции дегидрирования бициклогексила. Меньшее содержание платины в состоянии Pt° видимо, также является одной из причин снижения активности двухкомпонентных (Ni–Pt)-катализаторов по сравнению с однокомпонентными Pt-катализаторами. С другой стороны, присутствие никеля, в основном, в окисленном состоянии способствует электронному переносу с платины, и, соответственно, понижает дегидрирующие свойства двухкомпонентных (Ni–Pt)-катализаторов. Повышение температуры приводит к росту выхода продуктов крекинга.
Из литературы известно, что при дегидрировании циклогексана на катализаторах Ni/С с содержанием никеля 10, 20 и 40 мас. % был отмечен синергетический эффект при добавлении 0.5 мас. % Pt в катализатор 20Ni/С [9]. В настоящей работе добавление платины не привело к увеличению активности в реакции дегидрирования бициклогексила при использовании двухкомпонентных катализаторов 0.1Pt/3Ni/Сибох и 0.1Pt/10Ni/Sibox. В обоих случаях наблюдалось увеличение активности обоих катализаторов относительно соответствующих однокомпонентных Ni-катализаторов, но заметно снизилась активность по сравнению с чистым однокомпонентным катализатором 0.1Pt/Сибох, который оказался наиболее активным из всех исследуемых катализаторов. Превышение конверсии наблюдали только для двухкомпонентного (0.1Pt–10Ni)/Сибох катализатора по отношению к однокомпонентому катализатору 0.1 мас. %Pt/Сиб на неокисленном сибуните. Однако, активность катализаторов на окисленном сибуните выше, чем на неокисленном.
Таким образом, несмотря на меньшую стоимость, Ni-катализаторы демонстрируют худшие показатели по сравнению с Pt-катализаторами с точки зрения достижения высокой конверсии и, соответственно, объемов выделяемого водорода для топливных элементов. Способ приготовления и контролируемая функционализация носителя являются важными путями минимизации содержания Pt в катализаторах.
Исследование выполнено при финансовой поддержке Российского научного фонда (грант № 14-50-00126).
Список литературы
Bourane A., Elanany M., Pham T.V., Katikaneni S.P. // Int. J. Hydrogen Energy. 2016. V. 41. P. 23075.
Biniwale R.B., Rayalu S., Devotta S., Ichikawa M. // Ibid. 2008. V. 33. P. 360.
Okada Y., Sasaki E., Watanabe E., Hyodo S., Nishijima H. // Int. J. Hydrogen Energy. 2006. V. 31. P. 1348.
Coughlin R.W., Hasan A., Kawakami K. // J. Catal. 1984. V. 88. P. 163.
Hodoshima S., Hiroshi A., Shigeki T., Yasukazu S. // Int. J. Hydrogen Energy. 2003. V. 28. P. 1255.
Kalenchuk A.N., Bogdan V.I., Dunaev S.F., Kustov L.M. // Fuel Proc. Techn. 2018. V. 169. P. 94.
Stanislaus A., Cooper B.H. // Catal. Rev.-Sci. Eng. 1994. V. 36. P. 75.
Kariya N., Fukuoka A., Ichikawa M. // Appl. Catal. A Gen. 2002. V. 233. P. 91.
Shukla A.A., Gosavi P.V., Pande J.V. et al. // Int. J. Hydrogen Energy. 2010. V. 35. P. 4020.
Xiong L., Manthiram A. // J. Electrochem. Soc. 2005. V. 152. P. 697.
Xiong L., Kannan A.M., Manthiram A. // Electrochem. Commun. 2002. V. 4. P. 898.
Kalenchuk A.N., Bogdan V.I., Dunaev S.F., Kustov L.M. // Int. J. Hydrogen Energy. 2018. V. 43. № 12. P. 6191.
Webb P.A., Orr C. Analytical Methods in Fine Particle Technology. 1st Edition. Micromeritics Instrument. 1997.
Saveleva V.A., Papaefthimiou V., Daletou M.K. et al. // J. Phys. Chem. C. 2016. V. 120. № 29. P. 15930.
Kachala V.V., Khemchyan L.L., Kashin A.S. et al. // Russ. Chem. Rev. 2013. V. 82. № 7. P. 648.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии