Журнал физической химии, 2019, T. 93, № 7, стр. 1089-1096
Экстрагенты ионов тяжелых металлов на основе сшитого полиэтиленимина
А. С. Морозов a, И. В. Бессонов a, В. А. Даванков b, *
a АО “Перспективные медицинские технологии”
Москва, Россия
b Российская академия наук, Институт элементоорганических соединений им. А.Н. Несмеянова
Москва, Россия
* E-mail: davank@ineos.ac.ru
Поступила в редакцию 13.11.2018
После доработки 13.11.2018
Принята к публикации 15.01.2019
Аннотация
Синтезированы новые пористые полимерные материалы на основе сшитого сильноразветвленного полиэтиленимина (ПЭИ). В качестве сшивающих реагентов применялись эпихлоргидрин, диэтиленгликоль диглицидиловый эфир, а также, диэфиры хлоруксусной кислоты с этиленгликолем, диэтиленгликолем, триэтиленгликолем и полиэтиленгликолем-400. Варьировалось соотношение ПЭИ-сшивающий агент и методы полимеризации, сильно влияющие на влагопоглощение продуктов. Показана их высокая сорбционная активность по отношению к катионам металлов, образующим комплексы с аминогруппами ПЭИ: до 172 мг/г для меди(II), до 116 мг/г для кобальта(II) и до 106 мг/г для никеля(II) в ацетатном буферном растворе при pH 5.
В связи с быстрым развитием таких областей промышленности как нанесение гальванических покрытий, добыча полезных ископаемых, производство удобрений, химических источников тока и аккумуляторов и др., сброс отходов, содержащих тяжелые металлы, зачастую производится с нарушением требований охраны окружающей среды. В отличие от органических соединений, тяжелые металлы не деградируют в природных условиях и обладают выраженной тенденцией к накоплению в живых организмах. Многие из них обладают токсичным воздействием, проявляют канцерогенные свойства. Наиболее тревожащими с этой точки зрения являются промышленные отходы, содержащие цинк, медь, никель, кобальт, ртуть, кадмий, свинец и хром [1].
Одними из наиболее удобных и перспективных способов удаления тяжелых металлов из подобных жидких отходов являются адсорбция и ионный обмен. Эти методы привлекают внимание исследователей благодаря простоте использования, низкой стоимости, отсутствию дополнительных отходов. К сожалению, наиболее популярные адсорбенты на основе сульфированного полистирола или активированного угля не селективны по отношению к таким тяжелым металлам как медь, цинк или никель [2]. Для них характерно конкурентное связывание с такими, зачастую присутствующими в избытке катионами, как Na+, Ca2+, Mg2+, Fe2+, что снижает эффективность удаления токсичных веществ [3].
Для преодоления этого препятствия были предложены селективные адсорбенты, в состав которых входят хелатирующие группы, образующие прочные комплексы с катионами меди, цинка, никеля и кобальта [4, 5]. Примером подобного комплексообразующего реагента является разветвленный полиэтиленимин, положительно заряженный полиэлектролит, содержащий большое число первичных и вторичных аминогрупп; он обладает выдающейся хелатирующей активностью по отношению к ионам тяжелых металлов [6–8]. Поскольку ПЭИ является хорошо растворимым в воде веществом, большинство описанных в литературе материалов на его основе содержат его в качестве иммобилизованного лиганда на поверхности пористого носителя [9–11]. К преимуществам такого подхода можно отнести невысокую стоимость полученных сорбентов и их механическую стабильность. К недостаткам – низкое содержание функциональных групп в объеме сорбента, слабое набухание в водных растворах, также ограничивающее доступ раствора в объем адсорбента и препятствующее эффективному хелатированию растворенных ионов, что, в конечном счете, не позволяет достигнуть высоких значений сорбционной емкости.
В настоящей работе предложен принципиально отличный подход, в основе которого лежит получение нерастворимых в воде, сшитых полимеров, полученных в результате взаимодействия развлетвленного полиэтиленимина и бифункциональных электрофилов, таких как эпихлорогидрин и диглицидиловый эфир диэтиленгликоля. Ранее было показано, что полимерные сорбенты подобного строения способны набухать в воде на десятки процентов без существенной потери прочности, при этом эффективно сорбируя на своей поверхности микроводоросли и цианобактерии [12]. Мы ожидаем, что полимеры подобного строения могут оказаться полезными и в области защиты окружающей среды, так как должны обладать селективными хелатирующими свойствами и проявлять высокую сорбционную активность по отношению к солям меди, никеля, цинка и кобальта благодаря необычно большой концентрации аминных функциональных групп в адсорбентах подобного строения. А высокая степень их набухания в воде будет положительно коррелировать со степенью извлечения, что объясняется большим расстоянием между сольватированными полимерными цепями в набухшем адсорбенте, меньшими стерическими затруднениями и более эффективным доступом растворенных катионов к первичным и вторичным аминогруппам.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы и методы Материалы
В работе использовались следующие реагенты: сильно разветвленный полиэтиленимин (ПЭИ) с молекулярной массой Mw 50–100 kDa (50% водный раствор, MP Biomedicals, США); (±)-эпихлоргидрин (ЭХГ, ≥99%, Sigma-Aldrich, США), хлоруксусная кислота (99%, Sigma-Aldrich, США); натрия додецилсульфат (≥99%, Sigma-Aldrich, США). Остальные реагенты и растворители – отечественного производства марки “х.ч.”. Все реактивы и растворители использовались без дополнительной очистки.
Методы
Приготовление растворов. Ацетатный буфер (pH 5, 0.1 М) приготовили, используя деионизованную воду (1500 мл), уксусную кислоту (3.14 мл) и ацетат натрия (7.81 г). Раствор соли меди(II) получили, растворяя 5.00 г пентагидрата сульфата меди(II) в 200 мл ацетатного буфера (pH 5, 0.1 М). Раствор соли кобальта(II) получили, растворяя 4.76 г гексагидрата хлорида кобальта(II) в 200 мл ацетатного буфера (pH 5, 0.1 М). Раствор соли никеля(II) получили, растворяя 4.75 г гексагидрата хлорида никеля(II) в 200 мл ацетатного буфера (pH 5, 0.1 М).
Измерение весового набухания. Навеску сорбента (30–70 мг) помещали в стеклянную баночку, и прибавляли 2.0 мл ацетатного буфера. Через 30 мин растворитель удаляли с помощью шприца, сорбент взвешивали. Набухание рассчитывали по формуле:
Для каждого сорбента проводили три независимых измерения, в таблице 1 приведено среднее, доверительный интервал рассчитан для доверительной вероятности p = 0.9.
Таблица 1.
Эффективность извлечения катионов Cu2+, Co2+ и Ni2+ из 0.1 М раствора в 0.1 М ацетатном буфере при pH 5
| Шифр | Выход, % | Весовое набу-хание при pH 5 | Извлечение Cu2+, (мг/г) | Извлечение Co2+, % (мг/г) | Извлечение Ni2+, % (мг/г) |
|---|---|---|---|---|---|
| Т–ЭХГ–30 | 99 | 2.5 ± 0.2 | 34 ± 1 (65 ± 1) | 11 ± 2 (20 ± 3) | 22 ± 2 (31 ± 3) |
| Т–ЭХГ–15 | 97 | 6.3 ± 0.3 | 59 ± 5 (113 ± 9) | 24 ± 6 (42 ± 10) | 23 ± 4 (32 ± 6) |
| Т–ЭХГ–7.5 | 94 | 8.7 ± 0.4 | 82 ± 6 (156 ± 11) | 54 ± 15 (93 ± 27) | 34 ± 4 (49 ± 6) |
| Т–ЭХГ–3.8 | 94 | 10.4 ± 1.2 | 83 ± 10 (158 ± 19) | 53 ± 3 (91 ± 4) | 36 ± 4 (51 ± 5) |
| Т–ЭХГ–1.9 | 82 | 16.3 ± 1.5 | 87 ± 8 (165 ± 15) | 67 ± 9 (116 ± 16) | 57 ± 7 (81 ± 10) |
| Т–ЭХГ–0.9 | 70 | 13.1 ± 0.7 | 48 ± 6 (91 ± 12) | 35 ± 5 (60 ± 9) | 29 ± 3 (41 ± 4) |
| К–ДЭГ–120 | 96 | 3.7 ± 0.1 | 18 ± 2 (34 ± 5) | 11 ± 2 (18 ± 3) | 7 ± 4 (10 ± 6) |
| К–ДЭГ–60 | 94 | 4.2 ± 0.3 | 41 ± 6 (78 ± 11) | 32 ± 5 (56 ± 9) | 33 ± 7 (48 ± 10) |
| К–ДЭГ–30 | 96 | 6.3 ± 0.3 | 71 ± 5 (136 ± 9) | 34 ± 8 (59 ± 13) | 41 ± 3 (59 ± 4) |
| К–ДЭГ–15 | 82 | 8.1 ± 0.2 | 77 ± 7 (147 ± 13) | 34 ± 5 (59 ± 8) | 57 ± 3 (81 ± 4) |
| К–ДЭГ–7.5 | 76 | 8.6 ± 0.3 | 83 ± 4 (158 ± 7) | 42 ± 4 (73 ± 7) | 68 ± 4 (97 ± 6) |
| К–ДЭГ–3.8 | 61 | 8.6 ± 0.6 | 81 ± 5 (154 ± 10) | 60 ± 6 (103 ±10 ) | 70 ± 10 (100 ± 15) |
| К–ДЭГ–1.9 | 52 | 9.4 ± 0.4 | 66 ± 3 (126 ± 5) | 44 ± 10 (76 ± 18) | 48 ± 12 (69 ± 17) |
| К–ДЭГ–0.9 | 45 | 6.0 ± 0.7 | 14 ± 4 (27 ± 7) | 13 ± 4 (22 ± 7) | 19 ± 4 (27 ± 6) |
| К–ЭХГ–120 | 75 | 1.8 ± 0.4 | 10 ± 1 (20 ± 1) | 6 ± 7 (10 ± 12) | 3 ± 7 (5 ± 10) |
| К–ЭХГ–60 | 85 | 3.8 ± 0.4 | 52 ± 15 (99 ± 28) | 20 ± 3 (35 ± 4) | 30 ± 8 (42 ± 11) |
| К–ЭХГ–30 | 82 | 10.9 ± 0.6 | 61 ± 5 (117 ± 9) | 42 ± 4 (73 ± 7) | 52 ± 5 (74 ± 7) |
| К–ЭХГ–15 | 77 | 11.6 ± 0.1 | 68 ± 3 (130 ± 6) | 54 ± 8 (94 ± 14) | 59 ± 2 (85 ± 3) |
| К–ЭХГ–7.5 | 79 | 12.7 ± 0.6 | 81 ± 8 (154 ± 15) | 32 ± 7 (55 ± 12) | 59 ± 4 (84 ± 6) |
| К–ЭХГ–3.8 | 65 | 9.2 ± 0.4 | 33 ± 4 (63 ± 9) | 13 ± 3 (22 ± 5) | 21 ± 16 (30 ± 23) |
| К–ЭХГ–1.9 | 52 | 7.0 ± 0.6 | 26 ± 2 (50 ± 4) | 14 ± 3 (24 ± 5) | 20 ± 3 (28 ± 4) |
| К–ЭХГ–0.9 | 47 | 3.6 ± 0.3 | 16 ± 0 (30 ± 1) | 9 ± 7 (15 ± 12) | 16 ± 4 (22 ± 5) |
| Т–ДЭГ–30 | 83 | 7.4 ± 0.3 | 64 ± 1 (121 ± 1) | 39 ± 5 (67 ± 9) | 53 ± 7 (76 ± 10) |
| Т–ДЭГ–15 | 95 | 10.5 ± 0.3 | 78 ± 11 (150 ± 22) | 57 ± 4 (99 ± 6) | 58 ± 7 (83 ± 10) |
| Т–ДЭГ–7.5 | 99 | 10.4 ± 0.7 | 67 ± 10 (128 ± 19) | 44 ± 8 (75 ± 13) | 55 ± 5 (79 ± 8) |
| Т–ДЭГ–3.8 | 80 | 12.2 ± 0.6 | 68 ± 20 (129 ± 38) | 31 ± 9 (53 ± 15) | 56 ± 3 (80 ± 4) |
| Т–ДЭГ–1.9 | 73 | 12.8 ± 0.5 | 60 ± 3 (114 ± 6) | 34 ± 6 (59 ± 10) | 46 ± 3 (66 ± 4) |
| Т–ДЭГ–0.9 | 76 | 12.6 ± 0.6 | 60 ± 12 (114 ± 23) | 30 ± 10 (52 ± 17) | 46 ± 10 (66 ± 14) |
| К–ЭГ–ДХА–30 | 85 | 11.0 ± 0.7 | 90 ± 3 (171 ± 6) | 51 ± 4 (87 ± 6) | 56 ± 7 (79 ± 10) |
| К–ЭГ–ДХА–7.5 | 73 | 13.0 ± 0.9 | 82 ± 5 (156 ± 9) | 33 ± 5 (56 ± 9) | 34 ± 3 (48 ± 4) |
| К–ДЭГ–ДХА–30 | 81 | 9.7 ± 1.5 | 87 ± 0 (165 ± 1) | 62 ± 6 (106 ± 10) | 60 ± 1 (85 ± 1) |
| К–ДЭГ–ДХА–7.5 | 67 | 11.8 ± 0.4 | 75 ± 11 (143 ± 21) | 52 ± 6 (90 ± 10) | 43 ± 4 (61 ± 6) |
| К–ТЭГ–ДХА–30 | 71 | 11.5 ± 1.1 | 79 ± 18 (150 ± 35) | 52 ± 4 (90 ± 8) | 43 ± 4 (61 ± 6) |
| К–ТЭГ–ДХА–7.5 | 49 | 16.0 ± 1.8 | 60 ± 4 (115 ± 7) | 33 ± 3 (57 ± 5) | 40 ± 6 (57 ± 8) |
| К–ПЭГ–ДХА–30 | 53 | 9.7 ± 0.4 | 50 ± 5 (95 ± 9) | 21 ± 6 (36 ± 10) | 43 ± 2 (61 ± 3) |
| К–ПЭГ–ДХА–7.5 | 36 | 3.9 ± 1.2 | 23 ± 13 (43 ± 24) | 10 ± 4 (18 ± 6) | 27 ± 5 (39 ± 8) |
| Т–ЭГ–ДХА–30 | 75 | 7.7 ± 0.4 | 82 ± 5 (156 ± 10) | 65 ± 20 (112 ± 34) | 74 ± 5 (105 ± 8) |
| Т–ЭГ–ДХА–7.5 | 82 | 11.7 ± 1.1 | 77 ± 9 (148 ± 17) | 44 ± 6 (76 ± 10) | 68 ± 8 (97 ± 12) |
| Т–ЭГ–ДХА–1.9 | 55 | 5.3 ± 0.5 | 19 ± 7 (37 ± 14) | 8 ± 4 (14 ± 6) | 13 ± 5 (19 ± 7) |
| Т–ДЭГ–ДХА–30 | 72 | 8.4 ± 0.1 | 90 ± 8 (172 ± 15) | 52 ± 4 (89 ± 7) | 74 ± 6 (106 ± 9) |
| Т–ДЭГ–ДХА–7.5 | 69 | 13.1 ± 1.1 | 87 ± 1 (165 ± 2) | 37 ± 7 (63 ± 12) | 64 ± 12 (91 ± 17) |
| Т–ДЭГ–ДХА–1.9 | 44 | 8.9 ± 0.3 | 43 ± 21 (82 ± 39) | 24 ± 6 (41 ± 10) | 41 ± 1 (58 ± 1) |
| Т–ТЭГ–ДХА–30 | 72 | 7.9 ± 0.2 | 85 ± 4 (163 ± 7) | 65 ± 4 (112 ± 6) | 65 ± 4 (93 ± 6) |
| Т–ТЭГ–ДХА–7.5 | 67 | 16.8 ± 1.8 | 79 ± 6 (151 ± 12) | 54 ± 5 (93 ± 9) | 52 ± 4 (74 ± 6) |
| Т–ТЭГ–ДХА–1.9 | 49 | 5.9 ± 0.8 | 26 ± 7 (50 ± 13) | 15 ± 8 (26 ± 13) | 12 ± 3 (17 ± 5) |
| Т–ПЭГ–ДХА–30 | 56 | 7.2 ± 0.5 | 59 ± 16 (112 ± 30) | 28 ± 6 (48 ± 10) | 28 ± 4 (40 ± 6) |
| Т–ПЭГ–ДХА–7.5 | 55 | 7.2 ± 0.3 | 50 ± 4 (94 ± 7) | 21 ± 3 (36 ± 5) | 21 ± 5 (30 ± 7) |
| Т–ПЭГ–ДХА–1.9 | 19 | 7.2 ± 0.4 | 28 ± 10 (53 ± 19) | 9 ± 3 (16 ± 5) | 9 ± 4 (13 ± 6) |
Проведение адсорбции катионов. Навеску сорбента (30–70 мг) помещали в стеклянную баночку, и прибавляли раствор соответствующего катиона в ацетатном буфере. Объем раствора рассчитывали по формуле:
где V – объем раствора, мл; m – навеска сорбента, мг.Через 30 мин отбирали пробу и проводили анализ содержания катиона после сорбции. Эффективность сорбента оценивали как отношение концентрации катиона после сорбции к исходной концентрации, значение приводили в процентах.
Для каждого сорбента проводили три независимых измерения, в таблице 1 приведено среднее, доверительный интервал рассчитан для доверительной вероятности p = 0.9.
Определение катионов. 1) Медь(II). К 2.0 мл деионизованной воды прибавили 200 мкл 1% ПЭИ и 80 мкл исследуемого раствора. Через 1 мин определяли оптическую плотность при 625 нм. 2) Кобальт(II). К 0.72 мл ацетатного буфера прибавили 80 мкл исследуемого раствора, тщательно перемешали (раствор 1). К 2.0 мл деионизованной воды прибавили 200 мкл 1% ПЭИ и 80 мкл раствора 1. Через 10 мин определяли оптическую плотность при 310 нм. 3) Никель(II). К 2.0 мл деионизованной воды прибавили 200 мкл 1% ПЭИ и 200 мкл исследуемого раствора. Через 1 мин определяли оптическую плотность при 390 нм.
Для всех катионов концентрацию рассчитывали, используя ранее построенную калибровочную прямую.
ИК-спектроскопия. ИК-спектры в диапазоне 4000–650 см–1 регистрировали в режиме НПВО (измельченные сорбенты в твердом виде) на прибореNicolet iS10 FTIR spectrometer (ThermoFisherScientific, Inc., США).
Определение элементного состава. Элементный состав образцов определяли на элементном анализаторе Vario Micro cube (Германия) в режиме CHNS.
Получение сорбентов
Этиленгликоль ди(хлорацетат) (ЭГ–ДХА), диэтиленгликоль ди(хлорацетат) (ДЭГ–ДХА), триэтиленгликоль ди(хлорацетат) (ТЭГ–ДХА) и полиэтиленгликоль ди(хлорацетат) (ПЭГ–ДХА) получены по ранее описанным методикам [13].
Первая буква шифра сорбента обозначает метод полимеризации (Т – термический, К – крио), далее следует сокращенное название сшивающего агента (ЭХГ – эпихлоргидрин, ДЭГ – диэтиленгликоля диглицидиловый эфир, ЭГ–ДХА – этиленгликоль ди(хлорацетат), ДЭГ–ДХА – диэтиленгликоль ди(хлорацетат), ТЭГ–ДХА – триэтиленгликоль ди(хлорацетат), ПЭГ–ДХА – полиэтиленгликоль ди(хлорацетат)), в конце – его массовая доля по отношению к ПЭИ.
Общая методика получения сорбентов методом термической полимеризации
В двугорлой круглодонной колбе объемом 500 мл, снабженной обратным холодильником и капельной воронкой, смешали ПЭИ (50% в воде, 30.0 г), толуол (120 мл), затем прибавили раствор натрия додецилсульфата (50 мг) в дистиллированной воде (5.0 мл) и концентрированную соляную кислоту (7.5 мл) при перемешивании на магнитной мешалке. Реакционную смесь нагрели до 70°С. Сшивающий агент (ЭХГ, ДЭГ, ЭГ–ДХА, ДЭГ–ДХА, ТЭГ–ДХА или ПЭГ–ДХА в количестве от 0.9 до 30 мас. %) растворили в 10 мл толуола и медленно по каплям в течение 2 ч вносили в реакционную смесь при интенсивном перемешивании. Затем к реакционной колбе подсоединили насадку Дина–Старка объемом 50 мл, реакцию вели при кипячении до прекращения выделения воды (примерно 4 ч). Осадок отфильтровали на стеклянном фильтре, последовательно промыли этиловым спиртом (2 × 100 мл), 10% раствором гидроксида натрия (1 × 100 мл), затем дистиллированной водой до pH 8–9. Продукт лиофилизовали до постоянной массы. Выход 19–99%.
Общая методика получения сорбентов методом криополимеризации
К 40 мл 10% раствора ПЭИ в деионизованной воде прибавили сшивающий агент (ЭХГ, ДЭГ, ЭГ–ДХА, ДЭГ–ДХА, ТЭГ–ДХА или ПЭГ–ДХА в количестве от 0.9 до 120 мас. %). Смесь интенсивно перемешивали на минишейкере в течение 10 мин в пластиковой пробирке с завинчивающейся крышкой, затем поместили в морозильную камеру (–24°С) на ночь. После размораживания суспензию перенесли в круглодонную колбу объемом 250 мл, прибавили 100 мл этилового спирта и кипятили в течение 2–4 часов. Затем осадок отфильтровали на стеклянном фильтре, промыли последовательно этиловым спиртом (6 × 50 мл), дистиллированной водой (2 × 50 мл), насыщенным раствором гидрокарбоната натрия (1 × 100 мл), затем дистиллированной водой до pH 8–9. Продукт лиофилизовали до постоянной массы. Выход 36–96%.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Получение сорбентов
В качестве исходных веществ для получения сшитых полимерных материалов использовались водные растворы разветвленного полиэтиленимина и ряд бифункциональных сшивающих агентов. В качестве последних использовали как коммерчески доступные соединения: эпихлоргидрин, диглицидиловый эфир диэтиленгликоля, так и легко синтезируемые эфиры хлоруксусной кислоты с производными этиленгликоля, что позволяло варьировать длину сшивающего агента. Для получения сшитых полимерных материалов использовались две методики: сшивка сильноразветвленного полиэтиленимина при нагревании с бифункциональным сшивающим агентом, при этом пористая структура частично создается за счет пузырьков водяного пара [14]. Другой подход залючался в криополимеризации, когда при замораживании разбавленных водных растворов полиэтиленимина и сшивающих агентов происходило криоконцентрирование исходных веществ, а в роли порогена выступали формирующиеся микрокристаллы льда [15].
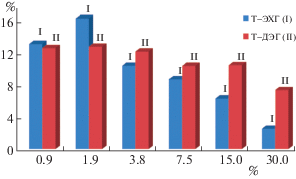
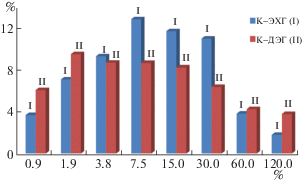
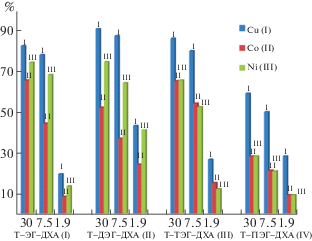
Все продукты после лиофильной сушки представляют собой хорошо набухающие в воде (в 2–12 раз по весу, рис. 1–4) белые или слегка желтоватые порошки (для высокой степени сшивки) или аморфные тестообразные продукты (для низкой степени сшивки). Естественно, привес при измерении весового набухания высокопористых сорбентов в воде приходится как на заполнение пространства пор так и на увеличение материала в объеме, для сильно набухающих полимеров – в пять и более раз; механическая прочность материала при набухании снижается.
Мы варьировали массовую долю сшивающего агента по отношению к полиэтиленимину от 0.9 до 30 мас. % в случае термической полимеризации и до 120 мас. % в случае криополимеризации. При большем содержании сшивающего агента, чем 30 мас. %, в случае термической полимеризации материал становится слишком хрупким и перестает в достаточной мере смачиваться водой, что делает его малопригодным к использованию. В случае криополимеризации возможно получение эффективных сорбентов с более высокими степенями сшивки, вплоть до 120 мас. %, однако попытки дальнейшего увеличения содержания сшивающего агента приводят к неполному его расходованию. В целом, при уменьшении количества сшивающего агента выход продукта снижается. Полимеры К–ЭГ–ДХА–1.9, К−ДЭГ–ДХА–1.9, К–ТЭГ–ДХА–1.9, К–ПЭГ–ДХА–1.9 вообще сшиты слишком слабо: происходило лишь гелирование без образования твердой полимерной массы. Также было отмечено, что в случае материалов, полученных методом термической полимеризации, выход, как правило, оказывался выше, чем в условиях криополимеризации при тех же соотношениях ПЭИ-сшивающий агент. При использовании ЭХГ и ДЭГ в качестве сшивающего агента выход продуктов варьировался в диапазоне 70–99% для термической полимеризации и 45–96% для криополимеризации. При использовании эфиров хлоруксусной кислоты в качестве сшивающих агентов, выход, в целом, был несколько ниже: от 19–56% для ПЭГ–ДХА производных до 55–85% для полимеров на основе ЭГ–ДХА.
Степень набухания ожидаемо снижается с повышением степени сшивки (рис. 1–4), однако эта зависимость не всегда однозначна. Так, для рядов К–ЭХГ и К–ДЭГ наблюдается наибольшее набухание полимеров для степени сшивки лежащей в диапазоне 7.5–30.0 мас. %, превышение которой снижает эффективность поглощения воды, вероятно, из-за высокой конверсии гидрофильных первичных аминогрупп в менее гидрофильные вторичные и третичные. Слабо сшитые полимеры из ряда К–ЭХГ и К–ДЭГ проявляют в разы более высокую степень набухания, чем аналогичные им по строению Т–ЭХГ и Т–ДЭГ. Таким образом, в величину степени набухания вносит вклад не только химическое строение полимера, но и метод его получения.
Настолько же однозначных зависимостей в рядах К-эфиры ДХА и Т-эфиры ДХА (рис. 3, 4) обнаружить не удалось, однако любопытно отметить, что наименьшая степень набухания соответствует полимерам, полученным путем сшивки ПЭИ самым длинным и подвижным линкером на основе полиэтиленгликоля.
Все сорбенты в сухом состоянии отличаются невысокой удельной поверхностью (не более 80 м2/г) при сорбции газов, однако ввиду их способности набухать в воде, их доступная поверхность в этой среде значительно больше, что подтверждается экспериментами по адсорбции культур микроводорослей [12, 16].
Состав полимерных материалов был подтвержден данными элементного анализа (отношение содержания C/N) и данными ИК-спектроскопии: все полимеры имеют полосы поглощения N–H групп (3259–3381 см–1), C–N групп (одна или две полосы в диапазоне 1633–1663 см–1 и 1295–1320 см–1), в случае использования ЭХГ и ДЭГ в качестве сшивающего агента наблюдается полоса поглощения O–H групп (одна или две полосы в диапазоне 1103–1118 см–1 и 1045–1060 см–1), для полимеров, полученных с использованием сшивающего реагента, содержащего сложноэфирную группу, дополнительно имеется полоса поглощения при 1730–1750 см–1, также, в ряде случаев, еще полоса поглощения при 1670–1685 см–1, что соответствует, по-видимому, образованию амидной связи.
Определение катионов
В качестве определяемых катионов были выбраны катионы меди(II), кобальта(II) и никеля(II), которые определяли спектрофотометрически по поглощению их комплексов с ПЭИ. Ввиду того, что из полимерных материалов, особенно с невысокой степенью сшивки, наблюдается незначительное вымывание остаточного полиэтиленимина, для нивелирования этого эффекта при определении катионов добавляли избыток ПЭИ. На первом этапе измеряли скорость образования комплексов, определяя изменение оптической плотности растворов со временем. Было показано, что в случае меди(II) и никеля(II) уже через 1 мин не происходит значимого (в пределах 10%) изменения оптической плотности, в случае кобальта(II), стабильный результат достигается приблизительно через 8–10 мин. Поэтому при анализе в случае меди(II) и никеля(II) измерения проводили через 1 мин, а в случае кобальта(II) – через 10 минут после добавления реагентов и перемешивания растворов. Остаточная концентрация катионов после сорбции определялась по калибровочным прямым, построенным для каждого катиона, по поглощению при 625 нм для меди(II), 310 нм – для кобальта(II) и 390 нм – для никеля(II).
Анализ эффективности сорбции катионов
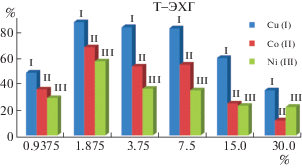
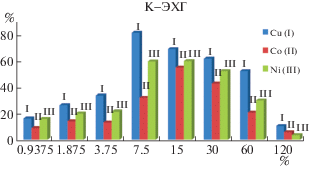
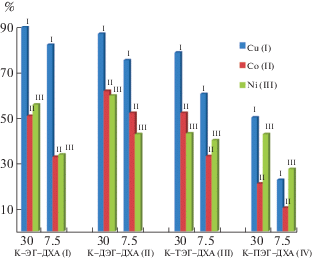
Эффективность сорбции катионов исследовали при pH 5, прибавляя 1 мл 0.1 М раствора соли в пересчете на 50 мг сухого полимерного материала. Было обнаружено, что медь(II) экстрагируется несколько более эффективно, чем кобальт(II) и никель(II), что согласуется с литературными данными [17–19]. В большинстве случаев, если сорбент показывает высокую эффективность при удалении меди, то он также эффективен в отношении других катионов (рис. 5–10).
Зависимость эффективности сорбции от степени сшивки более сложная: для каждого сшивающего агента имеется оптимальное значение степени сшивки, при уменьшении или увеличении которого эффективность снижается. Для ряда соединений, полученных методом криполимеризации, эти оптимумы выражены более отчетливо, чем для полимеров, сшитых при нагревании. Важно отметить, что при этом нет прямой корреляции со степенью набухания материалов в буферном растворе при том же значении pH (R2 равен 0.44 для Cu2+, 0.32 для Co2+ и 0.30 для Ni2+).
Наиболее эффективным сорбентом из представленных для удаления меди является материал К–ЭГ–ДХА–30, способный удалять 90% катионов меди в условиях эксперимента, что соответствует эффективности сорбции 172 мг/г. Для кобальта наиболее эффективен Т–ЭХГ–1.9 (67%, 116 мг/г), для никеля – Т–ДЭГ–ДХА–30 (74%, 106 мг/г). В целом наиболее эффективными материалами можно признать (в порядке уменьшения средней эффективности сорбции): Т–ЭГ–ДХА–30, Т–ДЭГ–ДХА–30, Т–ТЭГ–ДХА–30, К–ДЭГ–3.8, Т–ЭХГ–1.9, К–ДЭГ–ДХА–30, К–ЭГ–ДХА–30, Т–ДЭГ–15, К–ДЭГ–7.5, Т–ЭГ–ДХА–7.5, Т–ДЭГ–ДХА–7.5, Т–ТЭГ–ДХА–7.5, К–ЭХГ–15. Таким образом, обычно хорошие результаты дают материалы с массовой долей сшивающего агента от 7.5 до 30% в случае эфиров хлоруксусной кислоты, 3.8–7.5% – для ДЭГ и 1.9–15% – для относительно короткого эпихлоргидрина, причем оба метода: криополимеризация и термическая полимеризация могут использоваться для удобного и быстрого, хорошо масштабируемого получения эффективных сорбентов.
Работа выполнена при финансовой поддержке Российского научного фонда (грант № 16-14-00112).
Список литературы
Fu F., Wang Q. // J. Environ Manage. 2011. V. 92(3). P. 407.
Demirbas A. // J. Hazard Mater. 2008. V. 157(2–3). P. 220.
Dąbrowski A., Hubicki Z., Podkościelny P. et al. // Chemosphere. 2004. V. 56(2). P. 91.
Mokadema Z., Mekkia S., Saïdi-Besbes S. et al. // Arabian J. of Chemistry. 2017. V. 10. P. 1039.
Liu C., Bai R. // Current Opinion in Chemical Engineering. 2014. V. 4. P. 62.
Kobayashi S., Hiroishi K., Tokunoh M. et al. // Macromolecules. 1987. V. 20(7). P. 1496.
Say R., Tuncel A., Denizli A. // Journal of Applied Polymer Science. 2002. V. 83(11). P. 2467 .
Ghoul M., Bacquet M., Morcellet M. // Water Research. 2003. V. 37(4). P. 729.
Deng S., Ting Y.P. // Environ. Sci. Technol. 2005. V. 39(21). P. 8490.
Navarro R.R., Tatsumi K., Sumi K. et al. // Water Research. 2001. V. 35(11). P. 2724.
Amara M., Kerdjoudj H. // Talanta. 2003. V. 60(5). P. 991.
Vasilieva S., Shibzukhova K., Morozov A. et al. // J. Biotechnol. 2018. V. 281. P. 31.
Nuzhdina A.V., Morozov A.S., Kopitsyna M.N. et al. // Materials Science and Engineering C. 2017. V. 70. P. 788.
Chen D.P., Yu C., Chang C.-Y. et al. // Environmental Science & Technology. 2012. V. 46. P. 10718.
Beres N.R. // Dissertation. The University of Akron. 2010.
Васильева С.Г., Шибзухова К.А., Морозов А.С. и др. // Вестн. МГУ. Серия 16. Биология. 2018. Т. 73(1). С. 43.
Geckeler K., Lange G., Eberhardt H. et al. // Pure & Appl. Chem. 1980. V. 52. P. 1883.
Chen Y., Pan B., Li H. et al. // Environ Sci Technol. 2010. V. 44(9). P. 3508.
Larsson M., Nosrati A., Kaur S. et al. // Heliyon. 2018. V. 4(2). P. e00520.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии