Журнал физической химии, 2020, T. 94, № 1, стр. 60-64
Формирование структуры водных растворов хлоридов марганца, никеля, меди и цинка по данным рентгеноструктурного анализа
П. Р. Смирнов a, *, О. В. Гречин b
a Российская академия наук, Институт химии растворов им. Г.А. Крестова
Иваново, Россия
b Ивановский государственный химико-технологический университет,
НИИ термодинамики и кинетики химических процессов
Иваново, Россия
* E-mail: prs@isuct.ru
Поступила в редакцию 13.12.2018
После доработки 20.05.2019
Принята к публикации 18.06.2019
Аннотация
Методом рентгеноструктурного анализа (РСА) исследовано формирование структуры водных растворов хлоридов марганца, никеля, меди и цинка в широкой области концентраций. Проведена интерпретация малоугловых пиков. Осуществлен анализ изменения их интенсивности и положения в зависимости от концентрации и природы катионов. Проведено сравнение кривых интенсивности исследованных растворов с соответствующими функциями изученных ранее растворов хлоридов лантаноидов.
Структурные исследования водных растворов электролитов проводятся уже достаточно долгое время. Получен большой объем экспериментальных данных, описывающих структурные параметры ближнего окружения ионов, такие как координационные числа и межчастичные расстояния в первой и второй координационных сферах, а также образующиеся ионные пары и их вид. Однако в погоне за количественным описанием структуры гидратных комплексов ионов должным образом не рассматривалось влияние некоторых факторов на специфику структуроформирования растворов. Использование современного высокопроизводительного оборудования, в частности рентгеновского дифрактометра D8 Advance (Bruker AXS), позволяет проводить обширные систематические структурные исследования применительно к водным растворам электролитов за сравнительно короткое время, в отличие от разрозненных работ, реализуемых ранее. При этом появляется возможность: во-первых, на качественном уровне оценить соотношение парциальных вкладов собственной структуры растворителя и гидратных комплексов ионов, их роль в образовании внутреннего строения растворов и динамику изменения вкладов в зависимости от концентрации, и, во-вторых, сравнить тенденции в структурообразовании растворов однотипных электролитов.
Нами уже были исследованы водные растворы некоторых хлоридов лантаноидов [1, 2]. Особое внимание было уделено анализу так называемых предпиков или малоугловых максимумов на кривых интенсивности рассеянного рентгеновского излучения. Их детальное рассмотрение обусловлено тем, что малоугловые пики однозначно свидетельствуют о наличии в растворе упорядоченности, на расстояниях, превышающих условные радиусы вторых координационных сфер ионов. Поэтому можно полагать, что они характеризуют структуру конденсированных систем в более полном объеме, дополнительно к описанию ближнего порядка. Было установлено, что в случае высококонцентрированных растворов предпики отражают устойчивые взаимодействия трех видов: катион–катион, катион–анион и анион–анион. Для разбавленных растворов доминирующими вкладами в общую картину рассеяния, определяющими остаточные проявления малоугловых максимумов, являются расстояния, складывающиеся между полностью гидратированными ионами, без преимущественного разделения по межионным типам. Малоугловые пики проявляются не только на кривых интенсивности концентрированных растворов, но и на кривых интенсивности разбавленных систем (с невысокой интенсивностью). Это служит свидетельством сохранения в них упорядоченности средней удаленности.
С целью выявления влияния физико-химической природы катионов на структуроформирование водно-электролитных систем следующим шагом явился анализ структуры растворов солей d-металлов. В данной работе представляются экспериментальные данные, полученные на водных растворах высоких и умеренных концентраций хлоридов марганца, никеля, меди и цинка (как представителей d-металлов).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Близкие к насыщению растворы хлоридов готовились из соответствующих кристаллогидратов квалификации “х. ч.” и “ч. д. а.” на основе подкисленных кислотой (не более 0.1 M HCl) водных растворов. Подкисление являлось вынужденной мерой с целью частичного подавления протекающего гидролиза и получения гомогенных растворов. Дальнейшие разбавления проводились 0.01 М растворами.
Рентгенодифракционные данные получены с использованием МоKα-излучения (λ = 0.071 нм) по рентгенооптической схеме Брегга–Брентано. Проблема отсечения сопутствующего паразитного рассеяния при малых углах регистрации решалась посредством использования глубокой кюветы со свинцовыми краями, не контактирующими с раствором, и устанавливаемого над кюветой свинцового ножа при съемке до 30°. Интенсивность рассеяния от образцов регистрировали позиционно-чувствительным детектором VÅNTEC-1 (Bruker). Отснятые не менее трех раз первичные экспериментальные кривые интенсивности (КИ) усреднялись и сглаживались в программе Origin 7.5 посредством FFT-фильтрации [3].
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
На рис. 1, 2 представлены кривые интенсивности рентгеновского рассеяния (КИ) водных растворов хлоридов марганца и никеля (КИ водных растворов хлоридов меди и цинка выглядят аналогично, поэтому в целях экономии места не приведены). На них также, как и на КИ растворов хлоридов лантаноидов, наблюдается совокупность малоугловых пиков, т.е. пиков, располагающихся в малоугловой области (∼10.2–11.6 нм–1) до основного пика при ∼20 нм–1, характерного для воды и водных растворов. По нашему мнению, наличие малоугловых максимумов свидетельствует о проявлении в структуре растворов среднедальней упорядоченности (intermediate range order). Данный термин часто встречается в структурных исследованиях стеклующихся систем, и нами применяется с целью обособления данного понятия от терминов “ближний” и “дальний порядок”. Полагаем, что представление о ближнем окружении ионов ограничивается диапазоном расстояний, не превышающим условного радиуса вторых координационных сфер ионов. В то же время “дальний порядок” предполагает наличие строгой повторяемости жестко связанных структурных единиц. Из рисунков также видно, что КИ имеют общую тенденцию изменения своих форм с разбавлением, а именно уменьшение интенсивности предпиков и увеличение интенсивности основного “водного” пика. Характер этого изменения свидетельствует об очевидном процессе усиления вклада в структуроформирование от собственной структуры растворителя и уменьшения такового от ион-ионной составляющей с разбавлением.
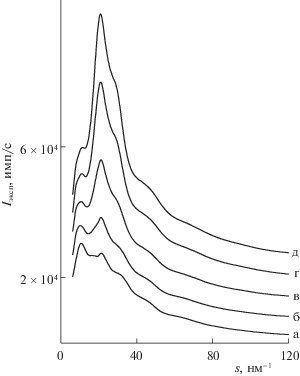
Рис. 1.
Экспериментальные зависимости интенсивности рассеяния рентгеновского излучения в растворах хлорида марганца мольных соотношений 1 : 9.3 (а), 1 : 20 (б), 1 : 40 (в), 1 : 80 (г) и 1 : 120 (д) от значения волнового вектора s.

Рис. 2.
Экспериментальные зависимости интенсивности рассеяния рентгеновского излучения в растворах хлорида никеля мольных соотношений 1 : 12.1 (а), 1 : 20 (б), 1 : 40 (в), 1 : 80 (г) и 1 : 120 (д) от значения волнового вектора s.
Следует обратить особое внимание на следующий нетривиальный факт. Наряду с уменьшением интенсивности предпиков по мере разбавления, наблюдается разнонаправленное смещение их положения, слабо видимое на общих кривых. При малом разбавлении до соотношений 1 : 20 происходит их смещение влево в малоугловую область, при больших степенях разбавления смещение происходит вправо. Данное наблюдение не поддерживает ранее известных результатов о преимущественно смещении малоугловых максимумов в сторону меньших значений волнового вектора и объяснении природы проявления данных максимумов только межкатионными расстояниями [4–7].
Рассмотрим процессы, происходящие в растворах с разбавлением, в рамках границ полной (ГПГ) и неполной гидратации. На основе несложных вычислений можно определить ГПГ для исследованных систем, то есть количество воды, необходимое для того, чтобы вся совокупность ионов имела собственное, неразделяемое с соседями гидратное окружение. Так преимущественно реализуемым гидратным числом (ГЧ) данных катионов следует считать шесть. Наиболее вероятные ГЧ аниона хлора лежат в пределе от шести до семи. Из этого следует, что для рассматриваемых электролитов (MeСl2) эта граница оценивается в 18–20 молекул воды на условную молекулу соли. По нашему мнению, в высококонцентрированных растворах, не достигших границы полной гидратации, в качестве причины проявления предпиков следует предполагать наличие некоторого псевдопериодического распределения обширных комплексных образований. В качестве условных центров этих комплексов выступают катионы, как частицы, имеющие наибольшую координирующую способность. В состав таких образований, помимо катионов, входят и анионы, поскольку дефицит растворителя позиционно ограничивает их трансляции по объему. Псевдопериодичность в отношении анионов не определяет их жесткое расположение в узлах некоторой псевдорешетки, но предполагает значительное диффузное размытие этих узлов, вследствие определенной свободы их передвижений вокруг катиона и слабой гидратирующей способности анионов. Соответственно межкомплексные анион-анионные расстояния имеют широкий интервал значений. В целом предполагаемый псевдопериод обуславливается сложением определяющих вкладов, а именно межкомплексных расстояний катион-катион, катион-анион и анион-анион. Незначительное разбавление приводит к некоторому “разбуханию” таких комплексов за счет добавляемой воды, и, следовательно, к увеличению межкомплексных расстояний. Этим и объясняется смещение положения предпиков в сторону меньших значений s на КИ.
При переходе границы полной гидратации структура растворов меняется значительно. Вся совокупность ионов приобретает собственные гидратные оболочки, позиционные ограничения для ионов значительно ослабевают. При этом проявление псевдопериодичности исчезает. Структуру растворов начинают определять отдельные межионные (катион-анионные и анион-анионные) взаимодействия на расстояниях значительно меньших псевдопериодических. Соответственно наблюдается и обратный ход смещения предпиков. Таким образом наблюдаемые “брутто”-изменения на КИ связаны с переходом от гидратнодефицитных к полногидратным ближайшим ионным окружениям в структуре растворов. Схожесть КИ исследованных систем и отмечаемая общая динамика их видоизменений в свою очередь свидетельствует о подобии в структурной организации обсуждаемых растворов и ее аналогичном изменении с разбавлением. В пользу этого однозначно свидетельствует вышеотмеченный факт, того, что рассматриваемые катионы (Mn–Ni–Cu–Zn) имеют одинаковое ГЧ. Кроме того, расстояния от катионов до их первых координационных сфер сравнительно близки [8]. Таким образом, можно заключить, что структура ближнего окружения ионов тесно связана с проявлением среднедальнего упорядочивания.
Отдельно следует отметить результаты сравнения экспериментальных данных для хлоридных растворов с катионами d- и f-металлов. Общей тенденцией, наблюдаемой, как у растворов хлоридов f-, так и d-металлов, является закономерное перераспределение интенсивности в сторону ее увеличения у основного (характерного для водных растворов) пика (при ∼21.5 нм–1) и уменьшения интенсивности предпиков, происходящие при разбавлении систем. Однако, существуют и некоторые различия. Для сравнения на рис. 3 приведены КИ водных растворов хлорида самария аналогичных мольных соотношений [1]. Следует отметить, что КИ растворов хлоридов других исследованных нами лантаноидов выглядят схожим образом. К различиям в формах КИ растворов d- и f-металлов названной концентрации можно отнести следующее. Прежде всего, предпики выражены более интенсивно, а характеристический пик воды – менее интенсивно у растворов хлорида самария. Это логично объясняется более высокой рассеивающей способностью ионов самария. Сравнительно более узкие основания у предпиков КИ высококонцентрированных растворов лантаноида указывают на меньший разброс в расстояниях типа катион-катион и анион-анион, определяющих псевдопериодичность этих растворов, по сравнению с таковыми для растворов двухвалентных ионов. Это может опосредованно указывать на более высокое структуроопределяющее действие катионов лантаноидов. Кроме того, КИ растворов хлорида самария имеют ряд дополнительных слабовыраженных деталей. Слабые перегибы КИ в области второго максимума, наблюдаемые для наиболее концентрированных растворов, и значительное перераспределение интенсивности в начальной области КИ раствора мольного соотношения 1 : 40 в целом в своей динамике отражают изменения приоритетных межионных расстояний, происходящих при переходе системой границы полной гидратации. При этом для раствора 1 : 40 первый двугорбый максимум КИ указывает на остаточные проявления псевдопериодического ионного распределения на фоне формирования всей совокупностью ионов независимого от соседей гидратного окружения. Подобные мелкие детали отсутствуют на КИ растворов хлоридов d-металлов. Объяснением этому могут служить как меньшее количество хлорид-ионов, присутствующих в растворах, так и меньшее электростатическое воздействие двухзарядных катионов на ближайшее к ним окружение.
Рис. 3.
Экспериментальные зависимости интенсивности рассеяния рентгеновского излучения в растворах хлорида самария мольных соотношений 1 : 15.67 (а), 1 : 20 (б), 1 : 40 (в), 1 : 80 (г), 1 : 160 (д) от значения волнового вектора s.

Таким образом, увеличение заряда катионов влечет за собой усложнение структуры водных растворов хлоридов металлов. Схожесть КИ и общая динамика их видоизменений свидетельствует о подобии в структурной организации растворов хлоридов d-металлов и ее последовательном изменении с разбавлением. Природа происхождения предпиков на КИ обусловлена упорядоченным межионным распределением, зависящим как от физико-химической природы катионов и анионов, так и от концентрации раствора. Псевдопериодическое межкомплексное распределение определяет проявление предпиков для высококонцентрированных растворов, тогда как предпики для разбавленных растворов определяются отдельными межионными (катион-анионными и анион-анионными) расстояниями.
Список литературы
Смирнов П.Р., Гречин О.В., Тростин В.Н. // Журн. физ. химии. 2013. Т. 87. № 5. С. 770. (Russian Journal of Physical Chemistry A. 2013. V. 87. № 5. P. 756) https://doi.org/10.7868/S0044453713050245
Смирнов П.Р., Гречин О.В., Тростин В.Н. // Журн. неорган. химии. 2013. Т. 58. № 8. С. 1124–1128. (Russian Journal of Inorganic Chemistry. 2013. V. 58, № 8. P. 1004) https://doi.org/10.7868/S0044457X13080230
OriginPro 7.5. Copyright 1991–2003. OriginLab Corporation. USA.
Caminiti R., Magini M. // Chem. Phys. Lett. 1978. V. 54. № 3. P. 600.
Дорош А.К., Скрышевский А.Ф. // Журн. структур. химии. 1967. Т. 8. № 2. С. 348.
Marques M.A., Cabaco M.I., Marques M.I.B. et al. // J. Phys.: Condens. Matter. 2001. V. 13. № 20. P. 4367.
Palinkas G., Kalman E. // Z. Naturforsch. 1981. B. 36. A. № 12. S. 1367.
Смирнов П.Р., Тростин В.Н. Структурные параметры ближнего окружения ионов в водных растворах неорганических электролитов. Иваново. Изд-во “Иваново”, 2011. 400 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


