Журнал физической химии, 2020, T. 94, № 4, стр. 528-532
Термодинамика адсорбции в системе целлюлоза–вода
Ю. Б. Грунин a, *, М. С. Иванова a, Д. С. Масас a, Л. Ю. Грунин a
a Поволжский государственный технологический университет
Йошкар-Ола, Россия
* E-mail: GruninYB@volgatech.net
Поступила в редакцию 24.05.2019
После доработки 24.05.2019
Принята к публикации 18.06.2019
Аннотация
Методами 1Н-ЯМР-релаксации изучены сорбционные свойства нативной целлюлозы и состояние воды, адсорбированной ее волокнами. Предложена схема надмолекулярной организации микрофибрилл целлюлозы. Разработана модель мономолекулярной адсорбции воды на гидрофильной поверхности целлюлозы, учитывающая пространственное расположение активных центров и характер формирования водородных связей. Установлена связь чистой теплоты адсорбции воды на целлюлозе с временами спин-спиновой релаксации в слоях прочносвязанной воды. Предложен способ определения константы адсорбционного равновесия, изменения энтропии и коэффициента поверхностного натяжения на границе раздела “твердое тело–жидкость”.
Целлюлоза – наиболее распространенный биополимер растительного и животного происхождения, который обладает уникальными свойствами: возобновляемостью ресурсов, способностью к биодеградации и возможностью получения материалов с заданными характеристиками [1–3]. Традиционно изучение состояния системы целлюлоза–вода осуществляется с помощью сорбционного метода, который чаще всего базируется на теории Брунауэра–Эммета–Теллера (БЭТ) [4]. Однако получаемые этим методом результаты зачастую коррелируют лишь в качественном отношении, что связано с известными ограничениями теории БЭТ [3, 4]. Особую сложность представляет оценка энергетических и энтропийных характеристик исследуемой системы, что обусловлено проведением трудоемких сорбционных измерений в широком диапазоне температур [5]. По нашему мнению, прогрессирующие в настоящее время методы протонного магнитного резонанса могут дать ценную информацию о термодинамических параметрах увлажненной целлюлозы [6].
Цель настоящего исследования – разработка механизма адсорбции молекул воды на активной поверхности целлюлозы и способов определения термодинамических функций их взаимодействия с помощью 1Н-ЯМР-релаксации.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Объектами исследования служили образцы Iβ-целлюлозы из хлопкового волокна (ГОСТ 595-79). Изотермы адсорбции паров воды на целлюлозных образцах получали с применением метода изопиестических серий [7]. Для этого предварительно высушенные в сушильном шкафу при температуре 105°С в течение 12 ч образцы выдерживали в эксикаторах с заданными значениями относительных давлений паров воды до постоянной массы при 20°С.
Изучение состояния системы целлюлоза–вода проводили с применением методик протонного магнитного резонанса. Измерения выполняли на ЯМР-релаксометре Spin Track [8] с рабочей частотой 20 МГц. Спад свободной индукции (ССИ) регистрировали с периодом нечувствительности приемного тракта менее 8 мкс, что оказалось очень важным для анализа сигналов от полисахаридов с короткими временами спин-спиновой релаксации. ССИ измеряли как отклики спиновой системы на одиночный 90° радиочастотный импульс. Поскольку ССИ использовали для анализа формы временного спада и преобразования в спектральную линию, измерения проводили на частоте, отличной от резонансной на 100 кГц, с целью минимизации помех. Время регистрации ССИ составляло 2 мс с шагом выборки отсчетов квадратурного сигнала в 0.2 мкс, количество накоплений составляло 100, время повторения сканов при накоплении сигнала – 1000 мс.
Времена спин-спиновой релаксации образцов хлопковой целлюлозы определяли методами ССИ и применением импульсной последовательности Карра–Парселла–Мейбума–Гилла (CPMG) [9, 10]. Длительности 90° и 180° радиочастотных импульсов составляли 1.8 и 3.6 мкс соответственно. Сигналы ССИ от увлажненной хлопковой целлюлозы аппроксимировали функцией [11, 12]:
(1)
$\begin{gathered} FID(t) = {{A}_{1}}\exp \left( { - \frac{1}{2}{{a}^{2}}{{t}^{2}}} \right)\cos \frac{1}{2}bt + \\ + \;{{A}_{2}}\exp \left( { - \frac{1}{2}M_{2}^{{am}}{{t}^{2}}} \right) + {{A}_{3}}\exp \left( { - {{{\left( {\frac{t}{{T_{2}^{{*w}}}}} \right)}}^{2}}} \right), \\ \end{gathered} $Поскольку амплитуды А1 и А2 пропорциональны протонным населенностям кристаллической и аморфной фаз целлюлозы, отношение А1 к общему числу ядер водорода в образце позволяет оценить степень кристалличности [7, 11–13]:
Нами было установлено [14], что при адсорбции паров воды на целлюлозе на одну ее поверхностную молекулу приходится в среднем одна молекула моноадсорбированной воды. Это дает основание связать степень кристалличности целлюлозы k с емкостью адсорбционного монослоя воды wм, величина которого рассчитывается на основе предварительно снятой изотермы адсорбции решением уравнения БЭТ [4]. Таким образом, степень кристалличности вычисляется с помощью соотношения [7, 11, 13, 14]:
Экспериментальные значения степени кристалличности образцов хлопковой целлюлозы, определяемые выражениями (2) и (3), коррелируют между собой и согласуются с результатами рентгеновских и ИК-измерений [7]. Приравнивая правые части уравнений (2) и (3), емкость моноадсорбционного слоя воды, рассчитывали по формуле:
Результаты вычисления емкости монослоя хлопковой целлюлозы с помощью выражения (4) и решения уравнения БЭТ применительно к изотермам адсорбции, снимаемым на тех же образцах, находятся в хорошем согласии.ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
На основе современных представлений о строении структурных элементов целлюлозы и собственных многолетних исследований [7, 11–14] нами предложена модель надмолекулярной организации микрофибриллы хлопковой целлюлозы со степенью кристалличности 0.7, учитывающая наличие щелевидных пор (рис. 1). В процессе биосинтеза за счет внутри- и межмолекулярных водородных связей макромолекулы целлюлозы агрегируют в кристаллическую элементарную фибриллу (ЭФ). Затем происходит объединение ЭФ в микрофибриллы (МФ), которые формируют более крупные образования [1, 15].
Рис. 1.
Схема поперечного разреза макрофибриллы, состоящей из агрегатов микрофибрилл, каждая из которых содержит по четыре элементарных фибриллы: 1 – элементарная фибрилла, 2 – микропора, 3 – мезопора.

Дадим краткую характеристику процесса адсорбции воды на активной поверхности нативной целлюлозы. По нашему мнению, молекула воды может адсорбироваться на глюкопиранозных кольцах поверхностных цепочек целлюлозы двумя способами. Если в качестве поверхностного активного центра (ПАЦ) выступает группа –СН2ОН, то молекуле воды удобнее адсорбироваться на нем через атом кислорода. В этом случае атом водорода молекулы воды может образовывать дополнительную водородную связь с O4, или с O5, или с глюкозидным кислородом в зависимости конформации группы –СН2ОН. В соседнем глюкопиранозном кольце целлюлозной цепочки, испытывающем конформационный переворот на 180°, центрами адсорбции являются атомы O2 и O3, с которыми молекулы воды образуют две водородные связи.
Как показывает расчет, базирующийся на современных представлениях о надмолекулярной организации нативной целлюлозы [1, 16], расстояние между ее ближайшими ПАЦ, в роли которых выступают OH-группы, составляет в среднем 6.5 Å. Таким образом, моноадсорбированные молекулы воды разобщены и образуют достаточно прочные водородные связи с ПАЦ целлюлозы [1, 7, 17]. Каждый предыдущий адсорбционный слой служит адсорбентом для последующего [4].
Обычно для изучения состояния системы целлюлоза–вода применяют термодинамический подход, в основе которого лежит анализ изотерм адсорбции с использованием уравнения БЭТ, позволяющего определять константу адсорбционного равновесия и емкость монослоя. Снимая изотермы адсорбции в некотором температурном интервале, можно определить энтальпии взаимодействия целлюлозы и монослоя воды, чистой теплоты адсорбции и характера вариации энтропии в слоях адсорбата. При определении указанных параметров часто возникают трудности, связанные с ограниченностью теории БЭТ [4].
Предлагаемые в данной работе методы 1H-ЯМР-релаксации совместно с сорбционными измерениями способны решить ряд вопросов, связанных со структурной организацией целлюлозы и характере ее взаимодействия с адсорбированной водой. Известно, что для моноадсорбированных молекул воды доминирует вращательное движение относительно водородных связей [9]. Это вращение может модулироваться тепловым колебательным движением, которое с ростом температуры возрастает по амплитуде. В случае превышения активационного барьера происходит обмен между молекулами первого и второго слоев. Таким образом, скачкообразные трансляционные и вращательно-колебательные движения составляют механизм протонной магнитной релаксации адсорбированной воды на активной поверхности целлюлозы [14, 18, 19].
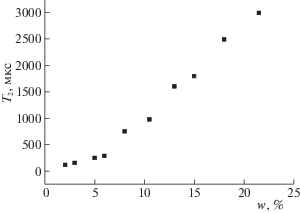
Рост времени спин-спиновой релаксации с увеличением влагосодержания целлюлозы (рис. 2) свидетельствует о том, что на начальной стадии адсорбции подвижность молекул воды сравнительно мала и возрастает от слоя к слою при дальнейшем увлажнении [6, 7, 11].
В рамках аррениусовских представлений [4] энергия активации адсорбированных молекул в монослое может превышать энтальпию взаимодействия молекул воды с активными центрами целлюлозы, а во втором слое – суммарную энергию межмолекулярного взаимодействия. Описанный процесс хорошо иллюстрируется временами корреляции теплового движения [9].
Заменяя времена корреляции молекул первого и второго слоев водного адсорбата через соответствующие им истинные времена спин-спиновой релаксации, можно определить чистую теплоту адсорбции с помощью соотношения [6]:
где ΔH0 – стандартная энтальпия адсорбционного взаимодействия; L – теплота конденсации адсорбтива; R – универсальная газовая постоянная; Т – абсолютная температура; $T_{2}^{1}$ и $T_{2}^{2}$ – истинные времена спин-спиновой релаксации в первом (монослое) и втором слоях адсорбированной воды соответственно.Учитывая, что функции, описывающие релаксацию поверхностных молекул целлюлозы и воды, автономны, можно полагать, что измеренное и истинное времена спин-спиновой релаксации монослоя эквивалентны. Истинное значение $T_{2}^{2}$ во втором слое может быть определено с использованием условия быстрого молекулярного обмена между первым и вторым адсорбционными слоями в рамках теории Бломбергена–Парселла–Паунда [9, 10]. Если содержание воды в целлюлозе соответствует удвоенному значению монослоя 2wм, то указанное условие может быть записано следующим образом:
(6)
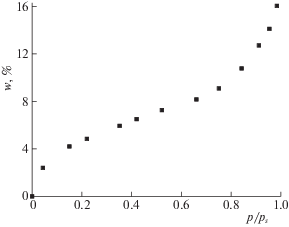
$\frac{{2{{w}_{{\text{м}}}}}}{{{{T}_{{{\text{2изм}}}}}}} = \frac{{{{w}_{{\text{м}}}}}}{{T_{2}^{1}}} + \frac{{{{w}_{{\text{м}}}}}}{{T_{2}^{2}}},$Обычно емкость монослоя и константа адсорбционного равновесия рассчитываются на основе предварительно снятой изотермы адсорбции решением уравнения БЭТ (рис. 3) [4].
Для экспресс-оценки емкости монослоя хлопковой целлюлозы нами предложен метод, связанный с установленным соответствием содержания моноадсорбированных молекул воды с количеством глюкозных остатков поверхностных цепочек целлюлозы (вычисления проводятся по формуле (4)). Емкость монослоя хлопковой целлюлозы со степенью кристалличности 0.73 по БЭТ составляет 0.031 г/г, по формуле (4) – 0.030 г/г, а константа адсорбционного равновесия по уравнению БЭТ С = 25.
Преобразуя уравнение (6), получаем:
Применительно к трехпроцентному влагосодержанию, характерному для монослоя хлопковой целлюлозы, $T_{2}^{1}$ составляет примерно 160 мкс, в то время как ${{T}_{{2{\text{изм}}}}}$ для бислоя воды – 280 мкс. Значение $T_{2}^{2}$ превышает по величине $T_{2}^{1}$ в 7 раз. Таким образом, чистая теплота адсорбции согласно соотношению (5) равна ΔH0 – L = 4.87 кДж/моль.Известно, что энергия Гиббса связана с константой адсорбционного равновесия уравнением Вант-Гоффа [4]:
где ΔG0 – стандартная энергия Гиббса. С другой стороны, энергия Гиббса связана с чистой теплотой адсорбции и энтропийным членом выражением [4]: где ΔS0 – стандартная энтропия адсорбата. При адсорбции выделяется часть теплоты, поэтому энтальпийный член взят со знаком плюс.Проведем анализ бислойной адсорбции молекул воды на активной поверхности целлюлозы. Модернизированное уравнение БЭТ (С > 1) для первого слоя имеет вид:
(10)
${{w}_{{\text{м}}}} = \frac{{{{w}_{{\text{м}}}}C}}{{\left( {\frac{{{{p}_{s}}}}{{{{p}_{1}}}} - 1} \right)\left[ {1 + C\frac{{{{p}_{1}}}}{{{{p}_{s}}}}} \right]}},$Процесс завершения заполнения адсорбционного бислоя описывается следующим уравнением:
(11)
$2{{w}_{{\text{м}}}} = \frac{{{{w}_{{\text{м}}}}C}}{{\left( {\frac{{{{p}_{s}}}}{{{{p}_{2}}}} - 1} \right)\left[ {1 + C\frac{{{{p}_{2}}}}{{{{p}_{s}}}}} \right]}},$(12)
$2 = \frac{{\left( {\frac{{{{p}_{s}}}}{{{{p}_{1}}}} - 1} \right)\left[ {1 + C\frac{{{{p}_{1}}}}{{{{p}_{s}}}}} \right]}}{{\left( {\frac{{{{p}_{s}}}}{{{{p}_{2}}}} - 1} \right)\left[ {1 + C\frac{{{{p}_{2}}}}{{{{p}_{s}}}}} \right]}}.$С помощью выражения (8) вычислим энергию Гиббса ΔG0 = 7.94 кДж/моль. После подстановки уравнений (5) и (8) в (9) выразим энтропию адсорбата:
Используя известные значения параметров, находим ΔS0 = 10.24 Дж/(K моль). Расчет термодинамических параметров был проведен применительно к бислойной адсорбции воды на хлопковой целлюлозе, а для полислойной – представлен в работе [6].Важное свойство адсорбированной воды – ее коэффициент поверхностного натяжения на границе раздела твердое тело–жидкость (σтж). Он характеризует работу, необходимую для формирования единицы площади поверхности раздела [20]. Известно, что работа по образованию поверхности раздела ΔA связана с уменьшением энергии Гиббса, которая определяется константой адсорбционного равновесия соотношением (8):
Применительно к 1 молю воды коэффициент поверхностного натяжения равен: Отсюда следует, что σтж определяется чистой теплотой адсорбции. Расчет на основе экспериментальных данных, указанных выше, показал, что σтж = 0.13 Дж/м2. Очевидно, это значение может быть использовано при анализе поверхностных и капиллярно-пористых явлений и адсорбции Гиббса на целлюлозе и материалов на ее основе.Таким образом, предложены схема структурной организации микрофибрилл нативной целлюлозы и механизм специфической адсорбции воды на ее гидрофильной поверхности. Разработаны альтернативные традиционные способы определения константы адсорбционного равновесия (при бислойной адсорбции) и емкости моноадсорбционного слоя целлюлозы с использованием 1Н-ЯМР-релаксации. Представлены методы определения чистой теплоты адсорбции с помощью ЯМР-релаксационных измерений; изменения энтропии адсорбата в ходе равновесного увлажнения целлюлозы и коэффициента поверхностного натяжения на границе раздела твердое тело–жидкость.
Список литературы
Brown R.M. // J. Pol. Science, Part A, Pol. Chem. 2004. V. 42. № 3. P. 487.
French A.D. // Cellulose. 2017. V. 24. № 11. P. 4605.
Роговин З.А. Химия целлюлозы. М.: Химия, 1972. 519 с.
Грег С., Синг К. Адсорбция, удельная поверхность, пористость. М.: Мир, 1984. 306 с.
Герасимов Я.И. Курс физической химии: в 2 т. М.: Химия, 1964. Т. 1. 624 с.
Grunin Yu.B., Grunin L.Yu., Masas D.S. et al. // Russ. J. Phys. Chem. A. 2016. V. 90. № 11. P. 2249.
Grunin L.Yu., Grunin Yu.B., Talantsev V.I. et al. // Pol. Science, Ser. A. 2015. V. 57. № 1. P. 43.
www.nmr-design.com.
Абрагам А. Ядерный магнетизм. М.: Изд-во иностр. лит., 1963. 551 с.
Чижик В.И. Ядерная магнитная релаксация. СПб.: СПбГУ, 2004. 385 с.
Grunin Yu.B., Grunin L.Yu., Talantcev V.I. et al. // Biophysics. 2015. V. 60. № 1. P. 43.
Grunin L.Y., Grunin Y.B., Nikolskaya E.A. et al. // Biophysics. 2017. V. 62. № 2. P. 198.
Грунин Ю.Б., Грунин Л.Ю., Гальбрайх Л.С. и др. // Химические волокна. 2017. № 5. С. 31.
Grunin Y.B., Grunin L.Y., Nikolskaya E.A. et al. // Pol. Science, Ser. A. 2012. V. 54. № 3. P. 201.
Carpita N.C. // Plant Physiol. 2011. V. 155. № 1. P. 171.
Nishiyama Y. // J. Wood Sci. 2009. V. 55. № 4. P. 241.
Grunin Yu.B., Grunin L.Yu., Nikolskaya E.A. et al. // Russ. J. Phys. Chem. A. 2013. V. 87. № 1. P. 100.
Kubo R., Tomita K. // J. Phys. Soc. Japan. 1954. V. 9. № 6. P. 888.
Grunin Yu.B., Grunin L.Yu., Nikolskaya E.A. // Russ. J. Phys. Chem. A. 2007. V. 81. № 7. P. 1165.
Савельев И.В. Курс физики, том 2. Электричество. Колебания и волны. Волновая оптика: Учеб. пособие в 3-х томах. СПб.: Изд-во “Лань”, 2007. 467 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии