Журнал физической химии, 2020, T. 94, № 6, стр. 932-937
Влияние техногенных факторов и биодеструкторов на термическое поведение блок-сополимера хитозана с полиметилакрилатом
Н. Н. Смирнова a, *, А. В. Маркин a, О. Н. Смирнова a, В. Ф. Смирнов a, А. В. Князев a
a Национальный исследовательский Нижегородский государственный университет
им. Н.И. Лобачевского
Нижний Новгород, Россия
* E-mail: smirnova@ichem.unn.ru
Поступила в редакцию 23.08.2019
После доработки 23.08.2019
Принята к публикации 17.09.2019
Аннотация
Впервые методами дифференциальной сканирующей калориметрии в области 250–510 K и термогравиметрии в области 300–850 K проведен термический анализ образцов блок-сополимера хитозана с полиметилакрилатом после воздействия на него электромагнитного поля, ультрафиолетового излучения, ультразвука и биодеструкторов. Впервые показано, что совместное воздействие физических факторов и биодеструкторов вызывает изменение физико-химических свойств: температур физических превращений, температур начала термодеструкции и характера термораспада.
Биологические свойства полимеров разнообразны, их способность противостоять воздействию живых организмов определяет их биостойкость, а биоразлагаемость характеризует их легкую утилизацию, что очень важно для защиты окружающей среды от воздействий на нее загрязнений и отходов производств [1–3]. Большие перспективы в этом направлении связывают с созданием на основе синтетических и природных полимеров биоразлагаемых, биоразлагаемых–биосовместимых (со)полимеров и композитов [4–6]. В последние десятилетия неуклонно растет производство синтетических полимеров, в частности, акриловых, их утилизация является чрезвычайно важной экологической проблемой [7]. Одним из природных полимеров, который может быть использован при создании биоразлагаемых композиций, является хитозан (ХТЗ), получаемый при деацетилировании природного хитина [8]. Он имеет уникальные физиологические и экологические свойства, такие как физиологическая активность при отсутствии токсичности, биоразлагаемость, биосовместимость, доступность и возобновляемость сырьевых источников [8]. В процессе эксплуатации полимерные материалы подвергаются воздействию различных факторов окружающей среды, как климатических так и техногенных, что может приводить к изменению их свойств, а соответственно и изменению их способности к деструкции под действием биодеструкторов. Для их рационального использования необходимо изучить влияние этих факторов на их физико-химические свойства. В связи с решением этой задачи для выявления воздействия электромагнитного поля (ЭМП), ультрафиолетового излучения (УФ), ультразвука (УЗ) и биодеструкторов (Aspergillus niger) на полимеры был выбран блочный сополимер хитозана с полиметилакрилатом (ХТЗ/ПМА) с соотношениями условных звеньев 1 : 2.4. Термодинамические свойства сополимера с таким же содержанием блоков (теплоемкость, энтальпии сгорания, термодинамические характеристики образования и синтеза) были изучены в работе [9], имеются данные о температурной зависимости теплоемкости, полиметилакрилата (ПМА) [10], хитозана (ХТЗ) [11, 12], а также результаты дифференциального термического анализа образцов хитозана различного происхождения [13], в работах [14–16] было подробно изучено влияние на термические свойства блок-сополимера ХТЗ/ПМА (соотношение звеньев 1 : 2.5) влажности, низких и высоких температур. Данные о влиянии других физических воздействий на термические свойства сополимера до настоящего времени отсутствуют.
Целью данной работы было изучение влияния природных факторов, а именно ЭМП, УФ, УЗ и гриба биодеструктора Aspergillus niger на термическое поведение блок-сополимера хитозана с полиметилакрилатом (ХТЗ/ПМА).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Характеристики изученных образцов. Поскольку известно, что ХТЗ обладает высокоупорядоченной стереорегулярной структурой и свойства его заметно различаются в зависимости от сырья, из которого он выделяется, а также от способов выделения и очистки [8], то для корректности обсуждения полученных результатов нами изучены также термодинамические и теплофизические свойства ХТЗ и ПМА, которые были использованы при синтезе изученного ХТЗ/ПМА.
Образец ХТЗ/ПМА получали в водно-уксуснокислом растворе полисахарида (3 мас. %) с концентрацией уксусной кислоты 6 мас. %, при 291–296 K, в течение 24 ч, в процессе радикальной деградации цепей полисахарида под действием инициирующей окислительно-восстановительной системы пероксид водорода–аскорбиновая кислота (ν(С6Н8О6)/ν(Н2О2) = 1 моль, (звено глюкозамина)/(Н2О2) = 75 осново-моль/моль), соотношение [МА]/[звено глюкозамина] = 2.5 моль/осново-моль). Соотношение звеньев ХТЗ : ПМА в исследуемом блок-сополимере равно 1 : 2.4.
Используемый хитозан (ХТЗ) приобретен в ЗАО “Биопрогресс” Московской обл., его степень деацетилирования (СД) равна 80%, молекулярная масса, определенная вискозиметрически 1.2 × 105.
Полиметилакрилат (ПМА) получали растворной полимеризацией МА в ацетоне при 333 K в присутствии ДАК (0.5 мас. % от массы мономера) до конверсии 7%. Полимер отделяли трехкратным переосаждением в диэтиловый эфир. Молекулярную массу ПМА (Мw = 6.0 × 105) определяли методом гель-проникающей хроматографии при Т = 313 K на жидкостном хроматографе Prominence LC-20VP “Shimadzu”.
Аппаратура и методика измерений. Для определения температур физических превращений в области 200–520 K использовали дифференциальный сканирующий калориметр DSC 204 F1 Phoenix производства фирмы Netzsch Gerätebau, Германия. Конструкция калориметра и методика работы описаны в работах [17, 18]. Калибровку калориметра осуществляли посредством определения в интервале 170–700 K температур и энтальпий плавления н-гептана, ртути, индия, олова, свинца, висмута и цинка (DSC Standard – Set 6.239.2-91.3). Измерения теплофизических характеристик проводили при средней скорости нагрева ампулы с веществом 5 K/мин в атмосфере аргона. Установлено, что используемые аппаратура и методика позволяют определять температуры фазовых превращений с погрешностью ±0.5 K, энтальпий переходов ±1%.
Термогравиметрический (ТГ) анализ изученных образцов проводили с помощью термомикровесов TG 209 F1 производства фирмы Netzsch Gerätebau, Германия в атмосфере аргона, в области 300–850 K [19]. Термомикровесы TG 209 F1 позволяют фиксировать изменение массы до ±0.1 мкг. Средняя скорость нагрева тигля с веществом составляла 5 K/мин. Методика проведения ТГ-анализа стандартная, согласно Netzsch Software Proteus.
Воздействие на образцы полимерных композиций ультрафиолетового излучения осуществлялось согласно нормативам ГОСТ 28202-89. “Основные методы испытаний на воздействие внешних факторов. Часть 2. Испытания. Испытание Sa: Имитированная солнечная радиация на уровне земной поверхности”. Образцы подвергались воздействию ультрафиолетового облучения (источник УФ-лампа ДБ-30; облученность в эффективном спектральном диапазоне 1.12 Вт/м2) по следующей методике: 24-часовой цикл, состоящий из 4-часовой фазы облучения и 20-часовой темновой фазы и повторяемый 3 раза. Доза облучения по данному методу составила 16.128 кВт/м2 за цикл, что приближается к наиболее жестким естественным условиям.
Воздействие на образцы полимерных композиций магнитного поля осуществляли, помещая образцы материала в импульсное магнитное поле. Характеристики поля: пачки из 20 импульсов длительностью 227 мкс с амплитудой 1.5 мТл (что в 30 раз превышает напряженность магнитного поля земли), следующих с частотой 15 Гц. Источник поля: генератор марки VL-2 фирмы Electro-Biology Inc., США. Экспозиция – 120 мин.
Воздействие на образцы полимерных композиций ультразвука осуществлялось при помощи оригинального автономного ультразвукового излучателя (модель “AND” UN-231, Япония) с частотой колебаний 2.5 МГц. Образцы подвергались озвучиванию в течение 20 мин.
В качестве биологического объекта в экспериментах по биоразлагаемости блок-сополимера использовался штамм гриба “Aspergillus niger”, который по результатам предыдущих исследований показал наибольшую эффективность для указанного сополимера, кроме того он является наиболее активным биодеградантом широкого круга промышленных и строительных материалов. Исследования проводили в течение 20 недель. Микромицеты были предоставлены Всероссийской коллекцией микроорганизмов (г. Пущино Моск. обл.). После этого система инкубировалась в течение 28 суток (4 недели). Суспензия представляла собой раствор сахарозы в воде (соотношение 1 : 15), в котором находились споры Aspergillus niger.
На основании исследования физико-механических свойств пленок ХТЗ/ПМА было показано, что при воздействии на пленки ХТЗ/ПМА ультрафиолетового облучения и электромагнитного поля происходит увеличение их прочности с 39 до 46 МПа и деформации с 6 до 15%, в то время как при действии ультразвука физико-механические свойства материала практически не изменяются. При обработке пленочных материалов, предварительно подвергшихся воздействию климатических факторов, микромицетами во всех случаях наблюдается падение физико-механических свойств – разрушающего напряжения и деформации при разрыве, которое свидетельствует о биодеградации полимеров.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Термогравиметрический анализ
Термогравиметрический анализ был проведен для образцов ХТЗ, ПМА, ХТЗ/ПМА, и сополимера ХТЗ/ПМА после воздействия на него УФ, УЗ, ЭМП и биодеструкторов. Нужно отметить, что полученные результаты показали, что все изученные образцы, включающие ХТЗ (ХТЗ, ХТЗ/ПМА до и после воздействия УЗ, УФ, ЭМП и биодеструкторов) содержали адсорбированную воду (3.5–6 мас. %), хорошая адсорбционная способность ХТЗ и его сополимеров отмечалась ранее в статьях [8, 15, 16]. В качестве примера на рис. 1 показаны подробные результаты, полученные при изучении разложения образца ХТЗ/ПМА (рис. 1) в области от 300 до 850 K.
Полученные данные показывают, что уменьшение массы образца происходит в несколько стадий. Так, до Т = 450 K происходит уменьшение массы образца на 3.5%, что связано с испарением адсорбционной воды, от 450 до 501 K масса образца практически не изменяется, заметная потеря массы обезвоженного ХТЗ/ПМА в среде аргона, связанная с разрушением образца, наблюдается в области температур 501–570 K (16%), далее при увеличении температуры на 50 K потеря массы возрастает на 34% и до 850 K масса образца уменьшается еще на 20%. Таким образом, в инертной среде обезвоженный образец ХТЗ/ПМА термически устойчив вплоть до 501 K, его термическое разложение происходит в три стадии.
Предварительно образец ХТЗ/ПМА был прогрет до 420 K, изотермически выдержан при этой температуре в течении 3 ч для полного удаления адсорбционной воды. Затем, уже для этого образца выполнен повторный анализ. Результаты двух независимых термогравиметрических измерений совпали, если учесть потерю массы адсорбционной воды (первое измерение, рис. 1).
В табл. 1 представлены результаты термогравиметрического анализа образцов ХТЗ, ПМА, ХТЗ/ПМА до и после воздействия на них УЗ, УФ, ЭМП и биодеструкторов (Aspergillus terreus). В табл. 1 приведено среднее значение по двум экспериментам. Во всех случаях исключено количество адсорбционной воды.
Таблица 1.
Результаты TГ-исследований образцов ХТЗ, ПМА, ХТЗ/ПМА и ХТЗ/ПМА после воздействия ультразвука, ультрафиолета, электромагнитного поля и биодеграданта
| Образец | ∆m адсорб. Н2О, мас. % | Тдестр, К | Интервалы деструкции, K | ∆m сухого образца, мас. % |
|---|---|---|---|---|
| ХТЗ | 5.2 | 501 | 501–604 | 40 |
| 604–850 | 20 | |||
| ПМА | – | 587 | 587–700 | 97 |
| 700–850 | 1.7 | |||
| ХТЗ/ПМА | 3.5 | 501 | 501–578 | 16 |
| 578–765 | 34 | |||
| 765–850 | 20 | |||
| ХТЗ/ПМА (УЗ + биодеградант) | 4.8 | 498 | 498–585 | 19.7 |
| 585–660 | 27.5 | |||
| 660–820 | 34.3 | |||
| ХТЗ-ПМА (УФ + биодеградант) | 3.6 | 503 | 503–580 | 18.3 |
| 580–653 | 29.4 | |||
| 653–733 | 13.8 | |||
| 733–840 | 5 | |||
| ХТЗ-ПМА (ЭМП + ГР) | 6 | 480 | 480–570 | 14.0 |
| 570–660 | 32.8 | |||
| 660–740 | 40.5 | |||
| 740–850 | 7.4 |
За температуру начала термодеструкции принята температура при потере массы 2 мас. % обезвоженных образцов, интервалы разложения образцов определены по первой производной зависимости потери массы от времени по методике фирмы Netzsch Gerätebau.
Наиболее устойчивым из изученных образцов является ПМА (Тдест = 587 К), что соответствует литературным данным [7, 9, 15], Тдест всех остальных образцов, как и следовало ожидать ниже и близки к Тдест хитозана 501 K, однако, если она соответствует и ХТЗ/ПМА, то в результате действия на него УФ и биодеструкторов наблюдается ее незначительное возрастание (503 K), то в случае воздействия УЗ и биодеструкторов она уменьшается на 3 K и наблюдается ее значительное уменьшение в случае действия ЭМП и биодеструкторов, в этом случае уменьшение составляет 21 K. Таким образом, подвергая ХТЗ/ПМА внешним воздействиям, таким как ЭМП и биодеструкторы, можно значительно изменить его термическую устойчивость.
ХТЗ разлагается в два этапа в интервале 501–604 K и 604–850 K, что согласуется с данными работы [20], в ней же указано, что эти стадии проходят с выделением энергии в форме теплоты. ПМА разлагается в две стадии, первая в интервале 587–700 K, где потеря массы составляет 97%, а затем до 850 K происходит потеря всей массы 1.7%. В работе [20] процесс деструкции был изучен методом термического анализа. В ней отмечается, что разложение идет с поглощением энергии в форме теплоты, первый эндотермический пик наблюдается при Тдест1 = 599 K, а второй при Т = = 670 K. Вероятно, несмотря на разный механизм процесса деструкции в интервале 587–700 K.
Деструкция ХТЗ/ПМА происходит в три этапа, переходящих друг в друга (табл. 1). Первый этап (501–578 K) связан, вероятнее всего, с началом разложения блока ХТЗ, затем (578–765 K) продолжает разлагаться, как и блок ХТЗ, так и начинается разложение блока ПМА, в интервале 765–850 K продолжают одновременно разлагаться оба блока.
Полученные нами результаты показали, что процесс разложения ХТЗ/ПМА зависит от воздействия на него УФ, УЗ и ЭМП и “Aspergillus terreus” (табл. 1). Так, если в случае с воздействием УЗ и биодеградантов имеется три этапа выраженного разложения, то при действии УФ, ЭМП и биодеградантов количество их увеличивается до четырех. Причем, на первом также происходит предположительно разложение блока ХТЗ, затем процесс разложения усложняется по сравнению с образцом ХТХ/ПМА, не подвергшимся воздействиям.
Таким образом, было установлено, что воздействие на образцы ХТХ/ПМА указанными выше факторами приводит к различным механизмам их термической деструкции.
Результаты ДСК-исследования
Дифференциальный сканирующий анализ был выполнен в области 250–850 K для ХТЗ, ПМА, ХТЗ/ПМА и ХТЗ/ПМА после воздействия УЗ, УФ, ЭМП и биодеградантов. В случае воздействия на ХТЗ/ПМА только УЗ, УФ, ЭМП ДСК исследования были проведены в области от 230 до 330 K для определения температуры расстеклования блока ПМА.
На рис. 2 в качестве примера представлены результаты ДСК исследований ХТЗ. Как было показано методом термогравиметрии, ХТЗ и все образцы изученных ХТЗ/ПМА содержали адсорбционную воду, вследствие чего на первоначальной ДСК-кривой (рис. 2, кривая 1) наблюдается значительный эндо-эффект, связанный с обезвоживанием образца. После нагрева образца до 480 K он изотермически выдерживался при этой температуре около 3 часов для полного обезвоживания, затем охлаждался до 250 K, после чего были выполнены его повторные измерения (рис. 2, кривая 2). Полученные результаты согласуются с литературными данным для ХТЗ с близкой степенью деацетилирования [10], где также наблюдался β-переход при Тβ = 320 К и две температуры расстеклования при T = 347 K и T = 413 K. β-Переход авторы работы [15] объясняют либрацией пиранозных колец вокруг глюкозидной связи, а два температурных интервала расстеклования – неоднородной структурой хитозана, который состоит из аморфных и высокоупорядоченных областей [16]. На рис. 3 представлены результаты исследований ПМА, обезвоженных образцов ХТЗ/ПМА до и после воздействия на них УФ, УЗ, ЭМП и биодеградантов. Полученная нами Тg(ПМА) = 288 ± 1 K хорошо согласуется с литературным значением Тg(ПМА) = 285 ± 1 K [10].
Рис. 2.
ДСК-кривые образца ХТЗ: первый прогрев, с содержанием адсорбированной воды (1), второй прогрев, после удаления адсорбированной воды (2).

Рис. 3.
ДСК-кривые образцов: ХТЗ/ПМА (1), ПМА (2), ХТЗ/ПМА (УФ + биодеградант) (3), ХТЗ/ПМА (ЭПМ + биодеградант) (4), ХТЗ/ПМА (УЗ + биодеградант) (5).
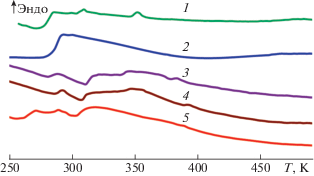
Во всех случаях на ДСК-кривых сополимеров проявляются переходы, характерные для ХТЗ и ПМА, характеристики которых приведены в табл. 2, в ней также указаны температуры расстеклования блока ПМА в сополимерах при воздействии на них только УЗ, УФ и ЭМП. Полученные результаты показывают, что ХТЗ и ПМА взаимно влияют на температуры физических превращений. Так, Тg(ПМА) в ХТЗ/ПМА уменьшается, также как и Тβ(ХТЗ), Тg1(ХТЗ) не изменяется, Тg2(ХТЗ) в ХТЗ/ПМА не проявилось. Интересно отметить, что воздействие всех рассматриваемых физических факторов уменьшает температуру расстеклования блока ПМА в сополимере, что, вероятнее всего, связано с уменьшением их размеров при воздействии УЗ, УФ и ЭМП.
Таблица 2.
Температуры физических переходов в ХТЗ, ПМА, ХТЗ/ПМА, ХТЗ/ПМА после воздействия ультразвука, ультрафиолета, электромагнитного поля и биодеграданта
| Образец | m образца, мг | Тпер ± 1, K | Тg(ПМА) ± ± 1, K | Тβ(ХТЗ) ± ± 1, K | Тg1(ХТЗ) ± ± 1, K | Тg2(ХТЗ) ± ± 1, K |
|---|---|---|---|---|---|---|
| ХТЗ | 30.214 | – | – | 325 | 347 | 390 |
| ПМА | 25.254 | – | 288 | – | – | – |
| ХТЗ/ПМА | 21.294 | – | 284 | 307 | 349 | – |
| ХТЗ/ПМА (УЗ) | 15.421 | – | 279 | Не определялись | ||
| ХТЗ/ПМА (УЗ + ГР) | 18.254 | 268 | 286 | 310 | ‒ | 386 |
| ХТЗ-ПМА (УФ) | 17.458 | – | 280 | Не определялись | ||
| ХТЗ-ПМА (УФ + биодеградант) | 17.267 | – | 285 | 313 | 343 | 381 |
| ХТЗ-ПМА (ЭМП) | 12.654 | – | 279 | Не определялись | ||
| ХТЗ-ПМА (ЭМП + биодеградант) | 21.874 | – | 288 | 310 | 345 | 390 |
Образцы ХТЗ/ПМА после УЗ, УФ и ЭМП подвергли биодеструкции штаммами Aspergillus niger и провели их ДСК-исследования. Температура расстеклования блока ПМА, первоначально уменьшенная при воздействии УЗ, УФ и ЭМП, после биодеструкции увеличилась и стала равной температуре расстеклования исходного ХТЗ/ПМА.
В случае воздействия УЗ- и биодеструкторов появился еще один физический переход с Тпер = = 268 ± 1 K, что связано с разной структурой ХТЗ/ПМА после воздействия УЗ по сравнению с УФ И ЭМП, а соответственно и разному механизму деструкции блока ПМА под действием биодеградантов.
Для всех образцов ХТЗ/ПМА, повергнутых воздействию указанными выше факторами, Тβ(ХТЗ) увеличилась. Одной из возможных причин этого является уплотнение структуры аморфных областей ХТЗ. Напротив, воздействия УФ и ЭМП уменьшают Тg1(ХТЗ) и Тg2(ХТЗ), что говорит о разрыхлении высокоупорядоченных областей ХТЗ [20].
Таким образом, в работе методами ДСК и термогравиметрии изучено влияние УЗ, УФ, ЭМП и биодеструкторов на термические свойства блок-сополимера ХТЗ/ПМА. Показано, что внешние воздействия оказывают существенное влияние на параметры их физических превращений, начало термодеструкции и характер разложения. Эти изменения необходимо учитывать при промышленном применении ХТЗ/ПМА.
Образцы для изучения предоставлены сотрудниками кафедры ВМС и коллоидной химии химического факультета ННГУ им. Н.И. Лобачевского проф. Л.А. Смирновой и д.х.н. А.Е. Мочаловой.
Работа выполнена в рамках Государственного задания № 4.5510.2017/8.9 с использованием оборудования Центра коллективного пользования “Новые материалы и ресурсосберегающие технологии” (ННГУ им. Н.И. Лобачевского).
Список литературы
Vroman I., Tighzert L. // Materials. 2009. № 2. P. 307.
Ahmed S., Ikram S. Chitosan: derivatives, composites and applications, Beverly: Scrivener Publishing LLC, 2017.
Rinaudo M. // Prog. Polym. Sci. 2006. V. 31. № 7. P. 603.
Ванников А.В. // Высокомолекуляр. соединения. А. 2009. Т. 51. № 4. С. 547.
Daniela Cupelli et al. // Solar Energy Materials and Solar Cells. 2009. V. 93. № 11. P. 2008.
Riva R., Ragelle H., des Rieux A. et al. // Adv. Polym. Sci. 2011. V. 244. P. 19.
Uryash V.F., Kalashnikov I.N., Smirnova L.A. et al. // In Biochemistry and Biotechnology: Research and Development / Ed. S.D. Varfolomeev, G.E. Zaikov, L.P. Krylova. NY: Nova Sci. Publ. Inc., 2012. P. 119–130.
Хитин и хитозан: Получение, свойства и применение / Под ред. К.Г. Скрябина, Г.А. Вихоревой, В.П. Варламова. М.: Наука, 2002. С. 119–129.
Смирнова Н.Н., Цветкова Л.Я., Смирнова Л.А. и др. // Вестн. Нижегородского университета им. Н.И. Лобачевского. 2012. Т. 5. № 1. С. 82.
Рабинович И.Б., Лебедев Б.В. // Труды по химии и химической технологии: Межвуз. сб. Горький: Изд-во ГГУ, 1967. Вып. 2 (18). С. 36.
Цветкова Л.Я., Новоселова Н.В., Голицин В.П. и др. // Журн. хим. термодинамики и термохимии. 1993. Т. 2. № 1. С. 88.
Урьяш В.Ф., Кокурина Н.Ю., Ларина В.Н. и др. // Вестн. Нижегородского университета им. Н.И. Лобачевского. 2007. № 3. С. 98.
Ur’Yash V.F., Larina V.N. et al. // Russ. J. Phys. Chem. 2012. V. 86. № 1. P. 1.
Зотов К.А., Захарова Е.А., Смирнова О.Н. и др. // Пластические массы. 2012. № 4. С. 59.
Uryash V.F., Uryash A.V., Gruzdeva A.E. et al. // Physical Organic Chemistry: New Developments / Ed. Karl T. Burley. NY: Nova Sci. Publ., Inc., 2010. P. 183–265.
Kalashnikov I.N., Uryash V.F., Smirnova L.A. et al. // Advances in Chitin Sciences (EUCHIS’11) / Eds. V. Varlamov, S. Bratskaya, I. Yakovleva, S. Senel. St.-Pb.: Euro. Chit. Soc. Publ., 2011. V. 11. P. 126.
Höhne G.W.H., Hemminger W.F., Flammersheim H.-J. Differential Scanning Calorimetry. 2nd ed. Berlin: Springer-Verlag Berlin Heidelberg GmbH, 2003. 310 p.
Drebushchak V.A. // J. Therm. Anal. Calorim. 2005. V. 79. № 1. P. 213.
ASTM E1131-08(2014). Standard Test Method for Compositional Analysis by Thermogravimetry. ASTM International, West Conshohocken, PA, United States, 2014.
Калашников И.Н. Биодеструкция композиционных материалов на основе хитозана и акриловых полимеров, вызванная микромицетами и факторами климатического старения. Дис. … к.б.н. Н. Новгород: ННГУ им. Н.И. Лобачевского, 2013.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии



