Журнал физической химии, 2021, T. 95, № 2, стр. 197-200
Кинетика образования молекулярного водорода при радиолизе гексана и смеси С6Н14–Н2О на поверхности n-ZrO2
Т. Н. Агаев a, *, Ш. З. Мусаева a, Г. Т. Иманова a
a Национальная академия наук Азербайджана, Институт радиационных проблем
AZ1143 Баку, Азербайджанская Республика
* E-mail: agayevteymur@rambler.ru
Поступила в редакцию 11.03.2020
После доработки 11.03.2020
Принята к публикации 26.04.2020
Аннотация
Исследована кинетика накопления молекулярного водорода при радиолизе гексана и смеси гексан–вода при различных содержаниях компонентов в присутствии n-ZrO2 при Т = 300 K. Установлено, что n-ZrO2 обладает радиационно-каталитической активностью в процессах разложения гексана и смеси гексан–вода, в результате чего скорость накопления молекулярного водорода увеличивается. Выявлено, что с увеличением температуры радиационно-химический выход молекулярного водорода G(H2) резко возрастает.
Радиационно-каталитические процессы получения молекулярного водорода из гексана и смеси гексан–вода представляет большой интерес при выявлении новых путей преобразования и использования ионизирующих излучений для получения универсального энергоносителя молекулярного водорода [1–6]. Полученные результаты исследований, могут быть полезными при уточнении механизмов процесса, протекающих в экспериментальных условиях под действием ионизирующего излучения в гексане и смеси гексан–вода, а также в естественных условиях нефтегазовых месторождений, под действием излучения природных радионуклидов. В последнее время, определенная часть водного бассейна мира, загрязнена тяжелыми углеводородами. С целью повышения производительности процесса и скорости получения энергоносителя из гексана и смеси гексан–вода, использованы катализаторы радиолитических процессов разложения. Поэтому, в связи с этими процессами выявления закономерностей радиационно-каталитических процессов накопления водорода из гексана и смеси гексан–вода в присутствии n-ZrO2, представлен большой интерес в области атомной водородной энергетике и решении экологических проблем [6]. В работе [7] было показано, что n-ZrO2 обладает радиационно-каталитической активностью в процессе радиолитического разложения воды.
Представленная работа посвящена изучению кинетики получения молекулярного водорода при радиационно-каталитическом разложении гексана и смеси гексан–вода при различных соотношениях компонентов при Т = 300 K. Таким образом, в последнее время радиолиз н-гексана изучают довольно подробно [8, 10–14].
Поэтому, радиолиз смесей углеводородов с водой, представляет интерес при выявлении новых путей преобразования и использования ионизирующих излучений для получения универсального энергоносителя – водорода [12]. Результаты этих исследований могут быть полезными при уточнении механизмов процесса, протекающих в экспериментальных условиях под действием ионизирующего излучения в смеси углеводород–вода.
В настоящей работе представлены результаты исследования кинетики накопления молекулярного водорода при радиолизе модельной системы н-гексан и смеси н-гексан–вода на поверхности n-ZrO2 при комнатной температуре под действием гамма-излучения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исследована кинетика накопления молекулярного водорода при радиационно-гетерогенном радиолизе гексана n-ZrO2 + н-С6Н14 и смеси n-ZrO2 + н-С6Н14–Н2О, который проведен в статических условиях, в запаянных ампулах, объемом Vамп = 20 см3, mкат = 5 × 10–2 г, под действием γ-излучения. Заполнение ампул компонентами системы проводят их из парового состояния на вакуумно-адсорбционной установке. Запаивание ампул проведены при замораживании компонентов жидким азотом при Т = 77 K. При этом экспериментально установлено, что при запаивании ампул с образцами, превращений углеводородов не происходит. Облучение ампулы с образцами проведены на изотопном источнике γ-квантов 60Со. Дозиметрия источника проводились химическими методами – ферросульфатным, гексановым [4]. Поглощенную дозу в исследуемых системах рассчитывали путем сравнения электронных плотностей в исследуемых и дозиметрических системах [4]. При расчете мощности поглощённой дозы облучения, системы гексан–вода учитывали содержанием каждого компонента.
Значения мощностей поглощенной дозы облучения в воде и гексане, определены на основе их электронных плотностей и дозиметрических систем. При мощности поглощенной дозы облучения в дозиметрических системах значения мощностей доз облучения в отдельных компонентах приведено в работе [2].
Ампулы вскрывали в специальной ячейке, откуда продукты радиолиза поступали в колонку хроматографа. Анализ Н2, СО, О2 проведен на хроматографе “Agilent-7890” . Использовали дистиллированную воду, н-гексан, производство “Made in EC”, марки “UN11208” с чистотой 99.0%. Чистоту н-гексана проверяли хроматографическим методом.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
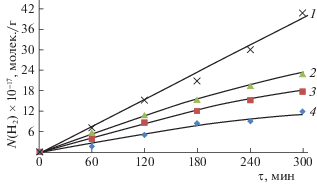
Изучена кинетика накопления Н2 при гетерогенном радиолизе н-С6Н14 и смеси н-С6Н14–Н2О при Т = 300 K. На основе кинетических кривых накопления Н2, приведенных на рис. 1, определены значения скоростей и радиационно-химических выходов молекулярного водорода. Радиационно-химический выход продуктов рассчитан двумя способами. Для сравнения полученных данных с таковыми для гомогенных систем и определения радиационно-каталитической активности n-ZrO2 рассчитаны радиационно-химические выходы G(H2) с учетом энергии, поглощенной каждым из компонентов и всей системой. Сравнение значений Gадс(Н2) = 31.5 молек./100 эВ при гетерогенном радиолизе н-С6Н14 со значением G(Н2) = 5.5 молек./100 эВ при гомогенном радиолизе н-С6Н14 в идентичных условиях свидетельствуют о том, что n-ZrO2 обладает радиационно-каталитической активностью в процессе разложения н-С6Н14.
Рис. 1.
Кинетика накопления молекулярного водорода при гетерогенном радиолизе н-С6Н14 и смеси н‑С6Н14–Н2О при Т = 300 K, D = 0.11 Гр/с: 1 – n-ZrO2 + + н-С6Н14, 2 – 11.5% Н2О + 88.5% С6Н14, 3 – 50% Н2О + + 50% С6Н14, 4 – 88.5% Н2О + 11.5% С6Н14.
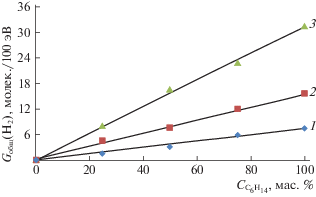
Энергетическая эффективность преобразования энергии ионизирующего излучения в энергию молекулярного водорода, охарактеризована с помощью Gобщ(Н2) и поэтому в дальнейшем обсуждении, использованы значения этой величины. На рис. 2 приведена зависимость Gобщ(Н2) от весового содержания н-С6Н14 в смеси н-С6Н14–Н2О при Т = 300–673 K. Как видно увеличение температуры от 300 до Т = 673 K по-разному влияет на выход молекулярного водорода при гетерогенном радиолизе различных систем. Эффект температуры растет с увеличением содержания н‑С6Н14 в смеси. На основе температурной зависимости радиационно-химического выхода молекулярного водорода определены значения энергий активации для радиационно-каталитического разложения Н2О, н-С6Н14 + Н2О и н-С6Н14, которые равны Е1 = 43.9, Е2 = 4.52 и Е3 = = 4.24 кДж/моль соответственно.
Рис. 2.
Зависимости радиационно-химического выхода молекулярного водорода при радиационно-каталитическом разложении системы н-С6Н14–Н2О в присутствии н-ZrO2 от содержания гексана в смеси при различных температурах, D = 0.12 Гр/с; Т = 300 (1), 473 (2), 673 K (3).
С целью выявления механизма радиационно-каталитического превращения в системах n-ZrO2 + + н-С6Н14 и ZrO2 + н-С6Н14–Н2О изучена кинетика накопления газообразных углеводородов. Значения радиационно-химических выходов углеводородов С1–С4, приведены в табл. 1.
Таблица 1.
Радиационно-химические выходы газообразных углеводородов (молек./100 эВ) при радиационно-каталитическом превращении в системах n-ZrO2 + н-С6Н14 и n-ZrO2 + н-С6Н14–Н2О при Т = 473 K
| Система | молек./100 эВ | $\sum\limits_i {{{G}_{i}}} $ | |||
|---|---|---|---|---|---|
| СН4 | С2Н6 | С3Н8 | суммарный выход С4 | ||
| n-ZrO2 + н-С6Н14–Н2О | 1.3 | 1.0 | 1.1 | 0.58 | 3.98 |
| n-ZrO2 + н-С6Н14 | 1.1 | 1.5 | 3.0 | 0.39 | 5.99 |
Как видно из таблицы, суммарный выход углеводородов С1–С4 при гетерогенном радиолизе н‑С6Н14 и н-С6Н14–Н2О в присутствии ZrO2 при 473 K составляет соответственно 6.0 и 4.0 молек./100 эВ. Наличие воды вызывает уменьшение выхода углеводородных продуктов при гетерогенном радиолизе н-С6Н14. При радиационно-каталитических процессах для переноса энергии от катализатора к веществу, подвергающемуся радиолизу, необходимо наличие сильной адсорбционной связи с поверхностью. На поверхности n-ZrO2 адсорбционная связь полярной молекулы Н2О с поверхностью сильнее, чем у насыщенных углеводородов [2]. Поэтому, при гетерогенном радиолизе в системе n-ZrO2 + н-С6Н14–Н2О, преобладает перенос энергии к молекулам воды. Выход первичных неравновесных носителей зарядов в оксидных диэлектриках определен экспериментально методом ЭПР [9].
Определены энергетические выходы неравновесных носителей (н.н.) зарядов и возбужденных состояний в n-ZrO2, которые равны G(н.н.) = 4.5–4.6 частицы/100 эВ и G(ех) = 2.8–3.0 частицы/100 эВ. Как видно, суммарно начальные выходы частиц, которые участвуют в переносе энергии в системе n-ZrO2 + н-С6Н14–Н2О, равны ΣG(S*) = 7–8 частицы/100 эВ.
Если учесть, что образование промежуточных продуктов гетерогенного радиолиза происходит по процессам, то выход первичных продуктов (п.п.) радиолиза будет составлять G(п.п.) = = 1/2G(н.н.з).
При гетерогенном радиолизе чистой воды обратные рекомбинационные процессы первичных продуктов радиолиза Н + ОН → Н2О преобладают процессами образования Н2 по Н + Н → Н2. Поэтому, выход водорода при Т = 673 K составляет G(Н2) = 1.9–2.1 молекул/100 эВ. При полной трансформации промежуточных атомов водорода, образовавшихся при радиационном-каталитическом разложении Н2О и н-С6Н14, в молекулы Н2, выход водорода достигает G(Н2) = 4.2–4.6 молекул/100 эВ.
Наблюдаемые выходы молекулярного водорода при радиационно-каталитическом разложении смеси н-С6Н14–Н2О при большом содержании С6Н14 превышают эти значения. Это свидетельствует о том, что в углеводородсодержащих смесях происходят вторичные процессы трансформации первичных продуктов радиолиза в молекулярный водород:
(2)
${\text{Н}} + н{\text{ - }}{{{\text{С}}}_{{\text{6}}}}{{{\text{Н}}}_{{{\text{14}}}}} \to {{{\text{Н}}}_{2}} + н{\text{ - }}{{{\text{С}}}_{{\text{6}}}}{{{\text{Н}}}_{{13}}},$(3)
${\text{ОН}} + н{\text{ - }}{{{\text{С}}}_{{\text{6}}}}{{{\text{Н}}}_{{{\text{14}}}}} \to {{{\text{Н}}}_{{\text{2}}}}{\text{О}} + н{\text{ - }}{{{\text{С}}}_{{\text{6}}}}{{{\text{Н}}}_{{13}}}.$Такие значения свидетельствуют о том, что в указанных условиях имеет место цепной режим трансформации первичных продуктов разложения н-С6Н14 и н-С6Н14–Н2О в молекулярный водород.
Список литературы
Пикаев А.К. Современная радиационная химия. Радиолиз газов и жидкостей. M.: Наука, 1986. 440 с.
Гарибов А.А., Агаев Т.Н. // Химия высоких энергий. 2004. Т. 38. № 5. С. 334.
Гарибов А.А., Агаев Т.Н. и др. // Азербайджанский хим. журн. 2004. № 4. С. 35.
Пикаев А.К. Дозиметрия в радиационной химии. M.: Изд-во иностр. лит., 1963. 312 с.
Пшежецкий С.Я. Механизм радиационно-химической реакции. M.: Химия, 1968. 368 с.
Вишнецкая М.В. // Соросовский образовательный журн. 2001. Вып. 7. № 3. С. 33.
Иманова Г.Т. Закономерности радиационно-гетерогенных процессов в наноразмерной системе ZrO2+Н2О / Автореферат, дис. на соис. уч. степ. док. филос. по физике. Баку, 2018. С. 25.
Гарибов А.А., Агаев Т.Н. и др. // Тез. докл. IV Всесоюзного совещания “Воздействие ионизирующего излучения на гетерогенные системы”, Кемерово, 1986. С. 21.
Пшежецкий С.Я. ЭПР свободных радикалов в радиационной химии. M.: Химия, 1972. 480 с.
Gyorgy I., Ishtvan D., Magda R., Laszvlo V. Radiation Chemistry of Hydrocarbons. M.: Science, 1986.
Gyorgy I., Szaner G. // J. Phys. Chem. 1982. Bd. 132. № 2. P. 241–245.
Uanye Y., Geimann T. Hydrocarbons Aspects of radiolysis. M.: Mir. 1971. 264 p.
Svollow A. Radiation chemistry of organic compounds. M.: Foreign Literature, 1963. 408 p.
Foldiak G. Radiation Chemistry of hydrocarbons. Budapest, akad. Kiado, 1981. 476 p.
Дзантиев Б.Г., Ермаков А.Н. // ХВЭ. 1982. № 4. С. 373.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


