Журнал физической химии, 2021, T. 95, № 3, стр. 434-442
Обнаружение и нейтрализация несимметричного диметилгидразина на поверхности конструкционных материалов
К. Е. Полунин a, А. В. Ульянов a, И. А. Полунина a, А. К. Буряк a, *
a Российская академия наук, Институт физической химии и электрохимии им. А.Н. Фрумкина
119071 Москва, Россия
* E-mail: akburyak@mail.ru
Поступила в редакцию 01.08.2020
После доработки 01.08.2020
Принята к публикации 10.08.2020
Аннотация
Методами хроматографии и масс-спектрометрии изучены конструкционные материалы, контактировавшие с несимметричным диметилгидразином, а также десорбционные растворы, полученные при обработке загрязненной поверхности металлов и сплавов водой и реагентами. Исследованы процессы нейтрализации несимметричного диметилгидразина с помощью озона и шунгита. Показано, что озонирование позволяет разрушать молекулы токсикантов, химически и физически адсорбированных на поверхности металлоконструкций, делая возможным их повторное использование и утилизацию. Шунгит эффективно адсорбирует и каталитически разлагает не только несимметричный диметилгидразин и продукты его трансформации, но и олигомерные соединения, образующиеся при хранении гидразинового горючего. Озонирование отработанного шунгита способно повысить эффективность деструктивных процессов и полноту его регенерации.
Загрязнение окружающей среды и конструкционных материалов различными токсичными соединениями происходит в процессе осуществления хозяйственной деятельности человека, при деградации топлив и промышленных продуктов, а также при использовании изначально ядовитых соединений. Например, гидразины, чрезвычайно токсичные для животных и человека, широко используются как ракетное топливо, в сельском хозяйстве, медицине, производстве пластмасс и других областях промышленности [1].
Несимметричный диметилгидразин (НДМГ) обладает высокой летучестью, хорошо адсорбируется на различных поверхностях, в том числе, металлических, смешивается с водой, нефтепродуктами и органическими соединениями, т.е. является мобильным токсикантом, легко мигрирующим по различным объектам окружающей среды [2]. НДМГ и большинство продуктов его трансформации не являются коррозионно-активными веществами для стальных конструкций, однако их разбавленные водные растворы вызывают повышенную коррозию алюминия и его сплавов [3, 4]. Высокая реакционная способность НДМГ приводит к образованию множества токсичных продуктов его окислительной трансформации, многие из которых достаточно стабильны и способны накапливаться в объектах окружающей среды [5–7].
Обнаружение и нейтрализация НДМГ и продуктов его трансформации в воздухе, воде, почве, на поверхностях конструкционных материалов является важнейшей экологической проблемой, которая не может быть решена без разработки чувствительных методов анализа этих соединений, их изолирования или превращения в нетоксичные вещества. Хроматография – высокоэффективный метод анализа, который дает возможность одновременного определения нескольких целевых соединений. Используя масс-спектрометрическую детекцию, можно значительно снизить пределы обнаружения веществ, повысить надежность и информативность анализа. Так как большинство продуктов трансформации НДМГ летучие, для их анализа используют газовую хроматомасс-спектрометрию (ГХ-МС) [7]. Для идентификации нелетучих веществ возможно использование десорбционных вариантов масс-спектрометрии, например, матрично-активированной лазерной десорбции/ионизации (МАЛДИ) или термодесорбционной (ТДМС) [8]. Хроматомасс-спектрометрия при анализе поверхностных загрязнений обычно основывается на предварительной пробоподготовке, получении смывов с поверхности, либо отборе проб для проведения пиролиза.
В настоящее время предложено множество способов нейтрализации НДМГ – термический, каталитический, сорбционный, радиационный и биохимический [9]. На практике нейтрализация техники, стационарных резервуаров, конструкций и хранилищ для топлива часто проводится промыванием их водными или органическими растворами. В результате образуется значительное количество токсичных сточных вод. Их экологическая опасность обусловлена большим объемом, высокой суммарной токсичностью, а также возможностью неконтролируемого распространения. Для нейтрализации НДМГ в сточных водах широко используются адсорбционные методы, которые позволяют концентрировать токсиканты для дальнейшего их уничтожения. С этой целью активно используются угли, торф, алюмосиликаты, сланцы, лигнин. В [7, 10] предложено использовать в качестве сорбента минеральный шунгит. Шунгит имеет богатый минеральный состав, содержит до 90% углерода, примеси каталитически активных металлов и оксидов, обладает высокой механической прочностью и истираемостью [11].
Деструктивные методы удаления НДМГ наиболее эффективны, они приводят к образованию газообразных и низкомолекулярных продуктов реакции. Озон – сильный окислитель и экологически чистый реагент, т.к. продуктом реакции в основном является кислород [12]. Глубокое окисление органических соединений происходит при комнатной температуре и атмосферном давлении. Металлы и их оксиды, катализаторы, УФ- и γ-излучение резко ускоряют озонолиз [13]. Окисление гидразинов озоном в газовой и жидкой среде протекает в 30 раз активнее, чем окисление кислородом, и приводит к преимущественному образованию диметилнитрозамина. Глубокому окислению до СО2, азота и воды при жидкофазном озонолизе подвергается всего 5% НДМГ [14]. Для усиления его деструкции предложен способ гетерофазного озонолиза НДМГ, предварительно сорбированного на Al2O3 [15].
В отличие от других углеродных сорбентов, шунгит способен каталитически разлагать НДМГ [10]. Он плохо поддается окислению озоном и заметных изменений в структуре шунгитового углерода в результате низкотемпературного озонирования не наблюдается [15]. Нестационарный характер колебательной кинетики озонирования шунгита и отсутствие СО2 в продуктах реакции отличает шунгит от большинства углеродных материалов [16]. В результате озонирования возрастает удельная поверхность шунгита, объем и количество микропор, усиливается его адсорбционная активность, растет число кислородсодержащих поверхностных групп [17].
Цель данной работы – физико-химическое исследование процессов нейтрализации НДМГ и продуктов его окислительной трансформации, загрязняющих поверхности конструкционных материалов, с помощью озона и шунгита. Поскольку до настоящего времени не создано методов эффективной нейтрализации объектов, загрязненных НДМГ, которые отвечали бы современным требованиям экологической безопасности, то поиск новых способов обезвреживания НДМГ с использованием доступных и экологически безопасных технологий является актуальной задачей.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали стандартное горючее, содержащее 98% НДМГ (ПО “Салаватнефтеоргсинтез”, ГОСТ Р ИСО 15859-7-2010). В качестве реальных образцов конструкционных материалов, находившихся в контакте с НДМГ, использовали резервуары ракет-носителей и фрагменты топливных баков, в которых длительное время хранилось гидразиновое горючее, а также алюминиево-магниевый сплав АМг6 (ГОСТ 4784-2019), содержащий до 93.7% Al, и образцы конструкционных материалов, закрепленных в планшетах на обшивке международной космической станции.
Был исследован порошок минерального шунгита-III Зажогинского месторождения (НПК “Карбон-Шунгит”, ТУ 5714-007-12862296-2016) с удельной поверхностью Sуд = 2 м2 г–1 и объемом пор 0.046 см3 г–1.
В качестве реагентов, удаляющих с поверхности конструкционных материалов НДМГ и продукты его трансформации, использовали ацетон (JT Baker, Нидерланды), м-нитробензойную кислоту (Вектон, Россия), а также деионизированную воду.
Озонирование 0.05–0.1% водных растворов НДМГ и загрязненных НДМГ стальных конструкций проводили в динамических условиях при 20°C в специально сконструированном устройстве для очистки металлических поверхностей и оборудования [18]. Концентрация озона в озоно-кислородной смеси 60 мг л–1, скорость газового потока 0.5 л ч–1. Обработка стальных поверхностей проводилась в емкости с циркулирующей озонированной водой (концентрации озона 3.4 мг л–1, расход 0.5–0.6 л ч–1).
Анализ состава жидкой фазы проводили методами ГХ-МС и ТДМС с помощью масс-спектрометра JMS-D300 (Jeol, Япония). Термодесорбцию соединений исследовали путем прямого ввода ампулы с образцом и нагревателем в область источника ионов. Скорость нагрева образца 10°С мин–1, ускоряющее напряжение 3 кВ, энергия ионизирующих электронов 70 эВ, диапазон регистрации массовых чисел 40–800 Да. Разделение веществ проводили на кварцевой капиллярной колонке (30 м × 0.5 мм) с жидкой неподвижной фазой DB-5 (J&W Scientific, США) с помощью газового хроматографа НР 5890 (Hewlett-Packard, США). Температура инжектора 280°C, скорость газа-носителя (гелия) 1 мл мин–1.
Для одновременного определения НДМГ и продуктов его трансформации в растворах использовалась методика дериватизации ацетоном [7]. Качественная идентификация веществ осуществлялась с помощью программ библиотечного поиска, опираясь на закономерности протекания реакций трансформации НДМГ, свойств и реакционной способности промежуточных и конечных продуктов реакции [8]. Для количественного анализа использовали подход, основанный на допущении равенства откликов масс-спектрометрического детектора ко всем веществам. Внутренним стандартом служил дейтеронафталин (Sigma-Aldrich, США) с m/z = 136.
Анализ материалов и соскобов с поверхности загрязненных металлов методом МАЛДИ-МС проводили на масс-спектрометре Bruker Daltonics Ultraflex II (Bruker, Германия), оснащенном времяпролетным масс-анализатором с рефлектоном, азотным лазером (λ = 337 нм, максимальная энергия 110 мкДж, частота импульсов 20 и 50 Гц). Использовали 2,5-дигидроксибензойную кислоту (Bruker Daltonics, Германия) в качестве матрицы и мишени из нержавеющей стали. Детектировали положительные ионы в диапазоне m/z 20–800 Да. Сбор и обработку масс-спектров проводили с помощью программного обеспечения FlexControl 3.4 и FlexAnalysis 3.4.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Часть НДМГ, попавшего на поверхность конструкционных материалов, медленно испаряется со скоростью 5% за сутки, а оставшийся НДМГ в результате окислительной трансформации постепенно превращается в диметилметиленгидразин, диметилнитрозамин, диметиламин, триметиламин, тетраметилтетразен, диазометан, формальдегид, закись азота. Под действием солнечного света и тепла НДМГ окисляется до цианистого водорода, аммиака, азота, метана, оксидов углерода и воды [2, 6].
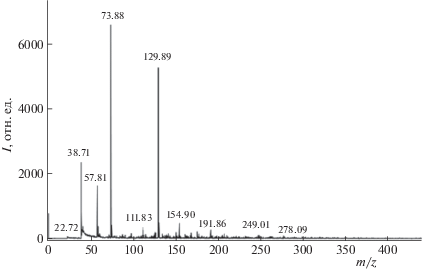
На рис. 1 приведен масс-спектр МАЛДИ водного раствора (смыва), полученного при отмывании топливного резервуара от хранившегося в нем гидразинового горючего.
Рис. 1.
Масс-спектр МАЛДИ соединений, смытых водой со стенок топливного резервуара, в котором хранилось гидразиновое горючее.
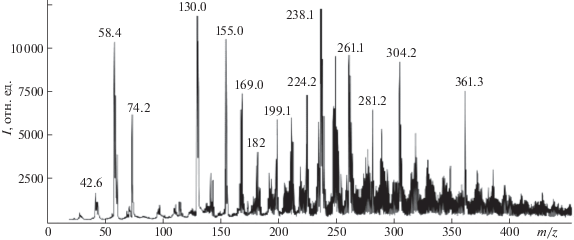
Смыв со стенок топливного резервуара представляет собой сложную смесь соединений. Его масс-спектр содержит сигналы от протонированных молекул НДМГ (m/z = 61), триметиламина (m/z = 60), диметилметиленгидразина (m/z = 73), диметилформамида и диметилтриазена (m/z = = 74), диметил-N-нитрозамина (m/z = 75), 1,1-диметилметилентетразена (m/z = 101), 1,1,4,4-тетраметил-2-тетразена (m/z = 117), N1,N1-диметил-N2-(диметиламино) формамидина (m/z = 116), диметилгидразона диметиламиноацетальдегида (m/z = 130), бис-диметилгидразона этандиаля и пропандиаля (m/z = 143 и 157), бис-диметилгидразин-3,4-диазо-1,3,5-гексатриена (m/z = 197). Другие N-содержащие соединения с молекулярной массой 200–600 Да представляют собой компоненты “черного осмола”, образующегося при длительном хранении гидразинового горючего в результате реакций окисления, присоединения, циклизации, конденсации и олигомеризации НДМГ.
Большое количество продуктов трансформации НДМГ обнаружено в смывах с материалов обшивки международной космической станции (табл. 1), использующей двигатели на гидразиновом горючем. Обработка смывов ацетоном обеспечивает благоприятные условия для разделения и детектирования этих соединений в виде гидразонов [7]. Обнаружено, что качественный состав смывов с материалов, побывавших в космосе, очень похож на состав продуктов окислительной трансформации НДМГ в наземных условиях. Аналогичные результаты позже были получены при анализе обшивки и солнечных батарей космической станции “Мир”. По-видимому, на земле окисляются те компоненты ракетного топлива, которые хемосорбировались и длительное время сохранялись на обшивке и материалах космических станций в условиях глубокого космического вакуума.
Таблица 1.
Качественный и количественный состав соединений, смытых ацетоном с материалов обшивки международной космической станции
| Вещество | τ, мин | m/z | m, мкг |
|---|---|---|---|
| Производное цианата | 1.8 | 56 | 5.43 |
| 1,3,5-Триазин | 2.4 | 81 | 5.80 |
| Диметилгидразон ацетона | 2.9 | 100 | 0.63 |
| Диметилнитрозамин | 3.6 | 74 | 4.23 |
| Диметиламиноацетонитрил | 3.7 | 83 | 25.02 |
| N-Метилформамид | 4.4 | 59 | 2.06 |
| N,N-Диметилформамид | 4.6 | 73 | 2.23 |
| 4,5-Дигидро-5,5-диметил-1Н-пиразол | 5.0 | 83 | 4.52 |
| Производное изоцианата | 5.3 | 56 | 7.06 |
| 3-Амино-N-метил-1Н-1,2,4-триазол | 5.4 | 97 | 0.99 |
| 4-Метилпиримидин | 6.0 | 94 | 1.01 |
| 4,5-Дигидро-1,5-диметил-1Н-пиразол | 6.1 | 98 | 1.53 |
| 1-Метил-1Н-1,2,4-триазол | 6.4 | 83 | 31.45 |
| 4,5-Дигидро-3,5,5-триметил-1Н-пиразол | 6.6 | 97 | 6.92 |
| 2,5-Диметилпиррол | 6.8 | 94 | 0.58 |
| Гуанидин | 7.2 | 59 | 6.83 |
| 2,6-Диметилпиридин | 7.4 | 107 | 0.29 |
| Тетраметиламидразон | 7.5 | 115 | 24.33 |
| N,N-Диэтилацетамид | 7.7 | 58 | 6.98 |
| Оксиметилтриазол | 7.9 | 42 | 24.03 |
| 3,5-Диамино-1Н-1,2,4-триазол | 8.2 | 99 | 3.22 |
| Диметилпиридин | 8.8 | 107 | 1.30 |
| Метилимидазол | 9.1 | 82 | 0.73 |
| Диметилтриазол | 9.4 | 97 | 7.73 |
| Тетраметилмочевина | 12.9 | 44 | 4.86 |
| Аминотриазол | 13.3 | 127 | 0.76 |
| 4-Нитро-1Н-пиразол | 14.9 | 113 | 0.71 |
| Диметилбензамин | 16.3 | 120 | 0.83 |
Содержание этих токсичных веществ в смывах с конструкционных материалов в десятки раз превышает предельно допустимые концентрации, определяемые гигиеническими нормативами [19]. Циановодород, гидразин, метилгидразин, НДМГ и диметилнитрозамин относятся к 1 классу особо опасных соединений, диметиламин и формальдегид – к 2 классу, тетраметилтетразен и диметилформамид – к 3 классу. К тому же в этой смеси обнаружены производные алкилтриазолов, цитотоксичность которых оказалась выше, чем у НДМГ [20]. Загрязнение космических станций гидразиновым горючим и токсичными продуктами трансформации НДМГ – это важная практическая проблема, от решения которой зависит жизнеобеспечение станции и безопасность экипажа.
Методами ГХ-МС и ТДМС возможно проводить анализ не только смывов с поверхностей материалов, но и самих материалов, например, сплава АМг6, контактировавшего с гидразиновым горючим. В масс-спектре электронной ионизации продуктов термодесорбции с поверхности загрязненного материала (рис. 2) присутствуют характеристические ионы как самого НДМГ, так и продуктов его окислительной трансформации [5–7].
Рис. 2.
Масс-спектр продуктов термодесорбции с поверхности сплава АМг6, загрязненного гидразиновым горючим.
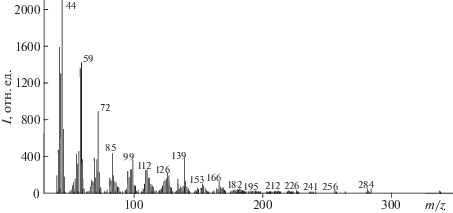
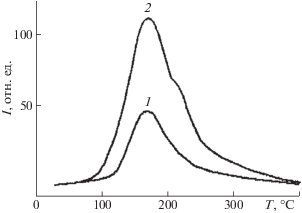
Анализ кинетики выделения продуктов термодесорбции с поверхности АМг6, загрязненного НДМГ, позволил установить, что максимальное количество соединений десорбируется при 150–250°С, т.е. достаточно прочно связано с поверхностью. После высокотемпературной обработки алюминиевого сплава водой и повторного загрязнения материала НДМГ количество десорбированных соединений значительно возрастает (рис. 3). Причем на масс-термограмме одного из основных фрагментных ионов НДМГ с m/z = 58 помимо пика с максимумом при 180°С появляется новый плохо разделенный пик в области 200–220°С (рис. 3б). Это свидетельствует об увеличении адсорбции НДМГ на гидроксилированной поверхности АМг6 и образовании более прочных поверхностных соединений. Таким образом, высокотемпературная обработка поверхности конструкционных материалов, загрязненных НДМГ, водой и водяным паром увеличивает адсорбцию и хемосорбцию НДМГ при последующем использовании таких материалов, сделанных на основе сплавов алюминия, и снижает вероятность их успешной регенерации.
Рис. 3.
Масс-термограмма (по иону с m/z 58) соединений, десорбированных с поверхности исходного (1) и гидроксилированного (2) образцов АМг6, загрязненных НДМГ.
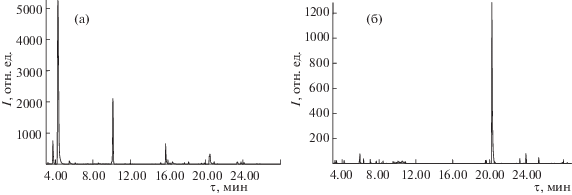
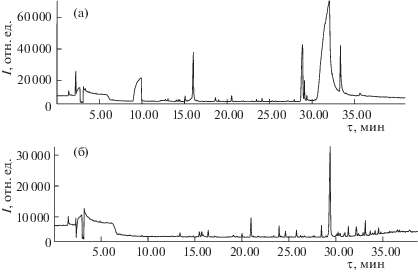
При исследовании материалов из нержавеющей стали, контактировавших с гидразиновым горючим, обнаружено, что до 150°С десорбируются физически адсорбированные молекулы токсикантов, а после 180°С и до 250°С – их химически адсорбированные молекулы. На хроматограмме водного смыва с поверхности загрязненной стали (рис. 4а) в диапазоне 3–20 мин появляются пики НДМГ, продуктов его трансформации, а также небольшого количества углеводородов. Обработка озоном этого раствора в течение 5 ч приводит к уменьшению концентрации НДМГ с 0.05 мас. % до 0. Как показал анализ озонированных растворов, одновременно в течение 3 ч нарастает концентрация диметилнитрозамина и других продуктов трансформации НДМГ. Их концентрации снижаются до безопасного уровня только после 7 ч озонирования водных растворов. В итоге в растворе остаются лишь незначительные примеси углеводородов из воды (рис. 4б).
Рис. 4.
Хроматограммы водного смыва с поверхности нержавеющей стали, загрязненной НДМГ, до (а) и после (б) 7 ч озонирования раствора (пик стандарта при 21 мин).
Но водой можно смыть только слабо связанные с поверхностью стали молекулы токсикантов. Другая их часть, более прочно связанная с поверхностью и проникшая вглубь металла, способна десорбироваться со временем при изменении температуры, давления и других внешних условий, создавая опасный “эффект натекания” НДМГ уже после нейтрализации его основного количества. Поэтому была проведена дополнительная обработка стальных конструкций в течение 3 ч циркулирующей озонированной водой (концентрация озона в воде 3.4 мг л–1, расход 0.5–1 л ч–1) в специально сконструированном устройстве [18]. Анализ состава газов, контактировавших с металлоконструкциями, спустя 3 ч и 10 суток после озонирования показал полное отсутствие “эффекта натекания” НДМГ, т.е. за 10 ч озонирования окислились как физически, так и химически адсорбированные на металле молекулы токсикантов. Отсутствие хемосорбированных молекул НДМГ на поверхности стали подтверждено также при исследовании продуктов термодесорбции методом ТДМС. Предложенный способ нейтрализации НДМГ озонированной водой эффективен при обработке крупногабаритных металлоконструкций, резервуаров-хранилищ, топливных баков ракет-носителей и транспортных и заправочных систем, когда другие способы нейтрализации НДМГ невозможны или опасны. Озонирование загрязненных НДМГ металлоконструкций делает возможным их повторное использование или безопасную утилизацию.
Отмывание металлических конструкций, загрязненных НДМГ, водными или органическими растворами часто приводит к появлению в смывах ингибиторов коррозии, которыми предварительно обрабатывали изделия. В качестве ингибиторов коррозии широко используются соли м-нитробензойной кислоты (МНБК) [4], они также входят в состав моющих растворов. Присутствие в смывах с загрязненных металлов до 5% этих реагентов [4] может негативно сказаться на результатах нейтрализации НДМГ, а также привести к загрязнению сточных вод. Исследование смывов, не содержащих и содержащих 0.5% МНБК (рис. 5), показало, что в обоих случаях НДМГ, продукты его трансформации, а также МНБК разлагаются до безопасного уровня после 10 ч обработки растворов озоном. Концентрация веществ в нейтрализуемом растворе через 10 ч озонирования не превышала их ПДК для воды хозяйственно-бытового назначения [19].
Рис. 5.
Хроматограммы водного смыва со стенки резервуара, загрязненного НДМГ и содержащего 0.5% МНБК, спустя 3 и 10 ч озонирования (а и б, соответственно).
Состав продуктов, оставшихся в смыве, содержащем НДМГ и МНБК, после 3 и 10 ч его обработки озоном приведен в табл. 2.
Таблица 2.
Концентрация веществ в водном смыве со стенки резервуара, загрязненного НДМГ и содержащего 0.5% МНБК, спустя 3 и 10 ч озонирования (концентрация НДМГ в смыве до озонирования – 500 мг л–1)
| Вещество | τ, мин | С, мг л–1 | |
|---|---|---|---|
| 3 ч | 10 ч | ||
| Нитрометан | 3.4 | 0.008 | – |
| Диметилнитрозамин | 9.9 | 1.7 | 0.0045 |
| Динитробензол | 28.8 | 0.51 | 0.2 |
| Метиловый эфир МНБК | 29.1 | 0.062 | 0.0006 |
| МНБК | 32.0 | 3.6 | 0.004 |
| Тринитробензойная кислота | 32.1 | 0.005 | 0.008 |
Озонирование НДМГ, адсорбированного на Al2O3, по данным [13, 14], существенно повышает эффективность деструкции этого токсиканта. Нами был исследован шунгит в качестве сорбента для НДМГ. Установлено, что шунгит хорошо сорбирует НДМГ из водных растворов и через 1 ч сорбционного контакта шунгита с 10% раствором НДМГ из масс-спектра раствора (рис. 6) исчезают сигналы токсичных НДМГ (m/z = 61), диметилнитрозамина (m/z 75) и тетраметилтетразена (m/z = 117), немного увеличивается интенсивность пика стабильного диметилформамида (m/z = 74) относительно диметилгидразона диметиламиноацетальдегида (m/z = 130), значительно уменьшаются или исчезают пики соединений с m/z > 200.
Рис. 6.
Масс-спектр МАЛДИ 10% водного смыва со стенок топливного резервуара, в котором хранилось гидразиновое горючее, после его контакта с шунгитом.
Для полной нейтрализация НДМГ и продуктов его трансформации в 10% растворе потребовалось 24 ч, а в 90% растворе (гидразиновое горючее) с помощью того же количества шунгита нейтрализация длилась 4 дня. Анализ смывов с образцов шунгита, сорбировавших НДМГ из растворов, показал отсутствие токсичных соединений. Они не обнаружены также в составе продуктов термодесорбции с их поверхности.
Нанесение шунгита на поверхность нержавеющей стали с адсорбированным НДМГ также эффективно приводит к разрушению молекул НДМГ и продуктов его трансформации (рис. 7).
Рис. 7.
МАЛДИ масс-спектры образцов из нержавеющей стали с адсорбированным НДМГ до (а) и после (б) нанесения шунгита.
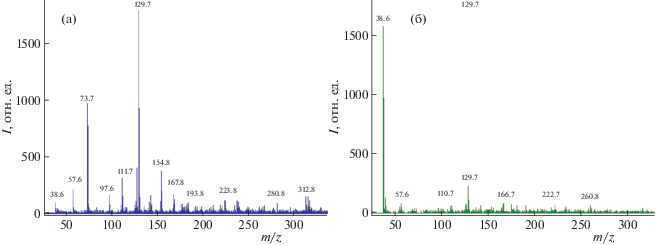
Проведенный для сравнения анализ смыва с поверхности Al2O3, контактировавшего с тем же раствором НДМГ, обнаружил присутствие в смыве как самого НДМГ, так и продуктов его трансформации (диметилнитрозамина, тетразена, токсичных триазолов, тетраметиламидразона и бис(диметилгидразон)этандиаля. Таким образом, в отличие от Al2O3, шунгит не только адсорбировал НДМГ и другие токсиканты из раствора, но и каталитически разложил их до низкомолекулярных продуктов [11]. Сравнение эффективности нейтрализации НДМГ в 10 и 90% растворах НДМГ показало, что при высокой токсической нагрузке для нейтрализации НДМГ потребуется увеличение количества шунгита или его дополнительная активация. Усилить адсорбционные и каталитические свойства шунгита позволяет его механохимическое и термоокислительное модифицирование, а также допирование солями переходных металлов [11, 21]. Низкотемпературное озонирование шунгита, как установлено в [15, 16], приводит к увеличению его удельной поверхности, объема пор, появлению микропор и росту поверхностных кислородсодержащих соединений, в результате увеличивается адсорбционная и каталитическая активность этого минерала [17]. С другой стороны, озонирование уже загрязненного НДМГ шунгита позволит ускорить окисление токсичных соединений и провести регенерацию сорбента без ущерба для экологии. Такой сорбент будет безопасен для повторного использования.
Таким образом, методами хроматографии и масс-спектрометрии изучены конструкционные материалы, контактировавшие с НДМГ, а также десорбционные растворы, полученные при обработке загрязненной поверхности металлов и сплавов растворами реагентов и водой. Показано, что технология нейтрализации НДМГ путем высокотемпературной обработки металлоконструкций из алюминиево-магниевого сплава водой или водяным паром увеличивает последующую адсорбцию и хемосорбцию на их поверхности НДМГ, что затруднит дальнейшее использование материалов и их утилизацию. Исследованы процессы нейтрализации НДМГ с помощью озона и шунгита. Показано, что в результате 7–10 ч обработки озонированной водой уровень токсичных загрязнений стальной поверхности снижается до безопасных значений. Одновременно от токсичных и химически активных реагентов очищаются сточные воды. Озонирование разрушает молекулы НДМГ, химически и физически адсорбированного на поверхности металлоконструкций, делая возможным их повторное использование и утилизацию. Использование шунгита позволяет эффективно сорбировать и каталитически разлагать не только НДМГ и продукты его трансформации, но и олигомерные соединения, образующиеся при хранении гидразинового горючего. Озонирование отработанного шунгита способно повысить эффективность деструктивных процессов и полноту его регенерации.
Работа выполнена в рамках Государственного задания ИФХЭ РАН и при частичной финансовой поддержке РФФИ (проект № 18-08-01224). Использовано оборудование Центра коллективного пользования ИФХЭ РАН.
Авторы заявляют об отсутствии конфликта интересов в данной статье.
Список литературы
Schmidt W.E. Hydrazine and its derivatives. 2nd Ed. New York: John Wiley & Sons Inc., 2001.
Экологический мониторинг ракетно-космической деятельности. Принципы и методы / Под ред. Н.С. Касимова и О.А. Шпигуна. М.: Рестарт, 2011.
Пыцкий И.С., Кузнецова Е.С., Ярцев С.Д., Буряк А.К. // Коллоидн. журн. 2017. Т. 79. № 4. С. 479.
Буряк, А.К., Сердюк Т.М., Ульянов А.В. // Коррозия: материалы, защита. 2008. № 4. С. 33.
Smolenkov A.D., Shpigun O.K. // Talanta. 2012. V. 102. P. 93.
Колесников С.В. Окисление несимметричного диметилгидразина (гептила) и идентификация продуктов его превращения при проливах. Новосибирск: Изд. СибАК, 2014.
Буряк А.К., Сердюк Т.М. // Успехи химии. 2013. Т. 82. С. 369. [Buryak A.K., Serdyuk T.M. // Russ. Chem. Rev. 2013. V. 82. № 4. P. 369].
Лебедев А.Т. Масс-спектрометрия в органической химии. М.: БИНОМ, 2003.
Методы и средства обеспечения химической безопасности / Под ред. А.В. Рощина. М.: Буки Веди, 2016.
Ульянов А.В., Полунина И.А., Полунин К.Е., Буряк А.К. // Коллоидн. журн. 2018. Т. 80. С. 102. [Ul`yanov A.V., Polunina I.A., Polunin K.E., Buryak A.K. // Colloid J. 2018. V. 80. P. 96.
Березкин В.И. Углерод. Замкнутые наночастицы, макроструктуры, материалы. СПб.: АтрЭрго, 2013. С. 280.
Лунин В.В., Попович М.П., Ткаченко С.Н. Физическая химия озона. М.: Изд-во МГУ, 1998.
Лунин В.В., Карягин Н.В., Ткаченко С.Н., Самойлович В.Г. Применение и получение озона. М.: Изд-во МГУ, 2006.
Горленко Л.Е., Емельянова Г.И., Стрельникова Ж.В., Страхов Б.В. // Журн. физ. химии. 1985. Т. 59. № 12. С. 2957.
Емельянова Г.И., Горленко Л.Е., Рожкова Н.Н. и др. // Там же. 2010. Т. 84. № 8. С. 1513.
Rozhkova N.N., Emel`yanova G.I., Gorlenko L.E. et al. // Smart Nanocomposites. 2010. V. 1. P. 71.
Горленко Л.Е., Емельянова Г.И., Тихонов Н.А. и др.// Журн. физ. химии. 2005. Т. 79. № 8. С. 1400.
Пат. РФ 2209853 (опубл. 2003). Способ очистки металлических поверхностей оборудования и устройство для его осуществления.
Справочник по токсикологии и гигиеническим нормативам (ПДК) потенциально опасных химических веществ / Под ред. В.С. Кушневой и Р.Б. Горшковой. М.: ИздАт., 1999.
Milyushkin A.L., Birin K.P., Matyushin D.D. et al. // Chemosphere. 2019. V. 217. P. 95.
Полунина И.А., Высоцкий В.В., Сенчихин И.Н. и др. // Коллоидн. журн. 2017. Т. 79. С. 192. [Polunina I.A., Visotskii V.V., Senchikhin I.N. et al. // Colloid J. 2017. V. 79. P. 244].
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


