Журнал физической химии, 2021, T. 95, № 6, стр. 894-897
Стабильность полимерных солей офлоксацина и ципрофлоксацина в водных растворах
М. С. Борисенко a, *, М. В. Соловский a
a Российская академия наук, Институт высокомолекулярных соединений
199004 Санкт-Петербург, Россия
* E-mail: aarghm@hq.macro.ru
Поступила в редакцию 09.07.2020
После доработки 30.09.2020
Принята к публикации 30.09.2020
Аннотация
Нейтрализацией аминогрупп сополимера N-винилпирролидона с 2-аминоэтилметакрилатом офлоксацином или ципрофлоксацином получены достаточно стабильные полимерные соли, проявляющие высокую противотуберкулезную активность и характеризующиеся постепенным выделением туберкулостатика из его полимерной формы в модельной среде. Методом электропроводности определены константы диссоциации полученных полимерных солей, равные (5.2 ± 0.8) × 10–3 моль/л для полимерной соли офлоксацина и (6.2 ± 0.5) × 10–3 моль/л для полимерной соли ципрофлоксацина.
Противотуберкулезные препараты из группы фторхинолонов офлоксацин (I) и ципрофлоксацин (II) – известные эффективные средства современной терапии туберкулеза [1]:
Одна из приоритетных задач борьбы с туберкулезом – разработка методов повышения эффективности действия существующих туберкулостатиков, в частности фторхинолонов, за счет их модификации. Разработка способов модификации ведется в разных направлениях, среди которых важнейшее место занимает модификация лекарственных веществ путем связывания их с полимером-носителем, позволяющим обеспечить постепенное пролонгированное выделение лекарственного вещества в организм.
Распространенным способом модификации лекарственных веществ полимером служит их солеобразование с синтетическими водорастворимыми биосовместимыми полиэлектролитами [2, 3]. В настоящей работе этот прием реализован для офлоксацина и ципрофлоксацина. В качестве полимера-носителя фторхинолонов синтезирован нетоксичный катионный сополимер N-винилпирролидона с 2-аминоэтилметакрилатом (III), содержащий 5.8 мол. % реакционноспособных первичных аминогрупп, с молекулярной массой 48 000 и характеристической вязкостью [η] = 0.3 дл/г:
Эффект пролонгирования противотуберкулезной активности фторхинолонов в составе полимерных солей на основе сополимера III будет определяться стабильностью полимерных солей в водных растворах.
Настоящая работа посвящена исследованию стабильности полимерных солей офлоксацина и ципрофлоксацина на основе сополимера III в водных растворах путем определения их констант диссоциации.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез низкомолекулярных сополимеров N-винилпирролидона 2-аминоэтилметакрилатом описан в [4]. Состав сополимера III устанавливали путем потенциометрического титрования первичных аминогрупп сополимера 0.1н. раствором HCl на pH-метре HJ 1210. Средневязкостную молекулярную массу этого сополимера Mη определяли вискозиметрическим методом, используя уравнение Марка–Куна–Хаувинка [η] = 5 × 10–4$M_{\eta }^{{0.56}}$, известное для поли-N-винилпирролидона [5]. Характеристическую вязкость [η] измеряли в вискозиметре Уббелоде в 0.1 н. растворе ацетата натрия в воде при 25°С.
Получение полимерной соли офлоксацина: 2 г сополимера III растворяли в 20 мл воды и добавляли при перемешивании раствор 0.374 г офлоксацина в 5 мл воды; полученный раствор перемешивали 30 мин и подвергали лиофильной сушке. Получено 2.24 г (94.4%) полимерной соли, содержащей по данным спектрофотометрии 15.8 мас. % офлоксацина.
Полимерную соль ципрофлоксацина получали аналогичным образом. Содержание фторхинолона в ней составило 16.2 мас. %.
Скорость высвобождения туберкулостатика из его полимерной соли оценивали методом диализа через полупроницаемую мембрану Spectra/Por с MWCO 500. В левую ячейку установки для диализа вносили раствор полимерной соли офлоксацина определенной концентрации в буфере с pH 2.0, в правую ячейку вносили буферный раствор. Установку помещали в термостат с температурой 37°С и отмечали время начала реакции. Затем через определенные промежутки времени отбирали пробы из правой ячейки и определяли в них методом УФ-спектроскопии содержание офлоксацина, прошедшего через мембрану.
Диссоциацию полимерных солей офлоксацина и ципрофлоксацина в водных растворах исследовали путем измерения их электропроводности по методу [6]. Удельную электропроводность κ рассчитывали из результатов измерения сопротивления (R) раствора в кондуктометрической ячейке с прямоугольными платиновыми электродами площадью (S) 0.00054 м2 и расстоянием между ними (l) 0.001 м по формуле κ = l/2SR (Ом–1 см–1).
Противотуберкулезную активность фторхинолонов и их полимерных солей определяли методом двукратных серийных разведений, описанным в монографии [7].
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Солеобразование фторхинолонов с сополимером-носителем проводили в водном растворе при соотношении 1 моль аминогрупп сополимера на 1 моль туберкулостатика. Полученные полимерные соли офлоксацина или ципрофлоксацина могут быть представлены соответственно формулами IV и V:
В сополимере-носителе III реакционноспособные –NH2-группы отделены от основной цепи полимера мостиковой развязкой –CO–O–CH2–CH2–, что может облегчить ионное взаимодействие носителя с фторхинолоном.
Найденные значения удельной электропроводности κ позволили рассчитать значения эквивалентной электропроводности: λ = κ × 1000/cb (см2/(Ом г-экв)), где b – количество солевых связей в мол. %. По зависимости значений λ от концентрации полимерных солей линейной аппроксимацией методом наименьших квадратов были определены величины эквивалентной электропроводности растворов солей λ0 при бесконечном разбавлении при с → 0 (рис. 1 и 2). По значениям λ и соответствующим им значениям λ0 были рассчитаны степени диссоциации полимерных солей α = λ/λ0 при различных концентрациях. Это позволило вычислить константы диссоциации, соответствующие различным концентрациям полимерной соли по формуле: KD = α2c/(1 – α). Средние значения KD для полимерных солей IV и V приведены в табл. 1. Как видно из этой таблицы, для полимерной соли офлоксацина KD = = (5.2 ± 0.8) × 10–3 моль/л. Для полимерной соли ципрофлоксацина, близкого по химическому строению к офлоксацину, найдено близкое значение KD = (6.2 ± 0.5) × 10–3 моль/л. Невысокие значения KD свидетельствуют о достаточной стабильности полученных полимерных солей в водных растворах, обусловленной тем, что ионное взаимодействие между полимером-носителем и туберкулостатиком стабилизировано гидрофобными взаимодействиями между молекулами фторхинолонов на макромолекулах сополимера III.
Рис. 1.
Зависимость эквивалентной электропроводности λ полимерной соли офлоксацина на основе сополимера III от ее концентрации в водном растворе.

Рис. 2.
Зависимость эквивалентной электропроводности λ полимерной соли ципрофлоксацина на основе сополимера III от ее концентрации в водном растворе.
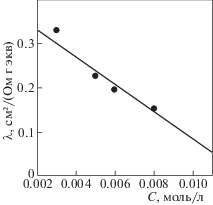
Таблица 1.
Свойства полимерных солей фторхинолонов
| Cоль | Фторхинолон | с, мас. % | KD × 103, моль/л | МПК, мкг/мл |
|---|---|---|---|---|
| IV | Офлоксацин | 15.8 | 5.2 ± 0.8 | 6.2 |
| V | Ципрофлоксацин | 16.2 | 6.2 ± 0.5 | 6.2 |
Достаточную стабильность полученных полимерных солей подтвердили опыты по изучению кинетики выделения офлоксацина из полимерной соли IV в модельной среде методом диализа через полупроницаемую мембрану. Поскольку для лечения туберкулеза офлоксацин применяется, в основном, перорально, в качестве модельной среды был выбран гликоколовый буфер с pH 2.0 (pH желудка). Температура опыта 37°С. Исходная концентрация офлоксацина (Cофл) в полимерной соли IV составляла 84.6 мкг/мл. Полученные результаты (табл. 2) свидетельствуют о постепенном высвобождении офлоксацина из полимерной соли в данных условиях: на 25.5% за 2 ч, на 31.5% за 8 ч, на 35.3% за 24 ч, на 57.0% за 50 ч. Такой характер выделения фторхинолона из полимерной соли IV может обеспечить пролонгирование противотуберкулезной активности офлоксацина.
Таблица 2.
Кинетика выделения офлоксацина из полимерной соли IV
| τ, ч | $C_{{{\text{офл}}}}^{'}$, мкг/мл | α, % |
|---|---|---|
| 1 | 3.7 | 4.4 |
| 2 | 21.6 | 25.5 |
| 4 | 22.2 | 26.3 |
| 8 | 26.6 | 31.5 |
| 24 | 29.8 | 35.3 |
| 50 | 48.2 | 57.0 |
В микробиологических исследованиях было установлено, как видно из табл. 1, что полимерные соли IV и V в низких концентрациях (МПК = = 6.2 мкг/мл) подавляют рост микобактерий туберкулеза. По своей противотуберкулезной активности они сопоставимы с немодифицированными полимерами фторхинолонами, для которых найдено значение МПК, равное 3.1 мкг/мл.
Таким образом, в результате проведенных исследований получены достаточно стабильные туберкулостатически активные полимерные соли офлоксацина и ципрофлоксацина с возможной пролонгированной противотуберкулезной активностью.
Работа выполнена при поддержке грантом РНФ № 18-13-0324.
Список литературы
Машковский М.Д. Лекарственные средства. М.: Новая волна, 2005. 1206 с.
Афиногенов Г.Е., Панарин Е.Ф. Антимикробные полимеры. СПб.: Гиппократ, 1993. 264 с.
Solovskiy M.V., Tarabukina E.B., Amirova A.I. et al. // J. Phys. Chem. 2014. V. 88. № 3. P. 428.
Ананьева Е.П., Баранов С.С., Караваева А.В. и др. // Антибиотики и химиотерапия. 2014. Т. 59. № 11–12. С. 3.
Павлов Г.М., Панарин Е.Ф., Корнеева Е.В. и др. // Высокомолекулярные соединения. 1990. Т. 32 (А). № 6. С. 1190.
Театсакис А.М., Штильман М.И., Алегакис Ф. и др. // Высокомолекулярные соединения. 1996. Т. 38 (Б). № 8. С. 1431.
Навашин С.М., Фомина И.П. Рациональная антибиотикотерапия. М.: Медицина, 1982. 495 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии





