Журнал физической химии, 2021, T. 95, № 8, стр. 1262-1268
Условия формирования и свойства адсорбента, полученного на основе модифицированного полиимидом оксида алюминия
Е. Ю. Яковлева a, b, *, Е. Е. Барановская a, b
a Российская академия наук, Сибирское отделение, Институт катализа им. Г.К. Борескова
Новосибирск, Россия
b Новосибирский государственный университет
630090 Новосибирск, Россия
* E-mail: yakovl@catalysis.ru
Поступила в редакцию 11.09.2020
После доработки 11.09.2020
Принята к публикации 30.10.2020
Аннотация
Методами низкотемпературной адсорбции азота, просвечивающей электронной микроскопии высокого разрешения и газовой хроматографии изучено изменение текстурных и хроматографических характеристик разделительных слоев, полученных на основе оксида алюминия, модифицированного полиимидом. В процессе термотренировки от 250 до 450°С в токе инертного газа удельная поверхность адсорбента γ-Al2O3 + 10 мас. % полиимида уменьшилась от 228.9 до 190.4 м2/г при незначительном увеличении размера пор от 83.6 до 86.5 Å. Равномерное расположение углерода на поверхностных слоях и приближенная к гауссовой форма пиков разделяемых компонентов свидетельствует о формировании однородной поверхности адсорбента, которую удалось достичь после удаления активных центров натрия, железа, титана в исходном γ-Al2O3, модификации его поверхности полиимидом и термотренировки при температуре 450°С. Моноксид и диоксид углерода селективно элюируют от сопутствующих постоянных газов и углеводородов.
Многочисленные исследования, проводимые в последние годы, направлены на разработку неорганических газоразделительных мембран, которые получают на основе органических прекурсоров и доступных неорганических материалов. В качестве неорганических подложек используют оксиды алюминия и кремния, а органическими прекурсорами служат фенольные и спиртовые смолы, поливинилиденхлорид, конденсированные полициклические ароматические соединения и полиимиды. Неорганическую подложку пропитывают прекурсором, затем проводят термообработку в инертной атмосфере при заданных температурах и получают материалы с определенными свойствами.
Особый интерес в качестве прекурсоров вызывают ароматические полиимиды, синтезированные на основе мономеров, содержащих в своей структуре объемные СН3-и СF3-группы. Известно, что полиимиды с такой структурой имеют более низкую упаковку цепей и, как следствие, более высокий коэффициент пропускания и свободный объем в полимере. Кроме того, ароматические полиимиды при термообработке при высоких температурах формируют карбонизированные прочные пленки. Материалы, полученные на основе полиимидов и неорганических адсорбентов (оксидов алюминия или кремния), характеризуются пористой структурой, термической стабильностью, химической инертностью и поэтому пригодны для использования в качестве электродов, мембран, носителей катализаторов, а так же перспективны для разработки новых хроматографических адсорбентов [1–3].
Условия термотренировки оказывают большое влияние на селективность и проницаемость полиимидных мембран. Например, при температуре 700°С получают носители близкие по структуре к углеродным молекулярным ситам.
Углеродные молекулярные сита интенсивно используют в газовой хроматографии для анализа постоянных газов (азот, кислород, водород, монооксид углерода, метан), легких углеводородов. Однако на сегодняшний день этот тип адсорбентов является дорогостоящим. Поэтому возникла необходимость создания материалов с подобными свойствами на основе доступного оксида алюминия.
В газовой, тонкослойной хроматографии в качестве адсорбента давно применяют γ-форму оксида алюминия. Исходный γ-Al2O3 гигроскопичен и его активность зависит от содержания воды, а также активных центров натрия, железа, титана на его поверхности. С целью уменьшения влияния гидроксильных групп и атомов металлов на разделительную способность рекомендуется проводить предварительную термическую обработку γ-Al2O3 либо его модифицировать органической жидкой фазой или неорганическими солями [4, 5].
В ранее опубликованных наших работах были исследованы адсорбционные, хроматографические свойства разделительных слоев, полученных на основе неорганических адсорбентов (диатомитового носителя, оксида алюминия) и высокофторированного полиимида, синтезированного через стадию получения полиамидокислоты (ПАК). В зависимости от температуры термотренировки (250, 450, 700°С) были сформированы поверхности адсорбентов, которые проявляют свойства неполярных неподвижных фаз, пористых полимеров и молекулярных сит при анализе смеси постоянных газов, легких углеводородов [6–10]. Удовлетворительное разделение компонентов вышеуказанной смеси наблюдали на модифицированном полиамидокислотой диатомитовом носителе после его тренировки в токе инертного газа при температуре 700°С, однако степень разрешения пиков ацетилена и этилена значительно меньше единицы [8–10]. Диоксид углерода элюируется широким затянутым пиком с поверхности другого носителя – оксида алюминия, модифицированного ПАК и термотренированного при температуре 450°С [7]. Эти недостатки, вероятно, связаны с частичной деформацией или разрушением полимерной пленки, образованной в процессе имидизации полиамидокислоты на поверхности адсорбента и его прогрева, и, как следствие этого, формированием недостаточно однородной поверхности. Полиамидокислота имеет более высокую адгезию к полярным поверхностям благодаря наличию кислотных групп. Однако растворы ПАК подвергаются гидролизу при стоянии и при нанесении на поверхность неорганических материалов, что приводит к уменьшению молекулярного веса полимера и значительной усадке полимерной пленки при последующей имидизации.
Чтобы исключить гидролиз ПАК и получить однородную поверхность адсорбента, в данной работе γ-Al2O3 пропитывали раствором высокомолекулярного полиимида, синтез которого описан в работе [11] и структура которого аналогична полимеру, получаемому через стадию имидизации полиамидокислоты. Кроме того, в исходном γ-Al2O3 предварительно были удалены активные центры натрия, железа, титана.
Целью данной работы является исследование адсорбционных и хроматографических характеристик адсорбентов γ-Al2O3/полиимид, полученных после термотренировки при различных температурах.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Использованные реактивы
2,4,6-триметил-м-фенилендиамин (2,4,6-TMmPDA) (99%, Aldrich-Supelco) использовали без дополнительной очистки, 2,2-бис-(3,4-ангидродикарбокси-фенил) гексафторпропан диангидрид (6FDA) (99%, Aldrich-Supelco) перед использованием сушили в вакууме при 140°C в течение 6 ч.
В качестве растворителей применяли диметилацетамид (ДМА), “х.ч.” (99.8%, Экос-1), который предварительно очищали перегонкой над P2O5 и хранили над молекулярными ситами 5А, остаточная влага <0.02%.
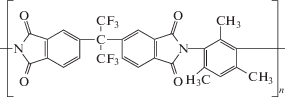
Синтез полиимида ПИ-1Б (рис. 1) на основе 2,4,6-триметил-м-фенилендиамина и диангидрида 2,2-бис(3',4'-дикарбоксифенил)гексафторпропана проводили в расплаве бензойной кислоты по методике, описанной в работе [11].
В качестве неорганического адсорбента использовали оксид алюминия (γ-Al2O3) (“х.ч.”) компании (Sasol Limited, ЮАР) (product No: 608 114, Si – 0.015%, Fe – 0.015%, Ti – 0.015%, Na – 0.01%, Sуд = 200–220м2/г), фракция 0.25 – 0.10 мм.
Подготовка адсорбента и приготовление насадочных колонок
Для удаления ионов кальция, натрия, железа, титана измельченный адсорбент заливали концентрированной соляной кислотой, оставляли на 20 минут. Затем адсорбент промывали дистиллированной водой до отсутствия ионов хлора, сушили при 90–100°С. После этого γ-Al2O3 кондиционировали в токе гелия при 230–240°С и пропитывали полиимидом предварительно растворенным в диметилацетамиде (ДМА).
ПИ-1Б растворяли в ДМА в количестве 10% от массы адсорбента, затем добавляли γ-Al2O3 и оставляли на 8 ч. Далее суспензию переносили в фарфоровую чашку и сушили до постоянного веса при температуре 90–100°С при постоянном перемешивании. Приготовленным адсорбентом заполняли насадочные колонки.
В табл. 1 представлены типы насадочных колонок, которые были приготовлены на основе адсорбентов и термотренированы в токе инертного газа при определенных температурах в течение 10 ч, каждая индивидуально.
Таблица 1.
Типы насадочных колонок размером 3 м × × 2 мм, заполненные γ-Al2O3 + 10 мас. % ПИ-1Б
| Колон-ки | Исходный γ-Al2O3 Ттр = 90–100°С |
γ-Al2O3 + 10 мас. % ПИ-1Б Ттр, °С |
|---|---|---|
| 1 | $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{без}}\;{\text{обработки}}\;{\text{HCl}}}}}$ | 250 |
| 2 | 450 | |
| 3 | $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ | 250 |
| 4 | 350 | |
| 5 | 450 |
Адсорбционные исследования проводили по изотермам адсорбции–десорбции N2 при 77 К, которые измеряли на установке ASAP-2400 фирмы Micromeritics (США) после тренировки образцов в вакууме при 150°С. Эти изотермы использовали для расчета суммарной поверхности методом Брунауэра–Эммета–Теллера, суммарный объем пор при давлении p/p0 ~ 0.982–0.983; объем микропор рассчитывали по сравнительному t-методу по де Буру; средний диаметр пор по формуле dпор(БЭТ) = 4000 × Vсумм/АБЭТ.
Исследование структуры и микроструктуры образцов осуществляли методом просвечивающей электронной микроскопии высокого разрешения (ПЭМВР) на электронном микроскопе JEM 2010 (JEOL, Japan) c ускоряющим напряжением 200 кВ и предельным разрешением по решетке 0.14 нм. Запись изображений осуществлялась с помощью ПЗС матрицы Soft Imaging System (Germany). Прибор оснащен энергодисперсионным спектрометром рентгеновского характеристического излучения (EDX) XFlash (Bruker, Germany) с полупроводниковым Si-детектором с разрешением по энергии 130 эВ.
Измерения хроматографических параметров проводили на хроматографе Кристалл 2000 с детектором по теплопроводности (ДТП). Газ-носитель (гелий) – 30 см3/мин. Температуру термостата колонок поддерживали с точностью ±0.5°С. Для обработки хроматографических данных использовали программное обеспечение “NetChrom”.
Для выполнения эксперимента готовили модельные смеси с определенной концентрацией на основе аргона в металлических баллонах емк. 10 л объемно-манометрическим методом. В баллоне 1 была приготовлена смесь из постоянных (Н2, О2, N2, СО, СО2) и углеводородных газов С1–С2; в баллоне 2 – смесь С3–С4 (10 об. % каждого). Жидкие предельные и непредельные С5–С8 углеводороды смешивали в отдельных пенициллиновых флаконах, не придерживаясь определенной концентрации компонентов.
Модельную смесь – постоянных и углеводородных газов из газовых баллонов, жидкие предельные и непредельные углеводороды отбирали из пенициллинового флакона шприцем и вводили в испаритель хроматографа.
ОБСУЖДЕНИЯ РЕЗУЛЬТАТОВ
В табл. 2 представлены текстурные характеристики адсорбентов, полученных на основе γ-Al2O3 + + 10 мас. % ПИ-1Б.
Таблица 2.
Текстурные характеристики адсорбентов
| Параметр | $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{без}}\;{\text{обработки}}\;{\text{HCl}}}}}$ | $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ | |||||
|---|---|---|---|---|---|---|---|
| $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{исх}}}}}$ | 10 мас. % ПИ-1Б | $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{исх}}}}}$ | 10 мас. % ПИ-1Б | ||||
| Ттр,°С | 250 | 250 | 450 | 250 | 250 | 350 | 450 |
| АВЕТ, м2/г | 227.0 | 166.4 | 167.5 | 228.9 | 227.8 | 234.6 | 190.4 |
| Vпор, см3/г | 0.54 | 0.31 | 0.34 | 0.53 | 0.55 | 0.56 | 0.53 |
| dпор, нм (по БЭТ) | 7.8 | 7.4 | 7.4 | 9.0 | 8.8 | 9.0 | 10.4 |
При измерении удельной поверхности среднеквадратичное отклонение (СКО) составляет 5% – для измерения объема и диаметра пор – 10%.
Анализ десорбционных кривых показал, что удаление активных центров, последующая модификация 10 мас. % ПИ-1Б оксида алюминия и его термотренировка при температуре 450°С позволили сформировать более однородную поверхность 190.4 м2/г, средний диаметр пор составляет 10.4 нм, микропоры отсутствуют, табл. 2. Следует отметить, что диаметр пор варьируется в более узком диапазоне от 5 до 11 нм, рис. 2б, тогда как для адсорбента с необработанной исходной поверхностью это величина составляет 1–13 нм и средний диаметр пор 6–7 нм, рис. 2а.
Рис. 2.
Десорбционная кривая азота с поверхности $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{без}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + 10 мас. % ПИ-1Б(а); $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + 10 мас. % ПИ-1Б(б) и термически обработанных при Ттр = 450°С.
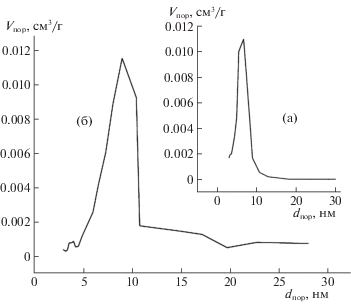
На рис. 2 представлены десорбционные кривые азота с поверхности γ-Al2O3 + 10 мас. % ПИ-1Б без и после обработки соляной кислотой исходного адсорбента.
Для проведения исследований на электронном микроскопе частицы образцов наносились на дырчатые углеродные подложки, закрепленные на медных или молибденовых сетках, с использованием ультразвукового диспергатора УЗД-1УЧ2, что позволяло добиться равномерного распределения частиц по поверхности подложки. Образец помещается в спирт, нанесенный на ультразвуковой диспергатор, после этого происходит испарение и последующее осаждение частиц образца на медную сеточку.
По данным ПЭМВР образец состоит из частиц γ-Al2O3, покрытых слоем аморфизированного углерода. Размеры частиц варьируются от 10 нм (одиночные кристаллиты) до нескольких микрон, рис. 3.
Рис. 3.
ПЭМВР-микрофотографии $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + 10 мас. % ПИ-1Б, размеры частиц, Ттр = 450°С.

При более высоких увеличениях видно, что поверхность частиц γ-Al2O3 покрыта слоем аморфизированного углерода, рис. 4. Толщина слоя варьируется от монослойного покрытия до нескольких слоев. Кроме того на снимках ПЭМВР видна пористая структура образца и размеры пор варьируются от 1 до 10 нм. Поры также покрыты слоем аморфизированного углерода.
Рис. 4.
ПЭМВР-микрофотографии $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + 10 мас. % ПИ-1Б, размеры пор, Ттр = 450°С.

По данным EDX, представленным в табл. 3, углерод располагается равномерно преимущественно на поверхностных слоях, однако присутствуют участки с относительно небольшим содержанием углерода.
Таблица 3.
Зоны анализа поверхности, элементный состав $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + 10 мас. % ПИ-1Б
| Зоны анализа | С | Al | Si | Cl |
|---|---|---|---|---|
| 1 | 24.39 | 73.38 | 0.49 | 1.73 |
| 2 | 28.68 | 71.07 | 0.06 | 0.19 |
| 3 | 24.00 | 75.38 | 0.06 | 0.56 |
| 4 | 5.02 | 94.56 | 0.09 | 0.33 |
Результаты ПЭМВР хорошо согласуются с данными текстурных характеристик для $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + 10 мас. % ПИ-1Б, термически обработанного при Ттр = 450°С, которые также подтверждают высказанное предположение о формировании однородной поверхности этого адсорбента.
Далее исследовали хроматографические свойства при анализе модельной смеси (см. табл. 4) на γ-Al2O3 + 10 мас. % ПИ-1Б и проводили сравнения с ранее полученными данными для γ-Al2O3 + + 10 мас. % ПАК с последующей имидизацией в ПИ-1Б.
Таблица 4.
Физико-химические свойства и времена удерживания компонентов модельной смеси
| Сорбат | М | Ткип,°С | $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{без}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + + 10 мас. % ПАК [8] | $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{без}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + + 10 мас. % ПИ-1Б | $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + + 10 мас. % ПИ-1Б | ||||
|---|---|---|---|---|---|---|---|---|---|
| Ттр, °С | |||||||||
| 250 | 450 | 250 | 450 | 250 | 350 | 450 | |||
| H2 | 2 | –252.7 | 0.81 | 0.52 | 0.65 | 0.70 | 0.74 | 0.58 | 0.65 |
| O2 | 32 | –182.9 | 0.93 | 0.60 | 0.75 | 0.82 | 0.83 | 0.67 | 0.77 |
| N2 | 24 | –210 | 0.93 | 0.60 | 0.75 | 0.82 | 0.83 | 0.67 | 0.77 |
| CO | 28 | –192 | 1.02 | 0.65 | 0.81 | 0.91 | 0.92 | 0.74 | 0.86 |
| CO2 | 44 | –78.6 (0.52 MПа) | 5.09 | 5.62 | 3.52 | 10.36 | 4.28 | 4.20 | 6.10 |
| CH4 | 16 | –161.6 | 1.12 | 2.71 | 0.99 | 1.07 | 1.13 | 0.88 | 1.12 |
| C2H2 | 26 | –83.8 | 14.10 | 11.05 | 9.79 | 11.16 | 9.04 | 9.31 | 11.55 |
| C2H4 | 28 | –103.7 | 5.14 | 8.66 | 4.58 | 5.45 | 4.28 | 4.62 | 7.11 |
| C2H6 | 30 | –88.6 | 3.41 | 6.62 | 3.52 | 3.99 | 3.61 | 3.12 | 5.19 |
| C3H6 | 42 | –47.8 | 12.66 | 15.82 | 9.79 | 10.36 | 9.98 | 9.31 | 12.19 |
| C3H8 | 44 | –42.1 | 8.83 | 9.78 | 8.23 | 8.51 | 8.51 | 7.43 | 10.35 |
| С4H10 | 58 | –0.5 | 15.92 | 12.95 | 12.46 | 12.80 | 13.62 | 11.83 | 15.16 |
| C5H12 | 72 | 36.1 | 21.78 | 16.70 | 12.52 | 16.13 | 14.12 | 14.94 | 17.76 |
| С6Н14 | 86 | 68.7 | 27.33 | 20.20 | 14.35 | 19.74 | 16.83 | 17.99 | 24.00 |
| С7H16 | 100 | 98.4 | 32.35 | 23.83 | 16.07 | 26.50 | 19.49 | 22.38 | 37.53 |
| C8H18 | 114 | 125.7 | 36.77 | 26.48 | 18.24 | 40.25 | 23.70 | 30.96 | – |
В опубликованной работе [8] нами был исследован оксид алюминия, модифицированный полиамидокислотой с последующей ее высокотемпературной имидизацией. Поверхность полученного материала достаточно развита 200.1 м2/г, чтобы удовлетворительно разделять постоянные газы и легкие углеводороды. Однако пик диоксида углерода имеет округлую широкую форму и это связано с неоднородностью поверхности, ранее высказанное предположение, и образованием пор более узкого диаметра 6–7 нм, табл. 2.
В работе [11] было показано, что способ пропитки раствором полиимида диатомитового носителя является наиболее удобным, потому что полиимид – устойчивое соединение в отличие от ПАК, которая подвергается гидролизу.
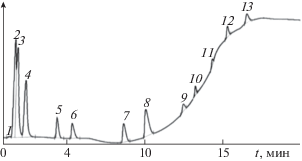
Поэтому, на следующем этапе $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{без}}\;{\text{обработки}}\;{\text{HCl}}}}}$ пропитывали раствором полиимида. Из представленных результатов в табл. 2 видим, что после термотренировки при температуре 250°С поверхность и объем пор значительно уменьшились, а диаметр пор практически не изменился. Результаты хроматографического анализа модельной смеси показали, что диоксид углерода элюирует вместе с этаном, ацетилен с пропиленом, рис. 5.
Рис. 5.
Хроматограмма разделения постоянных газов, СО2 и С1–С8 на $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{без}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + 10% ПИ-1Б, Ттр = 250°С. Условия хроматографирования: при Т = 30°С выдерживали 2 мин, затем программируемый нагрев со скоростью 10 К/мин до 230°С. 1 – водород, 2 – азот + кислород, 3 – СО, 4 – метан, 5 – этан + СО2, 6 – этилен, 7 – пропан, 8 – пропилен + + ацетилен, 9 – бутан, 10 – пентан, 11 – гексан, 12 – гептан, 13 – октан.
При дальнейшем повышении температуры (Ттр = 450°С) адсорбционные характеристики адсорбента $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{без}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + 10 мас. % ПИ-1Б не изменились (см. табл. 2) и порядок выхода компонентов анализируемой смеси остался прежний, хотя времена удерживания увеличились, табл. 4.
Далее были проведены исследования свойств γ-Al2O3 с исходной поверхности которого предварительно удалили активные центры (железо, натрий, титан) и отсутствие которых подтверждено данными EDX, табл. 3. Оксид алюминия заливали концентрированной соляной кислотой, выдерживали 30 мин, затем промывали дистиллированной водой до нейтральной реакции, высушивали до постоянного веса и модифицировали полиимидом, синтезированным по второму способу.
Как видно из табл. 2, предварительная обработка исходного оксида алюминия незначительно повлияла на его поверхность и объем пор, но при этом увеличился их диаметр: 7.8 нм для $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{без}}\;{\text{обработки}}\;{\text{HCl}}}}}$ и 9.0 нм для $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$.
При повышении температуры термотренировки до 450°С поверхность $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + + 10 мас. % полиимида значительно уменьшилась от 228.9 до 190.4 м2/г, а диаметр пор увеличился от 9.0 до 10.4 нм, табл. 2.
Изменения текстурных характеристик адсорбента оказывают существенное влияние на его хроматографические свойства. На рис. 6 представлено поведение сорбатов при элюции с поверхности исследуемого материала.
Рис. 6.
Хроматограмма разделения постоянных газов, СО2 и С1-С8 на $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + 10% ПИ-1Б ; Ттр = 250 (а), 350 (б), 450°С (в). Условия хроматографирования: при Т = 30°С выдерживали 2 мин, затем программируемый нагрев со скоростью 10 К/мин до 230°С; 1 – водород, 2 – азот + кислород, 3 – СО, 4 – метан, 5 – этан, 6 – СО2, 7 – этилен, 8 – пропан, 9 – ацетилен, 10 – пропилен, 11 – бутан, 12 – пентан, 13 – гексан, 14 – гептан, 15 – октан.

Образец, термотренированный при Ттр = 250°С (рис. 6а), склонен к разделению постоянных газов, ацетилен элюирует между пропаном и пропиленом, диоксид углерода выходит одним пиком с этиленом.
При увеличении температуры термотренировки до 350°С (рис. 6б) диоксид углерода теперь элюирует отдельным пиком и выходит между этаном и этиленом, а ацетилен не разделяется с пропиленом. При этом наблюдаем разделение водорода, азот с кислородом наполовину отделяется от монооксида углерода.
Дальнейшее увеличение температуры термотренировки до 450°С приводит к уменьшению поверхности и увеличению диаметра пор, табл. 2. Количество микропор при прокаливании уменьшается, преобладают поры одного диаметра ≈10.4 нм.
Результаты исследований, представленные в табл. 2 и на рис. 6в, свидетельствуют о создании адсорбента $\gamma {\text{ - A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\;{\text{после}}\;{\text{обработки}}\;{\text{HCl}}}}}$ + 10 мас. % полиимида, разделительная способность которого для любой пары компонентов больше 1, за исключением СО и азота+кислорода, для которых степень разрешения ≈0.5. Следует отметить, что симметричный пик диоксида углерода отделяется от этана и этилена, а пик ацетилена находится между пропаном и пропиленом.
Таким образом, предварительное удаление активных центров с поверхности оксида алюминия, модицифирование полиимидом и последующая термотренировка при температуре 450°С способствовали созданию перспективного хроматографического адсорбента (селективного слоя) с регулируемыми размерами пор диаметром 10.4 нм для разделения постоянных газов и их смесей с углеводородами С1–C8.
Работа выполнена при финансовой поддержке Министерства науки и высшего образования РФ в рамках государственного задания Института катализа СО РАН (проект AAAA-A21-121011390007-7).
Список литературы
Youn K.K., Ho B.P., Young M.L. // J. Memb. Sci. 2005. 255. P. 265. https://doi.org/10.1016/j.memsci.2005.02.002
Ohta N., Nishi Y., Morishita T. et al. // Carbon N. Y. 2008. V. 46. 1350. https://doi.org/10.1016/j.carbon.2008.05.019
Tin P.S., Xiao Y., Chung T.S. // Sep. Purif. Rev. 2006. V. 35. P. 285.https://doi.org/10.1080/15422110601003481
Чукин Г.Д. Строение оксида алюминия и катализаторов гидрообессеривания. Механизмы реакций, М.: 2010. 288 с.
Березкин В.Г., Пахомов В.П., Сакодынский К.И. Твердые носители в газовой хроматографии, М.: Химия, 1975, 200 с.
Shundrina I.K., Vaganova T.A., Kusov S.Z. et al. // J. Fluor. Chem. 2011. V. 132. P. 207–215. https://doi.org/10.1016/j.jfluchem.2011.01.008
Яковлева Е.Ю., Шундрина И.К., Ваганова Т.А. // Журн. аналит. химии. 2013. Т. 68. С. 1171. https://doi.org/10.7868/S0044450213100137
Yakovleva E.Y., Shundrina I.K., Gerasimov E.Y., Vaganova T.A. // Russ. J. Phys. Chem. A. 2014. V. 88. P. 521. https://doi.org/10.1134/S0036024414030297
Yakovleva E.Y., Shundrina I.K., Gerasimov E.Y. // Ibid. 2017. V. 91. https://doi.org/10.1134/S0036024417090321
Yakovleva E.Y., Shundrina I.K. // Adv. Mater. Technol. 2017. P. 049.https://doi.org/10.17277/amt.2017.04.pp.049-055
Яковлева Е.Ю., Барановская Е.Е. // Журн. физ. химии. 2020. Т. 94. С. 1099. https://doi.org/10.31857/S0044453720070328
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии