Журнал физической химии, 2021, T. 95, № 9, стр. 1353-1363
Обьемные свойства бинарных смесей бутиронитрил-диметилсульфоксид и бутиронитрил-диэтилсульфоксид
Е. А. Казоян a, Ш. А. Маркарян a, *
a Ереванский государственный университет
Ереван, Армения
* E-mail: shmarkar@ysu.am
Поступила в редакцию 25.11.2020
После доработки 14.12.2020
Принята к публикации 16.12.2020
Аннотация
Измерены плотности бинарных смесей бутиронитрила в диметил- и диэтилсульфоксиде во всем концентрационном диапазоне и в температурном интервале 298.15–323.15 К при внешнем давлении. Рассчитаны объемные параметры, а также параметры уравнения Редлиха–Кистера и стандартные отклoнения избыточных мольных объемов. Отклонение от идеального поведения этих растворов объясняется наличием конкурирующих гомо- и гетеромолекулярных взаимодействий, а также влиянием длины углеводородной цепи сульфоксидов на величины объемных параметров.
Изучение объемных свойств бинарных смесей является важной областью химии растворов. С одной стороны это относится к характеристике межмолекулярных взаимодействий, а с другой стороны к реакционной способности составляющих смесей компонентов.
В работе изучаемые системы включают бутиронитрил (БН), а также диметилсульфоксид (ДМСО) и диэтилсульфоксид (ДЭСО) в качестве полярных растворителей.
Данная работа является продолжением наших ранних работ по исследованию термодинамических свойств растворов соединений содержащих нитрильные группы [1–3].
Выбор БН обусловлен его использованием в качестве сырья для органического синтеза. БН также является одним из гомологов низкомолекулярных соединений содержащих полярные нитрильные группы.
Относительно второго компонента бинарных систем, следует отметить, что ДМСО и ДЭСО являются хорошими полярными растворителями и имеют важное биомедицинское значение [4–9].
Компоненты этих систем представляют собой самоассоцирующиеся полярные жидкости и в растворах образуются как гомо-, так и гетероассоциаты. Изучение этих систем представляет интерес с точки зрения влияния межмолекулярных взаимодействий на термодинамические свойства растворов.
Следует также отметить, что в литературе отсутствуют данные плотностей и объемных свойств диметилсульфоксидных и диэтилсульфоксидных растворов БН.
Ранее были исследованы бинарные смеси сульфоксидов (ДМСО и ДЭСО) с ацетонитрилом (АцН), пропионитрилом (ПН) и акрилонитрилом (АН), были исследованы с использованием методов денситометрии, вискозиметрии [1–14]. В этих работах рассматривалось взаимодействие между группами $ - {\text{C}}{\kern 1pt} \equiv {\kern 1pt} {\text{N}}$ и $ > {\kern 1pt} {\text{S}}{\kern 1pt} = {\kern 1pt} {\text{O}}$, приводящее к образованию межмолекулярных ассоциатов с диполь-дипольными взаимодействиями с циклической структурой.
В данной работе изучены объемные свойства бинарных смесей БН-ДМСО и БН-ДЭСО. Приведены результаты измерения плотностей этих бинарных смесей в температурном интервале 298.15–323.15 К. Рассчитаны избыточные мольные объемы, кажущиеся мольные объемы, парциальные и парциальные избыточные мольные объемы, а также параметры корреляций и коэффициенты объемного термического расширения. Одновременно проведено сравнение полученных данных объемных параметров исследуемых смесей со свойствами сульфоксидных растворов других нитрильных соединений (АцН, ПН и АН).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
БН (чистота >99%) и ДМСО (чистота 99.9%) были получены из Aldrich Chemical Cо и использованы без дальнейшей очистки.
ДЭСО получено и очищено по методике, описанной в работе [15]. Его чистота, проверенная с помощью газовой хроматографии (газ-носитель – He, Apiezon-Carbowax 20M, l = 1м), более 99.5%; содержание воды, определенное по ИК-поглощению в спектральной области 3500–3300 см–1, ниже 0.01%.
Плотности смесей измерены с помощью колебательно-резонансного денсиметра Anton Paar DMA 4500 с точностью измерения плотности и температуры соответственно ±5 × 10–5 г/см3 и ±0.03 К.
Смеси приготовлены гравиметрическим методом с точностью ±1 × 10–3 г с помощью аналитических весов Sartorius CPA6235.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Плотности и избыточные мольные объемы
Объемные свойства смесей исследованы методом денситометрии. Измерения плотности проводились в температурном интервале от 298.15 К до 323.15 К во всем концентрационном диапазоне. Экспериментальные данные плотностей ($\rho $) смесей БН-ДМСО и БН-ДЭСО в температурном интервале 298.15–323.15 К представлены в табл. 1.
Таблица 1.
Плотности ($\rho $) смесей БН(1)-ДМСО(2) и БН(1)-ДЭСО(2) в температурном интервале 298.15–323.15 К
| X2, мол. доли | $\rho \times {{10}^{{ - 3}}}$, кг м–3 | |||||
|---|---|---|---|---|---|---|
| 298.15 K | 303.15 K | 308.15 K | 313.15 K | 318.15 K | 323.15 K | |
| БН-ДМСО | ||||||
| 0.0000 | 0.78640 | 0.78184 | 0.77717 | 0.77248 | 0.76777 | 0.76305 |
| 0.0984 | 0.81110 | 0.80641 | 0.80172 | 0.79701 | 0.79229 | 0.78755 |
| 0.2068 | 0.83973 | 0.83500 | 0.83028 | 0.82556 | 0.82081 | 0.81606 |
| 0.3090 | 0.86806 | 0.86330 | 0.85856 | 0.85381 | 0.84905 | 0.84427 |
| 0.4036 | 0.89577 | 0.89098 | 0.88621 | 0.88144 | 0.87665 | 0.87185 |
| 0.4992 | 0.92398 | 0.91918 | 0.91439 | 0.90959 | 0.90478 | 0.89996 |
| 0.5977 | 0.95483 | 0.95001 | 0.94519 | 0.94036 | 0.93552 | 0.93067 |
| 0.7074 | 0.99018 | 0.98528 | 0.98041 | 0.97555 | 0.97066 | 0.96579 |
| 0.7849 | 1.01699 | 1.01206 | 1.00716 | 1.00226 | 0.99735 | 0.99244 |
| 0.8982 | 1.05738 | 1.05239 | 1.04744 | 1.04249 | 1.03753 | 1.03257 |
| 1.0000 | 1.09551 | 1.09049 | 1.08548 | 1.08047 | 1.07546 | 1.07044 |
| БН-ДЭСО | ||||||
| 0.0000 | 0.78640 | 0.78184 | 0.77717 | 0.77248 | 0.76777 | 0.76305 |
| 0.1089 | 0.81536 | 0.81074 | 0.80610 | 0.80145 | 0.79679 | 0.79211 |
| 0.2152 | 0.84201 | 0.83747 | 0.83288 | 0.82827 | 0.82365 | 0.81901 |
| 0.2987 | 0.86228 | 0.85777 | 0.85321 | 0.84863 | 0.84403 | 0.83943 |
| 0.4185 | 0.89010 | 0.88563 | 0.88111 | 0.87657 | 0.87203 | 0.86747 |
| 0.4955 | 0.90743 | 0.90298 | 0.89848 | 0.89397 | 0.88946 | 0.88493 |
| 0.5913 | 0.92773 | 0.92331 | 0.91885 | 0.91437 | 0.90989 | 0.90536 |
| 0.6883 | 0.94759 | 0.94315 | 0.93871 | 0.93426 | 0.92981 | 0.92535 |
| 0.7918 | 0.96755 | 0.96319 | 0.95878 | 0.95437 | 0.94995 | 0.94553 |
| 0.8952 | 0.98712 | 0.98279 | 0.97841 | 0.97402 | 0.96964 | 0.96525 |
| 1.0000 | 1.00616 | 1.00181 | 0.99745 | 0.99310 | 0.98875 | 0.98440 |
С помощью экспериментальных значений плотностей были вычислены значения избыточного мольного объема (табл. 2 и 3), используя уравнение:
(1)
${{V}^{E}} = \frac{{{{X}_{1}}{{M}_{1}} + {{X}_{2}}{{M}_{2}}}}{\rho } - \left( {{{x}_{1}}\frac{{{{M}_{1}}}}{{{{\rho }_{1}}}}} \right. + \left. {{{x}_{2}}\frac{{{{M}_{2}}}}{{{{\rho }_{2}}}}} \right),$Таблица 2.
Избыточные мольные объемы ($V_{m}^{E} \times {{10}^{6}}$, м3 моль–1) смеси БН(1)-ДМСО(2), и кажущиеся (${{V}_{{\varphi ,i}}} \times {{10}^{6}}$, м3 моль–1), парциальные (${{\bar {V}}_{i}} \times {{10}^{6}}$, м3 моль–1) и парциальные избыточные ($\bar {V}_{i}^{E} \times {{10}^{6}}$, м3 моль–1) мольные объемы компонентов (БН и ДМСО) в температурном интервале (298.15–323.15) K
| X2, мол. доли | $V_{m}^{E}$ | ${{V}_{{\varphi ,1}}}$ | ${{V}_{{\varphi ,2}}}$ | ${{\bar {V}}_{1}}$ | ${{\bar {V}}_{2}}$ | $\bar {V}_{1}^{E}$ | $\bar {V}_{2}^{E}$ |
|---|---|---|---|---|---|---|---|
| 298.15 K | |||||||
| 0.0000 | 0.000 | 87.88 | – | 87.88 | – | 0.000 | 0.000 |
| 0.0984 | 0.098 | 87.92 | 71.76 | 87.91 | 71.63 | 0.029 | 0.316 |
| 0.2068 | 0.207 | 87.96 | 71.63 | 87.93 | 71.46 | 0.053 | 0.139 |
| 0.3090 | 0.309 | 87.97 | 71.54 | 87.93 | 71.38 | 0.057 | 0.057 |
| 0.4036 | 0.404 | 87.98 | 71.48 | 87.92 | 71.35 | 0.045 | 0.027 |
| 0.4992 | 0.499 | 87.99 | 71.43 | 87.90 | 71.34 | 0.021 | 0.020 |
| 0.5977 | 0.598 | 88.00 | 71.40 | 87.87 | 71.34 | –0.006 | 0.022 |
| 0.7074 | 0.707 | 88.02 | 71.38 | 87.86 | 71.34 | –0.019 | 0.022 |
| 0.7849 | 0.785 | 88.05 | 71.37 | 87.88 | 71.34 | 0.000 | 0.018 |
| 0.8982 | 0.898 | 88.10 | 71.34 | 87.98 | 71.32 | 0.101 | 0.007 |
| 1.0000 | 0.000 | – | 71.32 | – | 71.32 | 0000 | 0.000 |
| 303.15 K | |||||||
| 0.0000 | 0.000 | 88.39 | – | 88.39 | – | 0.000 | 0.000 |
| 0.0984 | 0.098 | 88.44 | 72.15 | 88.43 | 71.99 | 0.038 | 0.344 |
| 0.2068 | 0.207 | 88.48 | 71.98 | 88.46 | 71.77 | 0.066 | 0.125 |
| 0.3090 | 0.309 | 88.49 | 71.87 | 88.46 | 71.68 | 0.067 | 0.030 |
| 0.4036 | 0.404 | 88.49 | 71.80 | 88.43 | 71.65 | 0.043 | 0.001 |
| 0.4992 | 0.499 | 88.49 | 71.75 | 88.39 | 71.65 | 0.002 | 0.002 |
| 0.5977 | 0.598 | 88.50 | 71.72 | 88.34 | 71.66 | –0.045 | 0.012 |
| 0.7074 | 0.707 | 88.51 | 71.70 | 88.31 | 71.67 | –0.077 | 0.020 |
| 0.7849 | 0.785 | 88.54 | 71.69 | 88.32 | 71.67 | –0.064 | 0.018 |
| 0.8982 | 0.898 | 88.60 | 71.67 | 88.44 | 71.65 | 0.049 | 0.007 |
| 1.0000 | 0.000 | – | 71.65 | – | 71.65 | 0.000 | 0.000 |
| 308.15 K | |||||||
| 0.0000 | 0.000 | 88.92 | – | 88.92 | – | 0.000 | 0.000 |
| 0.0984 | 0.098 | 88.97 | 72.44 | 88.96 | 72.29 | 0.039 | 0.311 |
| 0.2068 | 0.207 | 89.00 | 72.28 | 88.99 | 72.07 | 0.066 | 0.097 |
| 0.3090 | 0.309 | 89.01 | 72.17 | 88.98 | 71.98 | 0.063 | 0.007 |
| 0.4036 | 0.404 | 89.01 | 72.10 | 88.96 | 71.96 | 0.036 | –0.017 |
| 0.4992 | 0.499 | 89.00 | 72.06 | 88.91 | 71.97 | –0.011 | –0.011 |
| 0.5977 | 0.598 | 89.00 | 72.03 | 88.86 | 71.98 | –0.065 | 0.004 |
| 0.7074 | 0.707 | 89.01 | 72.01 | 88.82 | 71.99 | –0.104 | 0.016 |
| 0.7849 | 0.785 | 89.03 | 72.01 | 88.82 | 71.99 | –0.097 | 0.016 |
| 0.8982 | 0.898 | 89.09 | 72.00 | 88.93 | 71.98 | 0.009 | 0.007 |
| 1.0000 | 0.000 | – | 71.98 | – | 71.98 | 0000 | 0.000 |
| 313.15 K | |||||||
| 0.0000 | 0.000 | 89.46 | – | 89.46 | – | 0.000 | – |
| 0.0984 | 0.098 | 89.51 | 72.73 | 89.50 | 72.58 | 0.037 | 0.269 |
| 0.2068 | 0.207 | 89.53 | 72.57 | 89.52 | 72.38 | 0.062 | 0.066 |
| 0.3090 | 0.309 | 89.53 | 72.47 | 89.52 | 72.30 | 0.058 | –0.014 |
| 0.4036 | 0.404 | 89.53 | 72.41 | 89.49 | 72.28 | 0.029 | –0.031 |
| 0.4992 | 0.499 | 89.52 | 72.37 | 89.44 | 72.29 | –0.019 | –0.020 |
| 0.5977 | 0.598 | 89.51 | 72.35 | 89.38 | 72.31 | –0.076 | –0.001 |
| 0.7074 | 0.707 | 89.52 | 72.34 | 89.34 | 72.33 | –0.120 | 0.014 |
| 0.7849 | 0.785 | 89.54 | 72.33 | 89.34 | 72.33 | –0.117 | 0.015 |
| 0.8982 | 0.898 | 89.59 | 72.33 | 89.44 | 72.32 | –0.017 | 0.007 |
| 1.0000 | 0.000 | – | 72.31 | – | 72.31 | – | 0.000 |
| 318.15 K | |||||||
| 0.0000 | 0.000 | 90.01 | – | 90.01 | – | 0.000 | 0.000 |
| 0.0984 | 0.099 | 90.05 | 73.02 | 90.05 | 72.88 | 0.037 | 0.228 |
| 0.2068 | 0.209 | 90.07 | 72.87 | 90.07 | 72.68 | 0.061 | 0.034 |
| 0.3090 | 0.309 | 90.06 | 72.77 | 90.06 | 72.61 | 0.054 | –0.039 |
| 0.4036 | 0.404 | 90.05 | 72.71 | 90.03 | 72.60 | 0.021 | –0.050 |
| 0.4992 | 0.499 | 90.04 | 72.68 | 89.98 | 72.61 | –0.033 | –0.034 |
| 0.5977 | 0.598 | 90.03 | 72.66 | 89.91 | 72.64 | –0.096 | –0.009 |
| 0.7074 | 0.708 | 90.03 | 72.66 | 89.86 | 72.66 | –0.148 | 0.009 |
| 0.7849 | 0.785 | 90.05 | 72.66 | 89.86 | 72.66 | –0.151 | 0.013 |
| 0.8982 | 0.898 | 90.10 | 72.66 | 89.95 | 72.65 | –0.061 | 0.006 |
| 1.0000 | 0.000 | – | 72.65 | – | 72.65 | 0000 | 0.000 |
| 323.15 K | |||||||
| 0.0000 | 0.000 | 90.57 | – | 90.57 | – | 0.000 | 0.000 |
| 0.0984 | 0.098 | 90.60 | 73.32 | 90.60 | 73.18 | 0.036 | 0.190 |
| 0.2068 | 0.207 | 90.61 | 73.17 | 90.62 | 73.00 | 0.057 | 0.008 |
| 0.3090 | 0.309 | 90.61 | 73.08 | 90.61 | 72.93 | 0.049 | –0.057 |
| 0.4036 | 0.404 | 90.59 | 73.03 | 90.58 | 72.93 | 0.013 | –0.064 |
| 0.4992 | 0.499 | 90.58 | 73.00 | 90.52 | 72.94 | –0.043 | –0.044 |
| 0.5977 | 0.598 | 90.56 | 72.99 | 90.46 | 72.97 | –0.109 | –0.017 |
| 0.7074 | 0.707 | 90.56 | 72.99 | 90.40 | 72.99 | –0.166 | 0.005 |
| 0.7849 | 0.785 | 90.57 | 72.99 | 90.39 | 73.00 | –0.174 | 0.010 |
| 0.8982 | 0.898 | 90.61 | 72.99 | 90.47 | 72.99 | –0.096 | 0.006 |
| 1.0000 | 0.000 | – | 72.99 | – | 72.99 | 0.000 | 0.000 |
Таблица 3.
Избыточные мольные объемы ($V_{m}^{E} \times {{10}^{6}}$, м3 моль–1) смеси БН(1)-ДЭСО(2), и кажущиеся (${{V}_{{\varphi ,i}}} \times {{10}^{6}}$, м3 моль–1), парциальные (${{\bar {V}}_{i}} \times {{10}^{6}}$, м3 моль–1) и парциальные избыточные ($\bar {V}_{i}^{E} \times {{10}^{6}}$, м3 моль–1) мольные объемы компонентов (БН и ДЭСО) в температурном интервале (298.15–323.15) K
| X2, мол. доли | $V_{m}^{E}$ | ${{V}_{{\varphi ,1}}}$ | ${{V}_{{\varphi ,2}}}$ | ${{\bar {V}}_{1}}$ | ${{\bar {V}}_{2}}$ | $\bar {V}_{1}^{E}$ | $\bar {V}_{2}^{E}$ |
|---|---|---|---|---|---|---|---|
| 298.15 K | |||||||
| 0.0000 | 0.000 | 87.88 | – | 87.88 | – | 0.000 | 0.000 |
| 0.1089 | –0.092 | 87.80 | 104.89 | 87.86 | 104.88 | –0.014 | –0.646 |
| 0.2152 | –0.127 | 87.71 | 104.91 | 87.85 | 104.97 | –0.023 | –0.561 |
| 0.2987 | –0.163 | 87.63 | 104.95 | 87.83 | 105.08 | –0.045 | –0.453 |
| 0.4185 | –0.195 | 87.52 | 105.04 | 87.77 | 105.25 | –0.110 | –0.283 |
| 0.4955 | –0.224 | 87.46 | 105.11 | 87.70 | 105.35 | –0.174 | –0.183 |
| 0.5913 | –0.196 | 87.40 | 105.20 | 87.61 | 105.45 | –0.269 | –0.084 |
| 0.6883 | –0.170 | 87.37 | 105.30 | 87.51 | 105.51 | –0.370 | –0.020 |
| 0.7918 | –0.091 | 87.37 | 105.40 | 87.42 | 105.54 | –0.453 | 0.008 |
| 0.8952 | –0.050 | 87.41 | 105.48 | 87.41 | 105.54 | –0.470 | 0.007 |
| 1.0000 | 0.000 | – | 105.53 | – | 105.53 | 0.000 | 0.000 |
| 303.15 K | |||||||
| 0.0000 | 0.000 | 88.39 | – | 88.39 | – | 0.000 | 0.000 |
| 0.1089 | –0.087 | 88.31 | 105.34 | 88.38 | 105.33 | –0.010 | –0.662 |
| 0.2152 | –0.132 | 88.21 | 105.35 | 88.37 | 105.40 | –0.019 | –0.587 |
| 0.2987 | –0.171 | 88.13 | 105.39 | 88.35 | 105.51 | –0.044 | –0.480 |
| 0.4185 | –0.205 | 88.02 | 105.47 | 88.27 | 105.68 | –0.118 | –0.305 |
| 0.4955 | –0.234 | 87.95 | 105.55 | 88.20 | 105.79 | –0.190 | –0.200 |
| 0.5913 | –0.207 | 87.89 | 105.64 | 88.09 | 105.89 | –0.297 | –0.095 |
| 0.6883 | –0.175 | 87.85 | 105.74 | 87.98 | 105.96 | –0.409 | –0.026 |
| 0.7918 | –0.100 | 87.84 | 105.84 | 87.89 | 105.99 | –0.502 | 0.007 |
| 0.8952 | –0.058 | 87.88 | 105.93 | 87.87 | 106.00 | –0.521 | 0.007 |
| 1.0000 | 0.000 | – | 105.99 | – | 105.99 | 0.000 | 0.000 |
| 308.15 K | |||||||
| 0.0000 | 0.000 | 88.92 | – | 88.92 | – | 0.000 | 0.000 |
| 0.1089 | –0.092 | 88.83 | 105.76 | 88.91 | 105.75 | –0.011 | –0.704 |
| 0.2152 | –0.141 | 88.73 | 105.77 | 88.90 | 105.83 | –0.022 | –0.619 |
| 0.2987 | –0.182 | 88.65 | 105.81 | 88.87 | 105.95 | –0.048 | –0.505 |
| 0.4185 | –0.217 | 88.53 | 105.91 | 88.79 | 106.13 | –0.125 | –0.321 |
| 0.4955 | –0.247 | 88.46 | 105.98 | 88.72 | 106.24 | –0.200 | –0.211 |
| 0.5913 | –0.219 | 88.39 | 106.09 | 88.61 | 106.35 | –0.312 | –0.101 |
| 0.6883 | –0.185 | 88.35 | 106.19 | 88.49 | 106.42 | –0.430 | –0.029 |
| 0.7918 | –0.107 | 88.34 | 106.30 | 88.39 | 106.46 | –0.528 | 0.006 |
| 0.8952 | –0.062 | 88.38 | 106.39 | 88.37 | 106.46 | –0.553 | 0.007 |
| 1.0000 | 0.000 | – | 106.45 | – | 106.45 | 0.000 | 0.000 |
| 313.15 K | |||||||
| 0.0000 | 0.000 | 89.46 | – | 89.46 | – | 0.000 | 0.000 |
| 0.1089 | –0.097 | 89.37 | 106.17 | 89.45 | 106.17 | –0.013 | –0.746 |
| 0.2152 | –0.150 | 89.26 | 106.20 | 89.43 | 106.27 | –0.025 | –0.650 |
| 0.2987 | –0.193 | 89.17 | 106.24 | 89.41 | 106.39 | –0.052 | –0.529 |
| 0.4185 | –0.229 | 89.05 | 106.34 | 89.33 | 106.58 | –0.132 | –0.335 |
| 0.4955 | –0.259 | 88.98 | 106.42 | 89.25 | 106.70 | –0.209 | –0.220 |
| 0.5913 | –0.230 | 88.90 | 106.53 | 89.14 | 106.81 | –0.325 | –0.106 |
| 0.6883 | –0.194 | 88.86 | 106.64 | 89.01 | 106.89 | –0.446 | –0.031 |
| 0.7918 | –0.114 | 88.85 | 106.76 | 88.91 | 106.92 | –0.549 | 0.005 |
| 0.8952 | –0.065 | 88.88 | 106.85 | 88.88 | 106.92 | –0.579 | 0.007 |
| 1.0000 | 0.000 | – | 106.92 | – | 106.92 | 0.000 | 0.000 |
| 318.15 K | |||||||
| 0.0000 | 0.000 | 90.01 | – | 90.01 | – | 0.000 | 0.000 |
| 0.1089 | –0.104 | 89.91 | 106.59 | 89.99 | 106.60 | –0.015 | –0.792 |
| 0.2152 | –0.160 | 89.80 | 106.62 | 89.98 | 106.71 | –0.029 | –0.683 |
| 0.2987 | –0.203 | 89.70 | 106.67 | 89.95 | 106.84 | –0.058 | –0.553 |
| 0.4185 | –0.242 | 89.57 | 106.78 | 89.87 | 107.04 | –0.140 | –0.350 |
| 0.4955 | –0.273 | 89.50 | 106.87 | 89.79 | 107.16 | –0.219 | –0.231 |
| 0.5913 | –0.242 | 89.42 | 106.98 | 89.67 | 107.28 | –0.338 | –0.112 |
| 0.6883 | –0.204 | 89.37 | 107.10 | 89.55 | 107.35 | –0.463 | –0.034 |
| 0.7918 | –0.121 | 89.36 | 107.22 | 89.44 | 107.39 | –0.572 | 0.004 |
| 0.8952 | –0.069 | 89.40 | 107.32 | 89.40 | 107.40 | –0.609 | 0.007 |
| 1.0000 | 0.000 | – | 107.39 | – | 107.39 | 0.000 | 0.000 |
| 323.15 K | |||||||
| 0.0000 | 0.000 | 90.57 | – | 90.57 | – | 0.000 | 0.000 |
| 0.1089 | –0.109 | 90.46 | 107.01 | 90.55 | 107.03 | –0.018 | –0.836 |
| 0.2152 | –0.169 | 90.34 | 107.05 | 90.53 | 107.15 | –0.034 | –0.712 |
| 0.2987 | –0.215 | 90.25 | 107.11 | 90.50 | 107.29 | –0.064 | –0.574 |
| 0.4185 | –0.255 | 90.11 | 107.23 | 90.42 | 107.50 | –0.147 | –0.362 |
| 0.4955 | –0.285 | 90.03 | 107.32 | 90.34 | 107.62 | –0.227 | –0.239 |
| 0.5913 | –0.250 | 89.95 | 107.44 | 90.22 | 107.75 | –0.347 | –0.117 |
| 0.6883 | –0.214 | 89.90 | 107.56 | 90.09 | 107.83 | –0.476 | –0.037 |
| 0.7918 | –0.128 | 89.88 | 107.68 | 89.98 | 107.87 | –0.590 | 0.003 |
| 0.8952 | –0.073 | 89.92 | 107.79 | 89.93 | 107.87 | –0.635 | 0.007 |
| 1.0000 | 0.000 | – | 107.86 | – | 107.86 | 0.000 | 0.000 |
На рис. 1(а, б) приведены зависимости избыточных мольных объемов смесей от мольной доли сульфоксидов при температурах от 298.15 до 323.15 К.
Рис. 1.
Избыточные мольные объемы БН-ДМСО (а) и БН-ДЭСО (б) бинарных систем в температурном интервале от 298.15 до 323.15 К.

Как видно из рис. 1(а, б), обе зависимости имеют экстремальный характер. Однако, для смесей БН-ДМСО величены избыточных мольных объемов положительны, а для смесей БН-ДЭСО отрицательны.
Этот факт указывает на то, что в отличие от диметилсульфоксидных смесей, в системах БН-ДЭСО превалируют сильные межмолекулярные взаимодействия между группами $ - {\text{C}}{\kern 1pt} \equiv {\kern 1pt} {\text{N}}$ и $ > {\kern 1pt} {\text{S}}{\kern 1pt} = {\kern 1pt} {\text{O}}$, приводящие к образованию гетероассоциатов. А в системе БН-ДМСО наблюдаемые положительные значения избыточных мольных объемов означают, что здесь имеет место формирование гомоассоциатов. Из температурных зависимостей для обеих систем следует, что повышение температуры приводит к увеличению доли гетероассоциатов.
Другой особенностью изученных систем является влияние длины и структуры углеводородной цепи на межмолекулярные взаимодействия. Для представления общей картины, на рис. 2 и 3 приведены также зависимости полученные ранее для других соединений содержащие нитрильные группы (АцН, ПН и АН) [1, 2].
Рис. 2.
Избыточные мольные объемы бинарных смесей АцН-ДМСО (1), ПН-ДМСО (2), БН-ДМСО (3) и АН-ДМСО (4) при температуре 298.15 К.
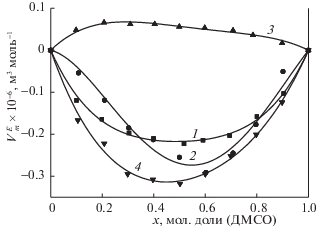
Рис. 3.
Избыточные мольные объемы бинарных смесей АцН-ДЭСО (1), ПН-ДЭСО (2), БН-ДЭСО (3) и АН-ДЭСО (4) при температуре 298.15 К.

Наблюдаемое различие (рис. 2 и 3) объясняется увеличением электронодонорности углеводородной цепи при переходе от
АцН к ПН. Более значительное отклонение для системы АН-сульфоксид обусловлено тем,
что помимо индуктивного эффекта в молекуле АН имеется также мезомерный эффект ( ), который одновременно с индуктивным эффектом приводит к значительному увеличению
полярности нитрильной группы.
), который одновременно с индуктивным эффектом приводит к значительному увеличению
полярности нитрильной группы.
На рис. 2 приведены зависимости избыточных мольных объемов смесей нитрилов с ДМСО от мольной доли сульфоксида при температуре 298.15 К. Как видно из рисунка, в смесях БН-ДМСО избыточный мольный объем имеет положительные значения, что говорит о существовании конкурирующих с диполь-дипольными связями взаимодействий. Предполагается, что с ростом молекулярной массы и длины углеводородной цепи предельных нитрилов эффективность дисперсионных сил, то есть, гидрофобных взаимодействий усиливается и имеет свой вклад в конкуренции формирования гомо- и гетероассоциатов. Такое объяснение соответствует теории о гидрофобных эффектах [15] и хорошо согласуется с результатами, полученными на основании исследования термодинамических свойств растворов ДМСО с некоторыми первичными и вторичными алканолями [16–18].
Это объяснение применимо и для смесей БН-ДЭСО, где имеет место уменьшение абсолютной величины отрицательного отклонения по сравнению с другими нитрилами (рис. 3).
С другой стороны, на межмолекулярные взаимодействия также действует длина углеводородной цепи сульфоксидов (рис. 1), чем и обусловлены более эффективные взаимодействия БН с ДЭСО по сравнению с ДМСО.
Проведена корреляция экспериментальных данных избыточных мольных объемов по уравнению Редлиха–Кистера [19–22]:
(2)
${{Y}^{E}} = {{x}_{1}}(1 - {{x}_{1}})\sum\limits_{i = {\text{o}}}^k {{{A}_{i}}{{{(2{{x}_{1}} - 1)}}^{i}}} .$(3)
$\sigma = {{\left[ {\sum\limits_{i = 1}^k {(Y_{{i,\exp }}^{E}} - Y_{{i,{\text{calc}}}}^{E}{{)}^{2}}{\kern 1pt} /{\kern 1pt} (т - n)} \right]}^{{1/2}}},$Значения корреляционных коэффициентов A0, A1, A2 исследованных растворов отличаются от нуля и значения A2 стремятся к максимуму (табл. 4), что согласно оригинальной работе Редлиха и Кистера [22], указывает в этих системах на формирование ассоциатов с помощью межмолекулярных взаимодействий.
Таблица 4.
Значения корреляционных коэффициентов (A0, A1, A2) и стандартных отклонений ($\sigma $)
| T, K | A0 | A1 | A2 | σ |
|---|---|---|---|---|
| БН-ДМСО | ||||
| 298.15 | 0.2275 | –0.1456 | 0.2231 | 0.0038 |
| 303.15 | 0.2055 | –0.1991 | 0.2933 | 0.0039 |
| 308.15 | 0.1602 | –0.2049 | 0.2984 | 0.0039 |
| 313.15 | 0.1145 | –0.1940 | 0.3002 | 0.0044 |
| 318.15 | 0.0623 | –0.1960 | 0.3025 | 0.0042 |
| 323.15 | 0.0205 | –0.1948 | 0.2909 | 0.0051 |
| БН-ДЭСО | ||||
| 298.15 | –0.8362 | 0.1254 | 0.3450 | 0.0130 |
| 303.15 | –0.8774 | 0.1004 | 0.3709 | 0.0111 |
| 308.15 | –0.9279 | 0.1077 | 0.3776 | 0.0109 |
| 313.15 | –0.9759 | 0.1191 | 0.3830 | 0.0109 |
| 318.15 | –1.0273 | 0.1306 | 0.3833 | 0.0114 |
| 323.15 | –1.0739 | 0.1442 | 0.3775 | 0.0113 |
Кажущиеся, парциальные и избыточные парциальные мольные объемы
На основе экспериментальных значений плотности, были также рассчитаны другие объемные характеристики: кажущиеся, парциальные, избыточные парциальные мольные объемы (табл. 2 и 3).
Кажущиеся мольные объемы ${{V}_{{\varphi ,1}}}$ и ${{V}_{{\varphi ,2}}}$ компонентов были вычислены по уравнению [17, 20]:
(4)
${{V}_{{\varphi ,1}}} = V_{1}^{*} + V_{m}^{E}{\text{/}}{{x}_{1}}\quad {\text{и}}\quad {{V}_{{\varphi ,2}}} = V_{2}^{*} + V_{m}^{E}{\text{/}}{{x}_{2}},$Парциальные мольные объемы (${{\bar {V}}_{i}}$) вычислены из избыточных мольных объемов согласно литературе [20, 23]:
(5)
${{\bar {V}}_{i}} = V{\kern 1pt} _{i}^{*} + V_{m}^{E}{\text{/}}{{x}_{i}} + {{x}_{i}}(1 - {{x}_{i}}){{(\partial (V_{m}^{E}{\text{/}}{{x}_{i}}){\text{/}}\partial {{x}_{i}})}_{{T,P}}},$Как следует из данных, приведенных в табл. 2 и 3, для смесей БН-ДМСО и БН-ДЭСО кажущиеся и парциальные мольные объемы компонентов в зависимости от концентрации и температуры изменяются не монотонно, что указывает на наличие конкурирующих взаимодействий.
Парциальные мольные объемы при бесконечном разбавлении ($V_{\varphi }^{{\text{o}}}$) получены методом экстраполяции по уравнению Мейсона:
Как видно из данных (табл. 5), значения предельных парциальных мольных объемов для БН увеличиваются с повышением температуры. Следует отметить, что при бесконечном разбавлении значения парциальных и кажущихся мольных объемов совпадают. Однако, по величине предельные парциальные мольные объемы по сравнению с молярным объемом чистого БН меньше в ДЭСО, что и доказывает наличие сильных взаимодействий между молекулами БН и ДЭСО. А в смесях с ДМСО, предельные парциальные мольные объемы БН больше мольных объемов чистого вещества. Это указывает на то, что в смесях БН-ДМСО доминирует образование гомоассоциатов.
Таблица 5.
Значения мольных ($V{\kern 1pt} * \times {{10}^{6}}$, м3 моль–1) и предельных парциальных мольных объемов ($V_{\varphi }^{\infty } \times {{10}^{6}}$, м3 моль–1) БН в сульфоксидных растворах в температурном интервале 298.15–323.15 К
| Т, К | $V{\kern 1pt} *{\kern 1pt} (БН)$ | $V_{\varphi }^{{\text{о}}}(БН)$ | |
|---|---|---|---|
| БН-ДМСО | БН-ДЭСО | ||
| 298.15 | 87.88 | 87.89 | 87.82 |
| 303.15 | 88.39 | 88.42 | 88.34 |
| 308.15 | 88.92 | 88.95 | 88.87 |
| 313.15 | 89.46 | 89.49 | 89.41 |
| 318.15 | 90.01 | 90.04 | 89.95 |
| 323.15 | 90.57 | 90.59 | 90.51 |
Парциальные избыточные мольные объемы компонентов исследуемых бинарных систем $\bar {V}_{i}^{E}$ оцениваются по уравнению (7) и представлены в табл. 2 и 3
Как видно из данных, величины парциальных избыточных мольных объемов в обеих системах уменьшаются при повышении температуры (рис. 4 и 5). В то же время, в смеси БН-ДЭСО парциальные избыточные мольные объемы компонентов монотонно увеличиваются с увеличением собственной молярной доли. Однако, в смеси БН-ДЭСО зависимость парциальных избыточных мольных объемов от концентрации как для БН, так и для ДМСО, имеет четко выраженный экспоненциальный характер, что и доказывает в этих смесях эффективность конкуренции гомо- и гетероассоциатов.
Рис. 4.
Парциальные избыточные мольные объемы компонентов бинарной смеси БН-ДМСО при температурах (298.15 и 323.15) K: БН – 298.15 K (1) и 323.15 K (2); ДМСО – 298.15 K (3) и 323.15 K (4).
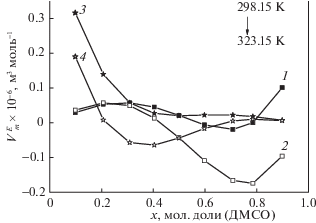
Рис. 5.
Парциальные избыточные мольные объемы компонентов бинарной смеси БН-ДЭСО при температурах (298.15 и 323.15) K: БН – 298.15 K (1) и 323.15 K (2); ДЭСО – 298.15 K (3) и 323.15 K (4).

Влияние температуры на объемные свойства, выраженные коэффициентом теплового расширения, рассчитаны на основе экспериментальных данных плотностей (табл. 6), согласно уравнению
(8)
${{\alpha }_{\rho }} = (1{\text{/}}V){{(\delta V{\text{/}}\delta T)}_{\rho }} = - (1{\text{/}}\rho ){{(\delta \rho {\text{/}}\delta T)}_{\rho }}.$Таблица 6.
Коэффициенты теплового расширения ($\alpha \times {{10}^{4}}$, K–1) смесей БН-ДМСО и БН-ДЭСО в температурном интервале 298.15–323.15 К
| X, мол. доли | 298.15 K | 303.15 K | 308.15 K | 313.15 K | 318.15 K | 323.15 K |
|---|---|---|---|---|---|---|
| X(ДМСО) | БН-ДМСО | |||||
| 0.0000 | 11.891 | 11.961 | 12.033 | 12.106 | 12.180 | 12.255 |
| 0.0984 | 11.611 | 11.679 | 11.747 | 11.817 | 11.887 | 11.959 |
| 0.2068 | 11.272 | 11.335 | 11.400 | 11.465 | 11.531 | 11.599 |
| 0.3090 | 10.957 | 11.017 | 11.078 | 11.140 | 11.202 | 11.266 |
| 0.4036 | 10.676 | 10.734 | 10.791 | 10.850 | 10.909 | 10.969 |
| 0.4992 | 10.396 | 10.450 | 10.505 | 10.560 | 10.617 | 10.673 |
| 0.5977 | 10.120 | 10.171 | 10.223 | 10.276 | 10.329 | 10.383 |
| 0.7074 | 9.849 | 9.898 | 9.947 | 9.997 | 10.047 | 10.098 |
| 0.7849 | 9.652 | 9.699 | 9.746 | 9.794 | 9.842 | 9.891 |
| 0.8982 | 9.381 | 9.425 | 9.470 | 9.515 | 9.560 | 9.606 |
| 1.0000 | 9.128 | 9.170 | 9.213 | 9.255 | 9.298 | 9.342 |
| X(ДЭСО) | БН-ДЭСО | |||||
| 0.0000 | 11.891 | 11.961 | 12.033 | 12.106 | 12.180 | 12.255 |
| 0.1089 | 11.406 | 11.471 | 11.537 | 11.604 | 11.672 | 11.741 |
| 0.2152 | 10.931 | 10.990 | 11.051 | 11.112 | 11.175 | 11.238 |
| 0.2987 | 10.606 | 10.662 | 10.719 | 10.777 | 10.836 | 10.895 |
| 0.4185 | 10.175 | 10.226 | 10.279 | 10.332 | 10.386 | 10.440 |
| 0.4955 | 9.923 | 9.971 | 10.021 | 10.072 | 10.123 | 10.175 |
| 0.5913 | 9.645 | 9.691 | 9.738 | 9.786 | 9.834 | 9.883 |
| 0.6883 | 9.387 | 9.432 | 9.476 | 9.521 | 9.567 | 9.613 |
| 0.7918 | 9.109 | 9.150 | 9.192 | 9.234 | 9.277 | 9.321 |
| 0.8952 | 8.868 | 8.907 | 8.947 | 8.987 | 9.028 | 9.069 |
| 1.0000 | 8.651 | 8.689 | 8.727 | 8.765 | 8.804 | 8.843 |
Как видно из табл. 6, в смесях БН-ДМСО и БН-ДЭСО, коэффициенты теплового расширения положительные и монотонно увеличиваются с повышением температуры и молярной доли БН.
Таким образом, полученные результаты по исследованию обьемных свойств бинарных смесей БН-ДМСО и БН-ДЭСО показывают, что имеют место конкурирующие гомо- и гетеромолекулярные взаимодействия. Установлено, также, значительное влияние длины углеводородной цепи компонентов на величины объемных параметров.
Исследование выполнено при финансовой поддержке КН РА в рамках научной программы базовой “Исследовательской лаборатории физической химии”.
Список литературы
Ghazoyan H.H., Grigoryan Z.L., Markarian S.A. // Chem. J. Armenia. 2017. V. 70. № 4. P. 462.
Ghazoyan H.H., Grigoryan Z.L., Gabrielyan L.S., Markarian S.A. // J. Mol. Liq. 2019. V. 284. P. 147.
Ghazoyan H.H. // Russ. J. Chem. & Chem. Tech. 2020. V. 63. № 2. P. 32−37.
Pagan O.R., Rowlands A.L., Urban K.R. // Neuroscience Letters. 2006. V. 407. P. 274.
Yu Z.W., Quinn P.J. // Biosci. Rep. 1994. V. 14. P. 259.
Jacob S.W., Herschler R. // Cryobiology. 1986. V. 24. P. 4.
Казоян Е.А., Терзян А.М., Маркарян Ш.А. // Журн. физ. химии. 2011. Т. 85. № 4. С. 689.
Markarian S.A., Bonora S., Bagramyan K.A. et al // Cryobiology. 2004. V. 49. P. 1.
Markarian S.A., Asatryan A.M., Grigoryan K.R. et al // Biopolymers. 2006. V. 82. P. 1–5.
Ritchie C.D., Pratt A.L. // J. Am. Chem. Soc. 1964. V. 86. P. 1571.
Fawcett W.R., Kloss A.A. // J. Phys. Chem. 1996. V. 100. P. 2019.
Fawcett W.R., Kloss A.A. // J. Chem. Soc. // Faraday Trans. 1996. V. 92. P. 3333.
Markarian S.A., Gabrielyan L.S., Bonora S. et al. // Spectrochim. Acta A. 2003. V. 59. P. 575.
Markarian S.A. // Patent of Republic of Armenia No 20010041. 2002.
Pratt L.R. // Annu. Rev. Phys. Chem. 1985. V. 36. P. 433.
Григорян З.Л., Казоян Е.А., Маркарян Ш.А. // Журн. физ. химии. 2015. Т. 89. № 10. С. 1588.
Nikam P.S., Jadhav M.C., Hasan M. // J. Chem. Eng. Data. 1996. V. 41. P. 1028.
Iloukhani H., Zarei H.A. // Phys. Chem. Liq. 2008. V. 46. P. 154.
Zarei H.A., Lavasani M.Z., Iloukhani H. // J. Chem. Eng. Data. 2008. V. 53. P. 578.
Ciocirlan O., Iulian O. // Ibid. 2012. V. 57. P. 3142.
Anouti M., Jacquemin J., Lemordant D. // Ibid. 2010. V. 55. P. 5719.
Redlich O., Kister A.T. // Ind. Eng. Chem. 1948. V. 40. P. 345.
Markarian S.A., Asatryan A.M., Zatikyan A.L. // J. Chem. Thermodyn. 2005. V. 37. P. 768.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


