Журнал физической химии, 2022, T. 96, № 8, стр. 1150-1154
Экстракция переходных металлов из солянокислых растворов полипропиленгликолем 425
М. И. Федорова a, А. В. Левина a, Ю. А. Заходяева a, *, А. А. Вошкин a
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Россия
* E-mail: yz@igic.ras.ru
Поступила в редакцию 03.12.2021
После доработки 28.12.2021
Принята к публикации 29.12.2021
- EDN: XVCWYW
- DOI: 10.31857/S0044453722080106
Аннотация
Предложено решение по переработке печатных плат, содержащих широкий ряд цветных и благородных металлов. Изучена экстракция ионов Ni(II), Zn(II), Al(III) и Fe(III) из кислых смешанных растворов в системе на основе полипропиленгликоля 425 и хлорида натрия. На основании состава печатных плат и экспериментальных данных по экстракции ионов цветных металлов из смешанных растворов при различном содержании хлорида натрия в системе разработана принципиальная технологическая схема переработки отработанных печатных плат. Представленная технологическая схема включает в себя последовательное кислотное выщелачивание металлов, экстракцию в экологически безопасной системе на основе полипропиленгликоля 425 и хлорида натрия, а также осаждение гидроксидов металлов, позволяющих осуществить комплексную переработку металлической фракции печатных плат.
Увеличение количества высокотехнологичных изделий, используемых в современном мире, а также стремление общества к приобретению более совершенных электронных устройств взамен устаревшим приводят к накоплению ненужной старой техники, требующей дальнейшей переработки. Одним из основных компонентов электронного оборудования являются печатные платы, необходимые для создания контакта между компонентами устройств. Состав печатных плат разнообразен и включает в себя металлическую (~30% от общей массы печатной платы) и неметаллическую фракции [1]. Наибольший интерес представляет переработка металлической фракции, поскольку она содержит в своем составе такие металлы, как Cu (10–80%), Al (0.7–10%), Zn (0.1–8%), Ni (0.2–3%), Fe (0.1–10%), Au (0.001–0.05%), Pd (0.01%), Pt (0.007%) [2–8]. Стоит отметить, что содержание благородных металлов в таких отходах сравнимо с их содержанием в рудах [9]. Таким образом, переработка отработанных печатных плат является решением проблемы загрязнения окружающей среды и повторного использования ценных металлов, что позволяет снизить нагрузку на добычу металлов из первичных источников.
К традиционным методам переработки отработанных печатных плат относят: сжигание, механическое, гравитационное, магнитное или электростатическое разделение [10], выщелачивание минеральными кислотами [11, 12] с введением окислителей [2, 13], комплексообразователей органического (например, тиомочевина [14], глицин [15]) или неорганического (цианаты щелочных металлов [16] и др.) происхождения, биовыщелачивание [17, 18] и последующее экстракционное разделение металлов из полученных растворов.
Одним из первых этапов переработки печатных плат является растворение твердого материала. Ввиду высокого содержания меди в данных изделиях и дороговизне золота значительная часть работ в настоящее время направлена на разработку способов получения концентратов данных металлов. Для отделения ионов Cu и Au от сопутствующих элементов (Ni, Zn, Al, Cd, Ag, Sn и др.) авторами [19] было предложено ступенчатое выщелачивание с последующей жидкостной экстракцией. На первой стадии выщелачивания (3М HNO3, 30°С, 120 мин) в раствор переходят Cu, Ni, Zn, Al, Cd, Pd, Pb; на второй стадии (3М H2SO4, 2М NaBr, 70°С, 60 мин) растворяются золото, олово и серебро. В работах [17, 19] была изучена экстракция ионов Cu и Au с использованием гидроксооксимов и замещенных амидов. Авторами было установлено, что из растворов выщелачивания, содержащих ионы Ni, Zn, Pb и др. Au и Cu могут быть извлечены количественно.
Альтернативным способом извлечения металлов из растворов выщелачивания печатных плат может являться экстракция в двухфазных водных системах, зарекомендовавших себя в качестве экологически безопасных экстракционных систем [20–26]. Так в работе [25] показана возможность комплексной экстракции металлов (Ni, Co, Mn, Cu, Zn, Al и Fe) в системе на основе полиэтиленгликоля 1500 и нитрата натрия, эффективность извлечения составляет более 60%. В работе [24] было изучено межфазное распределение ионов переходных металлов из нитратных и хлоридных сред в системе на основе катамина АБ с добавлением соляной, серной или азотной кислот. Было установлено, что Fe(III) извлекается более, чем на 90% за одну ступень экстракции в двухфазной водной системе на основе нитрата аммония и катамина АБ с добавлением серной кислоты. Авторами [23] было изучено межфазное распределение ионов Pt(IV) и Pd(II) в системе с полипропиленгликолем 425 (ППГ 425) и хлоридом натрия. Было установлено, что при содержании хлорида натрия в солевой фазе 3.2 моль/л достигается βPt/Pd = 71.5. В работе [26] показано, что золото количественно извлекается из кислых растворов выщелачивания электронных отходов с помощью системы на основе триблоксополимера L64 и сульфата лития.
В описанных выше работах для извлечения и разделения ионов металлов использовали экстракционные системы на основе водорастворимых полимеров и неорганических солей без введения дополнительных реагентов. В ряде работ [20, 22, 27–29] двухфазные водные системы показали себя не только как эффективные экстракционные системы, но и как экологически безопасная альтернатива органическим разбавителям, которые применяются в традиционных вариантах экстракции. Так, системы на основе полипропиленгликоля 425 [20, 22, 27] используются как разбавители для солей четвертичных аммониевых оснований и роданида калия и могут быть применены для решения задач извлечения и разделения ионов металлов Fe(III), Zn(II), Co(II), Ni(II), Al(III).
Таким образом, целью данной работы является исследование экстракции ионов Ni, Zn, Al и Fe в системе на основе полипропиленгликоля 425 и хлорида натрия для разработки технологической схемы переработки отработанных печатных плат.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для приготовления модельного раствора, состоящего из хлоридов никеля(II), цинка(II), алюминия(III) и железа(III), были взяты точные навески, взвешенные на аналитических весах AND HR-100AZ, соответствующих солей квалификации “х.ч.” в 1.4 М растворе соляной кислоты. Исходные концентрации ионов металлов в солевой фазе были выбраны на основании данных по элементному составу печатных плат [2] и представлены в табл. 1.
Таблица 1.
Исходные концентрации ионов металлов в солевой фазе, моль/л
| Ni | Zn | Al | Fe | Pt | Pd |
|---|---|---|---|---|---|
| 0.0211 | 0.0173 | 0.366 | 0.00487 | 4.2 × 10–4 | 3.0 × 10–3 |
Двухфазная водная система была приготовлена с использованием полипропиленгликоля 425 (Acros Organics) в концентрации 30 мас. % и хлорида натрия квалификации “х.ч.”.
Экстракцию ионов металлов проводили при температуре 25°С в градуированных центрифужных пробирках в термостатированном шейкере Enviro-Genie (Scientific Industries, Inc.) при скорости вращения 30 об./мин до установления термодинамического равновесия в течение 20 мин.
Концентрацию ионов Ni(II), Zn(II), Al(III), Fe(III) в исходном растворе и равновесных солевой и полимерной фазах после экстракции определяли методом атомно-эмиссионной спектрометрии с индуктивно связанной плазмой (Thermo Electron Corp., США).
Представленные экспериментальные данные являются результатом серии трех экспериментов и обработаны методами математической статистики.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Из литературы известно [30], что металлы способны растворяться в разбавленных растворах минеральных кислот. При растворении металлической фракции печатных плат в 2М соляной кислоте в раствор количественно переходят ионы Fe, Zn, Ni и Al. В твердом остатке остаются ионы Cu, Au, Pt и Pd. Далее осадок отфильтровывают и обрабатывают 3М раствором азотной кислоты, при этом в раствор переходит Cu. Далее растворение золота проводят по методике, описанной в [31] с использованием раствора тиомочевины (25–100 г/л) при рН = 0.5–2.0 при пропускании электрического тока. Твердый остаток, содержащий Pt и Pd, растворяют в 8М соляной кислоте с добавлением 30%-го раствора пероксида водорода при температуре 55°С в течение 2 ч со степенями извлечения 90 и 94%, соответственно [32]. В раствор переходят ионы Pt и Pd в виде комплексных металлокислот [32, 33]. Увеличением времени растворения может быть достигнуто количественное извлечение Pt и Pd. Платина и палладий из полученной смеси могут быть разделены осаждением хлоридом аммония. Предварительно раствор выщелачивания подвергается упариванию для удаления кислоты [32]. На рис. 1 представлена принципиальная схема осуществления последовательного растворения отработанных печатных плат. На основании предложенного ступенчатого выщелачивания печатных плат возникает задача разделения ионов Ni(II), Zn(II), Al(III) и Fe(III) в полученных растворах.
Ранее в работах [27, 34] было показано, что Fe и Zn в системе с полипропиленгликолем 425 и хлоридом натрия экстрагируются в виде анионных хлоридных комплексов. При этом ионы Al(III) и Ni(II) не извлекаются, поскольку находятся в растворе в виде катионных аквакомплексов. Поэтому экстракционная система на основе ППГ-425 и хлорида натрия позволяет отделить ионы Fe(III), Zn(II) от Al(III) и Ni(II).
На первом этапе экстракционного разделения нами было предложено решение по извлечению и концентрированию ионов цветных металлов и железа из 1.4 М солянокислого раствора выщелачивания. Поскольку ионы Fe(III) и Zn(II) экстрагируются по анионообменному механизму, нами было изучено межфазное распределение ионов Fe(III), Zn(II), Al(III) и Ni(II) из их смеси в экстракционной системе полипропиленгликоль 425 (30 мас. %) – хлорид натрия – вода в зависимости от содержания хлорида натрия (рис. 2). Из рис. 2 видно, что при содержании хлорида натрия в системе 10 мас. % степень извлечения ионов Fe(III) составляет 99.98% и Zn(II) – 83.3%, что указывает на возможность отделить ионы Fe(III) и Zn(II) от Al(III) и Ni(II) с высокими значениями коэффициентов разделения (табл. 2). Дальнейшее разделение пар Fe/Zn и Al/Ni может быть осуществлено путем осаждения гидроксидов металлов [35].
Таблица 2.
Коэффициенты разделения ионов металлов в системе полипропиленгликоль 425 (30 мас. %) – NaCl (10 мас. %) – Н2О, Т = 25°С
| Al(III) | Ni(II) | |
|---|---|---|
| Fe(III) | 2612 ± 130 | 2322 ± 116 |
| Zn(II) | 105 ± 5 | 90 ± 4 |
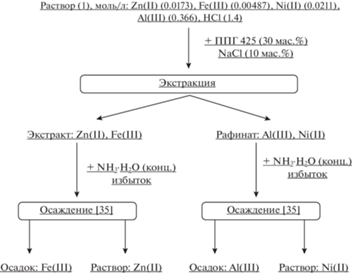
На основании полученных результатов и обработанного массива литературных данных нами была разработана принципиальная технологическая схема переработки отработанных печатных плат (рис. 3).
Таким образом, разработанная принципиальная технологическая схема решает задачу переработки отработанных печатных плат и позволяет разделить исследуемые металлы с получением их концентратов, используя экологически безопасные реагенты.
ЗАКЛЮЧЕНИЕ
В настоящей работе изучено межфазное распределение ионов Ni(II), Zn(II), Al(III), Fe(III) в двухфазной водной системе на основе полипропиленгликоля 425 и хлорида натрия. Показана возможность разделения ионов исследуемых металлов на индивидуальные компоненты путем введения экологически безопасного полимера без использования токсичных реагентов. Полученные экспериментальные данные по межфазному распределению ионов переходных металлов позволили создать оригинальную принципиальную технологическую схему переработки печатных плат, отличающуюся от существующих комплексным подходом, поскольку позволяют получить концентраты не только золота или меди, но и других стратегически важных металлов.
Исследование выполнено при финансовой поддержке Российского фонда фундаментальных исследований в рамках научного проекта № 18-29-24170 с использованием оборудования ЦКП ФМИ ИОНХ РАН.
Список литературы
Kumar A., Holuszko M.E., Janke T. // Waste Manag. 2018. V. 75. P. 94. https://doi.org/10.1016/j.wasman.2018.02.010
Huang Y.-F., Pan M.-W., Lo S.-L. // Resour. Conserv. Recycl. 2020. V. 163. P. 105090. https://doi.org/10.1016/j.resconrec.2020.105090
Segura-Bailón B., Lapidus G.T. // Hydrometallurgy. 2021. V. 203. P. 105699. https://doi.org/10.1016/j.hydromet.2021.105699
Zhao Q., Tong L., Kamali A.R. et al. // Ibid. 2020. V. 197. P. 105437. https://doi.org/10.1016/j.hydromet.2020.105437
Ilyas S., Ruan C., Bhatti H.N. et al. // Hydrometallurgy. 2010. V. 101. № 3−4. P. 135. https://doi.org/10.1016/j.hydromet.2009.12.007
Ilyas S., Srivastava R.R., Kim H., Ilyas N. // Chemosphere. 2022. V. 286. P. 131978. https://doi.org/10.1016/j.chemosphere.2021.131978
Li H., Eksteen J., Oraby E. // Resour. Conserv. Recycl. 2018. V. 139. P. 122. https://doi.org/10.1016/j.resconrec.2018.08.007
Rao M.D., Singh K.K., Morrison C.A., Love J.B. // Clean Eng. Technol. 2021. V. 4. P. 100180. https://doi.org/10.1016/j.clet.2021.100180
Wang H., Zhang S., Li B. et al. // Resour. Conserv. Recycl. 2017. V. 126. P. 209. https://doi.org/10.1016/j.resconrec.2017.08.001
Kaya M. // Waste Manag. 2016. V. 57. P. 64. https://doi.org/10.1016/j.wasman.2016.08.004
Yamane L.H., de Moraes V.T., Espinosa D.C.R., Tenório J.A.S. // Waste Manag. 2011. V. 31. № 12. P. 2553. https://doi.org/10.1016/j.wasman.2011.07.006
Barnwal A., Dhawan N. // Sustain. Mater. Technol. 2020. V. 25. P. e00164. https://doi.org/10.1016/j.susmat.2020.e00164
Kaya M. // Encyclopedia of Renewable and Sustainable Materials. 2020. V. 4. P. 677. https://doi.org/10.1016/B978-0-12-803581-8.11296-2
Birloaga I., Coman V., Kopacek B., Vegliò F. // Waste Manag. 2014. V. 34. № 12. P. 2581. https://doi.org/10.1016/j.wasman.2014.08.028
Mokhlis H., Drissi Daoudi R., Azzi M. // Mater. Today Proc. 2021. V. 37. P. 3973. https://doi.org/10.1016/j.matpr.2020.09.765
Debnath B., Chowdhury R., Ghosh S.K. // Front. Environ. Sci. Eng. 2018. V. 12. № 6. P. 2. https://doi.org/10.1007/s11783-018-1044-9
Akbari S., Ahmadi A. // Chem. Eng. Process – Process Intensif. 2019. V. 142. P. 107584. https://doi.org/10.1016/j.cep.2019.107584
Liu Q., Bai J., Gu W. et al. // Hydrometallurgy. 2020. V. 196. P. 105427. https://doi.org/10.1016/j.hydromet.2020.105427
Rao M.D., Singh K.K., Morrison C.A., Love J.B. // Sep. Purif. Technol. 2021. V. 263. P. 118400. https://doi.org/10.1016/j.seppur.2021.118400
Федорова М.И., Зиновьева И.В., Заходяева Ю.А., Вошкин А.А. // Теорет. основы хим. технологий. 2020. Т. 54. № 2. С. 202. https://doi.org/10.31857/S0040357120020037
Федорова М.И., Заходяева Ю.А., Зиновьева И.В., Вошкин А.А. // Изв. академии наук. Серия химическая. № 7. С. 1344. https://doi.org/10.1007/s11172-020-2908-2
Voshkin A.A., Zakhodyaeva Y.A., Zinov’eva I.V. // KnE Mater. Sci. 2020. P. 227. https://doi.org/10.18502/kms.v6i1.8072
Заходяева Ю.А., Зиновьева И.В. // Теорет. основы хим. технологий. 2021. Т. 55. № 2. С. 216. https://doi.org/10.31857/S0040357121020159
Исаева Ю.И., Елохов А.М., Денисова С.А. и др. // Журн. физ. химии. 2019. Т. 93. № 2. С. 220. https://doi.org/10.1134/S004445371902016X
Zakhodyaeva Y.A., Zinov’eva I.V., Tokar E.S., Voshkin A.A. // Molecules. 2019. V. 24. № 22. P. 4078. https://doi.org/10.3390/molecules24224078
Hespanhol M.C., Fontoura B.M., Quintão J.C., da Silva L.H.M. // J. Taiwan Inst. Chem. Eng. 2020. V. 115. P. 218. https://doi.org/10.1016/j.jtice.2020.10.027
Федорова М.И., Заходяева Ю.А., Вошкин А.А. // Теорет. основы хим. технологий. 2020. Т. 54. № 3. С. 304. https://doi.org/10.31857/S0040357120030021
Ferreira G.M.D., Hespanhol M.C., da Silva L.H.M., et al. // J. Mol. Liq. 2021. V. 327. P. 114803. https://doi.org/10.1016/j.molliq.2020.114803
Leite D. da S., Carvalho P.L.G., de Lemos L.R. et al. // Sep. Purif. Technol. 2019. V. 210. P. 327. https://doi.org/10.1016/j.seppur.2018.07.038
Wang Z., Guo S., Ye C. // Procedia Environ. Sci. 2016. V. 31. P. 917. https://doi.org/10.1016/j.proenv.2016.02.110
Аваева Т.И., Белов С.В., Середина Г.Д. Способ извлечения золота и серебра из полиметаллического сырья: Пат. 2258768 РФ // Бюл. 2005. № 23.
Ilyas S., Srivastava R.R., Kim H., Cheema H.A. // Sep. Purif. Technol. 2020. V. 248. P. 117029. https://doi.org/10.1016/j.seppur.2020.117029
Upadhyay A.K., Lee J., Kim E. et al. // J. Chem. Technol. Biotechnol. 2013. V. 88. № 11. P. 1991. https://doi.org/10.1002/jctb.4057
Заходяева Ю.А., Зиновьева И.В., Вошкин А.А. // Теорет. основы хим. технологий. 2019. Т. 53. № 5. С. 510. https://doi.org/10.1134/S0040357119050129
Лидин Р.А., Молочко В.А., Андреева Л.Л. Химические свойства неорганических веществ. М.: Химия, 2000. 480 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии