Физика металлов и металловедение, 2020, T. 121, № 1, стр. 53-59
Состав, структура и коррозионно-электрохимические свойства сплава медь–марганец после имплантации ионов аргона
О. Р. Бакиева a, *, И. К. Аверкиев a, Ф. З. Гильмутдинов a, А. А. Колотов a, Е. М. Борисова b, С. М. Решетников b
a Удмуртский Федеральный исследовательский центр УрО РАН
426000 Ижевск, ул. Т. Барамзиной, 34, Россия
b ФГБОУ ВО Удмуртский государственный университет
426034 Ижевск, ул. Университетская, 1, Россия
* E-mail: ftiran@mail.ru
Поступила в редакцию 06.03.2019
После доработки 13.08.2019
Принята к публикации 20.08.2019
Аннотация
Методами рентгеноэлектронной спектроскопии и рентгеноструктурного анализа исследованы химический состав и структура тонких поверхностных слоев сплава Cu80Mn20 до и после облучения ионами аргона в импульсно-периодическом режиме. Показано, что ионно-лучевое воздействие приводит к существенному перераспределению компонентов сплава на глубинах, превышающих среднюю длину проективного пробега ионов аргона. В поверхностной области облученного сплава Cu80Mn20 при относительной концентрации марганца, превышающей границу гомогенности твердого раствора (Cu, γMn), сохраняется ГЦК-структура с разными параметрами решетки по глубине. С помощью РФЭС показано накопление оксидных форм марганца на поверхности сплава, что приводит к улучшению его пассивационных характеристик. С этим обстоятельством можно связать повышение электрохимической активности сплава в реакции электровосстановления кислорода.
ВВЕДЕНИЕ
Известно, что адсорбционные, каталитические и коррозионно-электрохимические свойства металлических материалов определяются составом и свойствами поверхностных слоев. Особое место здесь занимают высокоэнергетические методы воздействия на металлические поверхности [1–5]. Характерно, что имплантация ионов инертных газов, например, аргона [4], не приводящая, естественно, к образованию каких-либо соединений атомов металла с молекулами этого инертного газа, вызывает изменения ряда физико-химических свойств меди. Как было показано [4], это связано с изменением состояния поверхности, ее разрыхлением, созданием неравновесных поверхностных структур, усилением адсорбционных свойств.
В этом аспекте определенный интерес представляют сплавы меди с марганцем. Их оксиды обладают уникальным сочетанием ряда физических, физико-химических и механических свойств, обусловливающих их широкое применение на практике [6]. При этом их каталитическая активность, коррозионная стойкость, контактное электросопротивление, механическая прочность и износостойкость во многом определяются составом и структурой поверхностных слоев. Одним из эффективных и широко применяемых методов поверхностной модификации материалов является ионная имплантация [2, 4, 5]. Как уже упоминали, радиационно-стимулированные процессы, связанные с ионно-лучевым перемешиванием, сегрегацией, генерацией дефектов, локальным разогревом, могут приводить к существенным изменениям состава, структуры и свойств поверхностных наноразмерных слоев [7]. Несмотря на многочисленные исследования обширного круга материалов [8–10], влияние ионнолучевого воздействия на сплавы системы Cu–Mn остается малоизученным. В данной работе исследованы химический состав и структура поверхностных слоев сплава Cu80Mn20 до и после облучения ионами аргона в импульсно-периодическом режиме. Изучено также влияние ионной модификации на коррозионно-электрохимическое поведение данного сплава. Для сравнения приведены некоторые результаты, касающиеся сплавов Cu–Mn с иным соотношением компонентов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Сплав Cu–Mn (твердый раствор) выплавлен в вакуумной индукционной печи в атмосфере аргона, без гомогенизирующего отжига. По данным рентгено-флуоресцентного анализа (спектрометр Inrov-X, α-2000 (USA)), состав сплава Cu80Mn20. Образцы сплава Cu80Mn20 в виде пластин 9 × 9 × × 2 мм были облучены ионами аргона в импульсно-периодическом режиме (энергия ионов 30 кэВ, плотность тока в импульсе 0.3 мА/см2, длительность импульса 1 мс, частота импульсов 200 Гц, флюенс 1017 ион/см2). Облучение проведено в ионном имплантпере с ионным источником ПИОН-1М при остаточном давлении в вакуумной камере имплантера 10–4 Па. Химический состав поверхностных слоев сплавов исследовали методом рентгеновской фотоэлектронной спектроскопии (РФЭС) на спектрометре SPECS с MgKα-возбуждением спектра фотоэлектронов. Экспериментальные данные обрабатывали с помощью пакета программ CasaXPS. Относительная погрешность измеренных концентраций элементов составляла 3%. Послойный РФЭС-анализ проведен с помощью распыления поверхности ионами аргона с энергией 4 кэВ при плотности ионного тока 30 мкА/см2. Средняя скорость травления составляла ~1 нм/мин. Рентгеноструктурный анализ тонких (~45–50 нм) приповерхностных слоев сплава Cu80Mn20 в геометрии скользящего пучка (0.1°) проведен на дифрактометре D8-Advance с использованием монохроматизированного CuKα-излучения.
КОРРОЗИОННО-ЭЛЕКТРОХИМИЧЕСКИЕ ИССЛЕДОВАНИЯ
Образцы до и после ионного облучения исследовали путем снятия анодных потенциодинамических кривых в нейтральной среде боратного буферного раствора (ББР) при pH 7.4 с помощью потенциостата Eco-Lab 2A-100, производства малого инновационного предприятия при Удмуртском государственном университете. Растворы готовили на дистиллированной воде. Аэрация растворов естественная, температура 20 ± 2°C. Использована стандартная электрохимическая ячейка ЯСЭ-2. Электрод сравнения – насыщенный хлорид–серебряный, относительно которого и приведены далее электродные потенциалы в тексте и на рисунках. Скорость сканирования потенциала при снятии потенциодинамических кривых 2 мВ/с.
До начала электрохимической поляризации образцы после погружения в ячейку с раствором выдерживали при катодном потенциале Е = –800 мВ в течение 15 мин. Такая катодная “тренировка” хотя и могла уменьшить концентрацию оксидных соединений на поверхности образцов, однако способствовала хорошей воспроизводимости получаемых далее поляризационных кривых, а также выявлению так называемых участков условно-активного или предпассивного растворения. После указанной выдержки при катодном потенциале включали анодную поляризацию. Катодный процесс в условиях естественно-аэрируемого нейтрального раствора связан с восстановлением растворенного в нем молекулярного кислорода [11, 12] по реакции
Учитывая достаточную буферную емкость ББР, изменением рН среды в ходе катодного процесса можно пренебречь [13, 14]. Анодный процесс преимущественно заключается в окислении поверхности медного сплава с образованием окисленных форм Cu и Mn. Потенциодинамические поляризационные кривые представляют собой вольтамперные характеристики сплава Cu–Mn после различных режимов облучения.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
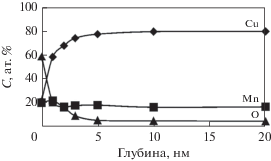
По данным РФЭС в исследованных образцах сплава Cu–Mn в исходном состоянии наблюдается снижение концентрации меди в сверхтонком (3 нм) поверхностном слое по сравнению с составом объема (рис. 1, рис. 2 – штриховые линии). В этом же слое концентрация кислорода достаточна для образования оксидов металлов. Вследствие селективного взаимодействия марганца с кислородом воздуха поверхностная оксидная пленка состоит преимущественно из марганца, окисленного до Mn2+ и, возможно, до Mn3+, а медь окислена до Cu+ лишь на самой поверхности. В более глубоких слоях (≥5 нм) соотношение C(Cu)/(C(Cu) + C(Mn)) (рис. 1) стремится к объемным значениям. Преимущественное самопроизвольное окисление поверхностных атомов марганца в сплаве Cu–Mn находится в соответствии с термодинамическими потенциалами образования оксидов этих металлов; ΔG(Cu2O) = –146.2; ΔG(CuO) = –127.1; ΔG(MnO) = –362.8 кДж/моль [13]. Как показано на рис. 3, для сплавов с содержанием меди 20 и 53 ат. % Cu на глубине около 10 нм наблюдается область, в которой относительная концентрация марганца превышает объемное значение. Концентрация кислорода снижается до 5–10 ат. % и находится на этом уровне по всей глубине анализа. Несмотря на низкую концентрацию, кислород, как и ожидалось, оказывает влияние на химическое состояние марганца, селективно взаимодействуя с ним.
Рис. 2.
Относительное содержание меди С(Сu)/(С(Cu) + С(Mn)) в поверхностных слоях сплавов Cu25Mn75 (1), Cu53Mn47 (2) Cu80Mn20 (3) в исходном состоянии (штриховые линии) и после имплантации ионов аргона (сплошные линии 1 ', 2 ', 3 ').
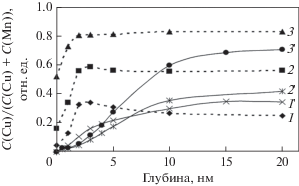
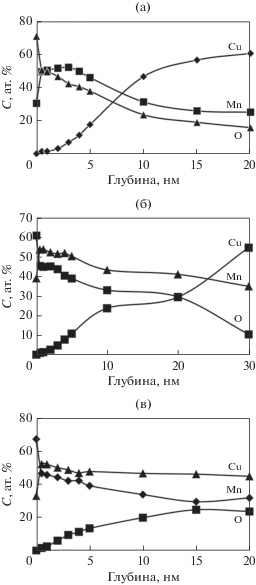
Рис. 3.
Распределение элементов в приповерхностных слоях сплава Cu80Mn20 (а), Cu53Mn47 (б) и Cu25Mn75 (в) после облучения ионами Ar+ в импульсно-периодическом режиме.
По данным рентгеноструктурного анализа в геометрии скользящего пучка поверхностный слой толщиной до 45 нм исходного образца сплава Cu80Mn20 имеет структуру ГЦК-твердого раствора (Cu, γMn) с параметром решетки 3.6908(5) Å. Признаки структуры оксидов методом РСА не выявлены. При этом в изначально однофазном поверхностном слое (толщиной до 45 нм) после ионного облучения сплава Cu80Mn20 ГЦК-структура сохраняется, но появляются два параметра решетки: а = 3.695(1) и 3.671(3) Å.
Структура с более высоким параметром решетки соответствует приповерхностной области сплава с повышенным содержанием марганца, а структура с меньшим параметром решетки – более удаленной от поверхности области с пониженным его содержанием. При удалении от поверхности наблюдается уменьшение полуширины дифракционных линий, что связано с ростом размеров областей когерентного рассеяния. Таким образом, данные РСА подтверждают данные РФЭС о неоднородном составе приповерхностной области по содержанию компонентов сплава. Признаков оксидных структур методом РСА не обнаружено, несмотря на то, что по данным РФЭС на поверхности присутствует значительное количество кислорода. Это можно объяснить тем, что оксиды локализованы в тонком поверхностном слое, глубина которого гораздо меньше глубины анализа РСА, и/или сформированные оксиды имеют наноразмерные масштабы, что приводит к их рентгеноаморфности.
Согласно фазовой диаграмме состояний системы Cu–Mn, граница твердого раствора (Cu, γMn) при температурах ниже 873 К располагается вблизи 30 ат. % марганца. В тонких пленках Cu–Mn, полученных магнетронным распылением в высоком вакууме, положение границы гомогенности ГЦК-твердого раствора соответствует 35 ат. % Mn, при этом в интервале С(Mn) = 35–45 ат. % обнаружено двухфазное состояние [4]. В данной работе, несмотря на высокое относительное содержание марганца в приповерхностной области облученного сплава Cu80Mn20, рентгеноструктурный анализ при малых углах не выявил признаков структур, отличных от ГЦК-твердого раствора (Cu, γMn), в том числе структуры на основе низкотемпературной фазы α-Mn или оксидов марганца в чистом виде. Полученные результаты позволяют говорить об эффекте сохранения ГЦК-структуры при ионной имплантации с образованием областей с разным содержанием марганца, в том числе с образованием областей упорядочения (MnCu3). Радиационно-стимулированная сегрегация способствует обогащению приповерхностной области марганцем, но при этом процесс ионно-лучевого перемешивания, по-видимому, предотвращает выделение фаз, характерных для сплава с высоким содержанием марганца, в частности – αMn. В целом сохранение ГЦК-структуры в приповерхностной области при относительно высокой концентрации марганца в этой области может быть связано с неравновесными условиями вблизи поверхности, возникающими в процессе ионной имплантации. Повышенное содержание кислорода может являться дополнительным фактором стабилизации ГЦК структуры, поскольку эта же структура характерна для низшего оксида марганца.
По данным РФЭС (рис. 4), для Mn2p и Cu2p3/2, а также оже-спектра Cu LVV, марганец в поверхностной области селективно взаимодействует с кислородом, при этом медь преимущественно находится в неокисленном состоянии.
Рис. 4.
РФЭС-спектры Mn2p (а), Сu2p3/2 (б) поверхностных слоев сплава Cu80Mn20 после имплантации ионов Ar+. 1 – поверхность, 2 – глубина 1 нм, 3 – глубина 3 нм, 4 – глубина 20 нм.
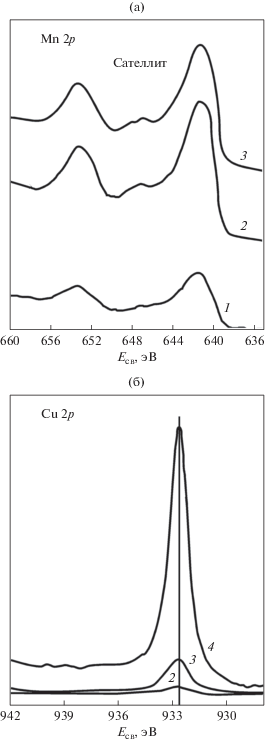
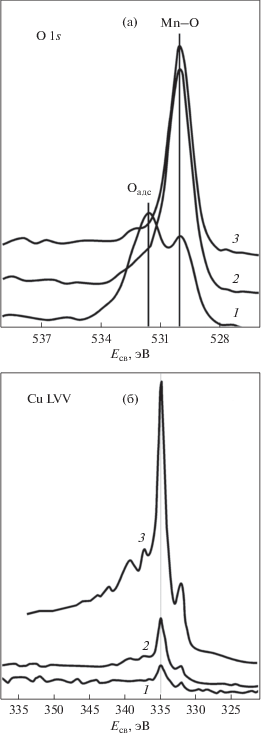
Из РФЭС данных (рис. 4, 5) видно, что в поверхностных слоях марганец окислен, при этом наличие сателлита на Есв = 646 эВ говорит о значительном количестве марганца в степени окисления +2. Признаки металлического марганца начинают проявляться лишь после 15 мин ионного травления ионами аргона с энергией 4 кэВ. Медь вблизи поверхности определяется в очень малых количествах, при этом преимущественно находится в металлическом состоянии: Есв Cu2p3/2 = 932.6 эВ. Параметры оже-спектра Cu LVV соответствуют металлической меди. На поверхности до травления кислород наблюдается в двух состояниях: адсорбированный (531.8 эВ) и в химической связи с марганцем (530.1–530.3 эВ). Адсорбированная компонента исчезает при ионном травлении в течение 0.5 мин. Т.е. слой адсорбированного кислорода очень тонкий и быстро удаляется, а весь внедренный кислород взаимодействует с марганцем.
Рис. 5.
РФЭС-спектры О1s (а) и Сu LVV (б) поверхностных слоев сплава Cu80Mn20 после имплантации ионов Ar+. 1 – поверхность, 2 – глубина 1 нм, 3 – глубина 3 нм, 4 – глубина 20 нм.
Внедрение кислорода в приповерхностные слои сплавов Cu–Mn может происходить как непосредственно в процессе ионнолучевой обработки из остаточной среды вакуумной камеры [5], так и в результате взаимодействия поверхности сплава с кислородом при последующем пребывании на воздухе после прекращения ионного облучения [6]. Внедрению кислорода может способствовать возрастание концентрации дефектов в приповерхностной области сплава в результате облучения.
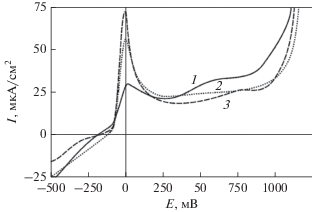
На рис. 6 предоставлены вольт-амперные характеристики сплава Cu80Mn20 в исходном состоянии и после облучения ионами аргона. Для определения тенденции изменения электрохимических свойств под воздействием ионного облучения приведены результаты электрохимических испытаний образцов, облученных с вариацией флюенса ионов: D = 5 × 1016 ион/см2 и D = 1017 ион/см2, энергия ионов составляла Е = 30 кэВ. Рассмотрим анодные участки кривых. Можно видеть, что на исходном образце имеется непродолжительная область предпассивного растворения сплава, максимальный ток при этом достигает 26 мкА/см2. Далее следует область пассивации, для которой характерен ток 24–27 мкА/см2 Приблизительно при потенциале 850–880 мВ наступает перепассивация и анодный ток вновь нарастает.
Рис. 6.
Потенциодинамические поляризационные кривые сплава Cu80Mn20 в ББР при pH 7.4. Сплав в исходном состоянии (1), облучение при Е = 30 кэВ, D = 5 × 1016 ион/см2 (2), облучение при Е = 30 кэВ, D = 1017 ион/см2.
Такой ход кривой анодной поляризации в нейтральных средах характерен для сплавов меди с более электроотрицательными металлами (бронза, латунь) [1, 4, 15]. Термодинамическую вероятность окисления металлов в электролитах можно приближенно оценить по величине нормального электродного потенциала [11]: $E_{{{{{\text{C}}{{{\text{u}}}^{{2 + }}}} \mathord{\left/ {\vphantom {{{\text{C}}{{{\text{u}}}^{{2 + }}}} {{\text{Cu}}}}} \right. \kern-0em} {{\text{Cu}}}}}}^{0}$ = = 0.34 В; $E_{{{{{\text{C}}{{{\text{u}}}^{ + }}} \mathord{\left/ {\vphantom {{{\text{C}}{{{\text{u}}}^{ + }}} {{\text{Cu}}}}} \right. \kern-0em} {{\text{Cu}}}}}}^{0}$ = 0.521 В; $E_{{{{{\text{M}}{{{\text{n}}}^{{2 + }}}} \mathord{\left/ {\vphantom {{{\text{M}}{{{\text{n}}}^{{2 + }}}} {{\text{Mn}}}}} \right. \kern-0em} {{\text{Mn}}}}}}^{0}$ = –1.18 В; $E_{{{{{\text{M}}{{{\text{n}}}^{{3 + }}}} \mathord{\left/ {\vphantom {{{\text{M}}{{{\text{n}}}^{{3 + }}}} {{\text{Mn}}}}} \right. \kern-0em} {{\text{Mn}}}}}}^{0}$ = –1.51 В; $E_{{{{{\text{M}}{{{\text{n}}}^{{4 + }}}} \mathord{\left/ {\vphantom {{{\text{M}}{{{\text{n}}}^{{4 + }}}} {{\text{Mn}}}}} \right. \kern-0em} {{\text{Mn}}}}}}^{0}$ = –1.84 В. Приведенные величины стандартных окислительно-восстановительных потенциалов указывают на вероятность окисления Mn до более высоких стадий окисления, чем это следует из данных РФЭС-анализа. Очевидно, что вероятность окисления марганца выше, чем меди. Именно этим процессом в первом приближении и определяется в целом кинетика анодного процесса на сплаве Cu80Mn20. Можно полагать, что после достижения критического потенциала и перехода в пассивное состояние процесс определяется накоплением на поверхности частиц, формирующих пассивную пленку. В данном случае, с учетом высокой термодинамической вероятности окисления более электроотрицательного марганца и нерастворимости продуктов его окисления, можно полагать, что в основном это оксиды (гидроксиды) марганца. После достижения потенциала перепассивации происходит разрушение пассивной пленки и появляется возможность перехода в раствор также и ионов меди.
Как следует из хода кривых 2 и 3 (рис. 6), облучение ионами аргона ускоряет процесс растворения сплава в условно активной (предпассивной) области. При этом с ростом дозы облучения анодный ток в этой области возрастает. Можно полагать, что разрыхление поверхности, селективный выход в поверхностный слой марганца способствуют росту анодного процесса. Однако после достижения критического потенциала, когда поверхность переходит в пассивное состояние, картина меняется на обратную. Чем выше доза облучения, тем глубже слой оксидных форм металлов, ответственных за переход поверхности в пассивное состояние. Заметим, что после облучения существенно возрастает и потенциал перепассивации – Епп (от Епп = 850 мВ для исходного образца, до Епп = 1000–1100 мВ для облученных). Таким образом, можно считать, что в данном случае облучение ионами аргона может привести к повышению коррозионной стойкости сплава Cu80Mn20, т.е. улучшению его пассивационных свойств.
Рассмотрим катодные участки вольтамперных кривых, которые на рис.6 приведены лишь частично. Как уже отмечалось, в нейтральных не деаэрированных средах катодный процесс может быть связан преимущественно с восстановлением кисорода, растворенного в электролите. Учитывая, что после ионной имплантации аргона возрастает концентрация оксидных форм (преимущественно марганца), часть катодного тока может быть связана с восстановлением кислорода, находящегося в поверхностном слое в связанном или хемосорбированном состоянии. Однако отметим, что перед началом снятия вольт-амперных кривых электроды проходили довольно длительную катодную поляризацию при Е = –800 мВ. Это, вероятнее всего, способствовало удалению, по крайней мере, легко восстанавливаемых оксидных форм на поверхности. Катодные участки вольт-амперных кривых при потенциалах от –100 до –500 мВ можно связать с электрохимическим восстановлением кислорода, имеющегося в электролите. Отметим, что представленная на рис.6 область катодных токов и потенциалов далека от области перехода процесса восстановления кислорода в диффузионный режим. В связи с этим можно считать, что представленные участки катодных кривых отвечают электрохимической (или электрокаталитической) активности исследуемых электродов. Из представленных катодных кривых следует, что облучение ионами аргона приводит к снижению перенапряжения восстановления кислорода, т.е. к росту плотности катодного тока при заданном потенциале. Так, например, при Е = –250 мВ плотность катодного тока для образца в исходном состоянии равна 2 мкА/см2, а после облучения флюенсами 5 × 1016 и 1017 ион/см2 – 4 и 2 мкА/см2 соответственно. Можно полагать, что в данном случае облучение разрыхляет поверхность сплава, что способствует увеличению уровня поверхностной энергии. Кроме того, учитывая, что катодное восстановление кислорода идет через образование оксидных форм металла [11], которые и являются активными электрокаталитическими центрами, образование таких оксидных форм в ходе ионной имплантации приводит к росту концентрации указанных активных центров и увеличению скорости электровосстановления кислорода. Таким образом, электрохимическая активность сплава Cu80Mn20 изменяется под влиянием ионной имплантации аргона и в случае проведения катодного электрохимического процесса.
ВЫВОДЫ
Облучение поверхности сплавов системы Cu‒Mn ионами аргона в импульсно-периодическом режиме с энергией 30 кэВ, дозой 1017 ион/см2 приводит к формированию неоднородного по составу и структурному состоянию приповерхностного слоя, глубина которого превышает средний проективный пробег ионов. Во всех случаях обнаружено обогащение приповерхностного слоя сплавов Cu–Mn марганцем, связанное с его селективным окислением и радиационно-индуцированной сегрегацией [7, 16]. Сохранение ГЦК-структуры в приповерхностной области при относительной концентрации марганца вблизи поверхности выше границы гомогенности твердого раствора (Cu, γMn) предположительно связано с неравновесным структурным состоянием поверхностного слоя, формируемым в процессе ионной имплантации.
На примере сплава Cu80Mn20 показано, что изменение структуры и состава поверхности, в частности, увеличение концентрации оксидных состояний марганца и, возможно, хемисорбированного кислорода, приводит к улучшению пассивационных характеристик сплава, что открывает возможность увеличения его коррозионной стойкости.
Накопление в ходе облучения оксидных форм на поверхности сплава повышает его электрокаталитическую активность в отношении реакции электрохимического восстановления кислорода.
Работа выполнена в рамках государственного задания МИНОБРНАУКИ России (тема № АААА-А17-117022250040-0) при частичной поддержке проекта РФФИ № 14-02-31488 и проекта Президиума РАН № 18-10-2-25.
Список литературы
Колотыркин В.И., Княжева В.М. Возможности высокоэнергетических методов обработки поверхностей металлов для защиты от коррозии // Защита металлов. 1991. Т. 27. № 2. С. 184–186.
Васильев В.Ю., Бетуганов М.А., Исаев Н.И., Кузьменко Т.Г., Яковлев В.Б., Шумилов В.Н. Влияние ионной имплантации на ЭХ характеристики сплавов // Защита металлов. 1981. Т. XVII. № 5. С. 543–545.
Паршутин В.В., Пышкин С.Л. Исследование свойств модифицированной поверхности сталей // Защита металлов. 1994. Т. 30. № 3. С. 276–281.
Решетников С.М., Гильмутдинов Ф.З., Борисова Е.М., Бакиева О.Р., Воробьев В.Л. Влияние имплантации кислорода на коррозионно-электрохимические свойства меди // Коррозия: материалы, защита, 2017. № 9. С. 21–30.
Сурнин Д.В., Воробьев В.Л., Гильмутдинов Ф.З., Мухгалин В.В., Бакиева О.Р., Колотов А.А., Ветош-кин В.М. Исследование химического состава и атомной структуры поверхности медно-марганцевого сплава после модификации ионами кислорода // Поверхность. Рентгеновские, синхротронные и нейтронные исследования, 2016. № 4. С. 74–79.
Двойные и многокомпонентные системы на основе меди / Под ред. Шухардина С.В. М.: Наука, 1979. 248 с.
Васильев М.А., Шалаев М.А. Радиационно- и термостимулированная поверхностная сегрегация// Металлофизика. 1988. Т. 10. Вып. 2. С. 64.
Губернаторов В.В. и др. Влияние ионного облучения и магнитного поля на первичную рекристаллизацию металлов // ФММ. 2009. Т. 107. № 1. С. 73.
Дмитриев В.В. и др. Взаимодействие внедренных атомов и конфигурационный вклад в их термодинамическую активность в V, Nb и Ta // ФММ. 2017. Т. 118. № 2. С. 111.
Катаев В.А. и др. Воздействие ионного облучения на процесс нанокристаллизации и магнитные свойства магнитомягкого сплава FeCuNbMoSiB // ФММ. 2017. Т. 118. № 2. С. 158.
Скорчеллетти В.В. Теоретические основы коррозии металлов. Л: Химия, 1973. 264 с.
Семенова И.В., Флорианович Г.М., Хорошилов А.В. Коррозия и защита от коррозии. М.: Физматлит, 2002. 336 с.
Wagman D.D., Evans W.H., Parker V.B., Schumm R.H., Halow I., Bailey S.M., Churney K.L., Nuttall R.L. The NBS Tables of Chemical of Chemical Thermodynamic Properties // J. Phys. Chem. Ref. Data. 1982. V. 11. Suppl. 2.
Справочник по электрохимии / Под ред. Сухотина А.М. Л.: Химия, 1981. 488 с.
Маршаков И.К. Анодное растворение и селективная коррозия сплавов. Воронеж: Изд-во Воронежского университета, 1988. 208 с.
Нефедов В.И., Черепин В.Т. Физические методы исследования поверхности твердых тел М.: Наука, 1983. 295 с.
Дополнительные материалы отсутствуют.
Инструменты
Физика металлов и металловедение