Генетика, 2019, T. 55, № 6, стр. 707-713
Исследование ассоциации между грудным вскармливанием и метилированием ДНК в клетках периферической крови младенцев
О. Ю. Наумова 1, 2, 3, *, В. В. Одинцова 2, 4, И. А. Аринцина 2, С. Ю. Рычков 1, Р. Ж. Мухамедрахимов 2, Ю. В. Шнейдер 1, А. Н. Грошева 1, О. В. Жукова 1, Е. Л. Григоренко 2, 3
1 Институт общей генетики им. Н.И. Вавилова Российской академии наук
119991 Москва, Россия
2 Санкт-Петербургский государственный университет, лаборатория междисциплинарных исследований
развития человека
119034 Санкт-Петербург, Россия
3 Техасский институт измерения, оценки и статистики, Хьюстонский университет
77204 Хьюстон, США
4 Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии
им. академика В.И. Кулакова
117198 Москва, Россия
* E-mail: oksana.yu.naumova@gmail.com
Поступила в редакцию 08.10.2018
После доработки 10.11.2018
Принята к публикации 13.12.2018
Аннотация
Представлены данные об ассоциации грудного вскармливания с метилированием ДНК в клетках периферической крови 37 детей в возрасте от 9 мес. до четырех лет. Полногеномные профили метилирования ДНК изучались с помощью биочипа высокой плотности Illumina MethylationEPIC. Поиск полно-эпигеномных ассоциаций позволил выявить связь между продолжительностью грудного вскармливания и уровнем метилирования 4276 CpG-сайтов: положительную ассоциацию для 2201 и отрицательную – для 2075 сайтов. В контексте геномной аннотации эти СpG-сайты были отнесены к 2635 генам. Среди функций, контролируемых этими генами, преобладают связанные с сигнальными клеточными системами, с развитием анатомических структур и клеток и в первую очередь – с развитием и функционированием иммунной системы и ЦНС. По результатам анализа предположена особая роль окситоцинового сигнального пути как одного из возможных триггеров слаженных эпигенетических изменений в генах, контролирующих функции ЦНС, в ответ на грудное вскармливание.
Известно, что грудное вскармливание оказывает положительное влияние не только на здоровье и развитие ребенка в младенческом и младшем детском возрасте, но и имеет долгосрочные эффекты на протяжении всей жизни [1]. Сегодня, в эру “омики”, активно обсуждается существование эпигенетических эффектов вскармливания грудным молоком, а именно – изменений в метилировании геномной ДНК (см., например, [2, 3]). Интерес к этому направлению исследований достаточно высок. Так, согласно одному из последних систематических обзоров литературы [4], на запрос “epigenetics breastfeeding” в поисковой системе Google на 2017 г. приходилось свыше 110 тыс. обращений и было найдено свыше 5 тыс. релевантных публикаций. Однако после тщательной их фильтрации и изучения авторами [4] было обнаружено лишь семь публикаций, в которых представлены результаты эмпирических исследований, где грудное вскармливание рассматривается как целевой фенотип или, гораздо чаще, как одна из значимых ковариат, а именно – один из факторов ранней среды развития.
Из этих семи работ пять были выполнены на человеке [5–9]. При этом они были крайне разнообразны в отношении выборок исследований, возраста когорты (средняя варьирует от 0 [9] до 57.5 [6] лет), исследуемой ткани (пуповинная [9] и периферическая кровь [5, 7–9], раковые клетки [6]), геномных мишеней метилирования и методов его оценки (отдельные CpG-сайты и гены [5, 6, 9] и полногеномный анализ [7, 8]) и категоризации грудного вскармливания (целевой фенотип [5] и ковариата [6–9]). По результатам этих исследований следует отметить следующее. У младенцев была установлена связь между продолжительностью грудного вскармливания и понижением уровня метилирования в промоторе лептина (LEP) – гормона, регулирующего энергетический обмен [5]. На когорте подростков был показан отдаленный модулирующий эффект грудного вскармливания на метилирование ряда CpG-сайтов в локусе 17q21 [8]. Также в качестве отдаленных эпигенетических эффектов было обнаружено, что отсутствие грудного вскармливания в младенчестве может быть связано с повышением метилирования промотора гена-супрессора опухолевого роста CDKN2A в пременопаузальных опухолях молочной железы [6].
Таким образом, недавние исследования предоставляют данные о потенциальном влиянии грудного вскармливания на метилирование геномной ДНК, которое, в свою очередь, может являться медиатором широкого спектра долгосрочных эффектов для развития и здоровья. Тем не менее работы эти крайне немногочисленны и, за редким исключением, они не фокусируются конкретно на факторе грудного вскармливания. Это определяет актуальность и новизну нашего исследования по поиску полно-эпигеномных ассоциаций с грудным вскармливанием и его продолжительностью.
МАТЕРИАЛЫ И МЕТОДЫ
Представленная здесь работа была выполнена на выборке из контрольной когорты детей, вовлеченных в исследование био-поведенческих эффектов ранней социальной депривации (грант № 14.Z50.31.0027), – это типично развивающиеся дети из полных семей со средним уровнем дохода, проживающих в г. Санкт-Петербург (N = 37; 20 девочек и 17 мальчиков в возрасте от 9 мес. до четырех лет; рис. 1,а). Источником информации о детях являлись медицинские карты, результаты когнитивно-поведенческого обследования детей [10] и опросы матерей. Критерии исключения из выборки были следующими: осложнения беременности и родов, задержки внутриутробного развития, наличие у ребенка врожденных патологий, тяжелых хронических и системных заболеваний. Продолжительность грудного вскармливания детей варьировала на момент их обследования от 0 до 34 мес., временной интервал между прекращением кормления грудью и обследованием ребенка составлял от 0 до 38.5 мес. (рис. 1,а), как следствие продолжительность грудного вскармливания не имела значимой корреляции с возрастом детей: r = 0.198; p = 0.109, в то время как интервал после прекращения кормления был высоко скоррелирован с возрастом: r = 0.746; p < 0.001. Статистически достоверных различий между девочками и мальчиками по демографическим показателям и показателям грудного вскармливания не наблюдалось.
Рис. 1.
Распределение выборочных показателей (а); слева направо: возраст, продолжительность грудного вскармливания и временной интервал между прекращением грудного кормления и обследованием ребенка; все показатели (ось абсцисс) приведены в мес.; на оси ординат отмечено число наблюдений. Распределение индивидов в пространстве первых двух ГК, вычисленных на основе распределения шести типов клеток крови, PCcells (б), и изменчивости показателей уровня метилирования 4276 CpG-сайтов, PCDNAme (г); пол ребенка отмечен цветом кружка: белый для мальчиков и серый для девочек; цифрами (в мес.) отмечены продолжительность грудного вскармливания и возраст ребенка (в скобках). График корреляции индивидуальных распределений шести типов клеток: гранулоцитов (Gran), CD4+ и CD8+ Т-лимфоцитов (CD4T и CD8T), В-лимфоцитов (Bcell), моноцитов (Mono) и NK-клеток (NK) с возрастом детей (в); для достоверных корреляций линия регрессии показана черным. Графики линейной регрессии, показывающие высокую положительную корреляцию первой ГК индивидуальной изменчивости уровня метилирования 4276 CpG-сайтов (PC1DNAme) и продолжительности грудного вскармливания в мес. (д) и второй ГК изменчивости метилирования (PC2DNAme) с первой ГК совокупной изменчивости клеточного состава крови (PC1cells) (е). Коэффициенты корреляции и детерминации приведены в тексте.
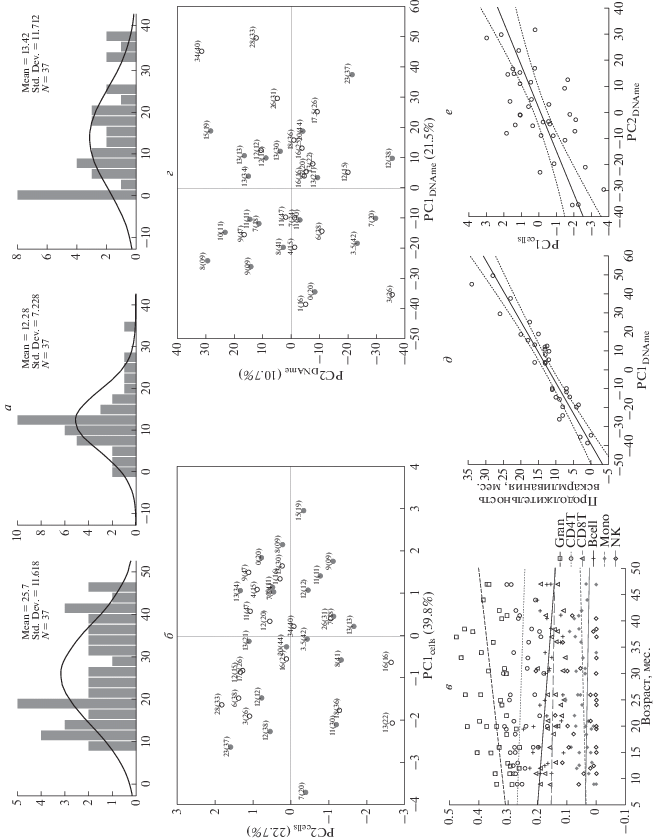
Полногеномные профили метилирования ДНК из периферической крови детей были получены с помощью микрочипа Illumina Infinium MethylationEPIC, который включает в себя свыше 860 тыс. проб для анализа уровня метилирования CpG-сайтов, расположенных в 96% известных CpG-островков (CGI), и сайтов за пределами CGI; панель EPIC покрывает около 99% RefSeq генов. Геномная ДНК была изолирована из 0.5–1 мл крови с помощью набора реагентов FlexiGene®DNA (Qiagen); бисульфитную конверсию ДНК проводили по протоколу Illumina с использованием набора EZ DNA Methylation (Zymo Research). Для обработки и анализа данных использовали R-пакет Minfi [11]; нормализацию сигналов с чипа проводили методом стратифицированной квантильной нормализации. Данные были отфильтрованы в соответствии со следующими критериями: уровень надежности детекции пробы (p < 0.05), ее хромосомная локализация (аутосомы) и отсутствие известных полиморфных вариантов в CpG-сайте (maf > 0.05). По результатам фильтрации оставалось 805 тыс. проб, из которых, в свою очередь, были исключены пробы, показавшие низкую (SDbeta < 0.05) межиндивидуальную вариабельность уровня метилирования; оставшиеся 102 368 проб были включены в последующий анализ.
Анализ ассоциации уровня метилирования CpG-сайтов с целевым фенотипом проводили на основе матрицы значений относительных уровней метилирования проб (бета-значения) и с помощью методов частной корреляции и линейной регрессии, при контроле эффектов пола и возраста ребенка и клеточной гетерогенности образцов крови, имеющих известный и значимый эффект на профили метилирования ДНК [12, 13], а также с помощью анализа главных компонент (далее ГК), вычисленных на основе корреляционных матриц. Индивидуальные распределения типов клеток (гранулоцитов, CD4+ и CD8+ Т-лимфоцитов, В-лимфоцитов, моноцитов и NK-клеток) оценивали с помощью алгоритма [13], разработанного для оценки клеточного состава крови из метиломов на основе эмпирических данных [14].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Выявленное распределение типов клеток не показало значимой связи с полом ребенка, как это видно из распределения индивидов в пространстве первых ГК (рис. 1,б) изменчивости индивидуальных частот типов клеток (далее PCcells). Однако наблюдались статистически значимые корреляции с возрастом детей, а именно – возрастание числа гранулоцитов, r = 0.408; p = 0.012, и убывание B-лимфоцитов, r = –0.399; p = 0.014 (рис. 1,в). При этом грудное вскармливание не привнесло значимого вклада в выявленные ассоциации: r = 0.412; p = 0.014 и r = –0.378; p = 0.032, для гранулоцитов и B-клеток соответственно. Следует отметить, что возможно в силу малой величины выборки продолжительность грудного вскармливания не показала значимой связи с иммуно-фенотипом (или клеточным составом крови) ребенка, ожидаемой, исходя из релевантных данных о различных темпах развития врожденного иммунитета у младенцев с различными, естественным и искусственным, типами вскармливания [15].
По результатам корреляционного анализа уровни метилирования 4276 CpG-сайтов показали статистически достоверную (2201 сайт – положительную, Rpartial = 0.361–0.760, и 2075 сайтов – отрицательную, Rpartial = –0.361–0.760; при p < 0.05) ассоциацию с продолжительностью грудного вскармливания. На рис. 1,г представлено распределение индивидов в пространстве первых двух ГК изменчивости уровня метилирования (бета-значений) 4276 CpG-сайтов (далее PCDNAme). По результатам анализа корреляции PC1DNAme и PC2DNAme, описывающих 21.5 и 10.7% изменчивости соответственно, с демографическими переменными (пол и возраст детей), частотами типов клеток и генеральными показателями совокупной их изменчивости (PCcells), а также с показателями грудного вскармливания, были получены следующие данные. Во-первых, изменчивость уровня метилирования рассматриваемых сайтов не показала значимой связи с полом и возрастом детей. Во-вторых, PC1DNAme была высоко скоррелирована с продолжительностью грудного вскармливания ребенка: r = 0.928; $r_{{{\text{adj}}}}^{2}$ = 0.858; p < 0.001 (рис. 1,д). Это, в свою очередь, подтверждает достаточно высокую степень надежности ассоциаций, выявленных методом частных корреляций, а также указывает на то, что как минимум 20% совокупной изменчивости уровня метилирования выявленных сайтов может быть обусловлено грудным вскармливанием и его длительностью. И, в-третьих, около 10% изменчивости метилирования (PC2DNAme) может быть связано, в первую очередь, с индивидуальной клеточной вариабельностью (PC1cells): r = 0.665; $r_{{{\text{adj}}}}^{2}$ = 0.426; p < 0.001 (рис. 1,е), причем эта корреляция значительно возрастает при учете такого фактора, как грудное вскармливание и его продолжительность: r = 0.794; $r_{{{\text{adj}}}}^{2}$ = 0.630; p < 0.001. Последнее свидетельствует о наличии связи грудного вскармливания с клеточным составом крови детей, не выявленном в предыдущем анализе на значимом пороге статистической достоверности.
В вышеизложенном анализе CpG-сайты рассматривались как независимые маркеры. В последующем анализе 4276 сайтов были рассмотрены в контексте их кометилирования, геномной колокализации и функций генов, с которыми они связаны. Геномное аннотирование сайтов было проведено согласно манифесту EPIC (Illumina) и в соответствии с БД UCSC [16] и GENCODE [17]. Поиск перепредставленных характеристик регуляторных элементов и генов проводили с использованием интегративных БД и аналитических ресурсов: DAVID [18], Enrichr [19] и g:Profiler [20].
По результатам геномной аннотации выявленные 4276 CpG-сайтов были связаны с 2635 генами. В контексте регуляторных геномных регионов (CGI и их фланкирующих регионов, генных промоторов и энхансеров, сайтов связывания факторов транскрипции и др.) выявленный список СpG не был значимо обогащен конкретными регуляторными регионами в сравнении с массивом таковых, представленных в панели EPIC. В то же время ряд биологических процессов и путей были найдены статистически перепредставленными в списке 2635 генов. Среди биологических процессов, определенных в терминах Генной Онтологии, GO [21], это процессы, связанные с сигнальными клеточными системами и их регуляцией, с развитием анатомических структур и клеток и в первую очередь с нервной и иммунной системами (табл. 1). Результаты анализа перепредставленности биологических путей KEGG [22] и PANTHER [23] также указывают на значимое обогащение списка из 2635 генов функциями, связанными с сигнальными системами, и функциями, связанными с активностью иммунной (диабет, реакция отторжения трансплантата, вирусные инфекции) и нервной (синапсы) систем (табл. 1).
Таблица 1.
Результаты анализа статистической перепредставленности биологических процессов и биологических путей среди таковых, контролируемых генами, чье метилирование ассоциированно с грудным вскармливанием и его продолжительностью
| Идентификационный код | Биологические процессы | PFDR |
|---|---|---|
| GO:0007399 | Развитие нервной системы | 2.80E-15 |
| GO:0048856 | Развитие анатомических структур | 1.40E-13 |
| GO:0048468 | Развитие клеток | 3.30E-12 |
| GO:0009653 | Морфогенез анатомических структур | 2.79E-11 |
| GO:0000902 | Морфогенез клеток | 1.74E-08 |
| GO:0022008 | Нейрогенез | 1.80E-07 |
| GO:0007155 | Клеточная адгезия | 4.46E-07 |
| GO:0030182 | Дифференциация нейронов | 1.72E-06 |
| GO:0007154 | Клеточные сигнальные пути | 7.93E-06 |
| GO:0030154 | Клеточная дифференциация | 1.22E-05 |
| GO:0060284 | Регуляция развития клеток | 2.50E-05 |
| GO:0007610 | Поведение | 7.68E-04 |
| GO:0061564 | Развитие аксонов | 1.20E-03 |
| GO:0007165 | Передача сигнала | 5.54E-03 |
| GO:0099536 | Синаптические сигнальные системы | 6.22E-03 |
| GO:0023051 | Регуляция сигнала | 2.20E-02 |
| GO:0002520 | Развитие иммунной системы | 4.15E-02 |
| Идентификационный код | Биологические пути | PFDR |
| hsa04921 | Окситоциновый сигнальный путь | 1.21E-04 |
| hsa04940 | Диабет I типа | 2.82E-04 |
| hsa04550 | Сигнальные пути, регулирующие плюрипотентность стволовых клеток | 8.82E-04 |
| hsa05330 | Реакция отторжения трансплантата | 3.60E-03 |
| hsa04725 | Холинергический синапс | 6.73E-03 |
| hsa04390 | Hippo сигнальный путь | 9.58E-03 |
| hsa05169 | Вирусная инфекция Эпштейна-Барра | 1.13E-02 |
| hsa04726 | Серотонинергический синапс | 3.48E-02 |
| hsa04724 | Глутаматергический синапс | 4.43E-02 |
| hsa04010 | MAPK сигнальный путь | 4.63E-02 |
| P00057 | Wnt сигнальный путь | 8.03E-03 |
| P00012 | Кадгериновый сигнальный путь | 9.28E-03 |
| P00005 | Развитие кровеносных сосудов | 9.52E-03 |
Перепредставленность среди списка генов, ассоциированных в настоящем исследовании с грудным вскармливанием, биологических путей, связанных с иммунной системой и ее функциями, была ожидаемой, учитывая специфику вовлеченной в анализ ткани (кровь) и многочисленные свидетельства о значимой роли грудного вскармливания в созревании иммунной системы младенцев (см., например, [15, 24]). Представляется примечательным значительное обогащение категорий, связанных с развитием и функциями нервной системы. Причем одним из первых (в числе ранжированных по значению p) биологических путей выступает окситоциновый сигнальный путь (табл. 1). Известно, что уровень окситоцина в крови у младенца превышает таковой у матери [25]. Возможно, зарегистрированный нами сигнал в ДНК-метилировании указывает на эпигеномную активацию окситоцинового пути у младенцев в ответ на материнское молоко и грудное вскармливание как таковое. Известно, что окситоцин является активатором секреции молока из лактирующей груди, он содержится в молоке (причем в максимальной дозе в самом начале лактации), а его кишечная проницаемость в кровяное русло установлена [26]. Предполагается, что окситоцин из материнского молока, полученный во время первых кормлений, является триггером систематического выделения этого гормона гипоталамусом младенца [25]. В дополнение тесный телесный контакт во время кормления также может стимулировать собственную выработку “гормона привязанности” окситоцина у ребенка [25]. Окситоцин зачастую действует как активатор широкого спектра систем и индуцирует выделение других гормонов и трансмиттеров [27]. Он оказывает прямое влияние на активность синапсов и возбудимость нейронов, действуя через свои рецепторы на синаптических мембранах. В настоящее время активно исследуется способность окситоцина модулировать нейрогенез и синаптическую пластичность [28].
Может ли являться индуцированная материнским кормлением активация окситоциновых путей тем триггером, который способен индуцировать множественные изменения в системах передачи сигналов, в том числе синаптических, что в итоге отражается на слаженных изменениях эпигенетических паттернов ряда генов, связанных с функциями ЦНС? Представленное в настоящем сообщении исследование фактически только открывает тему изучения возможных эпигеномных перестроек в ответ на систему питания на первых месяцах жизни, а результаты работы, на наш взгляд, представляют только “верхушку айсберга” из таких эффектов. Для ответа на заданный и многие другие вопросы, несомненно, нужны дополнительные полно-эпигеномные исследования на более обширной, стратифицированной в плане возраста, выборке детей при тщательной категоризации фенотипа – режима грудного вскармливания.
Сбор и молекулярно-генетический анализ образцов крови проводили при поддержке Правительства РФ (грант № 14.Z50.31.0027, рук. Е.Л. Григоренко); статистический и биоинформатический анализы данных проводили при поддержке РФФИ (грант № 17-06-00667, рук. В.В. Одинцова).
Авторы заявляют, что у них нет конфликта интересов.
Список литературы
Victora C.G., Bahl R., Barros A.J. et al. Breastfeeding in the 21st century: epidemiology, mechanisms, and lifelong effect // Lancet Psychiatry. 2016. V. 387. № 10017. P. 475–490. https://doi.org/10.1016/S0140-6736(15)01024-7
Mischke M., Plösch T. More than just a gut instinct-the potential interplay between a baby’s nutrition, its gut microbiome, and the epigenome // Am. J. Physiol. Regul. Integr. Comp. Physiol. 2013. V. 304. № 12. P. R1065–R1069. https://doi.org/10.1152/ajpregu.00551.2012
Verduci E., Banderali G., Barberi S. et al. Epigenetic effects of human breast milk // Nutrients. 2014. V. 6. № 4. P. 1711–1724. https://doi.org/10.3390/nu6041711
Hartwig F.P., Loret de Mola C., Davies N.M. et al. Breastfeeding effects on DNA methylation in the offspring: A systematic literature review // PLoS One. 2017. V. 12. № 4. P. e0175604. https://doi.org/10.1371/journal.pone.0173070
Obermann-Borst S.A., Eilers P.H., Tobi E.W. et al. Duration of breastfeeding and gender are associated with methylation of the LEPTIN gene in very young children // Pediatr. Res. 2013. V. 74. № 3. P. 344–349. https://doi.org/10.1038/pr.2013.95
Tao M.H., Marian C., Shields P.G. et al. Exposures in early life: associations with DNA promoter methylation in breast tumors // J. Dev. Orig. Health. Dis. 2013. V. 4. P. 182–190. https://doi.org/10.1017/S2040174412000694
Rossnerova A., Tulupova E., Tabashidze N. et al. Factors affecting the 27K DNA methylation pattern in asthmatic and healthy children from locations with various environments // Mutat. Res. 2013. V. 741–742. P. 18–26. https://doi.org/10.1017/S2040174412000694
Soto-Ramirez N., Arshad S.H., Holloway J.W. et al. The interaction of genetic variants and DNA methylation of the interleukin-4 receptor gene increase the risk of asthma at age 18 years // Clin. Epigenet. 2013. V. 5. № 1. P. 1. https://doi.org/10.1186/1868-7083-5-1
Simpkin A.J., Hemani G., Suderman M. et al. Prenatal and early life influences on epigenetic age in children: a study of mother-offspring pairs from two cohort studies // Hum. Mol. Genet. 2016. V. 25. № 1. P. 191–201. https://doi.org/10.1093/hmg/ddv456
Колесникова М.А., Жукова М.А., Овчинникова И.В. Особенности когнитивного развития и адаптивного поведения детей в домах ребенка в РФ // Клин. и спец. психология. 2018. V. 7. № 2. P. 53–69. https://doi.org/10.17759/psyclin.2018070204
Aryee M.J., Jaffe A.E., Corrada-Bravo H. et al. Minfi: A flexible and comprehensive Bioconductor package for the analysis of Infinium DNA Methylation microarrays // Bioinformatics. 2014. V. 30. № 10. P. 1363–1369. https://doi.org/10.1093/bioinformatics/btu049
Boks M.P., Derks E.M., Weisenberger D.J. et al. The relationship of DNA methylation with age, gender and genotype in twins and healthy controls // PLoS One. 2009. V. 4. № 8. P. e6767. https://doi.org/10.1371/journal.pone.0006767
Jaffe A.E., Irizarry R.A. Accounting for cellular heterogeneity is critical in epigenome-wide association studies // Genome Biol. 2013. V. 15. P. R31. https://doi.org/10.1186/gb-2014-15-2-r31
Reinius L.E., Acevedo N., Joerink M. et al. Differential DNA methylation in purified human blood cells: implications for cell lineage and studies on disease susceptibility // PLoS One. 2012. V. 7. № 7. P. e41361. https://doi.org/10.1371/journal.pone.0041361
Andersson Y., Hammarström M.L., Lönnerdal B. et al. Formula feeding skews immune cell composition toward adaptive immunity compared to breastfeeding // J. Immunol. 2009. V. 183. № 7. P. 4322–4328. https://doi.org/10.4049/jimmunol.0900829
Casper J., Zweig A.S., Villarreal C. et al. The UCSC Genome Browser database: 2018 update // Nucl. Acids Res. 2018. V. 46. № D1. P. D762–D769. https://doi.org/10.1093/nar/gkx1020
Harrow J., Frankish A., Gonzalez J.M. et al. GENCODE: the reference human genome annotation for The ENCODE Project // Genome Res. 2012. V. 22. № 9. P. 1760–1764. https://doi.org/10.1101/gr.135350.111
Dennis G.J., Sherman B.T., Hosack D.A. et al. DAVID: Database for Annotation, Visualization, and Integrated Discovery // Genome Biol. 2003. V. 4. № 9. P. R60.1–R60.11.
Chen E.Y., Tan C.M., Kou Y. et al. Enrichr: interactive and collaborative HTML5 gene list enrichment analysis tool // BMC Bioinformatics. 2013. V. 128. № 14. https://doi.org/10.1186/1471-2105-14-128
Reimand J., Arak T., Adler P. et al. g:Profiler – a web server for functional interpretation of gene lists (2016 update) // Nucl. Acids Res. 2016. V. 44. № W1. P. W83–W89. https://doi.org/10.1093/nar/gkw199
Consortium T.G.O. The Gene Ontology project in 2008 // Nucl. Acids Res. 2008. V. 36. P. D440–D444. https://doi.org/10.1093/nar/gkm883
Kanehisa M., Goto S. KEGG: Kyoto Encyclopedia of Genes and Genomes // Nucl. Acids Res. 2000. V. 28. № 1. P. 27–30.
Thomas P.D., Campbell M.J., Kejariwal A. et al. PANTHER: a library of protein families and subfamilies indexed by function // Genome Res. 2003. V. 13. № 9. P. 2129–2142. https://doi.org/10.1101/gr.772403
Jackson K.M., Nazar A.M. Breastfeeding, the immune response, and long-term health // J. Am. Osteopath. Assoc. 2006. V. 106. № 4. P. 203–207.
Uvnäs Moberg K., Prime D.K. Oxytocin effects in mothers and infants during breastfeeding // Infant. 2013. V. 9. № 6. P. 201–206.
Higashida H., Furuhara K., Yamauchi A.M. et al. Intestinal transepithelial permeability of oxytocin into the blood is dependent on the receptor for advanced glycation end products in mice // Sci. Rep. 2017. V. 7. № 1. P. 7883. https://doi.org/10.1038/s41598-017-07949-4
Ludwig M., Leng G. Dendritic peptide release and peptide-dependent behaviours // Nat. Rev. Neurosci. 2006. V. 7. P. 126–136. https://doi.org/10.1038/nrn1845
Bakos J., Srancikova A., Havranek T., Bacova Z. Molecular mechanisms of oxytocin signaling at the synaptic connection // Neural Plasticity. 2018. V. 2018. № 4864107. https://doi.org/10.1155/2018/4864107
Дополнительные материалы отсутствуют.


