Геохимия, 2022, T. 67, № 9, стр. 872-880
Флюидная эмиссия метана из донных отложений эстуария реки Черной (Севастопольский регион, Крым)
Т. В. Малахова a, *, А. И. Мурашова a
a Институт биологии южных морей им. А.О. Ковалевского РАН
299011 Севастополь, проспект Нахимова, 2, Россия
* E-mail: t.malakhova@imbr-ras.ru
Поступила в редакцию 19.04.2021
После доработки 14.10.2021
Принята к публикации 15.10.2021
- EDN: YSNBSC
- DOI: 10.31857/S0016752522080040
Аннотация
В четырех районах эстуарной зоны реки Черной ловушечным методом проведены измерения потоков флюидной метановой разгрузки из донных осадков. Станции отбора характеризовались различными гидролого-гидрохимическими условиями: пробы воды отличались соленостью, содержанием в ней биогенных элементов азотного и фосфорного комплексов (${\text{NО}}_{2}^{ - }$ от 12.2 до 29 мкг л–1; ${\text{NО}}_{3}^{ - }$ от 294 до 869 мкг л–1; ${\text{NH}}_{4}^{ + }$ от 57.9 до 130 мкг л–1; ${{{\text{H}}}_{{\text{2}}}}{\text{PO}}_{4}^{ - }$ от 28.2 до 127.8 мкг л–1), и геохимическими характеристиками донных отложений. Уменьшение содержания СН4 в донных осадках и воде так же, как минеральных форм азота и фосфора, пористости и влажности осадка происходило против градиента солености – в направлении от истока реки к устью. Концентрация СН4 в толще донных осадков на солоноватоводных ст. 1 и ст. 2 была на 2 порядка ниже по сравнению с пресноводными ст. 3 и ст. 4, где достигала 1.1 ммоль дм–3. Содержание СН4 в поровой воде донных осадков не превышало рассчитанные значения растворимости (от 1.53 до 1.68 ммоль л–1). Диапазон средних концентраций СН4 в воде на исследованных станциях составлял от 285 до 813 нмоль л–1. В воде отмечен колебательный характер изменения концентраций СН4, что предположительно связано с волновыми процессами в эстуарии. Тренд изменения концентрации СН4 во флюидных ловушках во времени соответствовал линейной зависимости. Для ст. 3 и ст. 4, расположенных выше по течению р. Черной, рассчитанный флюидный поток из дна составил 4 и 293 ммоль м–2 сут–1 соответственно. Более низкие потоки были получены для солоноватоводных ст. 1 и ст. 2 (0.3 и 0.4 ммоль м–2 сут–1), что, вероятно, связано с жизнедеятельностью метанотрофных бактерий, где в верхнем слое донных осадков при наличии сульфат-иона осуществляется окисление метана.
ВВЕДЕНИЕ
Оценка эмиссии природных парниковых газов является одним из важных вопросов в контексте проблемы глобального потепления климата. Особый интерес представляет изучение флюидных потоков из толщи осадков для определения их вклада в общий поток растворенных средообразующих газов и влияния на биологические и геохимические процессы на границе раздела сред. Количественные данные о поступлении метана из донных осадков в виде флюидной разгрузки или диффузионных потоков в настоящее время недостаточно полны, особенно это касается прямых in situ измерений (Torres et al., 2002; Linke et al., 2005; Малахова и др., 2020a).
Для оценки потоков растворенных газов из донных отложений многие исследователи используют расчетные методы на основе данных о концентрациях СН4 в донных осадках и придонном слое воды (Luff, Wallmann, 2003; Riedinger N., 2010; Treude et al., 2003; Малахова и др., 2012). Показано, что расчетные методы имеют ряд недостатков по сравнению с контактными, т. к. не учитывают всего комплекса параметров, которые могут влиять на искомую величину: изменчивость потоков во времени, пульсирующий характер газовыделений и биологические фильтры на границе дно-вода. Тогда как метод ловушек, как in situ метод, позволяет получить результирующую величину потока, которая суммирует все процессы метанового цикла, такие как молекулярный перенос, микробные процессы поглощения и продукции на границе раздела сред (Abril, 2002; Zhang et al., 2008; Sansone, 1998; Малахова и др., 2020а).
Раннее в Севастопольской акватории диффузионные потоки метана из дна были получены расчетным методом (Малахова и др., 2012). Было показано, что потоки направлены из донных отложений в воду: для открытых районов они не превышали 1.5 мкмоль м–2 сут–1, для внутренней части бухты величины потока изменялись от 10 до 544 мкмоль м–2 сут–1 (Малахова и др., 2012).
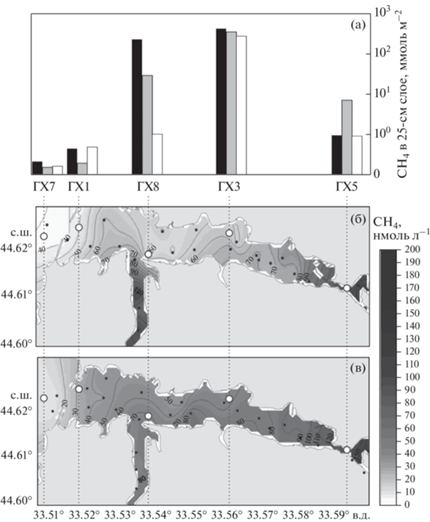
Исследования содержания метана в поверхностном слое воды Севастопольской бухты показали, что во все сезоны в кутовой части бухты наблюдались повышенные концентрации, которые осенью достигали 200 нмоль л–1 (рис. 1б, 1в) (Малахова и др., 2020б). Такое распределение типично для акваторий эстуарного типа, к которым также относится Севастопольская бухта (Малахова и др., 2020б). Считается, что для мелководных районов на содержание метана в воде значительное влияние могут оказывать его потоки из донных осадков (Borges et al., 2018; Малахова и др., 2020г; Малахова и др., 2012). Однако содержание метана в донных осадках показало, что максимальные концентрации определены в центральной части бухты, тогда как в месте впадения реки значения были на несколько порядков ниже во все сезоны года (рис. 1а) (Малахова и др., 2018). Это свидетельствует о том, что высокие концентрации метана в воде кутовой части бухты могут быть обусловлены поступлением с водой реки Черной.
Рис. 1.
Содержание метана в донных осадках в феврале (черные столбцы), мае (серые столбцы) и октябре (белые столбцы) 2016 г. (а); (Малахова и др., 2018); распределение метана в поверхностном слое воды Севастопольской бухты в августе 2017 г. (б) и в феврале 2018 г. (в) (Малахова и др., 2020б). Кружками отмечены районы отбора донных осадков.
В зонах эстуарного типа биогеохимические процессы трансформации веществ и формирование определенного гидрохимического режима протекают не равномерно, а локализуются в активных зонах, слоях или активных поверхностях, получивших название геохимических барьерных зон (Перельман, 1961). Как показано в работе (Орехова, 2018) предполагаемая граница зоны биогеохимического барьера р. Черной находится на расстоянии 1.2 км от места впадения в бухту вверх по течению. Цель работы заключалась в оценке потоков флюидной метановой разгрузки ловушечным методом из осадков мелководных районов с различной геохимической обстановкой в зоне биогеохимического барьера р. Черной.
МАТЕРИАЛЫ И МЕТОДЫ
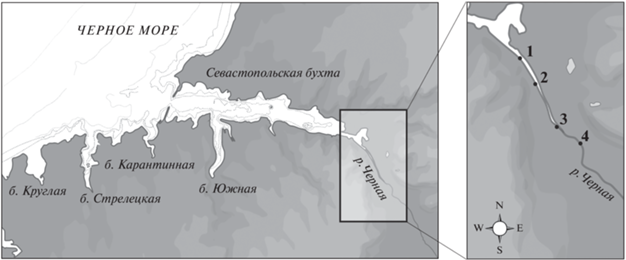
Исследования проводились 25 мая 2020 г. В направлении от устья вверх по течению р. Черной на 4 станциях были установлены флюидные ловушки (рис. 2). Расстояние между крайними станциями составляло около 1.5 км, соленость воды на станциях уменьшалась вверх по течению от 1 до 4 станции и была равна 14.7; 12.6; 3.9 и 0 PSU соответственно.
Рис. 2.
Карта-схема станций отбора проб и установки флюидных ловушек в зоне геохимического барьера р. Черной.
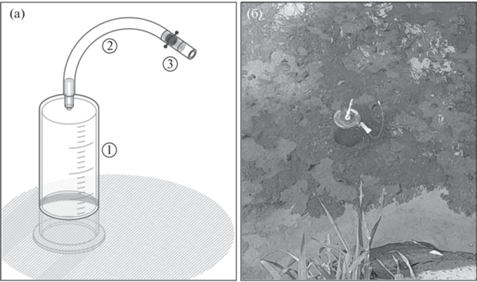
Ловушки представляли собой пластиковые цилиндрические контейнеры объемом 1.6 л с нижним открытым основанием, укомплектованные в верхней части шлангом и краном для отбора аликвоты воды (рис. 3). Ловушки были погружены открытым основанием в донные осадки, рабочий объем ловушки составлял 1 л. Для отбора аликвоты воды из ловушки к соединительному шлангу прикрепляли шприц объемом 60 мл, после чего кран открывали и проводили отбор 50 мл воды, которую тут же перемещали в две 25 мл виалы. Для всех ловушек первый пробоотбор был выполнен сразу после установки, затем еще 4 раза через каждый час. Таким образом, время экспозиции флюидных ловушек составило около 5 часов. Одновременно на каждой станции были отобраны фоновые пробы воды вне ловушки также в двух повторностях. Отбор проб донных осадков и придонной воды проводили на каждой станции акриловой грунтовой трубкой с вакуумным затвором. Керны донных осадков длиной до 13 см были разрезаны послойно в полевых условиях при помощи поршневого экструдера и в каждом слое была отобрана проба донных осадков объемом 2.5 мл для определения концентрации метана.
Рис. 3.
Флюидная ловушка: (а) схема: 1 – цилиндрический контейнер, 2 – соединительный шланг, 3 – кран для отбора проб, (б) подводное фото установленной на ст. 4 ловушки (в верхней части ловушки собрался пузырьковый газ).
Содержание CH4 измерялось газохроматографическим методом после фазово-равновесной дегазации в ЦКП “Спектрометрия и Хроматография” ФИЦ ИнБЮМ на газовом хроматографе Хроматэк Кристалл 5000.2 с пламенно-ионизационным детектором и набивной колонкой. Параметры хроматографической системы были следующими: температура испарителя 120°С, колонки – 50°С, детектора 200°С, газ носитель – азот. Ошибка определения метана не превышала 7%.
Флюидные потоки рассчитывали как отношение объема поступившего в ловушку газа за время экспозиции ловушки по формуле (1) (Abril, 2002; Zhang et al., 2008, Sansone, 1998, Малахова и др., 2020а).
(1)
${{F}_{{{\text{C}}{{{\text{H}}}_{4}}}}} = \frac{{{{V}_{{{\text{C}}{{{\text{H}}}_{4}}}}}}}{{S{\text{T}}}}~,$Объем газа рассчитывался по формуле (2):
(2)
${{V}_{{{\text{C}}{{{\text{H}}}_{4}}}}} = \left( {C{{2}_{{{\text{C}}{{{\text{H}}}_{{\text{4}}}}}}} - C{{1}_{{{\text{C}}{{{\text{H}}}_{{\text{4}}}}}}}} \right){{V}_{{inst}}},$Время оборота метана рассчитывалось как отношение интегрального содержания метана в опробованном слое донных осадков к соответствующему флюидному потоку из дна (3):
(3)
${\text{Т}} = \frac{{{{V}_{{{\text{C}}{{{\text{H}}}_{{4sed}}}}}}}}{{{{F}_{{{\text{C}}{{{\text{H}}}_{4}}}}}}}.$Растворимость метана в поровых водах оценивали из расчета коэффициента растворимости Бунзена, который зависит от температуры и солености окружающей среды (4):
(4)
$\begin{gathered} \ln \beta = {{A}_{1}} + {{A}_{2}}\frac{{100}}{T} + {{A}_{3}}\ln \frac{T}{{100}} + \\ + \,\,S\left[ {{{B}_{1}} + {{B}_{2}}\frac{T}{{100}} + {{B}_{3}}{{{\left( {\frac{T}{{100}}} \right)}}^{2}}} \right], \\ \end{gathered} $В расчет растворимости метана также была введена поправка на давление in situ в соответствии с первым законом Генри. Соленость и температуру поровой воды для всех слоев исследованных колонок принимали равной значениям в придонной воде на соответствующих станциях.
Для сравнения с растворимостью метана в поровой воде $\left( {{{C}_{{{\text{C}}{{{\text{H}}}_{{4pw}}}}}}} \right)$ его концентрация в донных осадках $\left( {{{C}_{{{\text{C}}{{{\text{H}}}_{{4sed}}}}}}} \right)$ была пересчитана на объем поровой воды по формуле (5):
(5)
${{C}_{{{\text{C}}{{{\text{H}}}_{{4pw}}}}}} = \frac{{{{C}_{{{\text{C}}{{{\text{H}}}_{{4sed}}}}}}}}{\varepsilon }.$Для этого была рассчитана пористость осадка ε (6):
где Vpw – объем, занимаемый поровой водой, л; Vsed – объем, занимаемый осадком, дм3.Содержание биогенных элементов (${\text{NО}}_{4}^{ - },$ ${\text{NО}}_{3}^{ - },$ ${\text{NH}}_{4}^{ + },$ ${{{\text{H}}}_{{\text{2}}}}{\text{PO}}_{4}^{ - }$) в воде и соленость определяли в соответствии с опубликованными методиками (Руководство, 1977).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Гидро- и геохимические характеристики исследованных районов
По химическому составу вода р. Черной относится к гидрокарбонатному классу группы кальциевых (HCO3 → Ca2+ + Mg2+) средней (0.3–0.5 г дм–3), иногда повышенной (>0.5–1.0 г дм–3) минерализации, слабощелочному (рН 6.8–8.5) типу (Овсяный, 2018).
Основные гидрохимические характеристики воды на исследованных станциях представлены в табл. 1. Изменение концентраций минеральных форм азота и фосфора по градиенту солености имеют сходный характер, уменьшаясь в направлении к устью. Исключение составляет ст. 3, на которой концентрации нитритных ионов, аммонийных и дигидрофосфат ионов (${\text{NO}}_{2}^{ - },$ N${\text{H}}_{4}^{ - }$, ${{{\text{H}}}_{{\text{2}}}}{\text{PO}}_{4}^{ - }$) значительно выше по сравнению как со ст. 2 так и ст. 4. Это может быть связано с дополнительным источником поступления биогенных элементов, который расположен ниже по течению относительно ст. 4.
Таблица 1.
Содержание биогенных элементов в воде, соленость воды, влажность и пористость донных осадков на исследованных станциях в эстуарии р. Черной
| № ст | Координаты | Вода | Донные осадки | |||||
|---|---|---|---|---|---|---|---|---|
| N${\text{O}}_{2}^{ - }$, мкг л–1 |
N${\text{O}}_{3}^{ - }$, мкг л–1 |
${\text{NH}}_{4}^{ + },$ мкг л–1 |
${{{\text{H}}}_{{\text{2}}}}{\text{PO}}_{4}^{ - }$, мкг л–1 |
S, PSU |
влажность, % | пористость, % | ||
| 1 | 44°36′06.03 N 33°36′18.45 Е |
12.2 | 294 | 85.6 | 28.2 | 14.7 | 49 | 63 |
| 2 | 44°36′00.94 N 33°36′21.66 Е |
18.6 | 365 | 77.5 | 49.6 | 12.58 | 55 | 61 |
| 3 | 44°35′45.94 N 33°36′32.61 Е |
29 | 682 | 130 | 127.8 | 3.98 | 68 | 78 |
| 4 | 44°36′06.03 N 33°36′18.45 Е |
27.6 | 869 | 57.9 | 48.3 | 0 | 75 | 85 |
Температура воды на исследованных станциях составляла около 14°С. Пористость осадков изменялась от 63 до 85% (табл. 1) вверх по течению реки, что свидетельствует о изменении гранулометрического состава донных осадков. С удалением от устья реки осадки характеризовались большим содержанием мелкодисперсной фракции и большей обводненностью. Известно, что пористость и влажность осадка характеризует его гранулометрический состав (Гавшин, 1988). Осадки с высоким значением влажности (до 90 и более %) образованы, как правило, тонкодисперсной взвесью биогенного происхождения (например, фрагментами отмирающих планктонных организмов), и, наоборот, низкие значения влажности (менее 40%) характерны для крупнодисперсных донных осадков, сформированных литогенным материалом, поступающим в водоемы в результате эрозии береговой зоны и со склоновым стоком воды. Полученные в данной работе величины влажности донных осадков от 49 до 75% (табл. 1) имеют промежуточные значения, что может свидетельствовать о примерно равном содержании в них биогенной и литогенной фракции.
Метан в донных осадках
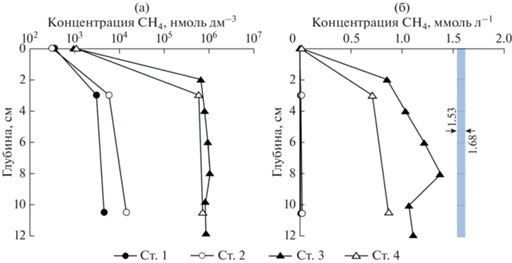
Концентрация СН4 в толще донных осадков на ст. 1 и ст. 2 была на 2 порядка ниже по сравнению со значениями на ст. 3 и ст. 4, которые достигали 1.1 ммоль дм–3 (ст. 3 – горизонт 8 см, рис. 4). Рассчитанные значения интегрального содержания метана для верхних 12 см донных осадков составили 0.9; 0.4; 102 и 76 ммоль м–2, соответственно для 1 – 4 ст. Проведенные ранее исследования в Севастопольской бухте также показали, что по содержанию СН4 в толще донных осадков выделяются 2 группы станций: с низким и высоким содержанием метана. К первой группе относятся станции в мористой и в устьевой части Севастопольской бухты, где концентрации не превышали 10 мкмоль дм–3, тогда как в центральной части бухты концентрации достигали 3.4 ммоль дм–3. Была показана зависимость концентрации СН4 от содержания Сорг (Малахова и др., 2018).
Рис. 4.
Профили распределения концентрации метана в донных осадках (а) и в поровой воде донных осадков в сравнении с растворимостью метана (б) на исследованных станциях в эстуарии р. Черной. Стрелками на рисунке (б) отмечен диапазон значений растворимости метана.
Невысокие концентрации солоноватоводных ст. 1 и ст. 2 вероятно связаны с жизнедеятельностью метанотрофных бактерий, где при наличии сульфат-иона осуществляется сульфатзависимое окисление метана (Пименов и др., 2013; Малахова и др., 2018). По данным предыдущих исследований скорости микробного метанокисления в устьевой части бухты достигали 0.122 ммоль м–2 сут–1 (Малахова и др., 2018). Тогда как для опресненных ст. 3 и 4 предположительно продукция метана превалирует над окислением.
С другой стороны, в донных осадках исследованных станций могут присутствовать различные типы органического вещества, отличающиеся лабильностью. Компонентный состав осаждающегося вещества из речной воды весьма разнообразен и отличается от состава морской воды. Органическая составляющая осаждающегося материала рек включает в себя биополимеры, полученные от разрушения растений, и геополимеры (гумусовые вещества). Установлено, что основное отложение почвенного материала происходит в районе биогеохимического барьера на границе пресная – морская вода. (Хорошевская, 2010). Состав автохтонного взвешенного вещества открытых морских вод в основном определяется величиной первичной продукции. Поступления биогенного материала в состав взвеси связывают обычно с пиком цветения кремнистых (диатомовых) и карбонатных (кокколитофорид) микроводорослей (Klyuvitkin et al., 2018). Было показано, что понижение концентрации растворенного аллохтонного легкоокисляемого органического вещества в барьерных зонах смешения “река-море” сопровождается увеличением концентраций метана в результате жизнедеятельности бактерий (Хорошевская, 2010).
Рассчитанные с учетом температуры, солености, пористости и глубины залегания осадка и глубины станции значения растворимости находились в диапазоне 1.53–1.68 ммоль л–1 (рис. 4б). Максимальные измеренные концентрации метана в поровой воде, которые достигали величины 1.4 ммоль л–1, были близки к значениям растворимости, однако же не превышали ее. При этом на ст. 3 и 4 в момент отрыва ловушек от дна наблюдалось интенсивное пузырьковое газовыделение. Также было отмечено, что во флюидной ловушке на ст. 4 за время 5-часовой экспозиции под верхней частью ловушки собралось 10 мл газа (рис. 3б). Вероятно, объем газа, превышающий величины растворимости, высвобождался из осадка во время механического воздействия в процессе отбора колонок.
То же самое наблюдалось в процессе акустических исследований осадочной толщи в Севастопольской бухте, проведенных в 2015 г. во время пробоотбора колонок донных осадков на эхограммах в точке входа пробоотборника наблюдались акустические аномалии, идентифицированные как пузырьковые газовыделения (Ulyanova еt al., 2021, Малахова и др., 2020в), что свидетельствует о газонасыщенности верхних слоев осадка Севастопольской бухты. Исследования, проведенные в Севастопольской акватории в 2011 г., показали, что содержание метана в верхних 50 см донных отложений внутренней части бухты достигало нескольких ммоль л–1 и для некоторых районов превышало значения его растворимости в поровой воде (Малахова и др., 2012).
Флюидные потоки
Линейный рост концентрации метана во времени во флюидных ловушках на ст. 3 и 4 (R2 = 0.81 и 0.79 соответственно) свидетельствовал о постоянном подтоке растворенного метана. На ст. 1 и 2 также наблюдался рост концентрации СН4 в ловушках, однако с меньшим градиентом и с низкими коэффициентами детерминации (рис. 5а). Концентрации метана вне ловушек, измеренные для всех временных точек, представлены на рис. 5б. Средние значения составили 285, 323, 678, 813 нмоль л–1 для 1 – 4 ст. соответственно. Рассчитанные величины потоков составили 4 и 293 ммоль м–2 сут–1 для ст. 3 и 4, соответственно (табл. 2). Предполагается, что невысокие концентрации и потоки метана для солоноватоводных ст. 1 и 2 связаны с жизнедеятельностью метанотрофных бактерий, где при наличии сульфат-иона осуществляется сульфатзависимое окисление метана в верхнем слое донных осадков (Пименов и др., 2013; Малахова и др., 2018).
Рис. 5.
Изменение концентрации метана во флюидных ловушках (а) и в воде вне ловушек (б) во время проведения in situ эксперимента на 4 станциях в эстуарии р. Черной.
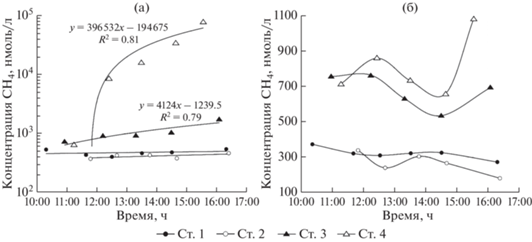
Таблица 2.
Рассчитанное значение растворимости метана, интегральное содержание метана, его удельный поток, а также рассчитанное время оборота в верхнем 10-см слое донных осадков для 4 исследованных станций в эстуарии р. Черной
| Станция | Растворимость, ммоль л–1 | Поток СН4 из дна, ммоль м–2 сут–1 | Содержание метана в 10-см слое осадка, ммоль м–2 | Время оборота, сут |
|---|---|---|---|---|
| 1 | 1.53 | 0.3 | 0.4 | 1.3 |
| 2 | 1.56 | 0.4 | 0.9 | 2.3 |
| 3 | 1.64 | 4 | 102 | 25 |
| 4 | 1.68 | 293 | 76 | 0.3 |
Из рисунка 5б видно, что изменение концентрации СН4 вне ловушек подчиняется некому колебательному процессу. Особенно это заметно на верхних по течению станциях, где наблюдался единый вектор изменения концентраций, а диапазон составлял 230 и 420 нмоль л–1 на 3 и 4 станциях соответственно. На мористых станциях 1 и 2 колебания были менее выражены по амплитуде, и находились в противофазе по отношению к ст. 3 и 4. Причиной таких цикличных изменений концентрации СН4 в воде могут быть сейши, наблюдавшиеся во время пробоотбора. Ранее было отмечено, что сейши наряду с паводками и сгонно-нагонными ветрами могут значительно влиять на термохалинные параметры вод кутовой части Севастопольской бухты (Болтачев и др., 2010). Масштаб времени таких процессов может составлять от нескольких десятков минут или часов до нескольких суток, а амплитуда колебания при этом в эстуариях рек варьирует от нескольких сантиметров до метра и более.
Судя по рис. 5б период такой волны в эстуарии р. Черной составил около 4 часов. Вероятно значительное изменение концентрации метана в воде связано с тем, что вследствие волновых процессов в эстуарии вверх по течению реки с частотой сейшевых колебаний приносятся воды с меньшим содержанием метана. Важно отметить, что внутри флюидных ловушек на ст. 3 и ст. 4 также было отмечено снижение концентраций СН4 относительно общей линии тренда в промежуток с 13 до 15 ч, в то же самое время, когда наблюдался тренд снижения концентраций вне ловушек (рис. 5б). Это свидетельствует о том, что не только процессы “разбавления” влияют на содержание метана в воде, но также возможно и флюидный поток метана изменяется в зависимости от фазы волны в эстуарии. Показано, что для мелководных районов значимым фактором, влияющим на эмиссию газа из донных осадков, является атмосферное и гидростатическое давление (Strack M. et al., 2016). Падение атмосферного давления (для приливных зон также снижение уровня воды) приводит к снижению давления на глубине, что в свою очередь влечет увеличение объема газовой фазы за счет расширения пузыря и, как следствие, последующее выделение газа.
ЗАКЛЮЧЕНИЕ
Проведена оценка потоков флюидной метановой разгрузки ловушечным методом из осадков мелководных районов с различной геохимической обстановкой в барьерной зоне р. Черной. Показано, что уменьшение концентрации метана в воде, донных осадках и флюидных потоков СН4 происходит в направлении от истока реки к устью. Концентрация СН4 в толще донных осадков на солоноватоводных станциях была на 2 порядка ниже по сравнению с распресненными районами, где концентрация СН4 достигала 1.1 ммоль дм–3. Содержание СН4 в поровой воде донных осадков не превышало рассчитанные значения растворимости, которые находились в диапазоне 1.53–1.68 ммоль л–1. Диапазон средних концентраций СН4 в воде на исследованных станциях составил 285–813 нмоль л–1. Для распресненных станций отмечен значительный диапазон концентраций СН4 в воде. Временная динамика содержания СН4 в воде на этих станциях имела колебательный характер, что предположительно связано с волновыми процессами в эстуарии. Тренд изменения концентрации СН4 во флюидных ловушках соответствовал линейной зависимости, что позволило рассчитать поток растворенного СН4 из донных осадков. Для расположенных выше по течению реки станций 3 и 4 рост концентрации СН4 в ловушках был более выражен по сравнению со станциями 1 и 2 в устье реки. Диапазон значений флюидных потоков составил 0.3–293 ммоль м–2 сут–1. Низкие значения потоков на ст. 1 и 2, вероятно, связаны бактериальным фильтром, за счет которого осуществляется сульфатзависимое окисление метана в верхнем слое донных осадков.
Новые данные, полученные по флюидным потокам метана из дна и его эмиссии в атмосферу в эстуарии реки Черной, показывают его значительный вклад в общий атмосферный поток, сопоставимый со вкладом источников на континенте. Дальнейшие исследования будут нацелены на исследование влияния волновых процессов на закономерности и скорости изменения концентрации метана в воде эстуарного района р. Черной для оценки суточных колебаний потоков метана в атмосферу.
Мы благодарим сотрудника отдела радиационной и химической биологии ФГБУН ФИЦ ИнБЮМ Д.Б. Евтушенко за помощь в создании флюидных ловушек, а также мы выражаем особую благодарность рецензентам за конструктивные замечания.
Работа выполнена в рамках тем ФИЦ ИнБЮМ “Молисмологические и биогеохимические основы гомеостаза морских экосистем” (номер гос. регистрации 121031500515-8) и регионального гранта РФФИ и города Севастополя 20-45-920004 р-а “Балансовое изучение влияния стока реки Черной на эвтрофикацию и загрязнение Севастопольской бухты антропогенными радионуклидами, тяжелыми металлами и хлорорганическими ксенобиотиками” (АААА-А20-120013090118-8).
Список литературы
Болтачев А.Р., Карпова Е.П., Данилюк О.Н. (2010) Особенности термохалинных параметров и ихтиоцена эстуария реки Черная (Севастопольская бухта). Морской экологический журн. 9(2), 23-36.
Гавшин В.М., Лапухов С.В., Сараев С.В. (1988) Геохимия литогенеза в условиях сероводородного заражения (Черное море). Новосибирск: Наука, 194 с.
Малахова Т.В., Егоров В.Н., Малахова Л.В., Пименов Н.В. (2012) Элементы баланса метана в донных осадках Севастопольской акватории. Екологічна безпека прибережної та шельфової зон та комплексне використання ресурсів шельфу. 26(1), 217-231.
Малахова Т.В., Канапацкий Т.А., Егоров В.Н., Малахова Л.В., Артемов Ю.Г., Евтушенко Д.Б., Гулин С.Б., Пименов Н.В.(2015) Микробные процессы и генезис струйных метановых газовыделений прибрежных районов Крымского полуострова. Микробиология. 84(6), 743-752.
Малахова Т.В., Канапацкий Т.А., Сидоров И.Г., Русанов И.И., Малахова Л.В., Проскурнин В.Ю., Пименов Н.В. (2018) Сезонная динамика микробных процессов в донных осадках Cевастопольской морской акватории. Океанология. 58(4), 21-29.
Малахова Т.В., Будников А.А., Иванова И.Н., Мурашова А.И. (2020а) Флюидная эмиссия метана из дна: сравнение потоков с площадки сипов в бухте Ласпи с потоками в других газовыделяющих районах. Процессы в геосредах. 3(25), 822-830.
Малахова Т.В., Малахова Л.В., Будников А.А., Иванова И.Н. (2020б) Пространственно-временная изменчивость содержания метана в Севастопольской бухте и его эмиссии в атмосферу. Вестник Московского университета. 5(3), 73-80.
Малахова Т.В., Егоров В.Н., Малахова Л.В., Артемов Ю.Г., Пименов Н.В. (2020в) Биогеохимические характеристики мелководных струйных метановых газовыделений в прибрежных районах Крыма в сравнении с глубоководными сипами Черного моря. Морской биологический журн. 5(4), 37-55.
Малахова Т.В., Мансурова И.М., Малахова Л.В., Минина Н.В., Заговенкова А.Д. (2020г) Особенности распределения метана в эвфотическом слое северной части Черного моря в летний сезон 2018 г. (по данным 102-го рейса НИС “Профессор Водяницкий”). Морской гидрофизический журн. 36(2), 186-201.
Овсяный Е.И., Орехова Н.А. (2018) Гидрохимический режим реки Черной (Крым): экологические аспекты. Морской гидрофизический журн. 1, 199.
Орехова Н.А., Медведев Е.В., Овсяный Е.И. (2018) Влияние вод реки Черной на гидрохимический режим Севастопольской бухты (Черное море). Экологическая безопасность прибрежной и шельфовой зон моря. 3, 84-91.
Пименов Н.В., Ульянова М.О., Канапацкий Т.А., Мицкевич И.Н., Сигалевич П.А., Немировская И.А., Сивков В.В. (2013) Сульфатредукция, образование и окисление метана в поверхностных осадках Вислинского и Куршского заливов Балтийского моря. Микробиология. 82(2), 228-238.
Руководство по методам химического анализа морских вод. Л.: Гидрометеоиздат. 1977. 208 с.
Хорошевская В.О. (2010) Закономерности формирования и распределения метана в прибрежных водах Азово-Черноморского бассейна. Автореф. дис. канд. биол. наук, РнД., 24с.
Abegg F., Anderson A. (1997) The acoustic turbid layer in muddy sedments of Eckernfoerde Bay, Western Baltic: methane concentrations, satration and bubble characteristics. Marine Geology. 137, 137-147.
Abril G., Iversen N. (2002) Methane dynamics in a shallow non-tidal estuary (Randers Fjord, Denmark). Marine ecology progress series. 230, 171-181.
Klyuvitkin A.A., Kravchishina M.D., Dara O.M. et al. (2018) Seasonal Variability of Vertical Fluxes of Dispersed Sedimentary Matter in the Black Sea. Dokl. Earth Sc. 483, 1558-1563.
Linke P., Wallmann K., Suess E., Hensen C., Rehder G. (2005). In situ benthic fluxes from an intermittently active mud volcano at the Costa Rica convergent margin. Earth Planet. Sci. Lett 235.
Luff R., Wallmann K. (2003) Fluid flow, methane fluxes, carbonate precipitation and biogeochemical turnover in gas hydrate-bearing sediments at Hydrate Ridge, Cascadia Margin: numerical modeling and mass balances. Geochim. Cosmochim. Acta. 67(18), 3403-3421.
Borges A.V. (2018) Productivity and temperature as drivers of seasonal and spatial variations of dissolved methane in the southern bight of the North Sea / A.V. Borges (et al.). Ecosystems. 21, 583-599.
Riedinger N., Brunner B., Lin Y.-S. et al. (2010) Methane at the sediment–water transition in Black Sea sediments. Chem. Geol. 274(1–2), 29-37.
Sansone F.J., Rust T.M., Smith S.V. (1998) Methane distribution and cycling in Tomales Bay, California. Estuaries. 21(1), 66-77.
Strack M., Kellner E., Waddington J.M. Dynamics of biogenic gas bubbles in peat and their effects on peatland biogeochemistry Global Biogeochem. Cycles, 19, GB1003, https://doi.org/10.1029/2004GB002330
Torres M.E., McManus J., Hammond D.E., de Angelis M.A., Heeschen K.U., Colbert S.L., Tyron M.D., Brown K.M., Suess E. (2002). Fluid and chemical fluxes in and out of sediments hosting methane hydrate deposits on Hydrate ridge, OR, I: hydrological provinces. Earth Planet. Sci. Lett. 201, 525-540.
Ulyanova M., Malakhova T., Evtushenko D., Artemov Yu., Egorov V. (2021) Comparison of methane distribution in bottom sediments of shallow lagoons of the Baltic and Black Seas. RJES. 21(1), 5.
Upstill-Goddard, R.C., Barnes, J., Frost, T., Punshon, S., Owens, N.J.P., (2000). Methane in the southern North Sea: Low-salinity inputs, estuarine removal, and atmospheric flux. Glob. Biogeochem. Cycles. 14(4), 1205-1217.
Yamamoto S., Alcauskas J., Crozier Th. (1976) Solubility of methane in distilled water and seawater. J. Chem. Eng. Data. (21), 78-80.
Zhang G., Zhang J., Liu S. et al. (2008) Methane in the Changjiang (Yangtze River) Estuary and its adjacent marine area: riverine input, sediment release and atmospheric fluxes. Biogeochemistry. 91, 71-84
Дополнительные материалы отсутствуют.


