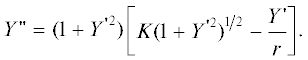Химическая физика, 2019, T. 38, № 2, стр. 52-62
Оценка скоростей химического превращения смесевых взрывчатых веществ, основанная на экспериментальных данных по псевдоидеальной детонации
Б. С. Ермолаев 1, *, А. А. Шевченко 1, 2, А. Ю. Долгобородов 1, 2, 3, И. В. Маклашова 2
1 Институт химической физики им. Н.Н. Семёнова Российской академии наук
Москва, Россия
2 Национальный исследовательский ядерный университет “МИФИ”
Москва, Россия
3 Объединенный институт высоких температур Российской академии наук
Москва, Россия
* E-mail: bse@chph.ras.ru
Поступила в редакцию 20.06.2018
После доработки 20.08.2018
Принята к публикации 06.08.2018
Аннотация
Рассмотрены условия, при которых на кривой зависимости скорости детонации взрывчатых смесевых композиций от диаметра заряда появляется платообразный участок, получивший название псевдоидеальная детонация. Для анализа использована теоретическая модель стационарной неидеальной детонации со слабо искривленным фронтом и двухстадийным механизмом химического превращения. Расчеты проведены для смеси тротила с 50% нитрата аммония и механоактивированной смеси перхлората аммония с 20% алюминия. В расчетах проводился подбор коэффициентов в уравнениях, описывающих глобальные скорости химического превращения компонентов. В обоих случаях зависимость скорости детонации от обратного значения диаметра заряда с платообразным участком получена при увеличении коэффициента скорости превращения основного взрывчатого компонента (тротила и перхлората аммония соответственно).
ВВЕДЕНИЕ
Зависимость скорости детонации от диаметра заряда, D(d), относится к тем видам информации, которые могут быть использованы для оценки скоростей экзотермического превращения в зоне реакции детонационной волны. Процедура оценки включает проведение теоретических расчетов зависимости D(d) и подбор коэффициентов скорости превращения (обычно это два коэффициента: константа скорости с размерностью 1/с и показатель степени в зависимости скорости превращения от давления), которые обеспечивают наилучшее согласие расчетной зависимости D(d) с экспериментом. Примеры таких исследований можно найти в работах [1, 2]. Значения коэффициентов подбираются с погрешностью, существенно меньшей 10%.
Трудности возникают в случае смесевых систем, когда экзотермическое химическое превращение с очевидностью протекает в несколько стадий. Типичным примером могут быть смеси двух взрывчатых компонентов типа тротил/нитрат аммония, где экзотермическое разложение тротила и нитрата аммония протекает с разными скоростями и, кроме того, имеется еще стадия химического взаимодействия продуктов разложения, которая приводит к дополнительному выделению энергии. Другой пример дают смеси окислитель/горючее (например, смеси перхлората аммония с алюминием или парафином); в этом случае также присутствуют две стадии: разложение окислителя и горение горючего компонента в продуктах разложения окислителя. Для смесей количество неизвестных коэффициентов скорости химического превращения увеличивается, и даже использование серии экспериментальных зависимостей скорости детонации от диаметра заряда, получаемых при изменении, например, соотношения компонентов смеси или размера частиц, чаще всего оставляет ситуацию с подбором коэффициентов скоростей химического превращения неопределенной.
Дополнительные возможности для анализа появляются, если использовать так называемую “псевдоидеальную детонацию” – зависимость D(d), имеющую платообразный участок. При изменении диаметра заряда на платообразном участке скорость детонации остается практически постоянной, тогда как вне этого участка увеличение d вызывает очевидный рост D. Такого вида немонотонную зависимость у ряда смесевых ВВ впервые обнаружили почти полвека назад Апин, Соснова и Воскобойников [3]. Теоретическая трактовка, предложенная авторами, связывает появление платообразного участка со стадийностью химического превращения, когда один компонент взрывчатой смеси (назовем его “быстрым” компонентом) реагирует с высокой скоростью, а другой – со скоростью, существенно более низкой. В этих смесях при малых диаметрах заряда скорость детонации определяется “быстрым” компонентом. В области средних значений диаметров скорость детонации выходит на плато, так как время пребывания продуктов детонации в зоне реакции превышает время разложения “быстрого” компонента, но недостаточно велико, чтобы медленная стадия химического превращения второго компонента внесла ощутимый вклад в энергетику процесса. Медленная стадия реализуется лишь при больших диаметрах заряда, когда скорость детонации вновь начинает расти. При этом уровень скорости детонации на участке плато определяется долей ВВ, реагирующего с низкой скоростью. Чем выше эта доля в исходной композиции, тем ниже скорость детонации на участке плато.
Свойства псевдоидеальной детонации (скорость детонации на плато, диаметр заряда, при котором начинается плато, длина участка плато) дают дополнительные условия, при использовании которых процедура подбора коэффициентов скоростей превращения компонентов смеси становится более строгой. Конечно, для осуществления этих возможностей, прежде всего необходимы подробные экспериментальные данные, которые в окрестности условий, где реализуется псевдоидеальная детонация, должны включать такую информацию, как влияние размера частиц и соотношения компонентов смеси. В настоящее время публикации, относящиеся к псевдоидеальной детонации [3–7], содержат весьма ограниченные экспериментальные данные, а теоретическое обсуждение носит качественный характер.
В данной работе псевдоидеальная детонация впервые рассматривается с применением численного моделирования. В качестве объектов рассмотрены смесь тротил/нитрат аммония состава 50/50 и механоактивированные смеси перхлората аммония с 20% алюминия. Получены оценки скоростей химического превращения компонентов смесей, при которых реализуются участки зависимости скорости детонации от диаметра заряда с близкой к платообразной формой, и приведены распределения концентраций реагентов и продуктов превращения вдоль зоны реакции детонационной волны. Обсуждаются вопросы, связанные с получением более точного согласия расчетных и экспериментальных зависимостей.
ТЕОРЕТИЧЕСКАЯ МОДЕЛЬ
Анализ зависимости скорости детонации от диаметра заряда проведен с помощью модели стационарной неидеальной детонации со слабо искривленным фронтом, которая представлена в работах [2, 8]. Модель разработана в рамках механики двухфазной односкоростной реагирующей среды [9] с механическим равновесием компонентов. Химическое превращение протекает в две стадии. Основы теории вместе с процедурой, позволяющей свести задачу к интегрированию системы обыкновенных дифференциальных уравнений с граничными условиями, заданными на ударном фронте волны, взяты из работ [10, 11].
Детонационная волна, бегущая вдоль оси цилиндрического заряда двухкомпонентной смеси, включает в себя ударный скачок, выпуклый в направлении распространения волны; к скачку примыкает зона химического превращения, которая заканчивается на звуковой поверхности (или поверхности Чепмена–Жуге); здесь в каждой точке скорость течения в системе координат, движущейся с фронтом волны, равна местной скорости звука. Кривизна фронта волны вызвана действием боковой волны разрежения, которая возникает на кромке заряда в результате разлета продуктов детонации в окружающую среду. В стационарной детонационной волне, распространяющейся с постоянной скоростью, действие боковой разгрузки достигает оси заряда, вызывая дивергенцию течения в осевой трубке тока и задавая кривизну фронта волны на оси заряда. По мере удаления вдоль фронта от оси заряда локальная кривизна фронта (K) растет. В системе координат Y (расстояние вдоль оси заряда) – r (радиальное расстояние от оси заряда) осесимметричную форму фронта детонационной волны можно получить, интегрируя следующее дифференциальное уравнение [10]:
Граничные условия на оси заряда:
Уравнение (1) интегрируется до кромки заряда (до точки r = r*), где для заряда без оболочки скорость течения на фронте волны принимается равной скорости звука. Эта точка определяет диаметр заряда. Для решения задачи нужно связать локальную кривизну фронта волны K с характеристиками течения в зоне реакции. Допуская, что в каждой точке вдоль фронта волны скорость волны по нормали к фронту, Dn, есть функция локальной кривизны фронта, а также что радиус кривизны фронта (2/K) много больше толщины зоны реакции, можно, следуя данным работ [10, 11], показать, что в каждой локальной трубке тока зоны реакции, начинающейся на фронте волны, течение оказывается близким к сферически симметричному случаю и эффект дивергенции потока вдоль трубки тока выражается следующей формулой:
(3)
$\frac{d}{{dx}}(\ln S) = ({{{{D}_{n}}} \mathord{\left/ {\vphantom {{{{D}_{n}}} U}} \right. \kern-0em} U} - 1)\frac{K}{{1 - {{Kx} \mathord{\left/ {\vphantom {{Kx} 2}} \right. \kern-0em} 2}}}.$Здесь x – расстояние вдоль данной трубки тока, значение x = 0 отвечает фронту волны; S – площадь сечения трубки тока, принятая равной единице на ударном фронте волны; U – скорость течения; Dn – скорость волны по нормали к фронту для данной трубки тока, связанная со скоростью детонации вдоль оси заряда уравнением
(4)
${{D}_{n}} = {D \mathord{\left/ {\vphantom {D {{{{(1 + {{Y}^{{'2}}})}}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}}}} \right. \kern-0em} {{{{(1 + {{Y}^{{'2}}})}}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}}}.$Реагирующая среда есть смесь исходных компонентов и продуктов их химического превращения, которое протекает в две стадии. К примеру, в случае смеси перхлората аммония с алюминием рассматриваются разложение перхлората аммония (стадия 1) и горение частиц алюминия в продуктах разложения перхлората аммония (стадия 2). Соответственно, реагирующая среда включает четыре компонента: перхлорат аммония (i = 1), продукты его разложения (i = 2), алюминий (i = 3) и продукты его горения (i = 4). Состояние среды в каждой точке определяется массовыми долями, плотностью и внутренней энергией этих компонентов с учетом их уравнений состояния и правил аддитивности, которые позволяют найти плотность и внутреннюю энергию среды по плотности и энергии компонентов. Компоненты находятся в локальном механическом равновесии, т.е., имеют одинаковое давление P и одинаковую массовую скорость U, тогда как значения их температуры, внутренней энергии и плотности различаются. Химическое превращение (горение) инициируется в процессе вязкопластического схлопывания пор в пределах фронта волны. Задержка инициирования мала в масштабе времени химического превращения, и ею пренебрегается. Квазиодномерное приближение, которое используется для расширяющегося потока реагирующей среды, позволяет свести задачу к интегрированию системы обыкновенных дифференциальных уравнений с граничными условиями, заданными на ударном фронте волны.
Уравнения, описывающие течение реагирующей среды в расширяющейся трубке тока, в системе координат, связанной с фронтом стационарной волны (при x ≥ 0), имеют следующий вид. Уравнения баланса массы, количества движения и энергии смеси:
Уравнения баланса массы для трех любых компонентов и энергии для двух любых i-тых компонентов, например,
(8)
$\begin{gathered} \rho U\frac{{d{{\eta }_{i}}}}{{dx}} = - {{M}_{i}},\,\,\,\,i = 1,2,3; \\ \frac{{d{{e}_{i}}}}{{dx}} - \frac{P}{{\rho _{i}^{2}}}\frac{{d{{\rho }_{i}}}}{{dx}} = 0,\,\,\,\,i = 1,3. \\ \end{gathered} $Уравнения состояния продуктов реакции и исходных компонентов смеси:
(9)
$\begin{gathered} P = {{\Gamma }_{i}}{{\rho }_{i}}({{e}_{i}} - {{e}_{{0i}}}) + {{B}_{i}}\rho _{i}^{m}\left( {1 - \frac{{{{\Gamma }_{i}}}}{{m - 1}}} \right), \\ i = 2,4, \\ \end{gathered} $(10)
$\begin{gathered} P = {{\Gamma }_{i}}{{\rho }_{i}}({{e}_{i}} - {{e}_{{0i}}}) + \\ + \,\,{{B}_{i}}\left[ {{{{\left( {\frac{{{{\rho }_{i}}}}{{{{\rho }_{{i0}}}}}} \right)}}^{l}}\left( {1 - \frac{{{{\Gamma }_{i}}}}{{l - 1}}} \right) - {{\Gamma }_{i}} - 1 + \frac{{{{\rho }_{i}}}}{{{{\rho }_{{0i}}}}}\frac{{{{\Gamma }_{i}}l}}{{l - 1}}} \right], \\ i = 1,3. \\ \end{gathered} $Уравнение, вытекающее из равенства температур продуктов химического превращения:
(11)
$P\left( {1 - \frac{{{{\Gamma }_{2}}{{c}_{{v2}}}}}{{{{\Gamma }_{4}}{{c}_{{v4}}}}}} \right) = {{B}_{2}}\rho _{2}^{m} - \frac{{{{\Gamma }_{2}}{{c}_{{v2}}}}}{{{{\Gamma }_{4}}{{c}_{{v4}}}}}{{B}_{4}}\rho _{4}^{n}.$Оно получено с использованием формулы P = $ = {{\Gamma }_{i}}{{с }_{{vi}}}{{T}_{i}} + {{B}_{i}}\rho _{i}^{m}.$
Алгебраические связи для смеси
(12)
$e = \sum {{{\eta }_{i}}{{e}_{i}}} ,\,\,\,\,{1 \mathord{\left/ {\vphantom {1 \rho }} \right. \kern-0em} \rho } = \sum {{{{{\eta }_{i}}} \mathord{\left/ {\vphantom {{{{\eta }_{i}}} {{{\rho }_{i}}}}} \right. \kern-0em} {{{\rho }_{i}}}}} ,\,\,\,\,\sum {{{\eta }_{i}}} = 1.$Здесь e – внутренняя энергия, ρ – плотность, η – массовая доля, S – площадь поперечного сечения трубки тока, Mi – скорость расхода i-го компонента смеси в единице объема, Г – коэффициент Грюнейзена, ${{c}_{v}}$ – теплоемкость при постоянном объеме, B, l, n и m – константы уравнений состояния, индекс “0” относится к начальным условиям. Теплота реакции разложения первого компонента равна разности Q1= e01 – e03.
Для первого компонента скорость химического превращения выражена следующей формулой:
(13)
$\begin{gathered} {{M}_{1}} = {{\rho }_{{10}}}{{({{{{\eta }_{1}}} \mathord{\left/ {\vphantom {{{{\eta }_{1}}} {{{\eta }_{{10}}}}}} \right. \kern-0em} {{{\eta }_{{10}}}}})}^{{{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}}}}{{G}_{1}}[{{({P \mathord{\left/ {\vphantom {P {{{P}_{{ref}}}}}} \right. \kern-0em} {{{P}_{{ref}}}}})}^{n}} + \\ + \,\,F{{({P \mathord{\left/ {\vphantom {P {{{P}_{{ref}}}}}} \right. \kern-0em} {{{P}_{{ref}}}}})}^{k}}]. \\ \end{gathered} $Эта формула включает в себя общепринятую зависимость от массовой доли взрывчатого компонента с показателем степени 2/3 [12] и зависимость от давления, которая содержит два слагаемых с показателями степени n и k. Показатель n выражает влияние давления на скорость химического превращения компонента в режиме взрывного горения [13], которое инициируется в горячих точках на фронте волны и протекает по поверхности частиц компонента. Его величина имеет значение, близкое к единице. Показатель k вместе с константой F выражает вклад реакций разложения, которые протекают в объеме частиц компонента; они реализуются при высоких давлениях. Величина показателя k ≈3. Коэффициент Pref = 1 ГПа введен для удобства, с тем чтобы коэффициент скорости G1 имел привычную размерность с–1 независимо от показателей степени по давлению.
Если вторым компонентом смеси также является взрывчатое вещество, то скорость его превращения описывается этой же формулой. Если же рассматривается смесь окислителя с горючей добавкой, например с алюминием, то скорость горения алюминия в продуктах разложения окислителя выражается другой формулой:
(14)
${{M}_{3}} = {{\rho }_{3}}{{G}_{3}}{{({{{{\eta }_{3}}} \mathord{\left/ {\vphantom {{{{\eta }_{3}}} {{{\eta }_{{03}}}}}} \right. \kern-0em} {{{\eta }_{{03}}}}})}^{{{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}}}}{{({P \mathord{\left/ {\vphantom {P {{{P}_{{ref}}}}}} \right. \kern-0em} {{{P}_{{ref}}}}})}^{r}}\left( {\frac{{{{C}_{{ox}}}}}{{1 + {{{{\eta }_{4}}} \mathord{\left/ {\vphantom {{{{\eta }_{4}}} {{{\eta }_{2}}}}} \right. \kern-0em} {{{\eta }_{2}}}}}}} \right).$Здесь Cox – концентрация кислородсодержащих газов, которые участвуют в окислении горючего компонента, в составе продуктов разложения окислителя. Обычно это O2, H2O и CO2; величина Cox определяется с учетом активности этих газов [14]. Формула (14) записана в предположении, что частицы алюминия горят в диффузионном режиме, скорость реакции зависит от давления с показателем степени r (хотя в данной работе используется предположение, что r = 0) и пропорциональна локальной концентрации кислорода в смеси, которая растет благодаря химическому превращению окислителя и снижается в ходе горения алюминия. Зависимость от исходного размера частиц в явном виде не входит в формулы (17) и (18). Она учитывается через константы скорости G1 и G3, которые используются в качестве варьируемых параметров и изменяются соответствующим образом при изменении размера частиц.
Коэффициенты, входящие в уравнения состояния исходных компонентов, определялись из литературных данных по ударно-волновой сжимаемости и коэффициенту Грюнайзена. Для продуктов химического превращения использовалась следующая процедура. С помощью термодинамической программы TDS [15] проводили серию расчетов параметров детонации Чепмена–Жуге, варьируя начальную плотность смеси в диапазоне, в котором расчетное давление детонации охватывало значения, ожидаемые для анализируемого процесса. Затем подбирали коэффициенты уравнения состояния (9), которые наилучшим образом воспроизводили расчетные данные по зависимости давления, скорости звука, плотности продуктов и скорости детонации от плотности смеси.
Система (5)–(12) включает восемь обыкновенных дифференциальных и восемь алгебраических уравнений для 16 независимых переменных. Уравнения интегрируются от фронта волны (х = 0). Условия на фронте волны, помимо стандартных уравнений сохранения массы, количества движения и энергии смеси на скачке и приведенных выше алгебраических соотношений и уравнений состояния для компонентов, включают также три дополнительных уравнения. Первое уравнение связано с предположением о распределении энергии ударного сжатия между исходными компонентами смеси. Здесь, следуя рассуждениям, приведенным в работе [16], мы предполагаем, что прирост энергии смеси в ударном скачке распределяется между двумя ее исходными компонентами обратно пропорционально квадрату их акустических импедансов, равных произведению плотности на скорость звука. Далее необходимо сделать определенные предположения о степени химического превращения во фронте волны. В данной работе предполагалось, что при ударном сжатии во фронте волны формируются горячие точки, в которых реагирует небольшое количество первого компонента (2%). И наконец, нужно было задать плотность продуктов разложения, для чего использовались результаты термодинамических расчетов, проводимых при подборе коэффициентов уравнения состояния.
Решение, отвечающее зоне реакции, должно проходить через особую сингулярную точку Чепмена–Жуге, в которой выполняется условие, что квадрат числа Маха (отношение скорости течения к скорости звука) M 2 = 1. Это решение находилось методом пристрелки. Найденное решение определяет кривизну фронта K при заданном значении скорости детонации, нормальной к фронту, Dn. Расчеты, проведенные для нескольких скоростей детонации, позволяют получить зависимость K(Dn). Затем эта зависимость используется при интегрировании уравнения (1), результатом которого является диаметр заряда, отвечающий заданной скорости детонации D.
ПРИМЕРЫ АНАЛИЗА ПСЕВДОИДЕАЛЬНОЙ ДЕТОНАЦИИ
Смесь тротила с нитратом аммония
В литературе можно найти экспериментальные данные по псевдоидеальной детонации для смеси тетранитрометана с крупнодисперсным гексогеном состава 70/30 [3] и для смеси гексогена с нитратом аммония [5]. Согласно работе [17], в случае смеси крупнодисперсного тротила с кристаллическим нитратом аммония 50/50 насыпной плотности псевдоидеальная детонация отсутствует. Тем не менее именно эта смесь привлекла наше внимание по следующим причинам. Во-первых, у нас имеются данные относительно скоростей химического превращения чистого тротила с частицами средним размером 0.5 мм и кристаллического нитрата аммония. Эти данные получены в работах [2, 18] путем анализа соответствующих экспериментальных данных по зависимости скорости детонации от диаметра заряда. Во-вторых, при измельчении тротила можно ожидать увеличения его скорости разложения в зоне реакции детонационной волны, и поэтому представляет интерес оценить условия, при которых становится возможной псевдоидеальная детонация этой смеси.
Расчеты проводились в предположении, что химическое превращение смеси проходит в две стадии. На первой стадии имеет место разложение тротила; коэффициенты скорости разложения, входящие в формулу (13) и полученные в работе [2] при обработке экспериментальных данных из работы [19], равны G1 = 0.04 мкс–1, n = 1, F = 0.3, k = = 2.8. Эти данные представляют собой зависимость скорости детонации от диаметра заряда, которая включает в себя две раздельные ветви – для нормальной и низкоскоростной детонации, расположенные одна над другой. Наличие двух ветвей позволяет с хорошей точностью определить все четыре коэффициента, входящие в формулу скорости превращения (13).
На второй стадии происходит разложение нитрата аммония и одновременно взаимодействие этих продуктов с продуктами разложения тротила. Предполагается, что время перемешивания продуктов пренебрежимо мало и взаимодействие с продуктами разложения тротила происходит сразу по мере того, как в газовой фазе появляются продукты разложения нитрата аммония. Коэффициенты скорости разложения кристаллического нитрата аммония в детонационной волне, полученные в работе [18], равны G3 = 0.011 мкс–1, n = 1.1, F = 0.
В расчетах использовались следующие коэффициенты уравнений состояния: для тротила ρ10 = = 1650 кг/м3, e10 = –0.276 МДж/кг, Г1 = 0.74, l = 6.9 и B1 = 1.366 ГПа; для продуктов разложения тротила e20 = –4.4 МДж/кг, Г2 = 0.5, m = 3.513 и B2 = 0.04735; для исходного нитрата аммония ρ30 = 1725 кг/м3, e30 = –4.56 МДж/кг, Г1 = 0.9, l = 6.8 и B1 = 1.22 ГПа; для конечных продуктов детонации смеси e40 = = –7.36 МДж/кг, Г4 = 0.45, m = 3.133 и B2 = 1.018.
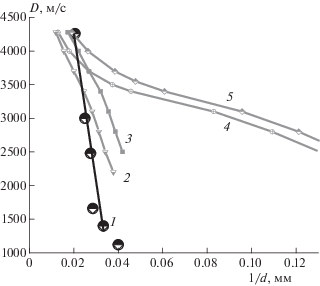
Результаты расчетов для смеси тротил/нитрат аммония состава 50/50 в виде зависимости скорости детонации от обратного значения диаметра заряда приведены на рис. 1. Здесь же представлена экспериментальная зависимость, взятая из работы [17]. Расчеты проведены для четырех вариантов, в которых величина константы скорости разложения тротила G1 варьировалась от 0.04 до 0.30 мкс–1 при постоянной величине константы скорости разложения нитрата аммония (G3 = = 0.011 мкс–1). Зависимость 2 получена при базовом значении константы G1 = 0.04 мкс–1; она, как и экспериментальная зависимость, имеет форму, близкую к линейной. Обе зависимости лежат примерно в одном диапазоне значений диаметров заряда, однако расчетная линия имеет более низкий наклон. Зависимость 5, полученная при G1 = 0.30 мкс–1, имеет отчетливый участок псевдоидеальной детонации в диапазонах значений скоростей 3400–3100 м/с и диаметров заряда от 36 до 14 мм. Зависимость 4, полученная при G1 = = 0.20 мкс–1, близка к зависимости 5 и также имеет участок, похожий на плато, но меньший по длине. Зависимость 3, полученная при G1 = 0.10 мкс–1, занимает промежуточное положение.
Рис. 1.
Зависимость скорости детонации от обратного диаметра заряда для смеси тротил/нитрат аммония состава 50/50: 1 – экспериментальные данные из работы [17]; результаты расчетов при постоянной величине константы разложения нитрата аммония (G3 = = 0.011 мкс–1) и различной константе скорости разложения тротила, G1, мкс–1: 2 – 0.04, 3 – 0.10, 4 – 0.20, 5 – 0.30.
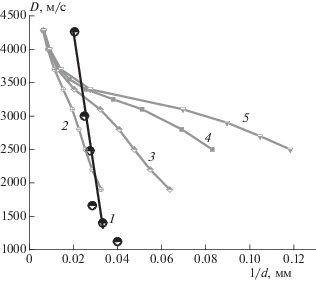
Распределения характеристик течения в зоне реакции на участке псевдоидеальной детонации при скорости детонации 3100 м/с в варианте с G1 = 0.30 мкс–1 и в случае базовой зависимости в варианте с G1 = 0.04 мкс–1 при той же скорости детонации приведены соответственно на рис. 2 и 3. Здесь, помимо концентраций компонентов реагирующей смеси, приведено распределение давления и величина (1 – М 2), которая обращается в нуль в точке Чепмена–Жуге. В варианте с псевдоидеальной детонацией длина зоны реакции равна 0.7 мм; в конце зоны реакции тротил полностью разложился, а доля прореагировашего нитрата аммония (относительно его исходного количества) составляет всего 3%. В варианте с G1 = 0.04 мкс–1 длина зоны реакции гораздо больше (5.2 мм), тротил полностью разложился, а нитрат аммония прореагировал на 11%.
Рис. 2.
Распределение характеристик течения в зоне реакции детонационной волны при скорости детонации 3100 м/с. Смесь ТНТ/нитрат аммония состава 50/50, G1 = 0.30 мкс–1; 1 – концентрация ТНТ, 2 – концентрация продуктов разложения ТНТ, 3 – концентрация нитрата аммония, 4 – концентрация продуктов детонации смеси, 5 – P(ГПа)/5, 6 – (1 – М 2).
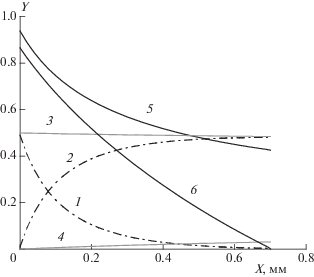
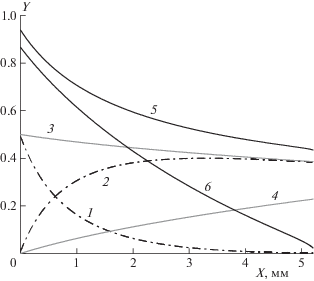
Рис. 3.
Распределение характеристик течения в зоне реакции детонационной волны при скорости детонации 3100 м/с. Смесь ТНТ/нитрат аммония состава 50/50, G1 = 0.04 мкс–1; 1 – концентрация ТНТ, 2 – концентрация продуктов разложения ТНТ, 3 – концентрация нитрата аммония, 4 – концентрация продуктов детонации смеси, 5 – P(ГПа)/5, 6 – (1 – М 2).
Эффект двух- и трехкратного увеличения коэффициента G3 при разных значениях коэффициента G1 показан на рис. 4. При G1 = 0.04 мкс–1 расчетные зависимости D(1/d) сдвинулись вправо, в область меньших диаметров заряда, сохраняя примерно линейную форму. Однако различие по наклону относительно экспериментальных данных осталось без изменения, как на рис. 1. При G1 = = 0.30 мкс–1 расчетные зависимости демонстрируют одинаковые участки псевдоидеальной детонации, расположенные один над другим. В целом, при равном диаметре заряда увеличение коэффициента G3 от 0.011 до 0.022 и далее до 0.033 мкс–1 вызывало увеличение скорости детонации на 110 м/с в каждом случае.
Рис. 4.
Влияние двух- и трехкратного увеличения коэффициента скорости разложения нитрата аммония на расчетную зависимость скорости детонации от обратного диаметра заряда для смеси тротил/нитрат аммония состава 50/50; 1 – экспериментальные данные из работы [15]; результаты расчетов при различных коэффициентах G1 и G3, мкс–1: 2 – 0.04 и 0.022, 3 – 0.04 и 0.033, 4 – 0.30 и 0.022, 5 – 0.30 и 0.022.
Таким образом, расчеты предсказывают, что 5–7-кратное увеличение коэффициента скорости разложения тротила, которое в опыте может быть достигнуто за счет приблизительно такого же уменьшения размера частиц тротила (от 500 мкм до 70–100 мкм), должно привести к появлению участка псевдоидеальной детонации. Уровень скорости детонации на участке плато может быть использован для уточнения значения константы скорости разложения нитрата аммония. Вопрос о том, как достичь количественного согласия расчетов с экспериментом по наклону зависимости D(1/d) в вариантах, где отсутствует участок псевдоиделаьной детонации, остается открытым. Наиболее вероятной причиной этого является рост скорости разложения нитрата аммония при повышенных давлениях, вызванный интенсификацией химических реакций, протекающих в объеме материала. Величина показателя степени по давлению для скорости превращения нитрата аммония (n = 1.1) получена путем обработки экспериментальных данных, в которых расчетное давление не превышало 3–4 ГПа. Это значение показателя степени отвечает химическим реакциям, локализованным на поверхности частиц. При более высоких давлениях, которые реализуются, когда скорость детонации смеси оказывается выше 3 км/с, вкладом объемных реакций, скорее всего, нельзя пренебрегать.
Смеси перхлората аммония с алюминием
Впервые в системе окислитель–горючее псевдоидеальная детонация была получена в смеси перхлората аммония (ПХА) с 10% парафина [3]. Для смесей мелкоизмельченного ПХА с алюминием до последнего времени (см., например, [20]) наблюдалась лишь зависимость скорости детонации от обратного значения диаметра заряда, имеющая обычную линейную форму, без участка псевдоидеальной детонации.
Новые исследования, выполненные недавно в механоактивированных смесях перхлората аммония с субмикронным порошком алюминием [6, 21], обнаружили платообразный участок на зависимости скорости детонации от обратного значения диаметра заряда. В этих опытах использовались следующие исходные компоненты: ПХА – полидисперсный порошок с частицами диаметром менее 20 мкм; алюминий трех видов – пудра марки ПП-2 (частицы в форме чешуек микронной толщины), ультрадисперсный сферический порошок марки “Alex” с частицами размером 150–200 нм (производство ООО “Передовые порошковые технологии”, Томск) и наноразмерный порошок алюминия (n-Al) с частицами размером около 100 нм (изготовлен в ИНЭПХФ РАН). Смешение и активация компонентов проводились в планетарной мельнице “Активатор-2SL” в стальных барабанах со стальными шарами. Для снижения механической чувствительности составов вводилась добавка 3% (по массе) фторопласта-42 (Ф-42). Подробности активации, смешения и сушки можно найти в работе [6]. Заряды цилиндрической формы собирались из таблеток, прессованных до заданной плотности, высотой 10–20 мм; диаметр заряда варьировался от 10 до 50 мм, длина зарядов составляла не менее 10 диаметров.
Экспериментальные данные по скорости детонации смесей ПХА с 20% алюминия трех разных типов в зарядах без оболочки при плотности заряда 1.54 г/см3 (относительная плотность около 0.75) приведены на рис. 5. Прямые линии 1 и 2 представляют детонацию смеси с алюминием марки ПП-2, время активации – 1 и 10 мин соответственно. Экстраполяция линий на бесконечный диаметр выходит в точку 6050 м/с, что согласуется с термодинамическим расчетом для идеальной детонации смеси, выполненным по программе TDS [15].
Рис. 5.
Зависимость скорости детонации от обратного диаметра заряда для смесей ПХА с 20% алюминия разных марок и разного времени активации. Экспериментальные данные: 1 – ПП-2, 1 мин активации; 2 – ПП-2, 10 мин активации; 3 – “Alex”, 10 мин активации. Численное моделирование: 4 – G1 = 0.18 мкс–1, F = 0 и G3 = 0.2 мкс–1; 5 – G1 = 0.12 мкс–1, F = 0.01 и G3 = 0.5 мкс–1; 6 – G1 = 0.32 мкс–1, F = 0.01 и G3 = 1.0 мкс–1; 7 – G1 = 0.4 мкс–1, F = 0.01 и G3 = 1.0 мкс–1.
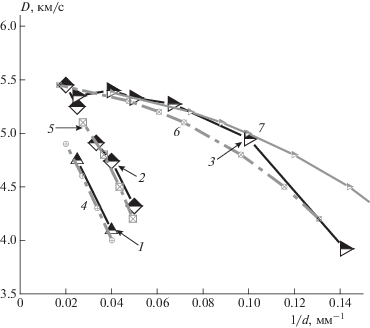
Кривая линия 3 на рис. 5 представляет детонацию смеси с наноразмерным порошком алюминия, время активации составляет 10 мин. В интервале значений диаметров заряда от 14 до 42 мм кривая имеет явно выраженный участок псевдоидеальной детонации при скорости детонации на уровне 5300 м/с. Очень близкие значения скорости детонации получены в смеси с ультрадисперсным алюминием марки “Alex”; эти данные на графике не приведены.
Теоретическое исследование неидеальной детонации смесей ПХА с алюминием проводилось в работе [8]. Для анализа использовались данные по детонации смесей ПХА (размер частиц – 8 мкм) с алюминием (7 мкм), полученные в работе [20], а также данные по детонации чистого ПХА [20, 22] в оболочках из целлофана. Показано, что две стадии химического превращения (разложение ПХА и диффузионное горение частиц алюминия) протекают с близкими скоростями в широком диапазоне дисперсностей компонентов. Наилучшее согласие этих данных с расчетом получено при G1 = = 0.43 мкс–1, n = 1, F = 0 и G3 = 0.6 мкс–1. Отличительной чертой детонации смесей ПХА с алюминием является то, что, несмотря на значительный рост теплоты взрыва, добавка алюминия обеспечивает лишь сравнительно небольшой прирост скорости идеальной детонации из-за уменьшения сжимаемости продуктов детонации. Резкое повышение активности детонации смесей, наблюдаемое в эксперименте при добавке алюминия, объясняется не столько ростом теплоты взрыва, сколько увеличением в несколько раз скорости разложения ПХА в смеси по сравнению с чистым ПХА. Причиной этого роста, предположительно, является тепловой поток из зоны диффузионного горения алюминия, которая окружает разлагающиеся частицы ПХА.
Расчеты по неидеальной детонации механоактивированной смеси ПХА с 20% алюминия проводили при следующих коэффициентах уравнений состояния: для ПХА ρ10 = 1950 кг/м3, e10 = –2.52 МДж/кг, Г1 = 0.92, l = 6.4 и B1 = 2.37 ГПа; для продуктов разложения ПХА e20 = –3.95 МДж/кг, Г2 = 0.48, m = = 3.692 и B2 = 8.08 ⋅ 10–3; для алюминия ρ30 = = 2700 кг/м3, e30 = –0.415 МДж/кг, Г1 = 1.7, l = 6.8 и B1 = 10.74 ГПа; для продуктов превращения смеси e40 = –6.8 МДж/кг Г4 = 0.23, m = 4.0743 и B2 = = 0.3639 ⋅ 10–3. Результаты расчетов, достаточно хорошо воспроизводящие экспериментальные зависимости скорости детонации от обратного диаметра заряда, приведены на рис. 5 вместе с результатами опытов.
Линия 4 на рис. 5, которая относится к детонации смеси с алюминием марки ПП-2 при времени активации 1 мин, получена при G1 = 0.18 мкс–1, n = = 1.2, F = 0 и G3 = 0.2 мкс–1. Значения коэффициентов скорости разложения оказались ниже, чем те, что были получены ранее при анализе экспериментальных данных работы [20] по детонации смеси с 10% алюминия при плотности 1.1 г/см3. Причиной, скорее всего, является высокая начальная плотность смеси (1.55 г/см3): снижение активности чистого ПХА и смесей на его основе по мере роста начальной плотности является тенденцией, хорошо известной из опытов по детонации [20]. Количественное выражение этого эффекта в виде изменения коэффициента скорости превращения можно найти в работе [8]: при детонации ПХА в диапазоне плотностей заряда от 1.0 до 1.25 г/см3 коэффициент скорости превращения снизился с 0.43 до 0.18 мкс–1. Впрочем, наличие двух стадий химического превращения смеси допускает определенный произвол: почти такой же результат можно получить при других значениях коэффициентов, например при G1 = 0.1 мкс–1 и G3 = 1.0 мкс–1. Наконец, более высокая величина показателя степени по давлению (n = 1.2 вместо 1.0) использована, чтобы наклон линии лучше соответствовал экспериментальным точкам. Вообще, при скоростях детонации от 4.5 км/с и выше давление в значительной части зоны реакции превышает 10 ГПа. При этих давлениях, по-видимому, необходимо учитывать усиление зависимости скорости химического превращения ПХА от давления за счет протекания объемного разложения.
Этот эффект был учтен при расчетах детонации смесей с временем активации, равным 10 мин. Использовался следующий набор констант, определяющих зависимость от давления в формуле (13): n = 1.2, F = 0.01 и k = 1.8. Следует, однако, отметить, что в отличие от тротила, для которого все три коэффициента, входящие в зависимость скорости превращения от давления, установлены с хорошей точностью благодаря наличию двух разных ветвей на зависимости D(d), для ПХА имеющихся данных недостаточно, и приведенные значения коэффициентов F и k пока выбраны произвольно. Расчеты, обеспечившие приемлемое согласие с экспериментом, проведены для смеси с алюминием марки ПП-2 при G1 = 0.12 мкс–1 и G3 = 0.5 мкс–1 (линия 5 на рис. 5) и для смеси с алюминием марки “Alex” при G1 = 0.32 мкс–1 и G3 = 1.0 мкс–1 (линия 6) и G1 = 0.4 мкс–1 и G3 = 1.0 мкс–1 (линия 7).
Сравнивая варианты расчетов, проведенных для смесей с алюминием марки ПП-2 при разном времени активации (линии 4 и 5 на рис. 5), можно отметить, что увеличение времени активации от 1 до 10 мин привело к росту скорости химического превращения ПХА, который благодаря второму слагаемому в формуле (13) составил от 2 до 5 раз в рассмотренном диапазоне скоростей детонации. Чтобы перейти от зависимости нормального вида (линия 5) к зависимости с участком псевдоидеальной детонации (линии 6 и 7), оказалось достаточным увеличить коэффициент скорости превращения ПХА G1 еще примерно в 2.5–3 раза. Линия 7 прекрасно воспроизводит экспериментальные данные на участке псевдоидеальной детонации, но спад скорости детонации при диаметрах заряда менее 10 мм происходит недостаточно круто. Линия 6 совпадает с экспериментом на участке спада, однако хуже согласуется с экспериментом на участке псевдоидеальной детонации.
Что касается величины коэффициента G3, то выбранные значения (0.5 и 1.0 мкс–1) достаточно произвольны. Изменение G3 в 2–3 раза приводит к незначительным изменениям зависимости D(1/d), которые можно легко компенсировать за счет небольшой коррекции коэффициента G1. Следует, однако, напомнить, что в эксперименте псевдоидеальная детонация механоактивированной смеси получена при замене чешуйчатого алюминия на порошки с частицами субмикронных размеров. Этому можно дать следующее объяснение. По-видимому, при механической обработке смесей активация ПХА в присутствии чешуек алюминия марки ПП-2, поперечные размеры которых при толщине около 1 мкм составляют десятки мкм, протекает менее энергично, чем в случае субмикронных порошков алюминия, состоящих из гораздо более мелких частиц сферической формы.
На рис. 6 приведены распределения характеристик течения в зоне реакции на участке псевдоидеальной детонации. Расчет проведен для варианта 7 рис. 5 при G1 = 0.40 мкс–1, диаметре заряда 36.1 мм, скорости детонации 5100 м/с). Аналогичные данные в случае зависимости нормальной прямолинейной формы (вариант 5 рис. 5, G1 = 0.12 мкс–1, диаметр заряда – 11.3 мм) при той же скорости детонации приведены на рис. 7. В варианте с псевдоидеальной детонацией длина зоны реакции равна 0.53 мм, в конце зоны реакции ПХА полностью разложился, а доля сгоревшего алюминия составила 6% из 20% (в исходном состоянии). Концентрация продуктов разложения ПХА быстро достигает максимальной величины (чуть более 40%) и затем медленно снижается. В варианте с прямолинейной зависимостью длина зоны реакции составляет 1.76 мм, ПХА также полностью разложился, доля сгоревшего алюминия достигла 7.5%, а максимальная величина концентрации продуктов разложения ПХА составила около 31%. Профиль давления вдоль зоны реакции имеет выпуклость вниз; давление на фронте волны равно 16.8 ГПа и снижается к концу зоны реакции почти в 2 раза (до 8.3 ГПа).
Рис. 6.
Расчетное распределение характеристик течения в зоне реакции детонационной волны при скорости детонации 5100 м/с в случае механоактивированной смеси ПХА/“Alex” состава 80/20, G1 = 0.4 мкс–1, F = 0.01 и G3 = 1.0 мкс–1: 1 – концентрация ПХА, 2 – концентрация алюминия, 3 – концентрация продуктов разложения ПХА, 4 – концентрация продуктов детонации смеси, 5 – P(ГПа)/20, 6 – (1 – М 2).
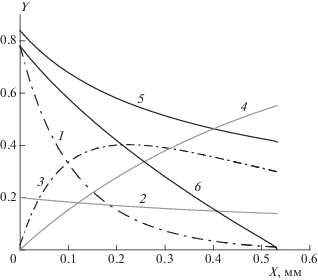
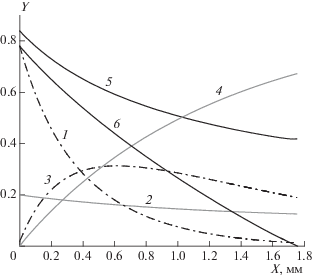
Рис. 7.
Расчетное распределение характеристик течения в зоне реакции детонационной волны при скорости детонации 5100 м/с в случае механоактивированной смеси ПХА c алюминием марки ПП-2, G1 = 0.12 мкс–1, F = 0.01 и G3 = 0.5 мкс–1: 1 – концентрация ПХА, 2 – концентрация алюминия, 3 – концентрация продуктов разложения ПХА, 4 – концентрация продуктов детонации смеси, 5 – P(ГПа)/20, 6 – (1 – М 2).
ОБСУЖДЕНИЕ
Псевдоидеальная детонация смесевых взрывчатых композиций (такое название получил платообразный участок на зависимости скорости детонации от диаметра заряда [3]) до сих пор остается сравнительно слабоизученным явлениям физики взрыва. Первое сообщение о нем появилось более 50 лет тому назад в публикации ученых из ИХФ РАН, однако оно не вызвало глубокого научного интереса. Качественное объяснение этого явления, связное со значительной разницей в скоростях химического превращения компонентов смеси, и некоторые оценки скорости детонации на участке плато, основанные на возможном вкладе компонентов в выделение химической энергии, составили основной позитивный результат этой первой и нескольких последующих публикаций, в которых затрагивалась тема псевдоидеальной детонации.
Вместе с тем экспериментальные данные по псевдоидеальной детонации могут представлять значительный интерес для развития работ, направленных на извлечение информации о скоростях химического превращения в зоне реакции детонационной волны. Подход, применяемый в исследованиях (см., например, работу [1]), состоит в подборе коэффициентов, входящих в предложенный закон скорости химического превращения, при использовании которых достигается наилучшее согласие результатов численного моделирования с экспериментальной зависимостью скорости детонации рассматриваемого ВВ от диаметра заряда. Для индивидуальных ВВ экспериментальная зависимость D(d) при заданных уравнениях состояния исходного ВВ и продуктов превращения позволяет с хорошей точностью определить значения коэффициентов, определяющих скорость превращения и ее зависимость от давления.
Однако в случае смесевых ВВ, когда химическое превращение включает как минимум две стадии, использование зависимости D(d) оставляет произвольным выбор значений коэффициентов. Даже если привлечь к анализу экспериментальные данные по скоростям превращения, полученные для отдельных компонентов смеси, то ситуация обычно не улучшается, так как скорость превращения основного компонента (например, перхлората аммония в смеси с алюминием) заметно увеличивается из-за присутствия алюминия [8]. В этом отношении псевдоидеальная детонация дает дополнительные возможности: уровень скорости детонации на участке плато, а также величины диаметра заряда, при которых начинается и заканчивается платообразный участок, – вся эта информация может быть использована для более точного определения коэффициентов скоростей химического превращения.
К сожалению, экспериментальные данные по псевдоидеальной детонации, имеющиеся в настоящее время, достаточно скудны и не могут удовлетворительно использоваться для систематического анализа. Как следствие, результаты данной работы, в которой численное моделирование было впервые применено к объектам псевдоидеальной детонации, носят в значительной мере иллюстративный характер.
Первым объектом, выбранным для анализа, была смесь тротила с нитратом аммония состава 50/50 насыпной плотности. В опытах, которые проводились в смеси с крупнодисперсным тротилом [17], псевдоидеальная детонация отсутствовала. В расчетах, которые были проведены при использовании значений коэффициентов скоростей превращения, подобранных ранее при анализе соответствующих экспериментальных данных для отдельных компонентов смеси, также была получена зависимость D(1/d) прямолинейной формы. Чтобы получить зависимость с платообразным участком при скоростях детонации на уровне 3100–3300 м/с, коэффициент скорости разложения тротила понадобилось увеличить в 5–7 раз. Это означает, что в опытах псевдоидеальную детонацию можно получить, измельчив крупнодисперсный тротил до размера частиц 70–100 мкм.
По результатам сопоставления расчетов с экспериментом для смеси тротила с нитратом аммония можно сделать следующие замечания. Тот факт, что при расчете детонации смеси оказалось возможным использовать коэффициенты превращения, подобранные для отдельных компонентов, означает, что взаимодействие компонентов данной смеси не оказывает влияние на скорости их превращения. Различие между расчетом и экспериментом, наблюдаемое по наклону зависимости D(1/d) для смеси с крупнодисперсным тротилом, скорее всего, вызвано тем, что разложение нитрата аммония протекает с более высоким показателем степени по давлению. Причина этого – заметно более высокие давления, которые наблюдаются при детонации смеси нитрата аммония с тротилом и которые недоступны в случае детонации чистого нитрата аммония. В результате наряду с реакциями взрывного горения, которые протекают по поверхности частиц нитрата аммония, становится ощутимым вклад химических реакций, протекающих в объеме материала. Однако для выбора надежных значений коэффициентов F и k, входящих в формулу (17), для нитрата аммония необходимо специальное исследование.
Вторым объектом анализа была выбрана псевдоидеальная детонация, обнаруженная на механоактивированных смесях перхлората аммония с субмикронным порошком алюминием [6, 19]. В экспериментах был использован алюминий нескольких марок, и было показано, что переход от зависимости D(1/d) прямолинейной формы к зависимости с платообразным участком происходит при замене чешуйчатого порошка марки ПП-2 на суб- и наноразмерные порошки с частицами сферической формы. Расчеты, проведенные применительно к смеси с алюминием марки ПП-2, подтвердили очевидное предположение, что увеличение времени механической активации приводит к росту скорости разложения перхлората аммония. Переход от зависимости D(1/d) нормальной формы также был получен целиком за счет увеличения коэффициента скорости превращения перхлората аммония G1 примерно в 2.5–3 раза. Этот результат позволяет предположить, что в присутствии чешуек алюминия марки ПП-2 активация перхлората аммония при механической обработке протекает менее энергично, чем в случае более мелких частиц субмикронных порошков, имеющих сферическую форму.
ЗАКЛЮЧЕНИЕ
Условия, при которых на зависимости скорости детонации взрывчатых смесевых композиций от диаметра заряда наблюдается платообразный участок (явление, названное псевдоидеальной детонацией), строго связаны с соотношением скоростей химического превращения компонентов смеси. В данной работе для анализа псевдоидеальной детонации впервые применено численное моделирование. Расчеты проводились для двух объектов: смеси тротила с 50% нитрата аммония и механоактивированной смеси перхлората аммония с 20% алюминия. В обоих случаях переход от зависимости D(1/d) нормального вида к зависимости с платообразным участком удалось получить путем увеличения коэффициента скорости превращения основного компонента (тротила и перхлората аммония соответственно). Для получения количественных результатов, включающих адекватные оценки скоростей химического превращения компонентов смесей, необходимы подробные экспериментальные данные по псевдоидеальной детонации, полученные с варьированием дисперсности и соотношения компонентов смесей. Такие данные в настоящее время отсутствуют.
Работа выполнена за счет субсидий, выданных ИХФ РАН на выполнение госзадания по темам 0082-2018-0002 (номер госрегистрации АААА-А18-118031490034-6) и 0082-2018-0011 (АААА-А17-117040610346-5) и ОИВТ РАН на выполнение госзадания по теме 0044-2014-0016 (АААА-А-16-116051810082-7).
Список литературы
Leiper G.A., Cooper J. // Proc. 10th Intern. Detonation Sympos. Boston: ONR, 1993. P. 267.
Ermolaev B.S., Khasainov B.A., Presles H.-N. // Proc. Europyro 2007 –34th IPS. V. 1. Broune, France: AFPYRO, 2007. P. 323.
Апин А.Я., Воскобойников И.М., Соснова Г.С. // ЖПМТФ. 1963. № 5. С. 115.
Апин А.Я., Димза Г.В. // ДАН СССР. 1970. Т. 192. № 4. С. 850.
Лавров В.В., Шведов К.К. // Хим. физика. 2003. Т. 22. № 9. С. 67.
Шевченко А.А., Долгобородов А.Ю., Кириленко В.Г., Бражников М.А. // Физика горения и взрыва. 2017. Т. 53. № 4. С. 103.
Лавров В.В. // Дис. … канд. физ.-мат наук. Черноголовка: ИПХФ РАН, 2008.
Ермолаев Б.С., Комиссаров П.В., Соколов Г.Н., Борисов А.А. // Хим. физика. 2012. Т. 31. № 9. С. 55.
Нигматулин Р.И. Динамика многофазных сред. Ч. 1. М.: Наука, 1987.
Swift D.C., Lambourn B.D. // Proc. 10th Intern. Detonation Sympos. Boston: ONR 33395-12, 1993. P. 386.
Bdzil J., Stewart D.S. // Phys. Fluids. A. 1989. V. 1. P. 1261.
Андреев С.Г., Бабкин А.В., Баум Ф.А. и др. Физика взрыва / Под ред. Орленко Л.П. Т. 1. М.: Физматлит, 2002.
Апин А.Я. // ДАН СССР. 1939. Т. 24. С. 922.
Beckstead M.W. // Proc. Internal Aerodynamics in Solid Rocket Propulsion. Rhode-Saint-Genèse, Belgium: RTO-EN-023, 2004. P. 5.
Викторов С.Б., Губин С.А., Маклашова И.В., Пепекин В.И. // Хим. физика. 2005. Т. 24. № 12. С. 22.
Мэйдер Ч. Численное моделирование детонации. М.: Мир, 1985.
Парфенов А.К., Воскобойников И.М. // Физика горения и взрыва. 1969. Т. 5. С. 347.
Ермолаев Б.С., Сулимов А.А. Конвективное горение и низкоскоростная детонация пористых энергетических материалов. M.: Торус пресс, 2017.
Парфенов А.К., Апин А.Я. // Научно-технич. проблемы горения и взрыва. 1965. № 1. С. 109.
Price D., Clairmont Jr. A.R., Erkman J.O. // Combust. and Flame. 1973. V. 20. P. 389.
Шевченко А.А., Кириленко В.Г., Бражников М.А., Долгобородов А.Ю. // Горение и взрыв. 2017. Т. 10. № 1. С. 84.
Andersen W.H., Pesante R.E. // Proc. 8th Sympos. (Intern.) on Combust. Baltimore, US: Williams Wilkins, 1961. P. 705.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика