Химическая физика, 2022, T. 41, № 1, стр. 25-33
Влияние благородных металлов на термоакустические колебания и границы области отрицательного температурного коэффициента при горении смесей н-пентан – воздух
К. Я. Трошин 1, *, Н. М. Рубцов 2, Г. И. Цветков 2, В. И. Черныш 2
1 Федеральный исследовательский центр химической физики им. Н.Н. Семёнова
Российской Академии наук
Москва, Россия
2 Институт структурной макрокинетики и материаловедения Российской академии наук
Москва, Россия
* E-mail: troshin@chph.ras.ru
Поступила в редакцию 19.02.2021
После доработки 16.03.2021
Принята к публикации 22.03.2021
- EDN: HQUVLU
- DOI: 10.31857/S0207401X22010162
Аннотация
Особенности воспламенения предварительно перемешанных стехиометрических смесей н-пентан – воздух изучены в области отрицательного температурного коэффициента скорости реакции (далее – ОТК) в статическом реакторе быстрого напуска в присутствии металлических платины и палладия. Показано, что в области ОТК в отсутствие благородных металлов происходят термоакустические колебания. Однако в присутствии платинового катализатора, который реагирует с кислородом при температуре пламени и генерирует каталитические центры, распространяющиеся в объем путем конвекции/диффузии, термоакустические режимы воспламенения исчезают. Другими словами, каталитическая поверхность платины устраняет определенную стадию кинетического механизма: вероятно, стадию ингибирования после возникновения холодного пламени, при этом явление ОТК исчезает. При наличии палладиевой каталитической поверхности, не генерирующей распространяющиеся в объем каталитические центры, явление ОТК наблюдается. Обнаруженные закономерности следует учитывать при численном моделировании этого явления в присутствии поверхности платины, т.е. приемлемый химический механизм должен описывать термоакустические колебания в области ОТК; исключение определенной стадии кинетического механизма (вероятно, поверхностного характера) должно вызвать исчезновение режима ОТК реакции в присутствии платинового катализатора. Стадия должна включать поверхностную реакцию активного промежуточного продукта горения на поверхности платины. В этой реакции более активные промежуточные продукты образуются из малоактивного продукта.
ВВЕДЕНИЕ
Изучение воспламенения углеводородов имеет очевидное практическое значение, однако нет полной ясности относительно природы необычных явлений, присущих этому процессу. К ним относятся стадийное воспламенение и отрицательный температурный коэффициент скорости реакции (далее – ОТК), наблюдаемые при сравнительно низких температурах. Явление ОТК проявляется в увеличении времени задержки самовоспламенения при росте температуры реактора в некотором интервале температур. Это вызывает нежелательные явления в двигателях внутреннего сгорания [1, 2]. Нет единого мнения относительно детальных механизмов окисления углеводородов в этом диапазоне температур, а также относительно понимания феномена ОТК.
Как известно, платиновый слой на поверхности реактора проявляет каталитическое действие на реакции окисления водорода и углеводородов [3]. Гетерогенные реакции с участием Pt увеличивают возможность самопроизвольного воспламенения газовой смеси на поверхности и заметно влияют на время задержки воспламенения. Состояние поверхности реактора является еще одним фактором, который определяет пространственную картину воспламенения. Некоторые расхождения в понимании проблемы по зажиганию легковоспламеняющихся газовых смесей каталитической проволокой проанализированы в работе [4]. Например, в работе [5] для определения температуры каталитического самовоспламенения легковоспламеняющуюся смесь медленно пропускали при атмосферном давлении над платиновым проводом или фольгой. Температуру катализатора повышали путем ступенчатого увеличения тока, подаваемого на катализатор. Однако в работе [6] расчеты температуры самовоспламенения сравнивали с данными для инициированного воспламенения [5], что неверно. Кроме того, в условиях течения газа температура зажигания смесей H2–O2 над палладиевой фольгой снижается для более бедных смесей [5], что согласуется с расчетами [5, 6]. Однако в статических условиях в нагретом химическом реакторе с платиновой проволокой внутри него температура самовоспламенения смеси H2–O2 увеличивается с ростом концентрации H2 в легковоспламеняющейся смеси [7]. В работе [5] рассмотрен детальный механизм адсорбции–десорбции и поверхностного окисления водорода на платине, приведены элементарные константы 23 элементарных реакций. Очевидно, что это лишь оценки, а не экспериментальные данные, поэтому достоверность расчетов сомнительна. Во всех рассмотренных выше работах предполагается, что температура вдоль проволоки равномерна; это противоречит эксперименту, приведенному в [4]. Поэтому конкретизация механизма каталитического действия Pt представляется преждевременной.
Подчеркнем, что конструкция и работа современных реакторов, таких как газовые турбины или стационарные и мобильные установки риформинга топлива, требуют надежных кинетических моделей для управления динамикой процессов горения. Явление ОТК вызывает снижение температуры смеси на входе [8]. Такое поведение известно как для высших углеводородов [9], так и для окисления метана. В практических условиях характеристики воспламенения углеводородного топлива можно разделить на два типа: с одностадийным самовоспламенением (ароматические соединения и спирты) и с многостадийным самовоспламенением (н-парафины, ненасыщенные и циклические углеводороды); при этом явление ОТК обычно наблюдается при температурах ниже 850 К. При двустадийном режиме воспламенение на первой стадии играет важную роль, поскольку воспламенение на второй стадии зависит от тепловыделения и промежуточных частиц, образующихся на первой стадии. Кроме того, режим ОТК охватывает температурный диапазон, который относится к детонации в двигателях и связанным с ней явлениям горения [10]. Поскольку углеводороды с двух- и многостадийным самовоспламенением обычно представляют основные топлива [11], процессы в двигателе согласно кинетике горения также будут происходить в две и более стадии; за низкотемпературной стадией тепловыделения следует высокотемпературная. Важно отметить, что топлива с двухступенчатым зажиганием обеспечивают значительные преимущества в управлении горением и расширении диапазона работы гомогенного воспламенения от сжатия [11, 12]. Следовательно, необходимо понимание явления ОТК для разработки новых стратегий контроля за экономией топлива и снижением выбросов загрязняющих веществ.
Отметим, что литературные данные часто ограничиваются экспериментами, проводимыми при относительно низких температурах и давлениях [13, 14]. Предсказать поведение системы для конкретных ситуаций, таких как присутствие разбавителей или при высоком давлении, довольно сложно. В работе [15] численно исследовали динамику горения в стратифицированной смеси н‑гептан – воздух и показали, что в богатых смесях со стратификацией топлива обнаруживаются стук и акустические явления.
Проводили одномерное моделирование для изучения самовоспламенения и распространения пламени в смеси н-гептан – воздух в широком диапазоне температур, включая режим ОТК, при повышенном давлении. Показано, что устойчивое распространение пламени в предварительно перемешанной смеси в условиях ОТК показывает двустадийное поведение, включая как горячее, так и холодное пламя [16].
Определить механизм зажигания систем углеводород – окислитель сложно. Согласно [17, 18], в ударной трубе и машине быстрого сжатия самовоспламенение локализовано в объеме. Мы показали [19], что воспламенение смесей н-пентан – воздух в статическом реакторе быстрого напуска смеси при давлении 1 атм начинается с появления первичного центра в наиболее химически активном месте на поверхности. Этот центр инициирует распространение фронта полусферического пламени с нормальной скоростью, соответствующей температуре стенок и составу газа; воспламенение включает стадии прогрева, локального воспламенения и распространения пламени. Реакция никогда не начинается в объеме, если объем не содержит активную поверхность, например аэрозоль [19].
Ранее мы провели следующие эксперименты, чтобы определить, оказывает ли поверхность реактора каталитический эффект на воспламенение углеводородов [20]. Мы ввели в нагретый реактор платиновую проволоку диаметром 0.3 мм и длиной 0.5 м. Было показано, что вдоль проволоки возникают центры зажигания. Без проволоки на поверхности реактора в интервале ОТК возникает только один центр зажигания.
Осциллограммы давления при зажигании в тех же условиях в отсутствие и присутствии каталитической поверхности показали, что в отсутствие катализатора холодное пламя, сопровождающееся небольшим разогревом, быстро превращается в горячее. Центры зажигания развиваются очень быстро, что указывает на возникновение горячего пламени, в то время как стадийное воспламенение и холодное пламя предшествуют стадии горячего пламени. Несмотря на то, что осциллограмма роста давления свидетельствует о холоднопламенном зажигании смеси, которое проявляется как небольшая ступень, предшествующая основному повышению давления и появляющаяся раньше, чем первичный центр зажигания, регистрируемый при видеосъемке, съемочные кадры не показывают холодного пламени.
Было также показано, что в различных температурных областях каталитическая поверхность по-разному воздействует на воспламенение. При сравнительно низкой температуре она не оказывает заметного влияния на время задержки воспламенения, но в температурной области, в которой обычно наблюдается ОТК, наличие этой же поверхности полностью его исключает [20]. В этом случае центры катализируемого воспламенения расположены вдоль поверхности проволоки, т.е. она служит источником воспламенения. Поскольку задержка зажигания в этом случае ведет себя так, как если бы не было разницы между холодным пламенем и горячим зажиганием в температурной области, соответствующей ОТК, можно предположить, например, что каталитическая поверхность устраняет определенную стадию кинетического механизма (стадию ингибирования) после появления холодного пламени. Этот факт представляется очень важным для выяснения природы промежуточных продуктов реакции, вызывающих существование ОТК. Однако остается неясным, как платиновая проволока, локализованная в небольшом объеме реактора, оказывает столь заметное влияние на объемный процесс.
Настоящая работа посвящена установлению особенностей воздействия благородных металлов (Pt, Pd) на режимы горения в области ОТК.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Воспламенение смесей н-пентан – воздух изучали в статическом реакторе быстрого напуска (рис. 1). Предварительно перемешанную топливовоздушную смесь из емкости для хранения пропускали через электромагнитный клапан в предварительно вакуумированный реактор и нагревали до требуемой температуры.
Рис. 1.
Принципиальная схема экспериментальной установки: 1 – реактор, 2 – электронагреватель, 3 – теплоизоляция, 4 – клапаны, 5 – смеситель, 6 – предохранительный клапан редуктора давления, 7 – съемная крышка, 8 – полусферическая вставка, 9 – датчик давления, 10 – система сбора данных на базе АЦП, 11 – цифровой вольтметр, 12 – схема зажигания, 13 – проволока из благородного металла.
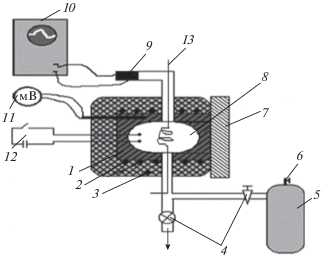
Реактор из нержавеющей стали внутренним диаметром 12 см и длиной 25 см состоял из двух полусферических частей и узкой цилиндрической части между ними. Конструкция нагревателя обеспечивала равномерное распределение температуры в объеме реактора [21], которое контролировали с помощью подвижной термопары, размещенной на поверхности реактора. В ряде экспериментов провода из Pt или Pd диаметром 0.3 мм и длиной 40 см размещали перпендикулярно оси реактора в его центральной части. Изменение давления во времени регистрировали пьезоэлектрическим преобразователем Karat-CI (4 кГц), сигнал от которого подавали через АЦП в компьютер. Перед каждым экспериментом реактор откачивали вакуумным насосом 2NVR 5D до 10–2 Торр. Давление в реакторе измеряли с помощью электронного и стандартного вакуумметров. Электромагнитный клапан использовали для открытия и закрытия газовых линий. Использовали н-пентан фирмы “Merck” (Germany) марки ХЧ, платина чистотой 99.9% и палладий чистотой 98.5%.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В предварительных опытах при измерениях температуры [21] в центре реактора диаметром и длиной 10 см тонкими термопарами длиной 25 мм при атмосферном давлении и температуре 800–980 К было показано, что время прогрева газовой смеси не превышает 0.2 с. Это намного меньше времени, получаемого при учете только теплопроводности.
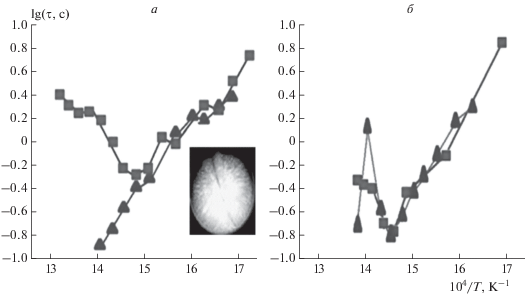
Перед некоторыми сериями экспериментов внутренний поверхностный слой реактора толщиной 0.5 мм удаляли механически. На рис. 2а сравниваются экспериментальные данные по времени задержки зажигания стехиометрической смеси н-пентан – воздух в отсутствие (первая серия экспериментов, прямоугольники) и в присутствии (вторая серия экспериментов, треугольники) каталитической поверхности платины. Как видно на рис. 2а, в области положительного температурного коэффициента при более низких температурах каталитическая поверхность Pt почти не влияет на время задержки зажигания. Однако в области отрицательного температурного коэффициента роль каталитической поверхности платины становится очень значительной в соответствии с изложенным в работе [20]. При наличии Pt-проволоки время задержки зажигания уменьшается только с увеличением температуры; явление ОТК отсутствует.
Рис. 2.
Температурная зависимость времени задержки воспламенения стехиометрической смеси н-пентан – воздух при начальном давлении 3 атм. Квадраты и треугольники представляют время задержки зажигания при отсутствии и наличии каталитической поверхности соответственно; а – платиновая каталитическая поверхность; б – палладиевая каталитическая поверхность, внутренняя поверхность реактора удаляется перед экспериментами. На вставке: фронт горения 40% смеси H2 + 60% воздух при температуре стенок реактора 316 °C; проволока из Pt помещена в реактор из нержавеющей стали [21, 22].
На рис. 3а, б показаны осциллограммы давления при зажигании в тех же условиях в отсутствие и в присутствии каталитической платиновой проволоки, которая служит источником воспламенения. Поскольку поведение времени задержки зажигания в этом случае такое, как если бы не было разницы между холодным пламенем и горячим зажиганием в температурной области, соответствующей ОТК [20], можно сделать вывод, что каталитическая поверхность Pt устраняет определенный этап механизма зажигания, например реакцию ингибирования после возникновения холодного пламени.
Рис. 3.
Осциллограммы изменения давления при воспламенении стехиометрических смесей н-пентан – воздух в области ОТК: а – в отсутствие каталитической поверхности, б – в присутствии платиновой проволоки, в – в отсутствие каталитической поверхности (внутренний поверхностный слой предварительно удаляют), г – в присутствии палладиевой проволоки.

Как видно из рис. 3а, воспламенение в отсутствие каталитической поверхности Pt в области ОТК сопровождается термоакустическими колебаниями; их максимальная амплитуда достигается примерно в середине области ОТК по температуре. Частота колебаний составляет около 500 Гц; это значение примерно соответствует первой моде колебаний полой емкости с размерами, близкими к параметрам реактора, используемого в данной работе [22, 23]. Однако колебания уже не наблюдаются в присутствии каталитической поверхности платины (рис. 3б).
В соответствии с принципом Рэлея [24] термоакустическая нестабильность возникает, когда тепловыделение согласовано по фазе с давлением. Это означает, что в присутствии Pt выделение тепла и изменение давления во время горения происходят в противофазе, что согласуется с приведенным выше утверждением о том, что каталитическая поверхность Pt исключает определенную стадию горения (стадию ингибирования) после возникновения холодного пламени. Эта стадия может представлять собой, например, разложение некоторого медленного реагирующего промежуточного пероксида на поверхности Pt с образованием более реакционноспособного поверхностного радикала, например О и/или ОН, который затем может быть десорбирован. Такой механизм был предложен в работе [25] для разложения перекиси водорода на поверхности платины. Это приводит к изменению скорости тепловыделения во время зажигания. Детальный механизм этой стадии окисления углеводородов, очевидно, требует дальнейшего рассмотрения, поскольку экспериментальные данные о реакциях газообразных алкилпероксидов на поверхности платины к настоящему времени весьма скудны.
Тонкая платиновая проволока занимает небольшой объем и, казалось бы, не может влиять на процесс горения в газе. Однако известно [26], что при температуре выше 500 °С молекулы или кластеры как оксида платины, так и самого металла находятся в газовой фазе. Ранее [7, 22] мы показали, что эти частицы попадают в объем реактора путем диффузии/конвекции (см. вставку на рис. 2) и действуют как каталитические центры, на которых происходит воспламенение в ходе распространения фронта пламени. Это центры, реакции которых сильно влияют на механизм горения.
В следующей серии экспериментов платиновую проволоку извлекали из реактора и снова измеряли зависимость логарифма времени задержки зажигания от обратной температуры стехиометрической смеси н-пентан – воздух в области ОТК. Оказалось, что ОТК отсутствовал. Очевидно, это обусловлено каталитическим действием содержащих платину частиц, осажденных на стенках реактора [26] после предыдущих воспламенений.
Для восстановления исходного материала поверхности (нержавеющая сталь) внутренний поверхностный слой реактора толщиной 0.5 мм удаляли механически. На рис. 2б сравниваются экспериментальные данные по времени задержки зажигания стехиометрической смеси н-пентан – воздух в реакторе в отсутствие (прямоугольники) и присутствии (треугольники) каталитической поверхности Pd. Как видно на рис. 2б, как в области положительного температурного коэффициента, так и в области отрицательного температурного коэффициента поверхность палладиевого катализатора почти не влияет на время задержки зажигания. Полученный результат согласуется с данными работ [27, 28]. В этих работах было показано, что в присутствии фольги из Pd ячеистая структура фронта пламени смесей H2–CH4–воздух не наблюдается по сравнению с результатами, полученными на поверхности Pt (см. вставку на рис. 2). Это связано с бóльшей стабильностью PdO по сравнению с нестабильным диоксидом PtO2, который разлагается при температуре свыше 500 °C (см. выше). На рис. 3в, г показаны осциллограммы давления при зажигании в тех же условиях в отсутствие (в) и в присутствии (г) каталитической поверхности Pd. Внутренняя поверхность реактора была подвергнута механической обработке, однако, как видно на рис. 3в, воспламенение как в отсутствие, так и в присутствии каталитической поверхности Pd в области ОТК сопровождается термоакустическими колебаниями, максимальная амплитуда которых достигается в середине области ОТК. Таким образом, в присутствии каталитической поверхности, которая при температуре пламени заметно не реагирует с кислородом и не генерирует распространяющиеся в объем каталитические центры, явление ОТК имеет место.
Мы предприняли попытку качественно проиллюстрировать влияние химического механизма и тепловыделения на простом примере последовательности двух цепных химических реакций на основе численного моделирования с использованием системы уравнений Навье–Стокса в сжимаемой реагирующей среде в приближении малого числа Маха. Приближение малого числа Маха получают из уравнений Навье–Стокса [29–31] для сжимаемой среды при разложении каждой переменной в ряд по степеням γM 2, где γ – показатель адиабаты, М – число Маха. Для каждой переменной оставляют член самого низкого порядка, за исключением давления P, которое разделено на два компонента: термодинамическое давление P0(t), однородное в пространстве, и гидродинамическое давление p2(x, y, t): P = P0(t) + γM2p2(x, y, t) + O(M3), где P0 вычисляется, как в [32]. Плотность ρ, температуру T, давление P и концентрацию С обезразмеривали по их начальным значениям: ρ0, T0, P0 = ρ0RT0, С0. Эта система представлена ниже и описывает распространение пламени в двумерной области.
Процесс горения был представлен элементарным цепным механизмом: реакцией C → 2n, характеризуемой скоростью w0, и реакцией n + C → 2n + + n1 + Продукты (характеризуемой параметрами β0, Q = β1) [31], а также реакцией n1 + C → n + + Продукты, характеризуемой параметрами β, Q = β2); Q – количество тепла, выделенного в соответствующей реакции. Уточним, что в процессе стационарного распространения пламени скоростью реакции зарождения цепи, w0, можно пренебречь [33]. В этом случае безразмерные уравнения Навье–Стокса для сжимаемой реагирующей среды в приближении малого числа Маха принимают вид
(3)
$\begin{gathered} \rho \left( {{{u}_{t}} + {v}{{{v}}_{y}} + u{{{v}}_{x}}} \right) + {{{{P}_{y}}} \mathord{\left/ {\vphantom {{{{P}_{y}}} {\gamma {{M}^{2}}}}} \right. \kern-0em} {\gamma {{M}^{2}}}} = \\ = {1 \mathord{\left/ {\vphantom {1 {{\text{Fr}}}}} \right. \kern-0em} {{\text{Fr}}}} + {\text{Sc}}\left( {{{\nabla }^{2}}{v} + \left( {{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}} \right){{K}_{y}}} \right), \\ \end{gathered} $(4)
$\begin{gathered} \rho \left( {{{{v}}_{t}} + {v}{{u}_{y}} + u{{u}_{x}}} \right) + {{{{P}_{x}}} \mathord{\left/ {\vphantom {{{{P}_{x}}} {\gamma {{M}^{2}}}}} \right. \kern-0em} {\gamma {{M}^{2}}}} = \\ = {1 \mathord{\left/ {\vphantom {1 {{\text{Fr}}}}} \right. \kern-0em} {{\text{Fr}}}} + {\text{Sc}}\left( {{{\nabla }^{2}}u + \left( {{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}} \right){{K}_{x}}} \right), \\ \end{gathered} $(5)
$\begin{gathered} \rho \left( {{{T}_{t}} + {v}{{T}_{y}} + u{{T}_{x}}} \right) - {{(\gamma - 1)} \mathord{\left/ {\vphantom {{(\gamma - 1)} {\gamma {{P}_{t}}}}} \right. \kern-0em} {\gamma {{P}_{t}}}} - \\ - \,\,(\gamma - 1){{M}^{2}}\left( {{{P}_{t}} + u{{P}_{x}} + {v}{{P}_{y}}} \right) = {{\nabla }^{2}}T + {{\beta }_{1}}W + {{\beta }_{2}}{{W}_{1}}, \\ \end{gathered} $(6)
$\rho \left( {{{C}_{t}} + {v}{{C}_{y}} + u{{C}_{x}}} \right) = {{\nabla }^{2}}C + {{w}_{0}} - {{\beta }_{0}}nW - \beta {{n}_{1}}{{W}_{1}},$(7)
$\rho \left( {{{n}_{t}} + {v}{{n}_{y}} + u{{n}_{x}}} \right) = {{\nabla }^{2}}n + {{w}_{0}} + 2{{\beta }_{0}}nW + \beta {{n}_{1}}{{W}_{1}},$(8)
$\rho \left( {{{n}_{{1t}}} + {v}{{n}_{{1y}}} + u{{n}_{{1x}}}} \right) = {{\nabla }^{2}}n + {{\beta }_{0}}nW - \beta {{n}_{1}}{{W}_{1}},$(9)
$W = C\exp \left( {\zeta - {\zeta \mathord{\left/ {\vphantom {\zeta T}} \right. \kern-0em} T}} \right),$(10)
${{W}_{1}} = C\exp \left( {{{\zeta }_{1}}--{{{{\zeta }_{1}}} \mathord{\left/ {\vphantom {{{{\zeta }_{1}}} T}} \right. \kern-0em} T}} \right),$(11)
${{P}_{{tt}}} - \left( {{1 \mathord{\left/ {\vphantom {1 {{{M}^{2}}}}} \right. \kern-0em} {{{M}^{2}}}}} \right){{\nabla }^{2}}P = q\left( {{{C}_{P}} - 1} \right)\left[ {{{\beta }_{1}}{{W}_{t}} + {{\beta }_{2}}{{{({{W}_{1}})}}_{t}}} \right],$Рис. 4.
Результаты численного анализа множества системы уравнений Навье–Стокса в приближении малого числа Маха (подробное объяснение приведено в тексте).
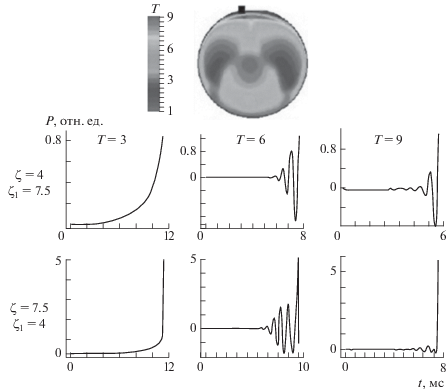
Значения параметров были приняты следующими: ζ = 4, ζ1 = 7.5 β0 = 0.1, β = 0.15, β1 = 0.22, β2 = 0.3. Коэффициенты диффузии Dn = ${{D}_{{{{n}_{1}}}}}$ = 0.3, Tt = T – T0.
Решение задачи осуществляли методом конечных элементов с использованием пакета FlexPDE 6.08, 1996-2008 PDE Solutions Inc. [37]. Результаты расчета термоакустических колебаний в системе (2)–(11) показаны на рис. 4. Вверху показан расчет температурного поля, внизу – кривые изменения давления, рассчитанные в точке реактора, обозначенной квадратом. Эти кривые соответствуют степеням превращения, указанным в верхней части рисунка. Каждая колонка соответствует начальной безразмерной температуре стенки, указанной в нижней части рисунка. Видно, что при температуре стенки Т = 6 колебания во время горения наиболее интенсивны, а при Т = 3 и Т = 9 колебания менее интенсивны; это качественно иллюстрирует экспериментальные результаты.
Из рис. 4 также видно, что взаимная замена энергий активации двух реакций приводит к изменениям в режимах термоакустических колебаний. Это происходит, скорее всего, потому, что тепловыделение и возмущение давления при ζ = 4, ζ1 = 7.5 во время горения происходят в противофазе, а при ζ = 7.5, ζ1 = 4 – приблизительно в фазе за счет изменения временны́х зависимостей тепловыделения при горении.
Следует отметить, что анализ единственной химической реакции при исключении второй (β = 0), что эквивалентно ее полному ингибированию, не приводит к эффекту, когда при повышении начальной температуры интенсивность термоакустических колебаний сначала увеличивается, а затем уменьшается. Таким образом, очевидно, что приемлемая кинетическая модель должна учитывать возникновение термоакустических колебаний; исключение определенной стадии кинетического механизма (вероятно, поверхностного характера) должно вызвать исчезновение режима ОТК. Очевидно, что установление детального механизма горения для опытов, проведенных в настоящей работе, требует большого количества вычислений с использованием бóльшей вычислительной мощности для анализа всех возможных вариантов механизма реакции.
ЗАКЛЮЧЕНИЕ
Особенности воспламенения предварительно перемешанных стехиометрических смесей н-пентан – воздух изучены в статическом реакторе быстрого напуска смеси в присутствии металлических Pt и Pd в области отрицательного температурного коэффициента (ОТК). Показано, что в отсутствие благородных металлов в области ОТК происходят термоакустические колебания. Однако в присутствии платинового катализатора, который реагирует с кислородом при температуре пламени и генерирует каталитические центры, распространяющиеся в объем, термоакустические режимы теплового воспламенения исчезают. Другими словами, каталитическая поверхность Pt устраняет определенную стадию ингибирования кинетического механизма после возникновения холодного пламени, и явление ОТК исчезает. Последняя может представлять собой, например, разложение некоторого промежуточного медленно реагирующего пероксида на поверхности Pt с образованием более реакционноспособного радикала. В присутствии каталитической поверхности (Pd), которая не реагирует при температуре пламени и не генерирует каталитические центры, распространяющиеся в объем, явление ОТК возникает.
Таким образом, обнаруженные закономерности должны учитываться при численном моделировании явления ОТК. Другими словами, исключение определенной стадии кинетического механизма (вероятно, поверхностного характера) должно вызвать исчезновение колебаний и режима ОТК в присутствии платинового катализатора, т.е. в условиях наших экспериментов. Стадия должна включать поверхностную реакцию активного промежуточного продукта горения на поверхности Pt, в которой более активные промежуточные продукты образуются из малоактивного промежуточного продукта.
В части изучения горения над поверхностью металлических платины и палладия при использовании скоростной цветной киносъемки работа выполнена в рамках госзадания (регистрационный номер АААА-А17-117011910011-09); в части изучения горения смесей водород–метан–воздух – в рамках госзаданий (регистрационные номера АААА-А17-117040610346-5 и АААА-А19-119010990034-5).
Список литературы
Мержанов А.Г., Хайкин Б.И. Теория волн горения в гомогенных средах, Черноголовка: ИСМАН, 1992.
Warnatz J., Maas U., Dibble C.R. Combustion. Physical and chemical aspects, modeling, experiments, formation of pollutants. Berlin: Springer, 2001.
Крылов О.В. Гетерогенный катализ. М.: ИКЦ Академкнига, 2004.
Rubtsov N.M., Tsvetkov G.I., Chernysh V.I., Troshin K.Ya. // Combust. and Flame. 2020. V. 218. P. 179.
Deutschmann O., Schmidt R., Behrendt F., Warnatz J. // Proc. Combust. Inst. 1996. V. 26. P. 1747.
Trevino C., Linan A., Kurdyumov V. // Ibid. 2000. V. 28. P. 1359.
Рубцов Н.М., Виноградов А.Н., Калинин А.П. и др. // Физико-химическая кинетика в газовой динамике. 2016. Т. 17. С. 1.
Griffiths J.F., MacNamara J.P., Sheppard C.G.W. et al. // Fuel. 2002. V. 81. P. 2219.
Qi Y., Wang Z., Wang J., He X. //Combust. and Flame. 2015. V. 162. P. 4119.
Farrell J.T., Cernansky N.P., Dryer F.L. et al. // SAE Technical Paper. 2007. 2007-01-020.
Kuwahara K., Tada T., Furutani M., Sakai Y., Ando H. // SAE Intern. J. Engines. 2013. V. 6. P. 520.
Shibata G., Oyama K., Urushihara T., Nakano T. SAE Technical paper. 2004. 2004-01-0553.
Healy D., Kopp M.M., Polley N.L. et al. // Energy Fuels. 2010. V. 24. P. 1617.
Sabia P., de Joannon M., Picarrelli A. et al. // Combust. and Flame. 2013. V. 160. P. 47.
Ju Y., Sun W., Burke M.P., Gou X., Chen Z. // Proc. Combust. Inst. 2011. V. 33. P. 1245.
Pan J., Wei H., Shu G., Chen Z., Zhao P. // Combust. and Flame. 2016. V. 174. P. 179.
Saytzev S.G., Soloukhin R.I. // Proc. 8th symposium (Intern.) on Combust. Pittsburgh: Combust. Inst., 1962. P. 2771.
Livengood J.C., Leary W.A. // Ind. Eng. Res. 1951. V. 43. P. 2797.
Борисов А.А., Рубцов Н.М., Скачков Г.И., Трошин К.Я. // Хим. физика. 2012. Т. 31. № 8. С. 30.
Борисов А.А., Кнорре В.Г., Кудряшова Е.Л., Скачков Г.И., Трошин К.Я. // Хим. физика. 1998. Т. 17. № 7. С. 80.
Зельдович Я.Б., Баренблатт Г.И., Либрович В.Б., Махвиладзе Г.М. Математическая теория горения и взрыва. М.: Наука, 1980.
Рубцов Н.М., Калинин А.П., Цветков Г.И. др. // Хим. физика. 2018. Т. 37. С. 42.
Goates C.B. Analytical Expressions for Acoustic Radiation Modes of Simple Curved Structures, Theses and Dissertations. Department of Physics and Astronomy Brigham Young University, 2019. P. 7494; https://scholarsarchive.byu.edu/etd/7494
Strutt J.W. The Theory of Sound. 2nd ed. V. 2. London–N.Y.: Macmillan and Co., 1894.
Serra-Maia R., Bellier M., Chastka S. et al. // ACS Appl. Mater. Interfaces. 2018. V. 10. P. 21224.
Chaston J.C. // Platinum Metals Rev. 1964. V. 8. P. 50.
Рубцов Н.М., Виноградов А.Н., Калинин А.П. и др. // Хим. физика. 2019. № 4. Т. 38. С. 53.
Калинин А.П., Рубцов Н.М., Виноградов А.Н. и др. // Хим. физика. 2020. Т. 39. С. 23.
Buckmaster J.D., Ludford G.S.S. Theory of Laminar Flames. Cambridge, London: Cambrige University Press, 1982.
Teleaga I., Seaid M. // Appl. Mathem. Modell. 2008. V. 32. P. 971.
Rubtsov N.M. The Modes of Gaseous Combustion. Switzeland: Springer Intern. Publ., 2016.
Nicoud F. // J. Comput. Phys. 2000. V. 158. P. 71.
Посвянский В.С. Дис. … канд. физ.-мат. наук. М.: ИХФ АН СССР, 1975.
Таблицы физических величин / Под ред. Кикоина И.К. М.: Атомиздат, 1976.
Абугов Д.И., Бобылев В.М. Теория и расчет твердотопливных ракетных двигателей. М.: Машиностроение, 1987.
Lighthill M.J. // Proc. Roy. Soc. Lond. A. 1954. V. 222. P. 1.
Backstrom G. Simple Fields of Physics by Finite Element Analysis. N.Y.: GB Publishing, 2005.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика


