Химическая физика, 2022, T. 41, № 4, стр. 63-71
Особенности использования полиэлектролитов в качестве пролонгаторов действия лекарственных веществ
А. С. Шуршина 1, А. Р. Галина 1, Е. И. Кулиш 1, *
1 Башкирский государственный университет
Уфа, Россия
* E-mail: onlyalena@mail.ru
Поступила в редакцию 25.02.2021
После доработки 01.03.2021
Принята к публикации 22.03.2021
- EDN: EJSTEJ
- DOI: 10.31857/S0207401X22040082
Аннотация
Работа посвящена изучению особенностей высвобождения лекарственных веществ (как электролитной, так и неэлектролитной природы) из растворов полиэлектролитов через полупроницаемую мембрану. В качестве полимеров использовали поликатион хитозан и полианион натриевую соль сукцинила хитозана, в качестве лекарственных веществ (ЛВ) – натриевую соль цефазолина, лидокаина гидрохлорид и диоксидин. В ходе работы установлен факт взаимодействия между полиэлектролитами и ЛВ, а также влияния конформационного и надмолекулярного состояния полимеров в растворе на значения коэффициентов диффузии высвобождения лекарственных препаратов из растворов полимеров через полупроницаемую мембрану. Показано, что взаимодействие между ЛВ и полиэлектролитами имеет ряд характерных особенностей, обусловленных ионогенной природой используемых полимеров и проявлением конформационно-надмолекулярного эффекта. Эти особенности приводят к тому, что существенное различие в количестве лекарственного вещества, прочно удерживаемого полимерной цепью, и значениями коэффициентов диффузии его высвобождения проявляются только в области разбавленных растворов. При переходе в область полуразбавленных растворов вследствие имеющих место изменений в структуре полимеров в растворе эти различия нивелируются, что сопровождается сближением значений коэффициентов диффузии высвобождения ЛВ различной природы из растворов полимеров через полупроницаемую мембрану.
ВВЕДЕНИЕ
Создание лекарственных форм пролонгированного действия на сегодняшний день невозможно представить себе без использования полимеров [1–10]. Даже просто смешивая полимеры с лекарственными веществами (ЛВ), можно за счет существенно большей вязкости макромолекул, чем у низкомолекулярных ЛВ, добиться определенного уровня пролонгирования. Пролонгирующее действие высокомолекулярных соединений можно усилить, если использовать полимеры, имеющие функциональные группы. В этом случае могут образовываться более прочные соединения типа комплексов или солей [11–15]. Перевод лекарственных соединений в полимерное состояние фактически позволяет не только задержать лекарство в крови, лимфе или межклеточной жидкости на более длительное время за счет затруднения диффузионных процессов, невозможности прохождения биологических барьеров напрямую и других факторов, но и уменьшить уровень токсичности лекарственного вещества [16–19].
Достаточно часто в качестве пролонгаторов используют полимеры с собственной физиологической активностью [20–23]. В этом случае биологическое действие (бактериостатическое, противовирусное, антикоагуляционное и другие) проявляется макромолекулой даже в том случае, если в ее структуру не введено никаких низкомолекулярных фармакологических веществ. Фактически тогда макромолекула не только выполняет функцию носителя ЛВ, но и дополнительную – биологически активного соединения.
В подавляющем большинстве случаев физиологически активные макромолекулы представляют собой полиэлектролиты, т.е. полимеры, несущие на своей цепи заряд. В частности, бактерицидная и бактериостатическая активность отмечена у катионных полиэлектролитов [20, 24]. Эти полимеры могут взаимодействовать с клеточными мембранами, вызывая распад и агглютинацию клеток или стимулируя поглощение микроорганизмов макрофагами. Полианионы весьма эффективны в борьбе с вирусными заболеваниями [20, 25]. В этом случае действие полимеров заключается как в стимулировании выработки в организме особого защитного вещества белковой природы – интерферона, так и в непосредственной инактивации вирусов.
Сложность использования полиэлектролитов в качестве основы создания полимерных лекарственных форм обусловлена тем, что из-за наличия кулоновских взаимодействий поведение водных растворов линейных полиэлектролитов существенно отличается от поведения неионогенных полимеров. Например, конформационное состояние полиэлектролитов в значительной мере определяется такими факторами, как степень связывания макроионами противоионов, химическая природа и концентрация низкомолекулярных солей. Поскольку ЛВ достаточно часто представляют собой низкомолекулярные электролиты, возникает необходимость исследовать возможное влияние полиэлектролитной природы некоторых полимеров, используемых в качестве носителей лекарственных средств, на взаимодействие полиэлектролит – лекарственное вещество. Таким образом, цель работы – изучение особенностей пролонгированного действия некоторых полиэлектролитов в отношении выхода лекарственных веществ как электролитной, так и неэлектролитной природы. В качестве полимеров использовали поликатион хитозан (ХТЗ) и полианион натриевую соль сукцинила хитозана (СХТЗ), в качестве лекарственных веществ – натриевую соль цефазолина, лидокаина гидрохлорид и диоксидин.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве объектов исследования использовали ХТЗ (ТУ 9289-067-00472124-03) со степенью деацетилирования 82%, М.м. = 113 кДа и характеристической вязкостью 7.8 дл/г производства ЗАО “Биопрогресс” (г. Щелково, Россия), а также натриевую соль СХТЗ с М.м. = 67 000 а.е.м. (ТУ 9284-027-11734126-08) производства ЗАO “Биoпрoгресс” (г. Щёлково, Россия). Степень замещения СХТЗ по аминогруппам составляет 75%. Степень деацетилирования исходного образца ХТЗ, из которого был получен СХТЗ, составляла 82%. В качестве растворителей в случае ХТЗ использовали 1%-ный водный раствор уксусной кислоты, а в случае СХТЗ – дистиллированную воду. Для полного растворения полимеров проводили перемешивание в течение 24 ч.
Для изучения взаимодействия указанных полимеров с ЛВ были исследованы УФ-спектры индивидуальных соединений, а также их смесей на спектрофотометре “UV-2600” с интегрирующей сферой ISR-2600Plus производства компании Shimadzu (Japan) в области длин волн 190–400 нм. Концентрация растворов полимеров, используемых в ходе исследования, составляла 10–5–10–1 моль/л, ЛВ – 10–4–10–3 моль/л. В качестве ЛВ использовали натриевую соль цефазолина (ЦФЗ) производства ОАО “Биосинтез” (г. Пенза, Россия), лидокаина гидрохлорид (ЛД) – ПАО “Биохимик” (г. Саранск, Россия), диоксидин (ДО) – ОАО “Новосибхимфарм” (г. Новосибирск, Россия). Лекарственные вещества использовали без дополнительной очистки. Состав и константу устойчивости образующихся комплексов определяли методом молярных отношений [26].
Для определения характеристической вязкости был применен подход Баранова [27], согласно которому значение $\frac{{\partial \ln ({{\eta }_{r}})}}{{\partial c}}$ в каждой точке на кривой зависимости lnηr от С может рассматриваться как “текущее” значение характеристической вязкости [η]*:
где ηr – значение относительной вязкости раствора полимера, С – концентрация полимера в растворе. Очевидно, что при С → 0 величина [η]* соответствует начальному наклону зависимости ln ηr от с и совпадает с величиной характеристической вязкости [η], описывающей поведение изолированной макромолекулы [28].Для определения протекания агрегационных процессов использовали следующие рассуждения. При описании вязкостных свойств разбавленных растворов, как правило, исходят из линейной зависимости приращения вязкости от концентрации полимерного раствора. Однако в случае полярных полимеров, к которым относится СХТЗ, существует вероятность протекания обратимых агрегационных процессов, которые могут иметь место не только в области полуразбавленных, но даже и в области разбавленных растворов. В этом случае вклад в вязкость вносят не отдельные частицы с объемом V0, а их агрегаты, объем которых V(n) зависит не только от числа n составляющих его частиц, но и от плотности их упаковки, характеризуемой фрактальной размерностью D:
(2)
$V\left( n \right) = {{V}_{0}}{{n}^{{{3 \mathord{\left/ {\vphantom {3 D}} \right. \kern-0em} D}}}}.$Следовательно, любое отклонение показателя δ от единицы свидетельствует о том, что данная система является структурированной.
Реологические исследования растворов полимеров, а также их смесей с ЛВ проводили на модульном динамическом реометре Haake Mars III при температуре (25 ± 1) °С в осцилляционном режиме в диапазоне частот от 0.01 до 10 Гц. Для проведения диализа ЛВ через полупроницаемую мембрану, представляющую собой мешок из целлофановой пленки, предварительно смешанный раствор полимера с ЛВ помещали внутрь целлофанового мешка, который, в свою очередь, опускали в сосуд, содержащий воду. Диализ проводили в термостатируемых условиях при температуре (25 ± 1) °С. Пробы объемом по 10 мл отбирали через определенные промежутки времени с момента начала эксперимента и определяли количество ЛВ (Gs) методом спектрофотометрии в УФ-области при длине волны, соответствующей максимуму поглощения ЛВ по калибровочной кривой. В качестве раствора сравнения использовали раствор соответствующего полимера. Момент установления в растворе постоянной концентрации ЛВ (G∞) считали моментом установления равновесия. Коэффициенты диффузии определяли, основываясь на подходе Кранка [29]. При условии Gs/G∞ ≤ 0.5 получаем
(4)
${{{{G}_{s}}} \mathord{\left/ {\vphantom {{{{G}_{s}}} {{{G}_{\infty }} = {{{\left( {{{16{{D}_{s}}t} \mathord{\left/ {\vphantom {{16{{D}_{s}}t} {\pi {{L}^{2}}}}} \right. \kern-0em} {\pi {{L}^{2}}}}} \right)}}^{{0.5}}},}}} \right. \kern-0em} {{{G}_{\infty }} = {{{\left( {{{16{{D}_{s}}t} \mathord{\left/ {\vphantom {{16{{D}_{s}}t} {\pi {{L}^{2}}}}} \right. \kern-0em} {\pi {{L}^{2}}}}} \right)}}^{{0.5}}},}}$ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Исследование разбавленных растворов изучаемых полимеров методом УФ-спектроскопии подтверждает, что взаимодействие ЛВ с полисахаридами имеет место. Максимумы поглощения в УФ-спектрах ЦФЗ наблюдаются при 273 нм, ЛД – при 262 нм. Спектр поглощения ДО в водном растворе имеет три максимума поглощения: при 235, 266 и 382 нм. При добавлении в раствор эквивалентного количества обоих изучаемых полисахаридов, которые при концентрации 10–5–10–1 моль/л в УФ-области не поглощают, интенсивность пика поглощения ЛВ заметно возрастает, а максимум поглощения батохромно сдвигается примерно на 3–5 нм.
Наблюдаемые изменения свидетельствуют о воздействии полимеров на электронную систему ЛВ и образовании аддуктов взаимодействия. По различию в значениях длин волн Δλ, соответствующих максимуму поглощения комплекса и индивидуального ЛВ, можно оценить энергию связи в комплексном соединении по формуле Планка:
где ΔE – энергия связи, h – постоянная Планка, c – скорость света.Значения энергии связи в комплексах ХТЗ и СХТЗ с изучаемыми ЛВ, оцененные по сдвигу максимумов поглощения в УФ-спектрах, составляют порядка 10–15 кДж/моль. Небольшие значения величин энергий связи позволяют предположить, что комплексообразование осуществляется посредством водородных связей.
Для определения константы устойчивости был применен метод молярных отношений. Совокупные данные представлены в табл. 1. Как видно из представленных в этой таблице данных, аддукты взаимодействия полимер–ЛВ в предельно разбавленных растворах могут быть отнесены к соединениям со средней устойчивостью, в принципе способным обеспечить определенный уровень пролонгирования действия лекарственных препаратов за счет закрепления их на полимерной цепи. Однако полиэлектролитная природа ХТЗ и СХТЗ может внести свои особенности в протекание реакции взаимодействия между полимером и ЛВ, особенно в том случае, когда разбавленные растворы заменяются на полуразбавленные и концентрированные.
Известно, что полимеры в растворе могут существовать в различных концентрационных режимах [30–32]. В режиме разбавленных растворов при концентрации С, меньшей, чем концентрация кроссовера (cross-over – переход) С * = 1/[η], где [η] – характеристическая вязкость, макромолекулы изолированы друг от друга. Они не взаимодействуют между собой, а вязкость раствора полимера увеличивается с ростом концентрации по линейному закону: η ∼ С δ, где δ = 1.00.
Повышение концентрации полимеров в растворе сопровождается закономерным уменьшением размера макромолекулярного клубка, т.е. значений “текущей” характеристической вязкости (рис. 1), и агрегацией макромолекулярных клубков между собой (рис. 2). Таким образом, при концентрации С, большей, чем С*, вязкость начинает зависеть от концентрации по степенному закону: η ∼ С δ, где δ > 1.00. Повышение концентрации приводит не только к росту степени агрегированности макромолекул, но и к формированию сетки зацеплений, характеризуемой концентрацией Се, определить которую легко по началу резкого прироста вязкости. Резкое увеличение интенсивности роста вязкости обусловлено тем, что при переходе от разбавленного раствора к полуразбавленному изменяется механизм массопереноса (с трансляционного на рептационный), что связано именно с формированием флуктуационной сетки зацеплений. Однако реологическое поведение полиэлектролитов имеет свои особенности [33].
Рис. 1.
Зависимость значения “текущей” характеристической вязкости от концентрации СХТЗ (а) и ХТЗ (б) в отсутствие (1) и в присутствии (2–4) лекарственного вещества ЛД (2), ЦФЗ (3) и ДО (4), взятых в концентрации 0.1 моль/моль полимера
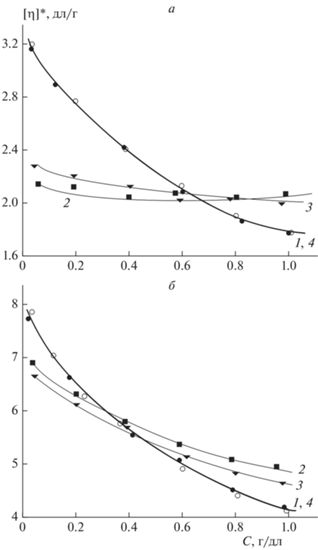
Рис. 2.
Зависимость показателя степени агрегированности от концентрации СХТЗ (а) и ХТЗ (б) в растворе в отсутствие (1) и в присутствии (2–4) лекарственного вещества ЛД (2), ЦФЗ (3) и ДО (4), взятых в концентрации 0.1 моль/моль полимера.
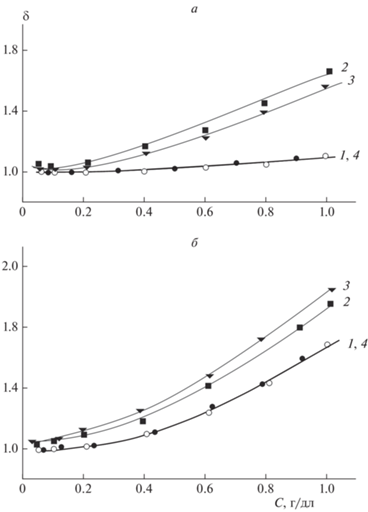
Во-первых, в отличие от растворов неионогенных полимеров, в которых флуктуационная сетка зацеплений формируется практически сразу после достижения точки кроссовера и значение С * совпадает со значением Се, в растворах полиэлектролитов существует область полуразбавленных растворов, в которых клубки уже соприкасаются друг с другом, а сетки зацеплений еще не образуют [28].
Действительно, резкое повышение динамической вязкости растворов ХТЗ и СХТЗ и переход из одного концентрационного режима (разбавленный раствор) в другой (полуразбавленный) происходит не при концентрации кроссовера С * = 1/[η], а несколько позже.
Концентрация формирования сетки зацеплений Се соответствует раствору с концентрацией СХТЗ и ХТЗ, равной 1.0 и 0.8 г/дл соответственно. Учитывая, что определенное методом Баранова начальное значение характеристической вязкости составило [η] = 3.20 дл/г для СХТЗ и [η] = 7.8 дл/г для ХТЗ, точка кроссовера для этих полимеров соответствует концентрации С * = 1/[η] 0.31 и 0.13 г/дл. Достижение точки кроссовера никак не сказывается на механизме течения полимеров. В связи с этим можно говорить о наличии переходной области от разбавленной области к полуразбавленной, в которой макромолекулы уже соприкасаются друг с другом, но сетки зацеплений еще не образуют. Очевидно, в переходной зоне с ростом концентрации происходит постепенное сжатие макромолекулярных клубков из-за их контакта и преодоления сил электростатического отталкивания. Только после этого в системе начинает формироваться сетка зацеплений.
Во-вторых, природа ЛВ сказывается на конформационном и надмолекулярном состояниях полимеров. Так, добавление ЛВ, представляющих собой низкомолекулярные электролиты, в раствор ионогенных ХТЗ и СХТЗ сказывается как на значениях характеристической вязкости (рис. 1), так и на степени агрегированности полимеров (рис. 2). Обращает на себя внимание тот факт, что для растворов полимеров в присутствии ЛД и ЦФЗ значения тангенса угла наклона касательных к кривой зависимости удельной вязкости от концентрации полимера в растворе в логарифмических координатах даже в области больших разбавлений становятся больше единицы. Также можно отметить, что и при переходе за область значений С * показатель δ больше, чем для растворов индивидуального полимера или раствора полимера в присутствии ДО.
При этом именно природа ЛВ (электролит или неэлектролит) играет принципиальное значение. В случае неэлектролитной природы ЛВ (диоксидина) изменения значений характеристической вязкости и степени агрегированности по сравнению с индивидуальными полимерами не наблюдается.
В-третьих, природа ЛВ сказывается и на значениях динамической вязкости. Добавление ЛД и ЦФЗ (в отличие от ДО) и к ХТЗ, и к СХТЗ сопровождается уменьшением разницы в значениях С * и Се, причиной чего является, безусловно, взаимодействие между полимером и ЛВ-электролитом.
Таким образом, в случае использования ионогенных полимеров и лекарственных препаратов, представляющих собой низкомолекулярные электролиты, их добавление к растворам полимеров в широком концентрационном диапазоне сопровождается изменениями в конформационном и надмолекулярном состояниях полимеров, что не может не сказаться на взаимодействии полимеров с ЛВ, а следовательно, и на способности полимеров к пролонгированию выхода ЛВ.
Поскольку аддукты взаимодействия изучаемых полимеров с ЛВ в предельно разбавленном растворе могут быть охарактеризованы как соединения со средней устойчивостью, они принципиально способны обеспечить определенный уровень пролонгирования действия ЛВ за счет закрепления их на цепи полимера. Выход ЛВ (в данном случае – ДО) из разбавленного раствора СХТЗ происходит достаточно медленно.
Однако ситуация изменяется при переходе от предельно разбавленных растворов к более концентрированным. Условно кинетические кривые выхода ДО (путем диализа через полупроницаемую мембрану) из растворов СХТЗ можно разделить на два участка. Первый участок соответствует выходу ДО, не закрепленному на полимерной цепи, посредством диффузии. Второй участок соответствует высвобождению ДО, удерживаемого за счет комплексообразования макромолекулой. Кинетические кривые выходят при этом на плато, соответствующее равновесному выходу ЛВ. По разнице между значениями оптической плотности, соответствующей равновесному выходу ЛВ и количеству ДО, введенного в раствор, можно определить значение равновесно закрепленного на макромолекулярной цепи количества ЛВ, βравн. Обращает на себя внимание тот факт, что в общем случае, чем выше концентрация СХТЗ в растворе, тем меньше значение βравн.
Влияние концентрации СХТЗ в растворе на количество ДО, прочно закрепленного на макромолекуле, показано на кривой 1 на рис. 3а. Видно, что в случае использования в качестве лекарственного препарата ДО значение βравн остается практически постоянным во всем диапазоне концентраций полимера вплоть до концентрации формирования сетки зацеплений Се, после чего количество ЛВ, прочно закрепленное на полимерной цепи, начинает резко уменьшаться вследствие происходящих при этом изменений конформационно-надмолекулярного состояния полимера. Аналогичные закономерности имеют место и для растворов ХТЗ (рис. 3б, кривая 1).
Рис. 3.
Зависимость количества ДО (1), ЛД (2) и ЦФЗ (3), прочно закрепленного на полимерной цепи, от концентрации СХТЗ (а) и ХТЗ (б) в растворе.
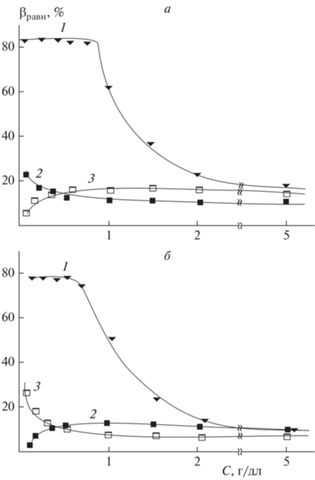
Зависимость коэффициентов диффузии высвобождения ДО из растворов СХТЗ и ХТЗ от концентраций последних представлена в табл. 2. Как показал анализ данных, приведенных в этой таблице, коэффициент диффузии высвобождения ДО увеличивается с ростом концентрации полимеров в растворе, поскольку сопровождается уменьшением количества ДО, прочно закрепленного на макромолекуле.
Таблица 2.
Значения коэффициентов диффузии высвобождения лекарственных веществ в присутствии СХТЗ и ХТЗ
| Полимер | ЛВ | Концентрация полимера в растворе, г/дл | D · 1010, см2/с |
|---|---|---|---|
| СХТЗ | ДО | 1.0 · 10–5 | 0.80 |
| 1.0 · 10–3 | 0.82 | ||
| 0.1 | 0.84 | ||
| 1.0 | 1.12 | ||
| 2.0 | 1.65 | ||
| 3.0 | 1.87 | ||
| 5.0 | 2.14 | ||
| ЦФЗ | 1.0 · 10–5 | 3.74 | |
| 1.0 · 10–3 | 3.62 | ||
| 0.1 | 3.36 | ||
| 1.0 | 3.07 | ||
| 2.0 | 2.72 | ||
| 3.0 | 2.68 | ||
| 5.0 | 2.52 | ||
| ЛД | 1.0 · 10–5 | 2.18 | |
| 1.0 · 10–3 | 2.26 | ||
| 0.1 | 2.64 | ||
| 1.0 | 2.75 | ||
| 2.0 | 2.82 | ||
| 3.0 | 2.91 | ||
| 5.0 | 2.98 | ||
| ХТЗ | ДО | 1.0 · 10–5 | 0.71 |
| 1.0 · 10–3 | 0.73 | ||
| 0.1 | 0.75 | ||
| 1.0 | 0.89 | ||
| 2.0 | 1.35 | ||
| 3.0 | 1.58 | ||
| 5.0 | 1.85 | ||
| ЦФЗ | 1.0 · 10–5 | 2.12 | |
| 1.0 · 10–3 | 2.27 | ||
| 0.1 | 2.37 | ||
| 1.0 | 2.50 | ||
| 2.0 | 2.67 | ||
| 3.0 | 2.79 | ||
| 5.0 | 2.88 | ||
| ЛД | 1.0 · 10–5 | 3.68 | |
| 1.0 · 10–3 | 3.60 | ||
| 0.1 | 3.55 | ||
| 1.0 | 3.37 | ||
| 2.0 | 3.13 | ||
| 3.0 | 2.84 | ||
| 5.0 | 2.58 |
Анализируя полученные данные, можно констатировать, что повышение вязкости раствора полимера, вызванное увеличением его концентрации, и в случае ХТЗ, и в случае СХТЗ не приводит к замедлению процесса диффузии ЛВ из раствора полимера, как можно было бы ожидать, поскольку сопровождается существенным уменьшением количества ЛВ, прочно закрепленного на полимерной матрице. Поскольку именно аддукт взаимодействия полимер–ЛВ обеспечивает медленное высвобождение ЛВ из раствора полимера, уменьшение его количества приводит к тому, что усиления пролонгирующего действия полимера при увеличении его содержания в растворе не наблюдается.
Так как в случае ионогененных полимеров значения характеристической вязкости, отражающей размер макромолекулярного клубка, зависят от присутствия низкомолекулярных электролитов, например ЦФЗ и ЛД, можно предположить, что для систем СХТЗ–ЦФЗ, СХТЗ–ЛД, ХТЗ–ЦФЗ и ХТЗ–ЛД характер кривых зависимости βравн от концентрации полимера будет не таким, как для изученных ранее систем на основе ионогенных СХТЗ и ХТЗ и не электролита ДО. Действительно, как видно из рис. 3, он различен для ДО, с одной стороны, а также для ЦФЗ и ЛД, с другой (рис. 3).
Можно отметить, что, во-первых, в случае ЦФЗ и ЛД значения βравн изменяются даже в области разбавленных растворов. Напомним, что именно при использовании в качестве ЛВ низкомолекулярных солей электролитов значения характеристической вязкости и степени агрегированности растворов закономерно изменялись как в случае растворов ХТЗ, так и в случае растворов СХТЗ даже в разбавленной области. Во-вторых, уменьшение размеров макромолекулярного клубка и увеличение степени агрегированности, приводящие к уменьшению доступности звеньев полимеров для взаимодействия с ЛВ, приводит к различным эффектам в случае реакции комплексообразования ЛВ с поликатионом и полианионом. И, в-третьих, имеет место различие в характере изменения βравн с изменением концентрации полимера в зависимости от того, что представляет собой ЛВ – анион или катион.
В качестве объяснения наблюдаемых явлений можно предложить следующее. При разбавлении раствора поликатиона ХТЗ повышается вероятность нахождения отрицательно заряженных ионов ЦФЗ около полимерной цепи, а при разбавлении раствора полианиона СХТЗ она, напротив, уменьшается. Соответственно, и вероятность комплексообразования для ЦФЗ и ЦФТ в случае разбавления раствора ХТЗ увеличивается, а в случае разбавления растворов СХТЗ – уменьшается. В случае положительно заряженного иона ЛД разбавление раствора ХТЗ приводит к уменьшению количества комплексно связанного ЛВ, а разбавление раствора СХТЗ – к его увеличению.
Изменения в структурно-физическом состоянии полимеров в растворе находят свое отражение не только в характере взаимодействия этих полимеров с анализируемыми в работе ЛВ, но и в значениях коэффициентов диффузии (табл. 1).
Анализ данных, приведенных в табл. 2, позволяет констатировать следующее:
Во-первых, аналогично изменению βравн, в случае использования в качестве лекарственного вещества ЦФЗ или ЛД коэффициент диффузии изменяется как в области разбавленных, так и в области полуразбавленных растворов. Напротив, в случае использовании в качестве ЛВ диоксидина, который не является электролитом и не оказывает принципиального влияния на конформационно-надмолекулярное состояние ни ХТЗ, ни СХТЗ, значения коэффициентов диффузии высвобождения ДО из раствора полимеров начинают существенно изменяться только в области полуразбавленных растворов.
Во-вторых, в том случае, когда в качестве ЛВ используются низкомолекулярные электролиты ЦФЗ и ЛД, характер их влияния на скорость определяется природой полимера. Когда для исследования взята система полианион СХТЗ – катион ЛД или поликатион ХТЗ – анион ЦФЗ, повышение концентрации полимера в растворе приводит к уменьшению βравн и, как следствие, увеличению значений коэффициентов диффузии. В случае исследования системы полианион СХТЗ – анион ЦФЗ или поликатион ХТЗ – катион ЛД имеет место обратная зависимость – повышение концентрации полимера в растворе приводит к некоторому увеличению βравн и уменьшению значений коэффициентов диффузии.
В-третьих, при переходе в область полуразбавленных растворов различие во влиянии природы ЛВ и полимерной матрицы на значения коэффициентов диффузии высвобождения лекарственного вещества из полимерного раствора через полупроницаемую мембрану практически нивелируется.
Также можно отметить, что значения коэффициентов диффузии для систем СХТЗ–ДО и ХТЗ–ДО меньше, чем у других исследованных ЛВ, что коррелирует со значениями констант устойчивости (см. табл. 1) и βравн. Следовательно, несмотря на то, что в случае использования систем ХТЗ–ЦФЗ, ХТЗ–ДО, СХТЗ–ДО и СХТЗ–ЛД увеличение концентрации полимеров в растворе приводит к уменьшению значения βравн, а для систем СХТЗ–ЦФЗ и ХТЗ–ЛД, напротив, к его увеличению, количество прочно закрепленного на полимерной матрице ЛВ в области полуразбавленных и концентрированных растворов невелико и составляет порядка 10–20% от общего количества введенного ЛВ.
Таким образом, изучение взаимодействия полисахаридов ХТЗ и СХТЗ с лекарственными веществами цефазолином, лидокаином и диоксидином методами УФ-спектроскопии, вискозиметрии и реологии показало, что это взаимодействие, осуществляемое посредством водородных связей, имеет ряд характерных особенностей, обусловленных ионогенной природой используемых полимеров и проявлением конформационно-надмолекулярного эффекта. Эти особенности приводят к тому, что существенное различие в характере взаимодействия полимеров с изучаемыми лекарственными веществами проявляется только в области разбавленных растворов. При переходе в область полуразбавленных растворов эти различия нивелируются вследствие имеющих место конформационно-надмолекулярных изменений в структуре полимеров, что приводит к сближению значений коэффициентов диффузии веществ различной природы из растворов полимеров через полупроницаемую мембрану. Следовательно, в полуразбавленной и концентрированной областях растворов определяющую роль играет не взаимодействие полимер – лекарственное вещество, а собственно надмолекулярная структура полимера в растворе.
ВЫВОДЫ
1. Показано, что смешение водных растворов ХТЗ и СХТЗ с водными растворами лидокаина и диоксидина сопровождается образованием аддуктов реакции, представляющих собой комплексные соединения средней устойчивости, образованные посредством водородных связей.
2. Доказано, что добавление лекарственного вещества диоксидина, представляющего собой вещество неэлектролитной природы, в раствор ХТЗ и СХТЗ в области разбавленного раствора не приводит к изменению конформационно-надмолекулярного состояния полимера, изменению количества лекарственного вещества, прочно удерживаемого полимерной цепью, и, как следствие, коэффициентов диффузии высвобождения лекарственных препаратов из растворов этих полимеров через полупроницаемую мембрану.
3. Добавление в раствор полимеров лекарственных веществ электролитной природы (цефазолина и лидокаина), напротив, сопровождается значительным изменением конформационно-надмолекулярного состояния полимера, количества лекарственного вещества, прочно удерживаемого полимерной цепью, и значений коэффициентов диффузии высвобождения лекарственных препаратов из растворов этих полимеров через полупроницаемую мембрану.
4. Показано, что повышение концентрации полимеров в исходном растворе по-разному сказывается на количестве аддукта реакции. В случае ХТЗ повышение концентрации полимера в исходном растворе приводит к увеличению количества аддукта реакции при использовании в качестве лекарственного вещества лидокаина и понижению его количества при использовании в этом качестве цефазолина и диоксидина, а в случае СХТЗ, напротив, – к увеличению количества аддукта реакции СХТЗ–цефазолин и понижению количества аддукта реакций СХТЗ–лидокаин и СХТЗ–диоксидин.
Список литературы
Koilybayeva M., Ustenova G., Mustafina K. et al. // Proc. Intern. Multidisciplinary Sci. GeoConf. Surveying Geology and Mining Ecology Management. V. 18. Albena, Bulgaris: SGEM, 2018. P. 761.
Filatova E.V., Iakovlev S.G., Bonartsev A.P. et al. // Appl. Biochem. Microbiol. 2012. V. 48. № 6. P. 598.
Bykov V.A., Demina N.B., Velikaya E.V. et al. // Pharm. Chem. J. 2005. V. 39. I. 5. P. 265.
Filatova E.V., Yakovlev S.G., Bonartsev A.P. et al. // Appl. Biochem. Microbiol. 2012. V. 48. № 6. P. 598.
Shiji R., Manu M. Joseph, K. Raveendran Pillai et al. // Intern. J. Biol. Macromol. 2020. V. 165. P. 568.
Shah B.M., Palakurthi S.S., Khare T. et al. // Ibid. P. 722.
Guo F., Li G., Ma S. et al. // Intern. J. Polymer. Mater. Polymer. Biomater. 2020. V. 69. № 18. P. 1178.
Mahima Bansal, Anusha Dravid, Zaid Aqrawe et al. // J. Controlled Release. 2020. V. 328. P. 192.
Ramesh Gannimani, Pavan Walvekar, Veluru Ramesh Naidu et al. // Ibid. P. 736.
Тернышная Ю.В., Лобанов А.В., Хватов А.В. // Хим. физика. 2020. Т. 39. № 11. С. 52.
Миронов В.Ф., Карасева А.Н., Цепаева О.В. // Химия и компьют. моделирование. Бутлеровские сообщ. 2003. Т. 4. № 3. С. 45.
Шуршина А.С., Галина А.Р., Чернова В.В. и др. // Хим. физика. 2018. Т. 37. № 2. С. 56.
Инагамов С.Я., Шадманов К.К., Мухамедов Г.И. // Amer. Scientific J. 2020. № 39. С. 23.
Totea A.M., Dorin I., Laity P.R. et al. // Europ. J. Pharm. Biopharm. 2020. V. 154. P. 270.
Jie Liu, Jian Guan, Xiaocao Wan et al. // J. Pharm. Sci. 2020. V. 109. № 3. P. 1356.
Rizwanullah M., Alam M., Harshitab Mir S.R. et al. // Curr. Pharm. Design. 2020. V. 26. № 11. P. 1206.
Farheen F., Elango K., Devi Damayanthi R., Santhana-lakshmi G. // Res. J. Pharm. Technol. 2011. V. 4. № 7. P. 1106.
Sengel-Tur C.T., Alcigi M.E., Ekim O. et al. // Europ. J. Pharm. Biopharm. 2020. V. 157. P. 211.
Bharathala S., Singh R., Sharma P. // Intern. J. Biol. Macromol. 2020. V. 164. P. 45.
Платэ Н.А., Васильев А.Е. Физиологически активные полимеры. М.: Химия, 1986.
Lazarus G.G., Singh M. // Nanotechnol. Rev. 2016. V. 5. № 5. P. 425.
Shahid Ud Din Wani, Surya Prakash Gautam, Zulfkar Latief Qadrie, Gangadharappa H.V. // Intern. J. Biol. Macromol. 2020. V. 163. № 15. P. 2145.
Radu I.C., Zaharia C., Iovu H. et al. // Drug Delivery. 2019. V. 26. № 1. P. 318.
Штильман М.И. // Соросовский образоват. журн. 1998. Т. 4. № 5. С. 48.
Relaño-Rodríguez I., Juárez-Sánchez R., Pavicic C. et al. // J. Nanobiotechnol. 2019. V. 17. № 1. P. 69.
Булатов И.П., Калинкин М.И. Практическое руководство по фотометрическим методам анализа. Л.: Химия, 1986.
Баранов В.Г., Френкель С.Я., Агранова С.А. и др. // Высокомолекуляр. соединения. Б. 1987. Т. 29. № 10. С. 745.
Базунова М.В., Шуршина А.С., Чернова В.В., Кулиш Е.И. // Хим. физика. 2016. Т. 35. № 12. С. 62.
Crank J. The Mathematics of Diffusion. Oxford: Clarendon Press, 1975.
Виноградов Г.В., Малкин А.Я. Реология полимеров. М.: Химия, 1977.
Malkin A.Ya. // Polym. Sci. A. 2009. V. 51. № 1. P. 80.
Ilyin S.O., Kulichikhin V.G., Malkin A.Ya. // Polym. Sci. A. 2013. V. 55. № 8. P. 503.
Базунова М.В., Шуршина А.С., Лаздин Р.Ю., Кулиш Е.И. // Хим. физика. 2020. Т. 39. № 7. С. 49.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика


