Химия твердого топлива, 2022, № 2, стр. 63-69
ИЗМЕНЕНИЕ СТРУКТУРНЫХ ХАРАКТЕРИСТИК И СОСТАВА ОКИСЛЕННОГО УГЛЯ ВСЛЕДСТВИЕ МЕХАНОХИМИЧЕСКОГО ВОЗДЕЙСТВИЯ
Е. В. Линкевич 1, *, Н. В. Юдина 1, **, А. В. Савельева 1, ***, Е. М. Березина 1, ****
1 ФГБУН Институт химии нефти СО РАН (ИХН СО РАН)
634055 Томск, Россия
* E-mail: maltseva2@gmail.ru
** E-mail: natal@ipc.tsc.ru
*** E-mail: anna@ipc.tsc.ru
**** E-mail: emberz@yandex.ru
Поступила в редакцию 19.11.2021
После доработки 24.11.2021
Принята к публикации 08.12.2021
- EDN: QMBGYE
- DOI: 10.31857/S0023117722020049
Аннотация
Показано увеличение содержания поверхностных кислых групп, сорбционной обменной емкости окисленного угля, выхода гуминовых кислот на 20–40% вследствие механического воздействия с щелочным и окислительно-щелочными реагентами. По данным ИК-спектроскопии углей и потенциометрического титрования кислых групп, отмечается снижение содержания карбоксильных групп в алифатических фрагментах за счет их максимальной сорбционной способности по отношению к ионам металлов. Гуминовые кислоты характеризуются значительным увеличением количества кислородсодержащих групп и устойчивых полисопряженных гетероароматических фрагментов в результате механохимического воздействия.
ВВЕДЕНИЕ
В зависимости от цели применения продуктов угольной переработки выбор технологии модификации бурого угля определяется его техническими характеристиками [1]. Бурые угли широко применяются в химической промышленности, в области газификации, а также в производстве жидкого топлива, адсорбентов и гуминовых препаратов. Для извлечения неорганических ионов из водных растворов применяют активированные угли, свойства которых определяются пористой структурой и химической природой поверхности [2, 3]. Химическую природу углеродных сорбентов определяют кислотные поверхностные группы, включающие карбоксильные, лактонные, фенольные, карбонильные, пероксидные. Сорбционные и ионообменные свойства углей обусловлены, главным образом, карбоксильными группами, активность которых зависит не только от их силы, но и от взаимного расположения на поверхности угля. Гуминовые кислоты (ГК), выделенные из торфа, угля, характеризуются высоким количеством кислородсодержащих групп и участвуют во взаимодействии не только с ионами тяжелых металлов, обеспечивая их детоксикацию, но и с макро- и микроэлементами, выполняя функцию питательного источника в жизнедеятельности растений [4, 5].
При создании углеродсодержащих сорбентов применяют технологии, позволяющие изменять количество и состав активных поверхностных групп. Для увеличения поверхностной концентрации оксигенированных функций активированного угля проводят его окисление с использованием термической обработки в присутствии реагентов щелочной и кислотной групп [6, 7]. Повышение содержания поверхностных функциональных групп в угле достигается при обработке фосфорной кислотой, диаммонийфосфатом водорода [8], жидкофазном окислении азотной кислотой или перекисью водорода [9].
Модифицирование поверхности угля может осуществляться путем механохимической активации (МА). Воздействие механических сил на уголь при определенных условиях проводит к качественным изменениям его химического состава и физико-химических свойств. При неравномерном силовом возмущении межатомных связей в нагруженном теле происходит изменение частоты колебаний и уменьшение энергетического барьера распада связи и появление напряжений, по которым будут развиваться структурные трансформации [10].
Цель работы – изучение структуры, состава и поверхностных свойств окисленного угля и выделенных ГК после механохимического воздействия с щелочными и окислительно-щелочными реагентами.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Объектом исследования являлся окисленный бурый уголь месторождения Чуй-Кэнул (Монголия). Техническая характеристика угля приведена в табл. 1. Присутствие влаги в угле вызывает слипания частиц в процессе его МА. Для предотвращения слипания частиц угля добавляли абразивный материал песок.
Таблица 1.
Техническая характеристика окисленного бурого угля
| Влажность, $W_{t}^{\alpha }$ | Зольность, Ad | Vd | Элементный состав, % на daf | ||||
|---|---|---|---|---|---|---|---|
| C | H | N | S | О | |||
| 16.8 | 16.7 | 44.3 | 68.1 | 9.0 | 2.2 | 0.7 | 20.0 |
Уголь (У1) предварительно измельчался в дезинтеграторе Nossen 8255 до размера частиц 1–3 мм (частота вращения измельчающих частей 3000 об/мин. Механоактивацию угля (У2) с песком в соотношении 3:1 проводили в мельнице планетарного типа. В присутствии реагентов и песка МА угля проводили с 8 мас. % твердого гидроксида натрия (У3) и комплекса окислительно-щелочных реагентов 7% NaOH, 3% Na4P2O7, 5% Na2CO3 ⋅ 1.5H2O2 (У4) в следующем режиме: частота вращения барабанов – 1820 об/мин–1 и центробежное ускорение – 600 м/с2. Мелющими телами являлись керамические шары диаметром 8–10 мм.
Гуминовые кислоты (ГК1) выделяли из исходных и механоактивированных образцов углей (ГК2, ГК3, ГК4) 0.1 н. NaОН при температуре 20°С и перемешивании в течение 1 ч. Щелочную экстракцию повторяли трижды. Гуминовые кислоты в щелочном растворе осаждали 4% НCl до значения рН 2. Бурый аморфный осадок ГК отделяли центрифугированием, затем отмывали дистиллированной водой до значения рН 7 и высушивали в чашке Петри в вакуумном шкафу до постоянной массы.
Содержание кислых ионогенных групп в углях определяли методом потенциометрического титрования. Навеску ГК растворяли в 0.1 н. NaОН и добавляли насыщенный раствор NаСl для создания постоянной ионной силы раствора. Полученную смесь титровали 0.1 н. раствором HCl.
Регистрацию ИК спектров ГК проводили на ИК-спектрометре Nicolet-5700 (“Thermo Electron”, США) в таблетках KBr в соотношении 1:300. Для идентификации органического вещества (ОВ) угля проведено его обеззоливание в присутствии 10% соляной кислоты при нагревании до 80°С в течение 1 ч. Полученный раствор центрифугировали, уголь промывали дистиллированной водой до рН 7 и сушили в вакуумном шкафу.
Удельную поверхность углей определяли методом БЭТ по низкотемпературной адсорбции поров азота на приборе “Sorbtometer M” фирмы КАТАКОН. Удельную поверхность и объем микропор устанавливали сравнительным методом. Образцы предварительно высушивали в сушильном шкафу 4 ч при 200оС, после чего перед измерением досушивались в приборе 1 ч при 200оС. Для расчета удельной поверхности использовали линейную формулу изотермы адсорбции:
Количественное определение минеральных элементов в углях и ГК проводили методом атомно-эмиссионной спектрометрии (комплекс “Гранд”, НПО “Оптоэлектроника”, Россия) с использованием дифракционного эмиссионного спектрометра высокого разрешения.
Термогравиметрический анализ и дифференциально-термический анализ (ДТА) образцов исходного угля и ГК 1–4 проводили на синхронном термоанализаторе NETZSCH STA 449 F1 в интервале температур 25–800°С со скоростью подъема температуры 10 К/мин в атмосфере воздуха. Измерение массы проб регистрировали с точностью до 1 мкг, точность измерения температуры по кривой ДТА составляла 0.001 К.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
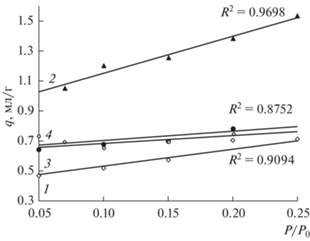
Структурные характеристики образцов угля рассчитывали из изотерм адсорбции азота. Методом БЭТ была проведена оценка сорбционной способности необработанного и механоактивированных углей. Определение площади удельной поверхности углей проводилось на начальном участке изотермы адсорбции при P/P0 в диапазоне 0.05–0.25 (рис. 1). На рисунке показано, что наименьшую адсорбционную способность проявляет образец У1. Лучшие адсорбционные свойства зафиксированы для образца У2, механообработанного угля без добавок. Введение щелочного и окислительно-щелочного реагента не оказывает существенного влияния на адсорбционные показатели У3, У4.
Рис. 1.
Изотермы адсорбции азота на угле в области парциальных давлений Р/Р0 от 0.05 до 0.25 в зависимости от условий механообработки: 1 –У1; 2 – У2; 3 –У3; 4 – У4.
В табл. 2 приведены значения площади удельной поверхности образцов, рассчитанных различными методами, и объем пор. Расхождение в значениях Sуд, рассчитанных одноточечным и сравнительным методами, указывает на участие мезопор угля в адсорбционном процессе. Величина Sуд для У1 составляет 2.5 м2/г. После МА площадь удельной поверхности увеличивается в 2 раза. Однако добавление щелочных, окислительно-щелочных реагентов и абразивного материала в виде песка снижает Sуд модифицированного угля до значений Sуд необработанного угля. Возможные причины данного явления связаны с увеличением на его поверхности количества кислородсодержащих групп кислотного характера, которые могут прочно фиксироваться на входе и/или на стенках пор, тем самым ограничивая объем пор, доступных для адсорбции азота, либо за счет уменьшения доли угля с добавками реагентов, пропорциональной количеству адсорбционных центров [9].
Таблица 2.
Адсорбционные характеристики углей
| Образец | СБЭТ | Многоточечный метод БЭТ Sуд, м2/г | Одноточечный метод БЭТ Sуд, м2/г | Сравнительный метод Sуд, м2/г | Vпор, см3/г |
|---|---|---|---|---|---|
| У1 | 128.4 | 2.527 | 2.205 | 2.133 | 0.001 |
| У2 | 60.7 | 5.119 | 5.189 | 5.107 | 0.002 |
| У3 | 448 | 2.678 | 2.559 | 1.707 | 0.001 |
| У4 | 235 | 2.625 | 2.623 | 2.160 | 0.001 |
На рис. 2 приведены спектры исходного и механоактивированного углей, свидетельствующие об идентичности структуры угольного вещества. В ИК-спектре углей в области 3400–2000 см–1 выделяется широкая полоса поглощения (п.п.) с характерным максимумом при 3400 см–1, относящимся к валентным колебаниям ОН-группы. Наличие п.п. при 1708–1700 см–1 указывает на присутствие карбонильных групп. Интенсивная полоса при 1600 см–1 соответствует ароматическим С=С-связям. Полоса поглощения 1380 см–1 приписывается [2] либо к деформационным колебаниям С–Н-, С—ОН-связи, либо симметричным колебаниям карбоксильной группы СОО–. В данной области возможно наложение полос карбоксилата металлов. Поглощение при 1260–1245 см–1 соответствует валентным колебаниям С(=О)—О-связей в составе ацетатной группы сложных эфиров, эпоксидного кольца, С—О-фенольной группы. Однако анализ кислородсодержащих фрагментов в области 1300–1000 см–1 затруднен из-за наложения п.п. минеральных веществ. Поглощение в области между 1300 и 900 см–1 связывают с фосфорными или фосфороуглеродистыми соединениями [2].
В диапазоне 700–900 см–1 могут проявляться п.п. внеплоскостных деформационных колебаний С-Н– в замещенных бензольных кольцах. В то же время в области 750–460 см–1 наблюдаются довольно сильные полосы дублета, относящиеся к колебаниям (Si–O–Si) колец из SiO4, а при 460 и 530 см–1 отмечаются п.п. валентных и деформационных колебаний тетраэдров кремнекислородного каркаса (O–Si–O и Si–O–Si).
По данным ИК-спектроскопии были рассчитаны спектральные коэффициенты, представляющие отношение значений оптической плотности полос поглощения к реперной п.п. 1600 см–1 (табл. 3). Данная п.п. хорошо разрешима с высокой интенсивностью. Для расчета были выбраны пп., по которым может происходить связывание ионов металлов в процессе механоактивации. Из данных табл. 3 видно существенное снижение значений спектральных коэффициентов D1720/D1600, D1245/D1600 для образцов У2, У3 и У4. Связывание ионов металлов с карбоксильными группами фиксируется по уменьшению интенсивности валентных колебаний 1720 и 1220–1270 см–1 и увеличению п.п. карбоксилат-иона при длине 1380 см–1.
Таблица 3.
Спектральные коэффициенты для окисленных бурых углей
| Уголь | D1720/ D1600 | D1380/ D1600 | D1260/ D1600 | D796/ D1600 | D773/ D1600 | D470/ D1600 |
|---|---|---|---|---|---|---|
| У1 | 0.64 | 0.65 | 0.73 | 0.16 | 0.17 | 0.16 |
| У1д | 0.97 | 0.63 | 0.89 | 0.23 | 0.25 | 0.17 |
| У2 | 0.62 | 0.66 | 0.61 | 0.18 | 0.20 | 0.19 |
| У2д | 1.01 | 0.63 | 0.89 | 0.24 | 0.25 | 0.20 |
| У3 | 0.56 | 0.68 | 0.59 | 0.21 | 0.25 | 0.39 |
| У3д | 1.05 | 0.59 | 0.93 | 0.37 | 0.42 | 0.51 |
| У4 | 0.56 | 0.69 | 0.61 | 0.19 | 0.22 | 0.29 |
| У4д | 1.05 | 0.57 | 0.91 | 0.33 | 0.37 | 0.37 |
Изменение значений интенсивности полос поглощения 796, 776 и 460 см–1 в ИК спектрах (рис. 2) и коэффициентов D796/D1600, D773/D1600, D460/D1600 (табл. 3) после механоактивации углей с песком и окислительно-щелочными реагентами объясняется повышением количества тетраэдров кремнекислородного каркаса (Si–O–Si и Al–O–Si). На рис. 2 приведен фрагмент ИК-спектра песка, подтверждающий данное предположение.
Для оценки влияния окислительно-щелочных реагентов при механоактивации угля проведена деминерализация образцов путем кислотной обработки. Из рис. 2 видно, что в ИК-спектре образца У4д после деминерализации возрастает интенсивность п.п. при 1710 и 1260 см–1 и снижается п.п. в области 1380–1400 см–1. При кислотной обработке образцов углей происходит десорбция ионов металлов в исходном и механоактивированных образцах угля, связанных с карбоксильными группами, и возрастает количество тетраэдров кремнекислородного каркаса (табл. 3). В углях У2, У3 и У4 разница значений коэффициентов D1720/D1600 до и после их деминерализации возрастает по сравнению с У1, что свидетельствует о дополнительном связывании ионов металлов при механохимическом воздействии.
Методом потенциометрического титрования определено количество кислородсодержащих функциональных групп в углях и выделенных из них ГК. Данные приведены в пересчете на органическую массу угля. Из табл. 4 видно, что исследуемый уголь обладает высокой сорбционной обменной емкостью (СОЕ) 15.1 мг-экв/г. После механоактивации угля не происходит существенного изменения значений СОЕ. Введение щелочного реагента в процессе МА образца У3 способствует возрастанию фенольных гидроксилов и значения СОЕ до 16.4 мг-экв/г. Наибольшая величина СОЕ зафиксирована для образца У4 с применением окислительно-щелочного реагента и соответствует 19.1 мг-экв/г. При этом наблюдается снижение доли карбоксильных групп на концах углеводородных цепочек периферической части ОВ угля.
Таблица 4.
Содержание кислых ионогенных групп в углях и выделенных ГК
| Образцы | Содержание ГК, мас. % | Количество функциональных групп, мг-экв/г | СОЕ, мг-экв/г |
||
|---|---|---|---|---|---|
| ArOH | ArCOOH | СnCOOH | |||
| У1 | 7.7 ± 0.1 | 4.9 ± 0.1 | 2.5 ± 0.1 | 15.1 | |
| ГК1 | 53.1 | 11.9 ± 0.1 | 7.9 ± 0.1 | 2.4 ± 0.1 | 22.2 |
| У2 | 7.5 ± 0.1 | 5.4 ± 0.2 | 2.4 ± 0.1 | 15.3 | |
| ГК2 | 57.4 | 12.6 ± 0.2 | 7.5 ± 0.2 | 2.0 ± 0.1 | 22.1 |
| У3 | 8.7 ± 0.2 | 5.5 ± 0.1 | 2.2 ± 0.1 | 16.4 | |
| ГК3 | 61.2 | 12.8 ± 0.2 | 8.0 ± 0.1 | 4.0 ± 0.1 | 24.8 |
| У4 | 10.6 ± 0.2 | 6.9 ± 0.2 | 1.5 ± 0.1 | 19.1 | |
| ГК4 | 80.4 | 13.0 ± 0.1 | 8.4 ± 0.2 | 3.7 ± 0.1 | 25.1 |
Сорбционная обменная емкость ГК значительно выше, чем для углей. Количество ионогенных групп в составе ГК3 и ГК4, выделенных после механоактивации угля с щелочным и окислительно-щелочным реагентами, возрастает в 1.5–2 раза.
Основной минеральный состав угля У1, ГК1, ГК2 и ГК3 представлен в табл. 5. Преобладающими элементами, содержащимися в угле, являются Ca, Fe, Al, P, Si, в меньшем количестве присутствуют Mg и Mn. Из данных табл. 5 видно, что ГК1 содержат те же элементы, что обнаружены в угле У1, но в большем количестве присутствуют Si, Al, P. В образцах ГК2 и ГК3, выделенных из механоактивированных углей У2 и У3, значительно повышается количество кремния, алюминия, кальция за счет перераспределения элементов, содержащихся в угле и песке.
Таблица 5.
Содержание минеральных компонентов в золе окисленного бурого угля
| Образец | Содержание, мас. % | |||||||
|---|---|---|---|---|---|---|---|---|
| Si | Al | Ca | Fe | Mg | Mn | P | зола | |
| У1 | 1.5 | 1.8 | 1.5 | 3.6 | 0.5 | 0.03 | 0.8 | 16.7 |
| ГК1 | 3.6 | 2.5 | 0.7 | 0.7 | 0.7 | 0.07 | 7.5 | 1.6 |
| ГК2 | 15.8 | 10.5 | 1.2 | 1.0 | 0.6 | 0.05 | 5.8 | 1.9 |
| ГК3 | 9.3 | 30.0 | 0.6 | 21.8 | 1.2 | 0.03 | 4.1 | 3.2 |
| Песок | 30.0 | 3.40 | 0.078 | 1.90 | 0.25 | 0.078 | Отс. | – |
Результаты термогравиметрического анализа (ДТА) угля У1 и гуминовых кислот приведены на рис. 3 и в табл. 6. При анализе дериватограмм выявлены три или четыре стадии основного разложения ОВ угля и гуминовых кислот. Первая стадия для всех образцов, где фиксируется эндотермический эффект на кривой ДТА в интервале 20–200°С, связана с испарением воды и выделением кислородсодержащих газов.
Рис. 3.
ДТА-кривые окисленного бурого угля и гуминовых кислот: 1 – У1, 2 – ГК1, 3 – ГК2, 4 – ГК3, 5 – ГК4.
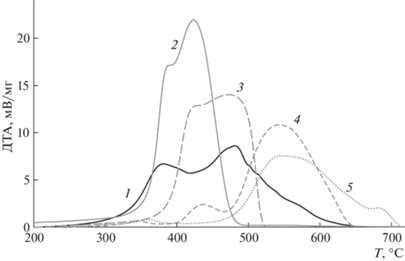
Таблица 6.
Потери массы образцов угля У1 и гуминовых кислот в различных температурных интервалах на стадиях разложения (по данным ДТА)
| Образец | Потеря массы, % | –ΔQ | +ΔQ | ||||
|---|---|---|---|---|---|---|---|
| 1-я стадия | 2-я стадия | 3-я стадия | 4-я стадия | >600 | |||
| У1 | 7.7 | 38.2 | 54.1 | – | 124.3 | 12 979 | |
| ГК1 | 6.5 | 44.4 | 49.1 | – | 121.0 | 14 531 | |
| ГК2 | 6.7 | 35.6 | 57.7 | – | 71.9 | 13 889 | |
| ГК3 | 8.1 | 12.5 | 17.1 | 62.3 | 165.2 | 14 836 | |
| ГК4 | 6.8 | 21.3 | – | 65.7 | 6.2 | ||
В интервале 200–400°С с максимумом 381°С в образце У1 протекают реакции деструкции кислородсодержащих функциональных групп и алифатических фрагментов с экзотермическим эффектом. Потеря массы угля в данной области составила 38.2 мас. %. Второй пик экзотермического эффекта с максимумом при 481°С соответствует деструкции ароматического каркаса, прочно связанного с минеральными компонентами угля. Потеря массы угля в области 400–600°С составила 54.1 мас. %.
Термогравиметрическая кривая ГК1 характеризуется двумя экзотермическими максимумами при 370 и 416°С в интервале температур 300–500°С. Потеря массы ароматического каркаса ГК на третьей стадии составила 49.1 мас. % (табл. 6). Выход летучих веществ после термодеструкции ГК1 практически соответствует угольному образцу за исключением сниженной доли ароматического каркаса с 54.1 до 49.1 мас. %. Следовательно, после щелочной экстракции угля в ГК1 переходят все функциональные группы, периферическая часть и частично ароматический каркас.
Механохимическая активация угля оказывает непосредственное воздействие на негидрализуемый остаток угля и изменяет структурный состав выделяемых ГК. Так, из рис. 3 видно, что в образце ГК2 наблюдается смещение максимумов экзотермических эффектов с 370°С для ГК1 до 404°С и с 416 до 473°С, что подтверждает получение более устойчивой структуры ГК2. Потеря массы на третьей стадии возрастает до 57.7%.
При введении щелочного реагента при МА угля на термогравиметрической кривой ГК3 зафиксировано три температурных максимума экзотермических эффектов: 370, 416 и 533°С. Смещение третьего пика в более высокотемпературную область может являться следствием образования более стабильных гетероциклических фрагментов молекул ГК под действием реагента и карбонизации органического вещества. Основная потеря массы 62.3 мас. % происходит на 4-й стадии деструкции ОВ.
Окислительно-щелочной реагент в процессе МА угля оказывает аналогичное действие на структуру ГК4, как и в случае применения щелочного реагента. В процессе термодеструкции для образца ГК4 зафиксирован наибольший экзотермический эффект при температуре 560°С. Доля летучих продуктов в диапазоне 480–600°С возрастает до 65.7 мас. %, что соответствует деструкции более устойчивых гетероароматических фрагментов. Выше 600 оС разрушается органоминеральный комплекс (рис. 3).
ВЫВОДЫ
1. Показано изменение структурных характеристик и состава окисленного бурого угля вследствие механохимического воздействия. Механоактивация угля без реагентов способствует увеличению в 2 раза удельной площади поверхности. Введение щелочных и окислительно-щелочных реагентов при механическом воздействии не изменяет величину удельной площади поверхности по сравнению с необработанным образцом, что связано с увеличением на поверхности угля количества кислородсодержащих групп кислотного характера. Результаты потенциометрического титрования подтверждают повышение сорбционной обменной емкости и содержания фенольных и карбоксильных групп в механоактивированных углях.
2. По данным ИК-спектроскопии углей, при механохимическом воздействии снижается содержание карбоксильных групп за счет связывания с ионами металлов. Подтверждением данного заключения является повышение интенсивности полос поглощения карбоксильных групп в ИК-спектрах угольных образцов после их деминерализации.
3. По результатам термогравиметрического анализа, в гуминовых кислотах и угле отмечается близость температурных интервалов разложения органического вещества. В ГК, выделенных после механохимического воздействия на уголь, высокотемпературные эффекты проявляются в интервале 480–600°С и связаны с окислением и деструкцией более устойчивых полисопряженных гетероароматических фрагментов.
Список литературы
Голицын М.В., Вялов В.И., Богомолов А.Х., Пронина Н.В., Макарова Е.Ю., Митронов Д.В. // Георесурсы. 2015. Т. 61. № 2. С. 41. https://doi.org/10.18599/grs.61.2.4
Qadeer R., Khalid N. // Separation science and Technology. 2005. V. 40. № 3. P. 845. https://doi.org/10.1081/SS-200028819
Babu B.V., Gupta S. // Adsorption. 2008. V. 14. № 1. P. 85. https://doi.org/10.1007/s10450-007-9057-x
Юдина Н.В., Савельева А.В., Ломовский О.И. // ХИВУР. 2019. Т. 29. № 4. С. 437. https://doi.org/10.15372/KhUR2019156
Юдина Н.В., Савельева А.В., Мальцева Е.В., Ломовский О.И. // ХИВУР. 2016. № 2. С. 263. https://doi.org/10.15372/KhUR20160221
Ge Z., Zeng M., Cheng Y., Wang H., Lie X. // Sustainability. 2019. V. 24. № 11. P. 7180. https://doi.org/10.3390/su11247180
Wan Daud W.M.A., Houshamnd A.H. // J. Natur. Gas Chem. 2010. V. 19. № 1. P. 267. https://doi.org/10.1016/S1003-9953(09)60066-9
Heidarinejad Z., Dehghani M.H., Heidari M., Javedan G. // Environmental Chem. Letters. 2020. V. 18. № 2. P. 393. https://doi.org/10.1007/s10311-019-00955-0
Xiaolan Song, Hongyan Liu, Lei Cheng, Yixin Qu. // Desalination. 2010. V. 255. № 1. P. 78. https://doi.org/10.1016/j.desal.2010.01.01
Ломовский О.И., Болдырев В.В. Механохимия в решении экологических задач. Новосибирск: ГПНТБ СО РАН, 2006. 221 с.
Дополнительные материалы отсутствуют.
Инструменты
Химия твердого топлива



