Химия твердого топлива, 2022, № 4, стр. 11-19
ХАРАКТЕРИСТИКА ЛИПИДНЫХ И ГУМИНОВЫХ СУБСТАНЦИЙ, ВЫДЕЛЕННЫХ ИЗ БУРОГО УГЛЯ ТЮЛЬГАНСКОГО МЕСТОРОЖДЕНИЯ
К. М. Шпакодраев 1, *, С. И. Жеребцов 1, **, Н. В. Малышенко 1, ***, К. С. Вотолин 1, ****, З. Р. Исмагилов 1, *****
1 ФИЦ угля и углехимии СО РАН
650000 Кемерово, Россия
* E-mail: shpakodraevkm@mail.ru
** E-mail: sizh@yandex.ru
*** E-mail: profkemsc@yandex.ru
**** E-mail: kostvot@mail.ru
***** E-mail: zinfer1@mail.ru
Поступила в редакцию 09.03.2022
После доработки 09.03.2022
Принята к публикации 30.03.2022
- EDN: OHVDSN
- DOI: 10.31857/S0023117722040089
Аннотация
С использованием элементного и технического анализа, ИК-, ЯМР-спектроскопии и хромато-масс-спектрометрии охарактеризованы образцы исходного угля Тюльганского месторождения Южно-Уральского бассейна, экстрагированных из него гуминовых кислот, битумов и остаточных углей. В экстракционных битумах установлено присутствие биологически активных веществ растительного происхождения. Исследована фитостимулирующая активность полученных гуминовых кислот и омыляемой составляющей смолы экстракционных битумов по отношению к семенам пшеницы сорта “Ирень”. Полученные субстанции могут быть использованы для рекультивации нарушенных земель, укрепления грунтов, стимулирования наземной растительности.
ВВЕДЕНИЕ
Комплексная переработка бурых углей – одно из ключевых направлений их эффективного использования. Более 50% разведанных запасов углей России относятся к бурым углям, являясь важнейшей составляющей теплоэнергетической базы страны. Но при таком применении данного вида сырья безвозвратно теряется его огромный потенциал, который можно раскрыть путем химической переработки, одним из способов которой является экстракция [1–3]. Применение такого способа переработки к бурым углям позволяет выделить несколько ценных продуктов: 1) щелочная экстракция – гуминовые кислоты; 2) экстракция органическими растворителями – битумы (горный воск); 3) остаточное угольное вещество.
Гуминовые кислоты – это высокомолекулярные системы нерегулярного строения, имеющие в составе разнообразные функциональные группы (карбонильные, карбоксильные, спиртовые и фенольные гидроксилы), ароматические и полисопряженные структуры. Уникальное строение и свойства гуминовых кислот обусловливают широкую область их применения: как сырье для высокоэффективных препаратов стимуляторов роста растений; препаратов для ремедиации и рекультивации деградированных и нарушенных почв; в качестве высокоэффективных сорбентов для борьбы с химическими загрязнениями, очистки промышленных стоков, извлечения катионов металлов из различных технических жидкостей и смесей водорастворимых техногенных отходов [2, 4].
Экстракционная переработка бурых углей с применением различных органических растворителей позволяет получить ценный продукт – битумы. Экстракционные битумы и продукты их переработки имеют широкое применение в различных отраслях промышленности – от металлургии до медицины. Стоимость 1 т горного воска сырца на мировом рынке приблизительно равна 3000 $. В битумах, как в восковой, так и в смоляной составляющей содержатся различные биологически активные вещества (БАВ), которые перешли в них из исходной растительности углеобразователя. Перспективной является возможность выделения из битумов БАВ в чистом виде или в виде узких фракций обогащенных БАВ с целью применения их в медицине, ветеринарии, косметике, сельском хозяйстве [5, 6].
Данная работа посвящена исследованию гуминовых и липидных субстанций, выделенных из бурого угля Тюльганского месторождения Южно-Уральского угольного бассейна, и их фитоактивности по отношению к семенам пшеницы сорта “Ирень”.
МЕТОДИЧЕСКАЯ ЧАСТЬ
Битумы и гуминовые кислоты были получены из бурого угля (ТБУ) марки 1Б Тюльганского месторождения Южно-Уральского бассейна (табл. 1).
Таблица 1.
Технический и элементный анализы образцов
| Образец | W a | Ad | V daf | Cdaf | Hdaf | H/Cатомн. | (O + N + S)daf по разности |
|---|---|---|---|---|---|---|---|
| мас. % | |||||||
| Бурый уголь | 9.1 | 21.5 | 65.9 | 57.3 | 6.3 | 1.3 | 36.4 |
| ГК из HumNa | 0.7 | 13.4 | – | 53.2 | 10.5 | 2.4 | 36.3 |
| Уост из HumNa | 4.5 | 45.4 | 60.1 | 49.8 | 7.2 | 1.7 | 43.0 |
| ГК из HumK | 5.5 | 2.7 | – | 59.0 | 7.1 | 1.4 | 33.8 |
| Уост из HumK | 4.7 | 33.2 | 76.4 | 71.2 | 7.0 | 1.2 | 21.8 |
Экстракция битумов проводилась из бурого угля (табл. 1) О-алкилированного под воздействием ультразвука частотой 22 kHZ [6]. Полученные битумы фракционировались на воск и смолу по методике, приведенной в работах [2, 7, 8]. С целью дополнительного фракционирования полученные воск и смола разделялись на омыляемую и неомыляемую составляющие в условиях реакции омыления [6]: среда – н-бутанол, KOH –до pH раствора 11–12, продолжительность процесса 3 ч, температура процесса 118 ± 5°С.
Для тестирования фитостимулирующей активности на семенах пшеницы сорта “Ирень” была выбрана фракция омыляемой составляющей смолы битумов. Данная фракция была выбрана в связи с ее полным растворением в слабо-щелочном водном растворе и наличием ряда биологически активных соединений [6].
Гуминовые кислоты (ГК), выделенные из гуматов натрия и калия (ГК из HumNa и ГК из HumK) бурого угля Тюльганского месторождения, получены по методике определения выхода свободных ГК (навеска угля (менее 0.2 мм) – 1 г, 1%-ный раствор NaOH или KOH – 100 мл, температура – 98°С, время – 2 ч) согласно ГОСТ 9517-94.
На биологическую активность тестировали водорастворимые соли гуминовых кислот – гуматы натрия и калия (HumNa и HumK).
Биологическую активность омыляемой фракции смолы (ОСм) экстракционных битумов и гуматов определяли по величине фитоактивности (ИФ) с учетом энергии прорастания семян (ЭП), длины корня (ДК) и высоты проростка (ВП). ИФ является обобщающим индексом и вычисляется как средняя величина суммы показателей ДК, ВП и ЭП, выраженное в долях единицы:
где ДК, ВП и ЭП – средние величины по трем лоткам (% к контролю) [9].В каждом эксперименте часть семян обрабатывалась 0.0005, 0.005 раствором ГК и ОСм, а часть обрабатывалась дистиллированной водой (контроль, ИФ = 1.0). Величина рН растворов составляла 7.0–8.2 и находилась в допустимых пределах для использованной культуры. Семена проращивали в специальных растильнях между слоями увлажненной фильтровальной бумаги. Повторность эксперимента трехкратная: по 50 семян в лотке для каждой концентрации удобрения и столько же для контроля. ЭП, ВП и ДК замеряли на 5-е сутки [9–12].
Групповой и компонентный составы исследуемых образцов изучали с привлечением методов ИК- (FTIR) и 13С-ЯМР (CPMAS)-спектроскопии, компонентный состав образцов битумов исследовался с привлечением метода хромато-масс-спектрометрии (ХМС).
Запись ИК-спектров проводилась на ИК-Фурье – спектрофотометре “Инфралюм-ФТ 801” при разрешении 4 см–1 с накоплением 16 сканов в диапазоне 4000–500 см–1 в сухом KBr.
Хромато-масс-спектрометрия (ХМС) проводилась на хроматографе Agilent 6890N с масс-селективным детектором Agilent 5973 при условиях: капиллярная колонка HP-5ms; температура испарителя – 290°C; удаление растворителя в течение 4 мин; деление потока в соотношении 50:1; скорость газа-носителя гелия – 1 мл/мин; объем пробы для анализа – 5.0 мкл; программируемое повышение температуры колонки от 50°C с выдержкой 3 мин до 280°C со скоростью 5°C мин; выдержка при 280°C – 60 мин. Содержание индивидуальных соединений регистрировалось по полному ионному току. Идентификация компонентного состава исследуемых образцов осуществлялась с использованием библиотеки спектров NIST-11 и Wiley.
Спектры ЯМР высокого разрешения в твердом теле регистрировали на приборе AvanceIII 300 фирмы Bruker на частоте 75 МГц с использованием стандартной методики кросс-поляризации с подавлением сигналов протонов и вращением под магическим углом (CPMAS). Производилось накопление 1024 сканов при комнатной температуре. Химический сдвиг отсчитывался от ТМС.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Отнесение полос поглощения ИК-спектров осуществлялось на основе литературных источников [13–16].
По данным ИК-спектроскопии (рис. 1), полученные битумы и их фракции – это сложные многокомпонентные смеси веществ. В спектрах образцов битумов присутствуют полосы поглощения, характерные для карбоновых кислот и их сложных эфиров (1750–1690 см–1), спиртов и фенолов (3400–3200 см–1), соединений с длинной алкановой цепочкой (3000–2800 см–1), соединений ароматического характера (1630–1575, 1175–1125 см–1).
Рис. 1.
ИК-спектры: (а) – воска 1, его омыляемой 2 и неомыляемой 3 составляющей; (б) – смолы 4, ее омыляемой 5 и неомыляемой 6 составляющей; (в) – исходный битум.
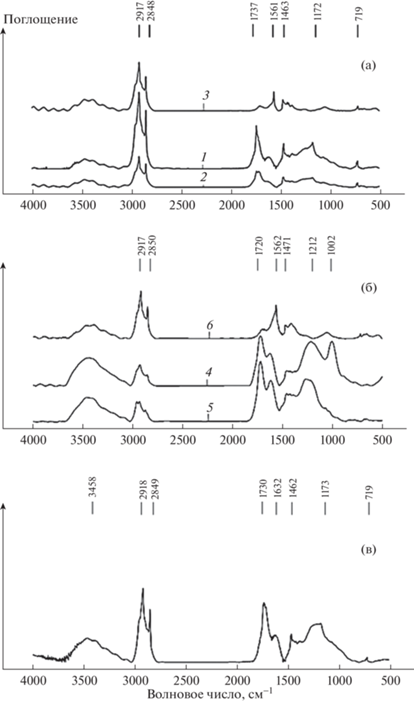
Широкая полоса поглощения в области 3650–3200 см–1 – валентные колебания О–Н-групп спиртов и фенолов; 3000–2800 см–1 – валентные колебания CH2- и CH3-групп, а также в области 1475–1450 см–1 – деформационные колебания CH2-групп; полосы поглощения в интервале 1750–1710 см–1 характерны для валентных колебаний С=О-групп алифатических сложных эфиров карбоновых кислот; полосы поглощения в области 1440–1400 см–1 деформационные колебания группы СН2- в –СН2–СО алкановых цепочек; полосы поглощения в области 1275–1150 см–1 – валентные колебания группы С–О-; полосы поглощения в интервале 1175–1125 см–1 – плоские деформационные колебания 1-, 1,3-, 1,2,3-, 1,3,5-соединений ароматического характера. В неомыляемой части воска и смолы имеются полосы поглощения в области ≈1562 см–1 – валентные колебания группы С=С– ароматических систем. В спектрах образцов исходной восковой фракции в области ≈719 см–1 имеются пики, характерные для маятниковых колебаний метиленовых групп длинных алкановых цепочек. В спектре исходной смолы (рис. 1, б) наблюдается интенсивный пик в области ≈1002 см–1, характерный для валентных колебаний группы С–О– в первичных и вторичных спиртах. Данный пик не просматривается в омыляемой и неомыляемой составляющей смолы, которые были получены в результате разделения в условиях реакции омыления. Предположительно данные вещества были удалены вместе с водной фазой, участвующей в процессе омыления, при отмывке органической фазы от кислоты.
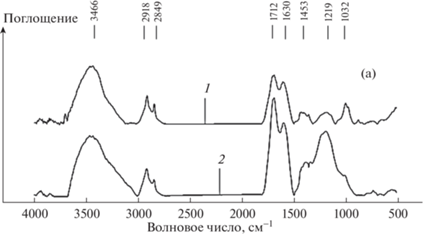
ИК-спектры гуминовых кислот, полученных при щелочной экстракции водным раствором NaOH и KOH с последующим осаждением из бурого угля Тюльганского месторождения, представлены на рис. 2. В спектрах ГК присутствует интенсивная полоса поглощения в интервале 3500–3300 см–1, характерная для валентных колебаний O–H-групп, связанных водородными связями. Полосы поглощения в области 2918, 2849 и 1453 см–1 характерны для ГК и показывают наличие CH3- и CH2-групп. Установлено наличие карбонильных групп C=O–, полосы поглощения в области 1712 см–1, а также ненасыщенных и ароматических связей C=C – полосы поглощения в области 1630 см–1. Полосы поглощения в области 1219 см–1 свидетельствуют о наличии связи C–O– карбоновых кислот, сложных эфиров, OH-фенолов. В спектре образца ГК из HumNa (см. рис. 2) присутствуют полосы поглощения в области 1100–1030 см–1, свидетельствующие о наличии минеральных компонентов и валентных колебаний C–O-связей спиртов и C–O–C-связей простых эфиров. В спектре ГК из HumK данный пик (1100–1030 см–1) представлен в виде плеча.
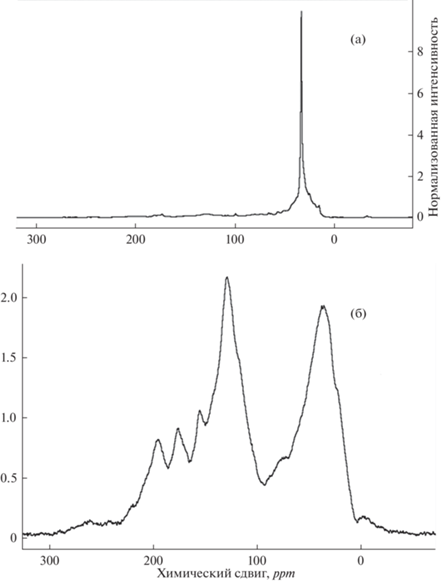
Отнесение сигналов при 13С-ЯМР (CPMAS)-исследовании проводилось на основе литературных данных [13–16]. На рис. 3 приведены типичные ЯМР-спектры образца битума и гуминовых кислот.
Согласно результатам 13С- ЯМР (CPMAS) в битумах (табл. 2), экстрагированных из Тюльганского бурого угля, преобладают соединения с длинными алкановыми цепями, принадлежащие в основном к эфирам, кислотам и спиртам жирного ряда. Пики в интервале 5–48 ppm указывают на наличие прямых алкановых цепей и алкильных групп. Пики в области 48–90 ppm показывают наличие веществ группы спиртов. В области 90–108 ppm имеются пики, указывающие на наличие ацетальных групп. Пики в области 108–145 ppm характерны для ароматической группы веществ. Наличие пиков в интервале 145–165 ppm характерно для веществ с ароматическим кольцом, имеющим гидроксильную группу. Вещества с карбоксильной группой представлены на спектре пиками в интервале 165–187 ppm. Пики в области 187–220 ppm свидетельствуют о наличии веществ с карбонильной группой.
Таблица 2.
Результаты 13С- ЯМР (CPMAS) -исследования образцов
| Образец | 220-187 С=О |
187-165 СООН |
165-145 Сar–O |
145-108 Car |
108-90 CO–alk–O |
90-48 Calk–O |
48-5 Calk |
Параметр | ||
|---|---|---|---|---|---|---|---|---|---|---|
| far | fal | far/al | ||||||||
| Битум до фракционирования | ||||||||||
| Битум | 3.1 | 4.0 | 2.9 | 9.2 | 3.2 | 13.8 | 61.8 | 12.2 | 78.8 | 0.15 |
| Воск | ||||||||||
| Воск | 1.9 | 2.8 | 1.8 | 5.6 | 2.8 | 10.5 | 72.9 | 7.4 | 86.2 | 0.09 |
| Омыляемая часть воска | 1.4 | 3.0 | 1.6 | 5.0 | 2.5 | 8.5 | 77.2 | 6.6 | 88.2 | 0.07 |
| Неомыляемая часть воска | 1.2 | 1.6 | 1.2 | 4.8 | 2.2 | 9.2 | 79.3 | 6.0 | 90.7 | 0.06 |
| Смолы | ||||||||||
| Смола | 6.5 | 7.3 | 7.8 | 23.6 | 4.7 | 16.3 | 31.1 | 31.4 | 52.2 | 0.60 |
| Омыляемая часть смолы | 5.6 | 7.4 | 6.7 | 20.5 | 4.4 | 17.4 | 35.8 | 27.2 | 57.6 | 0.47 |
| Неомыляемая часть смолы | 1.6 | 2.4 | 1.8 | 7.3 | 2.1 | 11.2 | 73.1 | 9.1 | 86.4 | 0.10 |
| Гуминовые кислоты | ||||||||||
| ГК из HumNa | 2.4 | 7.6 | 8.5 | 25.2 | 4.2 | 12.2 | 39.9 | 33.7 | 56.3 | 0.59 |
| ГК из HumK | 0.8 | 6.9 | 14.5 | 36.8 | 0.3 | 14.4 | 26.2 | 51.3 | 40.9 | 1.28 |
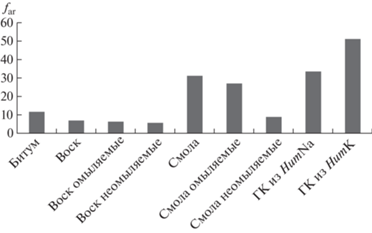
Расчет структурно-групповых параметров экстракционного битума (см. табл. 2) и его фракций на основании данных 13С-ЯМР (CPMAS) показал, что основная часть ароматических соединений (рис. 4) при разделении в условиях реакции омыления на омыляемую и неомыляемую составляющую концентрируется в первой. Структурно-групповые параметры рассчитывались по формулам [17]:
Рис. 4.
Распределение соединений ароматического характера в исследуемых образцах по данным 13С-ЯМР (CPMAS).
степень ароматичности
Результаты 13С-ЯМР (CPMAS), выделенных из Тюльганского бурого угля гуминовых кислот, представлены в табл. 2. Полученные данные показывают, что щелочная экстракция с применением едкого калия позволяет извлечь гуминовые кислоты с повышенным содержанием соединений ароматического характера (см. рис. 4), показатель far(ГК из HumK) = 51.3, т.е. в 1.5 раза выше, чем у ГК из HumNa.
В результате проведенной хромато-масс-спектрометрии образцов битумов и их фракций, с совпадением с базой данных NIST 11 более 80%, в их составе идентифицирован ряд индивидуальных соединений [6]: Dodecanoic acid; Hexacosane; Tetradecanoicacid; Nonanedioicacid; Pentadecanoicacid; 9-Hexadecenoicacid; Hexadecanoicacid; Ferruginol; Oleicacid; Octadecanoicacid; Eicosanoic acid; Sugiol; 1-Heneicosanol; Docosanoic acid; Tricosanoicacid; Docosane; Tetracosanoicacid; Hexacosanoicacid; Octacosanoicacid; Triacontanoicacid; Decanedioicacid; n-Tetracosanol-1; Oxacycloheptadecan-2-one; Octanedioicacid; Octacosanol; Erucicacid; 1-Heptacosanol; Pentacosanoicacid; Tetradecane; Betulin; Octadecane; Podocarpa-8,11,13-triene-7β,13-diol, 14-isopropyl-; Behenic alcohol; Heptacosanoicacid; Nonacosanoicacid; Butyl 15-methylhexadecanoate; Cholesta-3,5-diene; 9-Tetradecenoicacid и др. Среди идентифицированных соединений присутствуют вещества [6, 18, 19], обладающие биологической активностью (БАВ), некоторые из них представлены в табл. 3.
Таблица 3.
Некоторые из биологически активных веществ, обнаруженные в битумах методом ХМС
| Вещество [18, 19]* | Относительное содержание по данным ХМС, % | |||||
|---|---|---|---|---|---|---|
| воск** | смола** | |||||
| И | О | Н | И | О | Н | |
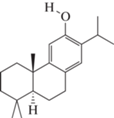 Ferruginol (C20H30O) |
0.7 | – | 1.7 | – | – | – |
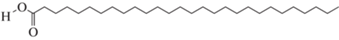 Octacosanoic acid (C28H56O2) |
14.3 | 21.0 | 14.0 | – | – | 9.1 |
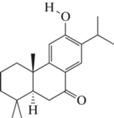 Sugiol (C20H28O2) |
0.7 | – | 1.2 | – | – | 0.4 |
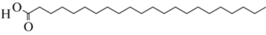 Docosanoic acid (C22H44O2) |
1.9 | 3.0 | 3.3 | – | – | 1.8 |
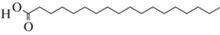 Octadecanoic acid (C18H36O2) |
0.4 | 0.5 | 0.3 | – | – | 3.3 |
 Behenic alcohol (C22H46O) |
2.2 | – | 6.0 | – | – | – |
Результаты лабораторных испытаний фитостимулирующей активности образцов ГК и ОСм битумов, выделенных из Тюльганского бурого угля, показали, что все тестируемые образцы, за исключением ГК из HumK 0.0005%, оказывают положительное влияние на ЭП семян пшеницы (табл. 4). Наибольшее влияние на ЭП достигнуто при обработке семян пшеницы водным раствором ОСм битума, при ее концентрации в растворе 0.0005%.
Таблица 4.
Величины тест-функций фитоактивности гуминовых кислот и омыляемой составляющей смолы битума
| Образец | Концен-трация, % | ДК | ВП | ЭП | ИФ |
|---|---|---|---|---|---|
| % к контролю | |||||
| ГК из HumNa | 0.0005 | 112 | 149 | 107 | 1.22 |
| 0.005 | 125 | 149 | 107 | 1.34 | |
| ГК из HumK | 0.0005 | 86 | 104 | 98 | 0.96 |
| 0.005 | 110 | 117 | 117 | 1.14 | |
| Омыляемая часть смо-лы битума (ОСм) | 0.0005 | 104 | 114 | 122 | 1.14 |
| 0.005 | 90 | 78 | 105 | 0.91 | |
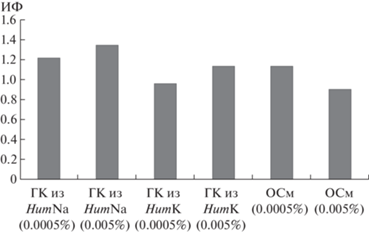
Из данных табл. 4 видно, что наибольшую фитоактивность среди исследуемых образцов демонстрируют ГК из HumNa. В полученных данных для гуминовых кислот прослеживается следующая зависимость – с увеличением концен-трации (в известных пределах) возрастает и их фитоактивность (рис. 5). Для образцов омыляемой составляющей экстракционной смолы (ОСм) данная зависимость носит обратный характер (см. табл. 4). Следует отметить, что показатель фитоактивности (ИФ) у ОСм (0.0005%) находится на уровне ГК из HumK (0.005%) и близок к показателям фитоактивности ГК из HumNa (0.0005%).
ЗАКЛЮЧЕНИЕ
В битумах, извлеченных из Тюльганского бурого угля, основная часть соединений имеет алифатический характер. Вещества ароматического характера сконцентрированы в смоляной фракции битумов, большая часть данных соединений омыляемые. По показателю ароматичности (far), экстракционные смолы близки к гуминовым кислотам, извлеченным из угля при обработке натриевой щелочью (ГК из HumNa). Следует отметить, что среди извлеченных из ТБУ субстанций ГК из HumK содержит в своем составе наибольшее количество ароматических соединений, на что указывает показатель far = 51.3.
Экстракционные битумы и их фракции содержат в своем составе различные ценные вещества, среди которых присутствуют вещества, идентичные таковым растительного происхождения, обладающие биологической активностью.
Результаты лабораторных испытаний фитостимулирующей активности исследуемых образцов показали, что наибольшей активностью на семена пшеницы сорта “Ирень” обладает ГК из HumNa при применении в концентрации 0.005%. Самые низкие результаты демонстрирует применение ОСм в концентрации 0.005% (ИФ = 0.91). При этом следует отметить, что фитоактивность ОСм в концентрации 0.0005% (ИФ = 1.14) находится на уровне ГК из HumNa и HumK при концентрациях 0.0005 и 0.005% соответственно. Наряду с этим ОСм 0.0005% среди исследуемых образцов демонстрирует наибольшее влияние на энергию прорастания семян (ЭП = 122%).
Таким образом, исследуемый бурый уголь Тюльганского месторождения Южно-Уральского бассейна – перспективное и ценное сырье для комплексной переработки с получением ряда продуктов: битумов и их производных, гуминовых кислот. Смоляная часть битумов, являющаяся в настоящее время отходом производства горного воска, а именно ее омыляемая составляющая, наряду с гуминовыми кислотами может быть применена для рекультивации нарушенных земель, укрепления грунтов, стимулирования наземной растительности, увеличения урожайности зеленой массы растений. Вместе с тем адгезионные свойства, характерные для экстракционных смол, делают возможным применение ОСм в качестве фитостимулирующей связующей добавки при производстве гранулированных гуматных удобрений.
Список литературы
Жеребцов С.И., Моисеев А.И. // ГИАБ. 2008. № S7. С. 114.
Жеребцов С.И. Алкилирование спиртами твердых горючих ископаемых низкой степени углефикации: Дис. … д-ра хим. наук. М.: МХТИ им. Д.И. Менделеева, 2017. 317 с.
Белькевич П.И. Битумы торфа и бурого угля. Минск: Наука и техника, 1989. 125 с.
Вотолин К.С. Разработка научных основ получения гуминовых субстанций с заданным структурно-групповым составом из бурых углей: Дис. … канд. хим. наук. Красноярск: ИХХТ СО РАН, 2021. 173 с.
Шпакодраев К.М., Жеребцов С.И., Малышенко Н.В., Исмагилов З.Р. // ХТТ. 2020. № 4. С. 34. [Solid fuel chemistry, 2020. V. 54. № 4. P. 19. https://doi.org/10.3103/S0361521920040059]
Шпакодраев К.М., Жеребцов С.И., Малышенко Н.В., Вотолин К.С., Исмагилов З.Р. // ХТТ. 2021. № 5. С. 45. [Solid fuel chemistry, 2021. V. 55. № 5. P. 312. https://doi.org/10.3103/S0361521921050050]
Аронов С.Г., Нестеренко Л.Л. Химия твердых горючих ископаемых. Харьков: Изд-во Харьковского гос. ун-та, 1960. 371 с.
Тайц Е.М., Андреева И.А. Методы анализа и испытания углей. М.: Недра, 1984. 301 с.
Воронина Л.П., Якименко О.С., Терехова В.А. // Агрохимия. 2012. № 6. С. 50.
Вавилов П.П., Гриценко В.В., Кузнецов В.С. Практикум по растениеводству. М.: Колос, 1983. 352 с.
ГОСТ 12038–84. Семена сельскохозяйственных культур. Методы определения всхожести. М.: Изд-во стандартов, 1984. 30 с.
ГОСТ Р 54221–2010. Гуминовые препараты из бурых и окисленных каменных углей. Методы испытания. М.: Стандартинформ, 2012. 10 с.
Родэ В.В., Папирова Е.А.// ХТТ. 1981. № 6. С. 52.
Pretsch E., Biihlmann P., Affolter C. Structure determination of organic compounds. Tables of spectral data. Berlin, Heidelberg: Springer, 2009. 431 p.
Interpreting Infrared, Raman, and NMR Spectra / Ed. Nyquist R.A. San Diego: Academic press, 2001. V. 1. 448 p.
Spectrometric identification of organic compounds. Seventh edition / Silverstein R.M., Webster F.X., Kiemle D.J. Hoboken: John Wiley & Sons. Inc. 2005. 502 p.
Калабин Г.А., Каницкая Л.В., Кушнарев Д.Ф. Количественная спектроскопия ЯМР природного органического сырья и продуктов его переработки. М.: Химия, 2000. 408 с.
PubChem (https://pubchem.ncbi.nlm.nih.gov)
PubMed (https://pubmed.ncbi.nlm.nih.gov)
Дополнительные материалы отсутствуют.
Инструменты
Химия твердого топлива