Кинетика и катализ, 2022, T. 63, № 4, стр. 484-490
Роль гетерогенного обрыва цепей в распространении пламени
В. В. Азатян a, *, М. И. Алымов b, В. М. Прокопенко b, С. К. Абрамов b, В. Б. Казанский c
a ФНЦ Научно-исследовательский институт системных исследований РАН
117218 Москва, Нахимовский просп., 36, корп. 1, Россия
b ФГБУН Институт структурной макрокинетики и проблем материаловедения РАН им. А.Г. Мержанова
142432 Московская область, Черноголовка, ул. Акад. Осипьяна, 8, Россия
c ФГБУН Институт органической химии РАН им. Н.Д. Зелинского
119991 Москва, Ленинский просп., 47, Россия
* E-mail: vylenazatyan@yandex.ru
Поступила в редакцию 27.09.2021
После доработки 04.02.2022
Принята к публикации 29.03.2022
- EDN: PSLVHG
- DOI: 10.31857/S0453881122040025
Аннотация
Показано, что кинетические характеристики распространяющегося пламени зависят от химических свойств контактирующей твердой поверхности и от скоростей гетерогенной рекомбинации активных промежуточных частиц. Установлено, что пламя влияет на химические свойства поверхности, что в свою очередь сказывается на характеристиках распространения пламени. Распространение пламени протекает в пульсирующем режиме, характеристики которого также зависят от химических свойств поверхности. В силу пульсирующего характера горения и изменчивости в ходе горения свойств поверхности и кинетических параметров гетерогенных реакций достоверность математического моделирования распространения пламени крайне мала.
ВВЕДЕНИЕ
Известно, что основным макрокинетическим режимом горения газов является распространение пламени. Кинетические закономерности реакций в распространяющемся пламени и его тепловой режим – это важнейшие характеристики процесса как для теории горения, так и для практики. Именно этот режим реализуется также в силовых и нагревательных установках, в которых пламя контактирует с поверхностью реактора. В традиционной теории теплового горения газов и в работах, выполненных в соответствии с этой теорией, цепная природа реакции не учитывалась. Гипотетически считалось, что реакция протекает одностадийно с участием только исходных молекул. Также гипотетически приписывали реакции первый или второй кинетический порядок. Соответственно, единственным фактором самоускорения процесса считался саморазогрев. Поэтому зависимость характеристик распространения пламени от диаметра реактора объясняли изменением только скорости кондуктивного теплоотвода (например, [1–3]). В некоторых работах допускалось, что в энергоотводе играет роль и излучение. Роль стенок реактора, контактирующих с газом, сводили к кондуктивному теплоотводу и при интерпретации горения в узких каналах и порах в так называемом фильтрационном горении.
Однако в серии комплексных исследований (например, [4–7]) было обращено внимание на то, что скорости межмолекулярных реакций в силу их больших энергий активации, превышающих 50 ккал/моль [8, 9], в тысячи раз меньше скоростей реакций горения. Вопреки общепринятым представлениям было показано, что горение газов протекает по цепным механизмам не только при давлениях в десятки и сотни раз ниже атмосферного, но также при более высоких давлениях, в том числе, в распространении пламени, во взрыве и в детонации. Во всех этих режимах расходование исходных реагентов в процессах горения с точностью до сотых долей процента происходит исключительно в реакциях с активными промежуточными частицами. Реакции горения протекают только по законам неизотермических цепных процессов, принципиально отличным от законов нецепных реакций.
В связи с этим встал вопрос о роли контактирующей поверхности в газофазном горении. Было обращено внимание на то, что в энергоотводе, осуществляемом столкновениями частиц газа со стенками реактора, наряду с молекулярными компонентами участвуют свободные атомы и радикалы [7, 10]. В отличие от молекулярных компонентов эти частицы, обладающие свободными валентностями, при столкновении с твердой поверхностью не только отражаются, но способны также адсорбироваться, рекомбинировать, реагировать с материалом поверхности. В таких гетерогенных реакциях свободных атомов и радикалов уничтожаются свободные валентности частиц, и тем самым теряется наиболее рациональный для химического превращения вид химической энергии, обеспечивающий протекание реакций с малыми энергиями активации и, значит, с большими скоростями. Из сказанного выше следует, что реакции гетерогенной гибели свободных атомов и радикалов, приводящие к обрыву цепей, блокируют цепной процесс. Таким образом, вместо прежней теории о распространении пламени, в которой роль поверхности сводилась только к отводу тепла, стало необходимым выяснить возможность зависимости распространения пламени от гетерогенных реакций атомов и радикалов. Было установлено, что, действительно, скорость пробега пламени зависит от химической природы поверхности реакционной трубки [10].
Другой проблемой, связанной с гетерогенными реакциями атомов и радикалов, является взаимное влияние газофазной цепной реакции и химических свойств поверхности. Этот вопрос в работе [10] не был рассмотрен. Взаимное влияние кинетики воспламенения в замкнутом реакторе при давлениях в сотни раз ниже атмосферного и химических свойств поверхности описано в работах [7, 11, 12]. Прессованную таблетку силикагеля с изучаемой поверхностью помещали в кювету спектрометра, служащую одновременно также реактором. Изменение состава адсорбционного слоя регистрировали по ИК-спектрам. Была найдена корреляция между изменениями ИК-спектров и кинетикой воспламенения. Сильные различия условий и характеристических времен реакций в вакууме, соответствующие опытам [7, 11, 12], и свойств распространения пламени при атмосферном давлении, изученного в [10], исключают возможность проведения аналогий в механизмах процессов даже в общих чертах. В настоящей работе представлены данные, демонстрирующие взаимное влияние характеристик распространения пламени и химических свойств поверхности. Приводятся также результаты, демонстрирующие наличие пульсаций пламени и указывающие на ячеистый характер горения.
С целью выяснения относительных ролей гетерогенного обрыва реакционных цепей и кондуктивного теплоотвода в энергоотводе при распространении пламени были изучены характеристики распространения пламени горения водорода с воздухом в трубках из молибденового стекла с варьируемой способностью стенок обрывать реакционные цепи. Для изменения свойств поверхности в разных опытах трубки предварительно споласкивали раствором борной кислоты, дистиллированной водой или разбавленной тонкой суспензией оксида магния. Выбор этих способов обработки стенок определялся тем, что коэффициенты гетерогенной рекомбинации ведущих активных частиц горения водородсодержащих веществ, т.е. атомов Н и О, на создаваемых таким образом покрытиях поверхности существенно разные [3, 7, 13]. Соответственно, следовало ожидать, что горение, например, над оксидом магния протекает медленнее, и поэтому скорость пламени будет меньше, чем над поверхностью стекла, промытой водой и кислотой. Постановка эксперимента заключалась в том, что если над поверхностями, обработанными MgO и борной кислотой, несмотря на сильное различие эффективностей гетерогенного обрыва цепей, скорость пламени окажется практически одинаковой, то, значит, роль обрыва цепей на поверхности несущественна, и роль стенок определяется только кондуктивным теплоотводом, как это считалось ранее. Если же скорость пламени над MgO окажется меньше, чем над борной кислотой, то, следовательно, наблюдаемая тормозящая роль стенок, обработанных MgO, во многом обусловлена гетерогенным обрывом цепей.
Задачей настоящей работы являлось также изучение взаимного влияния цепного горения и свойств контактирующей поверхности. Это – одна из актуальных проблем теории гетерогенных реакций, в том числе горения при контакте с твердой поверхностью. Вместе с тем изменения свойств поверхности в ходе горения связаны с проблемой количественного описания и объяснения кинетики горения, со степенью достоверности численного моделирования горения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
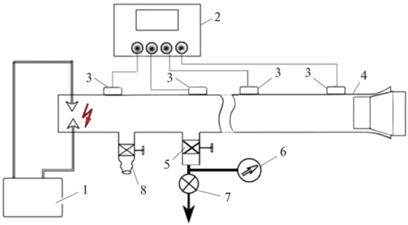
Схема экспериментального стенда представлена на рис. 1. Распространение пламени изучали при атмосферном давлении в горизонтальных трубчатых реакторах из молибденового стекла диаметром 1.2 см и длиной 224 см с одним открытым концом, а также в стальной трубе диаметром 5 см и длиной 5 м. На стенке этой металлической трубы проделаны окошечки с установленными фотодатчиками. Смесь 15% водорода с воздухом составляли в резервуаре за 24 ч до измерений. Горение инициировали с помощью искры с энергией 3.6 Дж у закрытого конца трубки. Пробег пламени регистрировали по хемилюминесценции с помощью четырех фотодатчиков (интервал длин волн чувствительности – 300–600 нм), расположенных на равных расстояниях между собой вдоль реактора. С целью устранения помех от посторонних источников света стеклянная трубка была обернута черной бумагой с прорезями для фотодатчиков. Сигналы от датчиков передавали в четырехканальный осциллограф (“TEKTRONIX”, США) и обрабатывали на компьютере. Регистрировали осциллограммы при прохождении пламени мимо каждого из четырех окон. По этим осциллограммам строили x–t-диаграммы пробега пламени (где х – пробег пламени, а t – время), которые в данном случае являются аналогами кинетических кривых. После каждого опыта реактор откачивали.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
При интерпретации результатов мы учитывали, что распространение пламени представляет собой последовательное самовоспламенение каждого последующего слоя горючей смеси. На рис. 2а и 2б приведены осциллограммы хемилюминесценции пламени в молибденовой трубке над поверхностью, сполоснутой борной кислотой, в двух последовательных опытах 1 и 2, на рис. 3а, 3б и 3в – осциллограммы хемилюминесценции пламени в молибденовой трубке над поверхностью, сполоснутой MgO, в трех последовательных опытах 3, 4 и 5. Этим осциллограммам соответствуют x–t-диаграммы на рис. 4. Видно, что над борной кислотой пламя вдоль реактора распространяется с ускорением. К моменту достижения последнего фотоумножителя скорость в обоих опытах (1 и 2) близка к 25 м/с.
Рис. 2.
Осциллограммы хемилюминесценции пламени в реакторе, сполоснутом Н3ВО3, в последовательных опытах 1 (а) и 2 (б). Номера осциллограмм соответствуют номерам датчиков. Начало отсчета на оси ординат (в вольтах) произвольное.

Рис. 3.
Осциллограммы хемилюминесценции пламени в реакторе, сполоснутом суспензией MgO, в трех последовательных опытах: 3 (а), 4 (б) и 5 (в). Номера осциллограмм соответствуют номерам датчиков. Начало отсчета на оси ординат (в вольтах) произвольное.

Рис. 4.
x–t-диаграммы пробега пламени над поверхностью борной кислоты (1, 2) оксида магния (3, 4, 5). Номера кривых на рисунке соответствуют последовательности опытов.

Различие осциллограмм, так же как и x–t-диаграмм, соответствующих опытам 1 и 2, показывает, что после опыта 1 поверхность оказалась обработанной пламенем.
Распространение пламени над окисью магния подчиняется существенно другим закономерностям. Из кривых 3, 4 и 5 на рис. 4 (опыты 3, 4 и 5 соответственно) видно, что пламя над MgO (в отличие от пламени над борной кислотой) от опыта к опыту ускоряется все сильнее, причем в опытах 4 и 5 скорости становятся близкими к скоростям пламени над поверхностью, обработанной борной кислотой (кривые 1 и 2 на рис. 4, соответствующие опытам 1 и 2). Таким образом, горящий газ воздействует на химические свойства поверхности оксида магния. Это проявляется в том, что характеристики распространения пламени существенно различаются в разных опытах с одним и тем же покрытием. В опыте 3 над свежей поверхностью MgO, не контактировавшей с горящим газом, пламя распространяется значительно медленнее, чем в последующих двух опытах 4 и 5. В опыте 3 (кривая 3) наклон x–t-диаграммы, начиная с 100 мс, остается постоянным, и, значит, скорость пламени вдоль трубы монотонно падает; после 0.8 м скорость пламени составляет лишь 1.5 м/с, т. е. почти в 13 раз меньше, чем в четвертом и в пятом опытах (кривые 4, 5). Очевидно, что это свидетельствует о повышении интенсивности горения. В опыте 5 (кривая 5) скорость пламени еще больше. Изменение формы кривых по ходу распространения пламени показывает, что разные участки поверхности вдоль трубы обладают разной эффективностью обрыва цепей. Изменение вида осциллограмм, соответствующих опытам с оксидом магния, также является результатом изменения свойств поверхности под воздействием пламени. Изменение свойств поверхности проявляется также в различиях осциллограмм в опытах 1 и 2 с одной и той же смесью.
Таким образом, характеристики распространяющегося пламени зависят не только от начального химического состава поверхности, но также от ее изменяющихся химических свойств под влиянием промежуточных продуктов горения. Известно, что при длительном контакте с пламенем смеси данного состава свойства поверхности стабилизируются и приходят в соответствие с пламенем.
Поскольку, в отличие от скоростей гетерогенных реакций, скорость кондуктивного теплоотвода не зависит от химической обработки поверхности, то обнаруженное различие скоростей пламени над поверхностями с разными химическими свойствами вызвано только различием эффективностей гетерогенного обрыва цепей. Значительное превышение скорости пламени при слабом гетерогенном обрыве цепей над скоростью пламени при интенсивном гетерогенном обрыве означает, что при интенсивной гетерогенной рекомбинации тормозящее влияние поверхности на горение обусловлено в основном не теплоотводом, а гетерогенным обрывом цепей.
В распространении пламени гетерогенный обрыв реакционных цепей и изменение его интенсивности под воздействием горения оказывают значительное действие на величину скорости пламени и в энергоотвод. В кинетике роль гетерогенного обрыва цепей в энергоотводе особенно велика при небольших диаметрах трубок, например, в фильтрационном горении.
Известно, что поверхность нержавеющей стали, например, марки Х17, покрыта слоем оксида хрома, защищающего металл от окисления. На оксидах других металлов гетерогенная рекомбинация атомов Н, О и радикалов ОН протекает так же эффективно, как и на MgO [3]. Это значит, что в реакторе из нержавеющей стали воздействие стенок на распространения пламени подобно влиянию MgO и определяется в основном гетерогенным обрывом цепей, а не кондуктивным теплоотводом, вопреки прежним представлениям.
Изменение химического состава поверхности в гетерогенных реакциях атомов показывают также эксперименты, использующее явление быстрого вытеснения атомов металлов из их солей атомарным реагентом пламени [14]. В этих экспериментах реактор споласкивали раствором хлористого калия. После откачки реактора поверхность оказывалась покрытой тонким слоем KCl. В быстрой реакции атомарного водорода с твердой солью образуется атомарный калий, который в условиях пламени интенсивно излучает характерный фиолетово-красный свет при длинах волн 766.5 и 769.9 нм. Излучение, легко наблюдаемое визуально, также служит индикатором изменения химических свойств поверхности под воздействием носителей реакционных цепей.
В работе [15] было показано, что доступ активных частиц к поверхности облегчен эстафетным характером диффузии благодаря их участию в реакциях по пути к стенке.
Приведенные выше данные являются примером известной подверженности химических свойств поверхностей и кинетических характеристик гетерогенных реакций воздействию горящей смеси [4, 7]. Хорошо известна также обусловленная этим изменчивость свойств поверхности, проявляющаяся часто в плохой воспроизводимости кинетики гетерогенных реакций, отмеченная, например, в [4, 5].
Таким образом, закономерности распространения пламени во многом зависят от характера и скорости гетерогенных реакций активных промежуточных частиц и, прежде всего, от интенсивности гетерогенного обрыва цепей. В свою очередь пламя влияет на химические свойства поверхности. Вследствие неизвестности констант скорости гетерогенных реакций и изменений состояния поверхности под влиянием пламени получение достоверных результатов математического моделирования горения в условиях гетерогенного обрыва цепей практически невозможно.
ФИНАНСИРОВАНИЕ
Работа выполнена при финансовой поддержке РФФИ (грант № 18-03-00489), а также Минобрнауки России по государственному контракту № 05.607.21.0304 (идентификатор контракта RFMEFI60719X0304) “Разработка эффективных способов химического ингибирования гомогенных и гетерогенных процессов горения и создание демонстрационного образца детонационного конвертора техногенных отходов” в рамках Федеральной целевой программы “Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2014–2020 годы”.
Работа выполнена при финансовой поддержке Министерства науки и высшего образования РФ (соглашение № 075–15–2020–806 от 29 сентября 2020 г.).
Список литературы
Франк-Каменецкий Д.А. Основы макрокинетики, диффузия, теплопередача в химической кинетике. Долгопрудный: Интеллект, 2008. 407с.
Зельдович Я.Б., Баренблат Г.И., Либрович В.Б., Махвиладзе Г.М. Математическая теория горения. Москва: Наука, 1980. 478 с.
Lewis B., Von Elbe G. Combustion, explosions and flame in gases. New York–London: Acad. Press, 1987. 592 p.
Азатян В.В. // Успехи химии. 1999. Т. 68. № 12. С. 1122.
Азатян В.В., Павлов В.А., Шаталов О.П. // Кинетика и катализ. 2005. Т. 46. № 6. С. 835.
Азатян В.В. // Журн. физ. химии. 2011. Т. 85. № 8. С. 1405.
Азатян В.В. Цепные реакции в процессах горения, взрыва и детонации газов. Москва: Изд. РАН, 2017. 448 с.
Baulch D.L., Bowman C.T., Cobos C.J., Cox R., Just T., Kerr J., Pilling M., Stocker D., Troe J., Tsang W., Walker R.W., Warnatz J. // Evaluated Kinetic Data for Combustion Modeling: Supplement II. 2005. V. 34. № 3. P. 757.
Srinivasan N.K., Michael J.V., Harding L.B., Klippenstein S.J. // Comb. Flame. 2007. V. 149. № 1–2. P. 104.
Азатян В.В., Абрамов С.К., Борисов А.А., Прокопенко В.М., Чапышева Н.В. // Журн. физ. химии. 2013. Т. 87. № 3. С. 403.
Азатян В.В., Айвазян Р.Г., Кадушин А.А., Калканов В.А., Шавард А.А. // Кинетика и катализ. 1986. Т. 27. № 2. С. 405.
Азатян В.В., Айвазян Р.Г., Калканов В.А., Синельникова Т.А., Филипенко В.Т., Шавард А.А. // Кинетика и катализ. 1987. Т. 28. № 6. С. 1290.
Семенов Н.Н. Избранные труды. Т. 3. Москва: Наука, 2005. 498 с.
Азатян В.В., Рубцов Н.М., Черныш В.И., Цветков Г.И. // Кинетика и катализ. 2006. Т. 47. № 3. С. 333.
Азатян В.В., Прокопенко В.М., Абрамов С.К. // Журнал физической химии. 2019. Т. 93. № 4. С. 622.
Дополнительные материалы отсутствуют.
Инструменты
Кинетика и катализ