Кинетика и катализ, 2022, T. 63, № 5, стр. 652-660
Гранулированный иерархический цеолит Y и деалюминированные образцы на его основе в олигомеризации пентена
Д. В. Серебренников a, *, Н. Г. Григорьева a, **, А. Н. Хазипова a, З. С. Самигуллина b, Б. И. Кутепов a
a Институт нефтехимии и катализа УФИЦ РАН
450075 Уфа, просп. Октября, 141, Россия
b ФГБОУ ВО Уфимский государственный нефтяной технический университет
450062 Уфа, ул. Космонавтов, 1, Россия
* E-mail: d25c25@yandex.ru
** E-mail: ngg-ink@mail.ru
Поступила в редакцию 01.03.2022
После доработки 21.05.2022
Принята к публикации 25.05.2022
- EDN: ZPVPRN
- DOI: 10.31857/S0453881122050100
Аннотация
Исследованы каталитические свойства ряда образцов цеолита FAU (Y) (микропористый цеолит H-Y, гранулированный иерархический цеолит H-Yh, деалюминированный с помощью термопаровой обрабоки (ТПО) цеолит H-USYh и деалюминированный с помощью ТПО и кислоты цеолит H-USYh a.t.) в олигомеризации пент-1-ена. Образцы охарактеризованы методами рентгенофлуоресцентного анализа, рентгеновской порошковой дифракции, низкотемпературной адсорбции–десорбции N2, сканирующей электронной микроскопии (СЭМ), термопрограммированной десорбции (ТПД) аммиака. Установлено, что суммарный выход олигомеров пентена в изученных условиях (150°С, 10 мас. % катализатора, 5 ч) уменьшается в ряду: H-USYh a.t. (93%) ≈ H-Yh (93%) < H-Y (74%) < < H-USYh (70%). Деалюминированный образец H-USYh a.t., обладающий наибольшим объемом мезопор, показал высокую стабильность в олигомеризации пент-1-ена при 180°С. Конверсия мономера в его присутствии не изменялась в течение 5 циклов работы без регенерации катализатора, выход олигомеров пентена после 5 циклов снижался на 39%. Микропористый цеолит H-Y терял активность уже после 2-ого цикла.
ВВЕДЕНИЕ
Благодаря своим уникальным свойствам – кислотности, высокой термической и гидротермальнойя стабильности, формоселективности – цеолиты широко используются как катализаторы и адсорбенты в различных сферах, в особенности, в нефтепереработке и нефтехимии [1]. Поэтому важное значение имеет разработка эффективных цеолитных материалов, обладающих не только высокими активностью и селективностью, но и более длительным сроком службы. Одним из самых перспективных подходов в этом направлении является получение цеолитов с иерархической пористой структурой, т.е. таких, в которых помимо микропор есть поры большего размера, например, мезо- и/или макропоры [2].
Цеолиты с иерархической пористой структурой показали себя эффективными катализаторами в различных процессах [2, 3], поскольку наличие в них транспортных пор обеспечивает хорошую доступность активных центров и упрощает диффузию для молекул, участвующих в реакции.
Одной из промышленно важных реакций, где эффективность иерархических цеолитов была выше, чем микропористых цеолитов, является олигомеризация легких олефинов С3–С6 [4–7]. Олигомеры легких олефинов С3–С6 используют для получения высококачественных моторных топлив, в которых отсутствует сера и ароматические соединения.
Corma и др. [4] изучили влияние диффузии и концентрации кислотных центров на протекание реакции олигомеризации пропилена и пентена в присутствии образцов цеолитов ZSM-5 с различным размером кристаллов, концентрацией кислотных центров и пористостью. Установлено, что в олигомеризации пропилена решающими факторами были малый размер кристаллов цеолита и высокая концентрация кислотных центров, а создание мезопористости в цеолите ZSM-5 приводило лишь к незначительному увеличению конверсии пропилена. В тоже время в олигомеризации пентена микро-мезопористый образец (получен обработкой щелочью) обеспечивал повышенный выход дизельной фракции и стабильную работу при максимальной конверсии. Аналогичные наблюдения сделаны авторами других работах, которые использовали иерархический цеолит ZSM-5 (получен постсинтетической обработкой щелочью) в олигомеризации бутилена [5] и гексена [6, 7]. Отмечено, что ZSM-5 с иерархической пористой структурой проявлял высокую стабильность в олигомеризации как бутилена, так и гексена, поскольку в нем, благодаря улучшенной диффузии, значительно медленнее протекала блокировка пор продуктами реакции и дезактивация вследствие образования кокса. К тому же облегченный масcоперенос и наличие мезопор позволяли увеличить выход олигомеров с более высокой молекулярной массой.
Существует три подхода к синтезу иерархических цеолитов: 1) методы прямого синтеза, так называемый подход “снизу вверх”, с применением темплатов или без них; 2) пост-синтетические, деструктивные методы (подход “сверху вниз”) – извлечение атомов алюминия или кремния из кристаллической решетки цеолитов; 3) смешанные методы, объединяющие предыдущие два подхода [8–11].
В лаборатории приготовления катализаторов ИНК УФИЦ РАН разработаны способы прямого синтеза иерархических цеолитных материалов в виде гранул [12–15], представляющих собой сростки кристаллов исходного цеолита и образовавшихся нанокристаллов. В процессе гидротермального синтеза в гранулах между сростками кристаллов формируются мезо- и макропоры. Сочетание микропор кристаллов цеолита и пор межкристаллического пространства создает многоуровневую, т.е. иерархическую систему пор (микро-мезо-макропоры) [14, 15]. Важное достоинство данного материала – то, что он гранулированный, так как в промышленности используют именно экструдированные цеолитные катализаторы. В отличие от классических экструдатов, состоящих из смеси цеолита и связующего вещества, приготовленные гранулы на 95–99% являются цеолитом определенного структурного типа, что положительно сказывается на адсорбционных и каталитических свойствах материала.
Синтезированный по указанному способу гранулированный иерархический цеолит H-Yh был исследован нами в качестве катализатора олигомеризации пент-1-ена. Результаты сравнивали с данными, полученными при олигомеризации пент-1-ена на микропористом цеолите H-Y и образцах цеолита H-Yh, подвергнутых деалюминированию с помощью: а) термопаровой обработки (ТПО); б) последовательной ТПО и кислотной обработки.
В настоящей работе приведены результаты изучения активности, селективности и стабильности указанных образцов в олигомеризации пент-1-ена.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реагенты и катализаторы
В работе использовали пент-1-ен (97%, “Acros”).
Цеолит Na-Y (SiO2/Al2O3 = 5) синтезировали в ООО “Ишимбайский специализированный химический катализаторный завод”. В Н-форму его переводили ионным обменом в растворе NН4NО3 и последующей термообработкой на воздухе (степень обмена ионов Na+ на Н+ α = 0.97).
Гранулированный цеолит высокой степени кристалличности с иерархической (микро-мезо-макропоры) пористой структурой Na-Yh (SiO2/Al2O3 = = 5.7) синтезировали по описанному ранее методу [12–15]. С помощью многократного ионного обмена в растворе NН4NО3 и промежуточных термообработок на воздухе получали образец H-Yh (α = 0.95).
Для приготовления образца H-USYh цеолит H-Yh подвергали высокотемпературной обработке в среде 100%-ного водяного пара (ТПО) при 550°С в течение 3 ч.
Образец H-USYh a.t. получали из H-USYh в три стадии: 1) ТПО при 540°С, 3 ч; 2) обработка 1.0 Н раствором лимонной кислоты; 3) прокалка в воздухе при 540°С в течение 3 ч.
Перед каталитическими испытаниями образцы цеолитов подвергали термообработке в течение 4 ч на воздухе при 450°С.
Методы исследования катализаторов
Химический состав синтезированных образцов определяли методом рентгенофлуоресцентного анализа на приборе EDX-720/900HS (“Shimadzu”, Япония). Фазовый состав изучали с помощью рентгеновского дифрактометра XRD-7000 (“Shimadzu”, Япония) в монохроматизированном CuKα-излучении в области углов от 5° до 40° по 2θ с шагом 0.5°/мин и временем накопления в каждой точке 20 с. Cтепень кристалличности рассчитывали по отношению суммарной интегральной интенсивности от кристаллической фазы к суммарной интегральной интенсивности от кристаллической и аморфной фаз. Решеточный модуль цеолитов вычисляли по уравнению Брека–Фланегена, исходя из рассчитанных параметров элементарной ячейки [16].
Размеры и морфология кристаллов образцов проанализированы при помощи сканирующей электронной микроскопии (СЭМ) на приборе Regulus SU8220 (“Hitachi”, Япония). Изображения получены в режиме регистрации вторичных электронов при ускоряющем напряжении 2 кВ.
Характеристики пористой структуры определяли методом низкотемпературной адсорбции–десорбции азота (77 К) на сорбтометре NOVA 1200e (“Quantachrome”, США). Удельную поверхность рассчитывали по методу БЭТ, распределение размера пор – по десорбционной кривой методом BJH, общий объем пор – методом BJH. Объем микропор в присутствии мезопор находили t-методом.
Кислотные свойства образцов цеолитных катализаторов исследовали с помощью термопрограммированной десорбции (ТПД) аммиака.
Олигомеризация пент-1-ена
Олигомеризацию пент-1-ена осуществляли в непрерывно вращающихся автоклавах при 150–180°С. Массовое содержание цеолитного катализатора в расчете на олефин составляло 10%. После опыта охлажденную жидким азотом реакционную смесь отделяли от катализатора фильтрованием и разделяли на две фракции: “амиленовую” и “олигомерную”. Для этого реакционную массу помещали в 2-горлую колбу, соединенную с приемником, помещенным в низкотемпературную баню (–80°C). В колбу подавали азот для выдувания пентенов, которые собирали в приемнике, а затем анализировали методом газовой хроматографии на приборе Кристаллюкс-4000М (“Мета-Хром”, Россия) с детектором по теплопроводности (насадочная колонка длиной 6 м, фаза – 20% дибутилфталата на диатомитовой глине). Олигомеры анализировали методом газожидкостной хроматографии на хроматографе HRGC 5300 Mega Series (“Carlo Erba”, Италия) с пламенно-ионизационным детектором (стеклянная капиллярная колонка 25 м, фаза – SE-30) и методом высокоэффективной жидкостной хроматографии на приборе LC-20 Prominence (“Shimadzu”, Япония) с полистирольной колонкой “Plgel 500Å” и рефрактометрическим детектором.
Продукты идентифицировали методом хроматомасс-спектрометрии (прибор GCMS-2010 Ultra, “Shimadzu”, Япония), хроматограф которого снабжен 50 м капиллярной кварцевой колонкой DB 560).
Для оценки стабильности образцов отработанные катализаторы использовали повторно без регенерации.
Активность катализаторов оценивали величиной суммарной конверсии пент-1-ена Х:
(1)
${\text{\;}}{{X}_{{{\text{ol}}}}} = \frac{{\left[ {С{{{\left( {{\text{С}}_{5}^{ = }} \right)}}_{0}} - C{{{\left( {{\text{C}}_{5}^{ = }} \right)}}_{{\text{t}}}}} \right]{\text{\;}} \times {\text{\;}}100}}{{С{{{\left( {{\text{С}}_{5}^{ = }} \right)}}_{0}}}},$(2)
${{X}_{{{\text{is}}}}} = \left( {100 - {{X}_{{{\text{ol}}}}}} \right) \times \frac{{C{{{\left( {iso{\text{C}}_{5}^{ = }} \right)}}_{{\text{t}}}}}}{{C{{{\left( {{\text{C}}_{5}^{ = }} \right)}}_{{\text{t}}}}}},$Селективность образования изомеров и продуктов олигомеризации пента-1-ена рассчитывали по следующим формулам:
где Sol – селективность образования олигомеров; Sis – селективность образования изомеров; Ci, Si – концентрация в реакционной массе, мас. %, и селективность образования одной из фракций продуктов олигомеризации (димеры, тримеры, олигомеры n ≥ 4, олигомеры продуктов крекинга); γi – выход продуктов.РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Физико-химические характеристики катализаторов
В табл. 1 приведены физико-химические характеристики исследованных образцов цеолитных катализаторов.
Таблица 1.
Физико-химические характеристики цеолитов H-Y
| № | Образец | αNa | СК | SiO2/ Al2O3 | SiO2/ Al2O3* |
SБЭТ, м2/г |
Vмикро, см3/г |
Vмезо, см3/г |
Vмакро, см3/г |
Vобщий, см3/г |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | H-Y | 0.97 | 96 | 5.0 | 6.2 | 725 | 0.30 | 0.03 | – | 0.33 |
| 2 | Na-Yh | – | 97 | 5.7 | 5.8 | 635 | 0.27 | 0.06 | 0.19 | 0.52 |
| 3 | H-Yh | 0.95 | 93 | 5.7 | 7.3 | 639 | 0.23 | 0.10 | 0.20 | 0.53 |
| 4 | H-USYh | 0.95 | 90 | 5.7 | 10.5 | 536 | 0.19 | 0.14 | 0.18 | 0.51 |
| 5 | H-USYh a.t. | 0.97 | 97 | 11.9 | 13.7 | 638 | 0.20 | 0.18 | 0.20 | 0.58 |
По данным РФА (рис. 1, табл. 1) установлено, что как микропористый, так и иерархический образцы цеолита Y в Na-форме обладают высокой степенью кристалличности (СК): 100% для цеолита Na-Y (в таблице не приведено) и 97% для Na-Yh.
Процесс декатионирования приводит к небольшому снижению кристалличности: СК образца H-Y – 96%, H-Yh – 93%. После деалюминирования образца Н-Yh методом ТПО наблюдается дальнейшее уменьшение СК – до 90% (образец 4, табл. 1). Последующая кислотная обработка ультрастабилизированного цеолита H-USYh позволяет повысить СК до 97% (образец 5, табл. 1).
Деалюминирование образцов должно способствовать увеличению мольного соотношения SiO2/Al2O3. Действительно, величина SiO2/Al2O3, рассчитанная по параметру элементарной ячейки a0, возрастает для образцов H-USYh и H-USYh a.t. В тоже время соотношение SiO2/Al2O3, определенное по данным элементного анализа, для образца H-USYh, полученного с помощью ТПО, остается неизменным (5.7). Это связано с тем, что выходящий при ТПО из каркаса цеолита алюминий переходит во внерешеточное состояние [9], поэтому найденная по результатам элементного анализа степень деалюминирования меньше действительных значений. Более точными являются значения, полученные по данным РФА, поскольку изменение параметра кристаллической решетки чувствительно только к изменению отношения каркасных атомов в решетке цеолита. После обработки образца H-USYh раствором лимонной кислоты (H-USYh a.t.) соотношение SiO2/Al2O3, определенное по данным химического анализа увеличивается до 13.1, а по параметру элементарной ячейки – до 13.7. Это свидетельствует о том, что раствор кислоты позволяет очистить поверхность образца H-USYh a.t. от внекаркасных отложений алюминия, и согласуется с наблюдаемым ранее (рис. 1) ростом степени кристалличности для данного образца.
На основании значений SiO2/${\text{A}}{{{\text{l}}}_{2}}{\text{O}}_{3}^{*}$, найденных по параметру элементарной ячейки (табл. 1), можно заключить, что деалюминирование происходит не только в ходе ТПО и при обработке кислотой, но и при декатинировании образцов в Na-форме. Так, для образца НYh мольное соотношение SiO2/Al2O3 возрастает в 1.3 раза по сравнению с исходным Na-Yh.
Удельная поверхность цеолита H-Yh по данным низкотемпературной адсорбции азота составляет 639 м2/г, объем микропор – 0.23 см3/г, мезопор – 0.10 см3/г, макропор – 0.20 см3/г (табл. 1). После ТПО объем микро- и макропор снижается, а объем мезопор возрастает. Известно, что в результате термопаровой обработки в решетке цеолита происходит гидролиз алюминия, который затем может откладываться как в микропорах, так и на внешней поверхности. Некоторые подвижные частицы кремния могут мигрировать и встраиваться в образовавшиеся силанольные гнезда, из-за чего образуются пустоты большего размера, представляющие собой внутрикристаллическую мезопористость [9, 17]. После ТПО рекомендуется очищать поверхность цеолитов от внекаркасных отложений кислотой, что позволяет улучшить характеристики пористости образца и обеспечить хороший доступ к активным центрам [18]. Действительно, обработка H-USYh раствором лимонной кислоты увеличивает объем мезопор образца H-USYh a.t. на 29%.
Влияние обработок на морфологию и размер кристаллов изучали методом СЭМ. Кристаллы порошкообразного цеолита Н-Y имеют кубическую форму, их средний размер составляет около 1 мкм (рис. 2а). В образце цеолита H-Yh видны агломераты кристаллов и их сростки различной формы (рис. 2б). Средний размер кристаллов равен 1 мкм, присутствуют как более крупные кристаллы размером до 2 мкм, так и нанокристаллы размером от 15 до 100 нм.
ТПО приводит к сглаживанию граней кристаллов цеолита (рис. 2в). Кроме того, на внешней поверхности кристаллов появляются поры диаметром 5–20 нм. После комбинированной обработки (ТПО, затем кислота) грани кристаллов становятся еще более “размытыми”, наблюдается заметное увеличение количества мезопор на гранях кристаллов (рис. 2г).
На профилях ТПД NH3 цеолитов наблюдаются два пика: низкотемпературный с максимумом в области 100–350°С, соответствующий слабым кислотным центрам, и высокотемпературный с максимумом в интервале выше 350°С, относящийся к сильным кислотным центрам. По данным ТПД аммиака (табл. 2) иерархический цеолит H-Yh обладает меньшим количеством кислотных центров, чем микропористый H-Y. Поскольку в цеолитах число кислотных центров связано с содержанием алюминия в кристаллической структуре, то деалюминирование закономерно приводит к уменьшению их концентрации. После термопаровой обработки суммарное количество кислотных центров существенно падает – почти вдвое, а количество сильных кислотных центров уменьшается в 2.2 раза. Дальнейшее деалюминирование лимонной кислотой незначительно влияет на концентрацию кислотных центров.
Олигомеризация пент-1-ена в присутствии цеолитов Y. Олигомеризация пент-1-ена
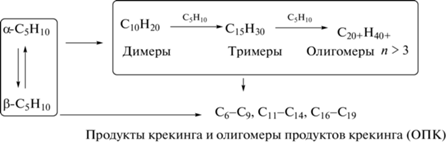
Установлено, что олигомеризация на цеолитных катализаторах протекает с образованием димеров (C10H20), тримеров (C15H30) и некоторого количества олигомеров со степенью олигомеризации n = 4–6. Помимо превращения в олигомеры, пент-1-ен (α-C5H10) на кислотных центрах цеолита изомеризуется в цис- и транс-пент-2-ен (β-C5H10). Скелетная изомеризация в изученных условиях почти не наблюдается. При температуре выше 150°C олигомеры пентена подвергаются деструкции с последующей олигомеризацией образующихся продуктов крекинга.
Схема 1 . Олигомеризация пент-1-ена на цеолитах.
Сравнение каталитических свойств микропористого и иерархического цеолитов Y в олигомеризации пент-1-ена (рис. 3) свидетельствует о более высокой эффективности последнего. Благодаря присутствию мезо- и макропор обеспечивается хорошая доступность кислотных центров для реагирующих молекул, поэтому активность цеолитного катализатора H-Yh в олигомеризации выше, несмотря на меньшее по сравнению с цеолитом H-Y количество кислотных центров. В изученных условиях конверсия пент-1-ена полная, суммарный выход олигомеров составляет 94%, выход изомеров в продуктах незначительный – 6%. На образце H-Yh наблюдается повышенный выход димеров и олигомеров с n ≥ 3–62 и 30% соответственно, тогда как на цеолите H-Y – 52 и 25%.
Рис. 3.
Конверсия пент-1-ена и селективность образования продуктов реакции на микропористом цеолите H-Y и иерархических образцах H-Yh, H-USYh, H-USYh a.t. Условия реакции: 150oС, 10 мас. % катализатора, 5 ч.
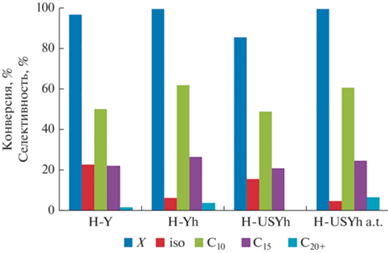
Образец H-USYh по активности в олигомеризации пент-1-ена заметно уступает исходному образцу H-Yh (рис. 3), что связано, по-видимому, с понижением концентрации кислотных центров после ультрастабилизации и негативным влиянием внекаркасных частиц алюминия, блокирующих кислотные центры [19]. Конверсия пент-1-ена и суммарный выход олигомеров на H-USYh ниже, чем на цеолите H-Yh, в составе олигомеров присутствуют только димеры и тримеры, а более высокомолекулярные соединения отсутствуют.
Последующая обработка ультрастабилизированного образца лимонной кислотой (образец H‑USYh a.t.) способствует возрастанию его активности в олигомеризации пент-1-ена. Конверсия мономера на образце H-USYh a.t. практически полная, выход олигомеров близок к полученному на исходном образце H-Yh. В составе олигомеров появляются тетрамеры, причем выход их в 3.5 раза больше, чем на образце H-USYh. Повышенная активность образца H-USYh a.t. и достигаемое на нем более широкое молекулярно-массовое распределение олигомеров пентена, являются, по-видимому, результатом увеличения объема мезопор, приводящего к снижению диффузионных ограничений при перемещении молекул мономеров и олигомеров.
Исследование стабильности действия микропористого и иерархических образцов цеолита Y в олигомеризации пент-1-ена показало (рис. 4), что на иерархических цеолитах H-Yh и H-USYh a.t. конверсия пент-1-ена практически не изменяется после пяти циклов олигомеризации, в то время как на микропористом цеолите H-Y снижение этого показателя начинается уже во 2-м цикле.
Рис. 4.
Сравнение стабильности действия образцов H-Y, H-Yh, H-USYh a.t. в олигомеризации пент-1-ена. Условия реакции: 180°C, 10 мас. % катализатора, 5 ч.

Состав продуктов после каждого цикла реакции олигомеризации без регенерации катализаторов приведен в табл. 3.
Таблица 3.
Выход продуктов олигомеризации пент-1-ена, полученных на образцах H-Y, H-Yh, H-USYh a.t., в пяти циклах олигомеризации
| Цикл | Выход продуктов, % | ||||
|---|---|---|---|---|---|
| i-С5 | C10 | C15 | C20+ | ОПК | |
| H-Y | |||||
| 1 | 3 | 53 | 30 | 10 | 4 |
| 2 | 12 | 60 | 18 | 5 | 3 |
| 3 | 22 | 54 | 13 | 3 | 1 |
| 4 | 27 | 45 | 5 | 0 | 0 |
| 5 | 32 | 35 | 2 | 0 | 0 |
| H-Yh | |||||
| 1 | 1 | 42 | 30 | 17 | 10 |
| 2 | 19 | 48 | 19 | 8 | 6 |
| 3 | 28 | 56 | 9 | 2 | 1 |
| 4 | 30 | 57 | 8 | 1 | 1 |
| 5 | 43 | 42 | 6 | 0 | 0 |
| H-USYh a.t. | |||||
| 1 | 0 | 45 | 31 | 15 | 9 |
| 2 | 4 | 61 | 27 | 7 | 1 |
| 3 | 11 | 64 | 17 | 4 | 1 |
| 4 | 19 | 63 | 11 | 2 | 1 |
| 5 | 29 | 53 | 7 | 1 | 0 |
Дезактивация катализаторов приводит к тому, что в каждом последующем цикле суммарный выход олигомеров пентена сокращается, а выход изомеров пентена растет. Заметно снижается вклад реакции крекинга, поскольку после 3–4 цикла количество ОПК становится минимальным. На микропористом цеолите H-Y уменьшение выхода олигомеров происходит быстрее, чем на иерархических образцах H-Yh и H-USYh a.t. В составе олигомеров повышается доля димеров, а доля тримеров и олигомеров C20+ падает.
ЗАКЛЮЧЕНИЕ
В результате изучения активности, селективности и стабильности образцов цеолита FAU (Y), отличающихся текстурой, химсоставом, кислотными свойствами (микропористый цеолит H-Y, иерархические цеолиты H-Yh и H-USYh a.t.), в олигомеризации пент-1-ена, установлено:
– в изученных условиях (150°С, 10 мас. % катализатора) на всех исследованных образцах цеолитов олигомеризация идет с образованием изомеров пент-1-ена, олигомеров пентена с числом мономерных звеньев n = 2–6, олигомеров продуктов крекинга (ОПК);
– выход олигомеров пентена максимален (93%) на цеолитном катализаторе H-USYh a.t., синтезированном деалюминированием цеолита H-Yh с помощью ТПО и обработки лимонной кислотой, который имеет самый высокий среди изученных образцов объем мезопор. Увеличение мезопористости приводит к получению на указанном образце олигомеров пентена со степенью олигомеризации n = 3–6 в большем количестве по сравнению с другими образцами.
Образец H-USYh a.t. близок по активности и селективности цеолиту H-Yh: конверсия пентена – 100%, выход олигомеров – 93%. Ультрастабилизированный цеолит H-USYh по этим показателям уступает как исходному цеолиту H-Yh, так и образцу H-USYh a.t.;
– наиболее высокую стабильность в олигомеризации пент-1-ена (при 180°С, 10 мас. % катализатора) продемонстрировал образец H-USYh a.t., на котором конверсия мономера не изменялась в течение 5 циклов работы без регенерации катализатора. Микропористый цеолит H-Y терял активность уже после 2-ого цикла. Выход олигомеров пентена на цеолите H-USYh a.t. после 5 циклов снижался на 39%, на микропористом цеолите H-Y – на 57%.
Список литературы
Cejka J., Corma A., Zones S. Zeolites and catalysis: synthesis, reactions and applications. Weinheim: Wiley-VCH. 2010. 918 p.
Kerstens D., Smeyers B., Van Waeyenberg J., Qiang Zhang Q., Yu J., Sels B.S. // Adv. Mater. 2020. V. 32. № 44. 2004690.
Chen L.-H., Sun M.-H., Wang Zh., Yang W., Xie Z., Su B.-L. // Chem. Rev. 2020. V. 120. V. 20. P. 11194.
Corma A., Martínez C., Doskocil E. // J. Catal. 2013. V. 300. P. 183.
Zhang L., Ke M., Song Z., Liu Ya., Shan W., Wang Q., Xia Ch., Li Ch., He Ch. // Catalysts. 2018. V. 8. № 8. P. 298.
Moon S., Chae H.J., Park M.B. // Appl. Catal. A: Gen. 2018. V. 553. P. 15.
Monama W., Mohiuddin E., Thangaraj B., Mdleleni M.M., Key D. // Catal. Today. 2020. V. 342. P. 167.
Chal R., Gérardin C., Bulut M., van Donk S. // Chem. Cat. Chem. 2011. V. 3. P. 67.
Wei Y., Parmentier T.E., de Jong P.K., Zečević J. // Chem. Soc. Rev. 2015. V. 44. P. 7234
Feliczak-Guzik A. // Micropor. Mesopor. Mater. 2017. V. 259. P. 33.
Jia X., Khan W., Wu Z., Choi J., Yip A.C.K. // Adv. Powder Technol. 2019. V. 30. P. 467.
Пaтeнт PФ №2456238, 2012.
Пaтeнт PФ №2739350, 2020.
Kutepov B.I., Travkina O.S., Agliullin M.R., Khazipova A.N., Pavlova I.N., Bubennov S.V., Kostyleva S.A., Grigor’eva N.G. // Petrol. Chem. 2019. V. 59. P. 297.
Travkina O.S., Agliullin M.R., Filippova N.A., Khazipova A.N., Danilova I.G., Grigor’eva N.G., Narender N., Pavlov M.L., Kutepov B.I. // RSC Adv. 2017. V. 7. P. 32581.
Брек Д. Цеолитовые молекулярные сита. Москва: Мир. 1976. 788 с. (Breck D.W. Zeolite Molecular Sieves: Structure, Chemistry, and Use. New York: John Wiley and Sons. 1973. 771 р.)
Silaghi M.-Ch., Chizallet C., Raybaud P. // Micropor. Mesopor. Mater. 2014. V. 191. P. 82.
van Donk S., Broersma A., Gijzeman O.L.J., van Bokhoven J.A., Bitter J.H., de Jong K.P. // J. Catal. 2001. V. 204. P. 272.
Verboekend D., Chabaneix A.M., Thomas K., Gilson J.-P., Pérez-Ramírez J. // CrystEngComm. 2011. V. 13. P. 3408.
Дополнительные материалы отсутствуют.
Инструменты
Кинетика и катализ