Коллоидный журнал, 2020, T. 82, № 5, стр. 594-603
Изотермы сжатия пленок полидофамина
О. Ю. Миляева 1, *, А. В. Акентьев 1, А. Г. Быков 1, А. В. Зеров 1, Н. А. Исаков 1, Б. А. Носков 1, **
1 Санкт-Петербургский государственный университет, кафедра коллоидной химии
198504 Санкт-Петербург, Университетский просп., 26, Россия
* E-mail: o.milyaeva@spbu.ru
** E-mail: borisanno@mail.ru
Поступила в редакцию 06.05.2020
После доработки 10.05.2020
Принята к публикации 12.05.2020
Аннотация
Образование полидофамина в результате полимеризации гидрохлорида дофамина (ГДА) в слабощелочной среде (pH 8.5) происходит как в объеме раствора, так и на границе жидкость–газ. При этом в качестве окислителя выступает кислород воздуха и кислород, растворенный в объеме раствора. В работе определялись изотермы сжатия пленок полидофамина, образовавшихся на межфазной границе за различное время и при разной начальной концентрации ГДА. Исходная концентрация ГДА влияет на скорость формирования пленки полидофамина, но слабо влияет на ее структуру. При низкой концентрации ГДА (1 г/л) и большом времени жизни поверхности (720 мин) изотермы сжатия и зависимости статической поверхностной упругости от поверхностного давления оказываются близкими к соответствующим зависимостям для пленок полидофамина, образовавшимся при относительно высокой концентрации ГДА (5 г/л) и меньшем времени жизни поверхности (240 мин). Зависимости статической поверхностной упругости от поверхностного давления в отличие от соответствующих зависимостей динамической поверхностной упругости оказываются немонотонными. В первом случае достигаются значительно более высокие значения поверхностного давления, однако в области низких поверхностных давлений (<7 мН/м) полученные результаты близки. Максимальная статическая поверхностная упругость равна 150 мН/м для сплошных однородных пленок полидофамина. Такие пленки при дальнейшем сжатии начинают разрушаться с образованием трехмерной полислойной структуры.
ВВЕДЕНИЕ
Полимеризация гидрохлорида дофамина (ГДА) на межфазной границе во многом аналогична процессам, происходящим в некоторых живых организмах [1–3]. Так, беспозвоночные мидии способны прочно прикрепляться практически к любым поверхностям за счет полимеризации 3,4-дигидрокси-L-фенилаланина (DOPA) и агрегатов белков с высоким содержанием лизина. Эти наблюдения послужили толчком для создания и изучения свойств новых полимерных адгезивов на основе мономеров, близких по структуре к DOPA, прежде всего, полидофамина [4, 5]. Высокая адгезионная способность полидофамина позволяет получить на его основе широкий набор различных покрытий, изменяя поверхностные функциональные группы [6]. Формирование тонких микро- и наноструктурированных пленок на основе подобных материалов открывает новые возможности при создании биосовместимых мембран и их применения в качестве носителей для биосенсоров и биокатализаторов [6–11]. В то же время образование таких пленок непосредственно на твердых подложках не всегда позволяет получить материалы с хорошо контролируемыми свойствами из-за несоответствия размеров элементарных ячеек кристаллической решетки подложки и мономера или из-за высокой шероховатости поверхности [12, 13].
Полимеризация на границе жидкость–газ представляет одно из наиболее многообещающих направлений получения тонких пленок с высокой адгезивной способностью [13]. Значительная подвижность молекул на поверхности жидкости способствует устранению дефектов структуры и получению более однородной пленки, часто позволяет проводить синтез в более мягких условиях, решает проблему шероховатости. Однако информация о свойствах пленок полидофамина на поверхности жидкости крайне ограничена [14, 15], что, по-видимому, обусловлено ограниченным набором экспериментальных методов, чувствительных к изменениям конформации полимеров на этой поверхности.
Полимеризация дофамина протекает самопроизвольно в слабощелочной среде за счет окисления кислородом воздуха и растворенным кислородом [16]. При этом на поверхности раствора формируется пленка полидофамина, а его частицы различного размера образуются в объеме раствора [15, 17, 18]. На процесс полимеризации влияют такие факторы как pH и ионная сила раствора, исходная концентрация ГДА, концентрация кислорода в растворе [19–22].
Недавно было показано, что методы дилатационной поверхностной реологии совместно с эллипсометрией и микроскопией под углом Брюстера позволяют получить новую информацию о процессе формирования и структуре пленки полидофамина на поверхности воды [15]. Анализ кинетических зависимостей поверхностных свойств позволил предложить следующий механизм формирования пленки: сначала образуются первичные домены полидофамина, их взаимодействие в поверхностном слое приводит к росту поверхностной упругости и поверхностного давления. При начальной концентрации ГДА 2 г/л и выше эти домены объединяются по мере старения поверхности, образуя сплошную пленку. После образования однородной пленки ее толщина растет, достигая 80 нм при концентрации ГДА 2 г/л и времени жизни поверхности около 5 ч.
В классической химии поверхностных явлений изотермы поверхностного давления используются в качестве основной характеристики нерастворимых монослоев поверхностно-активных веществ [23, 24]. Анализ таких изотерм позволяет также получить новую информацию о нанесенных пленках нано- и микрочастиц на водной поверхности [25–27]. В данной работе этот подход применяется к пленкам полидофамина в процессе их формирования. В этом случае оказывается, что свойства пленки определяются в первую очередь химической реакцией на межфазной границе, а не процессом адсорбции или распределением нанесенного вещества вдоль поверхности. Анализ полученных изотерм поверхностного давления совместно с результатами атомно-силовой микроскопии (АСМ) и микроскопии под углом Брюстера позволяет определить основные этапы формирования пленки полидофамина и найти зависимость ее свойств и морфологии от степени сжатия.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Динамическую упругость пленок полидофамина определяли методом осциллирующего кольца спустя 12 ч с момента образования поверхности. Колебания площади поверхности создавались за счет колебаний стеклянного кольца, частично погруженного в раствор, вдоль его оси, перпендикулярной поверхности жидкости. Периодическое изменение площади мениска у внутренней поверхности кольца приводит к соответствующим колебаниям поверхностного натяжения. Амплитуда и частота осцилляций площади поверхности составляли 7% и 0.1 Гц соответственно. В случае малой амплитуды колебаний комплексная динамическая дилатационная поверхностная упругость E определяется соотношением
(1)
$E{\text{(}}\omega {\text{)}} = {{E}_{{{\text{re}}}}}{\text{ + }}i{{E}_{{{\text{im}}}}} = \frac{{\delta \gamma }}{{\delta \ln A}},$Для определения изотерм поверхностного давления пленок полидофамина был использован прибор ISR (KSV NIMA, Финляндия). Синхронное движение двух барьеров вдоль краев ванны Ленгмюра приводит к уменьшению площади поверхности жидкости между барьерами и, следовательно, к уменьшению поверхностного натяжения, измеряемого методом пластинки Вильгельми. Пластинку из фильтровальной бумаги шириной 1 см располагали в центре ванны параллельно барьерам. Все измерения проводили при постоянной скорости сжатия. Бóльшая часть экспериментов была проведена при скорости сжатия 50 мм/мин. Для оценки влияния скорости сжатия были проведены также измерения при ее значениях 20 и 5 мм/мин.
Статическую поверхностную упругость εst оценивали численным дифференцированием полученных изотерм сжатия.
Для определения мезоскопической морфологии пленок полидофамина была применена микроскопия под углом Брюстера (прибор BAM 1, Nanofilm Technology, Германия).
Микроскопическую морфологию исследовали с помощью АСМ. Пленки полидофамина, соответствующие различным степеням сжатия, переносили на поверхность слюды по методу Ленгмюра–Шеффера. После переноса образцы высушивали в течение двух дней в эксикаторе при комнатной температуре и далее исследовали с помощью атомно-силового микроскопа Ntegra Prima (Nte-MDT, Россия). Измерения осуществляли в полуконтактном режиме.
ГДА чистотой 98% (Sigma-Aldrich, Германия) был использован без дополнительной очистки. Растворы ГДА готовили в Тризма-буфере (Sigma Aldrich) с ионной силой 0.01 M и pH 8.5. Для приготовления растворов использовали трижды дистиллированную воду. Поверхностное натяжение буферного раствора совпадало с поверхностным натяжением чистой воды (72.8 мН/м). Все измерения проводили при температуре 20 ± 1°C.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Микро- и макроморфология пленок, соответствующих различным областям изотермы сжатия, определялась с помощью АСМ и микроскопии под углом Брюстера. На рис. 1 и 2 представлены результаты для пленки, полученной из раствора ГДА с концентрацией 1 г/л при времени жизни поверхности 12 ч.
Рис. 1.
АСМ-изображения пленок полидофамина, сжатых до различных значений поверхностного давления и перенесенных на поверхность слюды. Пленки формировались из раствора ГДА с концентрацией 1 г/л в течение 12 ч.

Рис. 2.
Изображения пленки полидофамина, полученные с помощью микроскопии под углом Брюстера при ее сжатии. Пленка формировалась из раствора ГДА с концентрацией 1 г/л в течение 12 ч.

На изображениях, полученных с помощью АСМ для пленок полидофамина, сформированных без дополнительного сжатия, видна небольшая шероховатость, когда различия в высоте различных участков пленки не превышают нескольких нанометров (рис. 1а, 1б). При уменьшении площади до 65% от первоначальной, что соответствует началу роста поверхностного давления, пленка становится более плотной и появляются более гладкие участки (рис. 1в, 1г). При этом средняя толщина пленки не изменяется. Дальнейшее увеличение поверхностного давления до 45 мН/м приводит к появлению складок в пленке (рис. 1д, 1е). Поверхностному давлению 55 мН/м соответствует частично разрушенная пленка, на поверхности которой видны отдельные агрегаты полидофамина (рис. 1ж, 1з).
На изображениях, полученных с помощью микроскопии под углом Брюстера, видно, что при уменьшении площади поверхности до 90% от первоначального значения макроморфология пленки почти не изменяется (рис. 2). Такой пленке соответствует значения поверхностного давления, близкие к нулю. Когда площадь поверхности уменьшается до 75%, на изображениях появляются складки, свидетельствующие о начале разрушения однородной пленки. При дальнейшем сжатии морфология пленки становится более сложной, появляются полосы, соответствующие ее локальным изгибам и утолщениям. Сжатие до 10% от первоначальной площади приводит к образованию более сложной трехмерной полислойной структуры.
Изотермы поверхностного давления определяли для пленок полидофамина, формировавшихся в течение от 10 мин до 12 ч, при концентрации исходного ГДА в диапазоне 1–5 г/л. Для каждого образца выполнялось три цикла растяжения–сжатия. Однако уже после первого цикла начиналось необратимое разрушение пленки. Полученные пленки можно условно разделить на две группы. При относительно малых концентрациях ГДА и/или временах жизни поверхности (концентрации 1 и 2 г/л при временах жизни поверхности 60, 120, 240 мин и концентрация 5 г/л при временах жизни поверхности 10 и 30 мин) полидофамин в поверхностном слое находится в виде отдельных доменов [15]. С увеличением концентрации ГДА и времени жизни поверхности (концентрации 1 и 2 г/л при времени жизни поверхности 720 мин и 5 г/л при временах жизни поверхности > 120 мин) формируются сплошные пленки, видимые невооруженным глазом.
На рис. 3а представлены изотермы поверхностного давления для растворов ГДА с концентрацией 1 г/л, полученные спустя 10, 30, 60, 240 и 720 мин после образования поверхности (первый цикл сжатия). С увеличением времени жизни поверхности от 10 до 240 мин поверхностное давление при почти девятикратном сжатии растет от 2 до 60 мН/м. При времени жизни поверхности 720 мин заметный рост поверхностного давления наблюдается уже при сжатии на 15–20%. При этом на изотерме сжатия наблюдаются две области почти постоянного поверхностного давления, равного примерно 45 и 55 мН/м (области плато).
Рис. 3.
Изотермы сжатия пленок полидофамина при временах жизни поверхности 10 (1), 30 (2), 60 (3), 120 (4), 240 (5), 720 мин (6). Исходная концентрация раствора ГДА 1 (а), 2 (б) и 5 г/л (в).
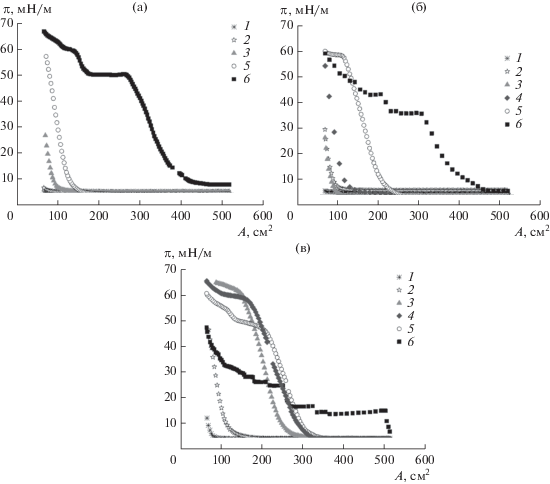
В случае более высоких концентраций ГДА области плато возникают при меньших временах жизни поверхности (рис. 3б и 3в). Для концентрации 5 г/л и времени жизни поверхности 240 мин области плато также наблюдались при значениях поверхностного давления около 45 и 55 мН/м (рис. 3в). Некоторое подобие изотерм сжатия, полученных при низких концентрациях ГДА и больших временах жизни поверхности, и изотерм для высоких концентраций ГДА и средних времен жизни поверхности, может быть связано с ростом скорости полимеризации при увеличении исходной концентрации ГДА. При этом структура пленки, по-видимому, почти не изменяется с ростом концентрации ГДА. Отметим, что изотерма сжатия сплошной пленки полидофамина, сформированной в течение 720 мин на поверхности раствора с исходной концентрацией ГДА 5 г/л, заметно отличается от других изотерм для сплошных пленок полидофамина. В этом случае рост поверхностного давления начинается практически сразу после начала сжатия. При этом максимальные достигаемые значения поверхностного давления меньше, чем для других сплошных пленок полидофамина. Можно предположить, что в этом случае разрушение пленки начинается при меньших значениях поверхностного давления.
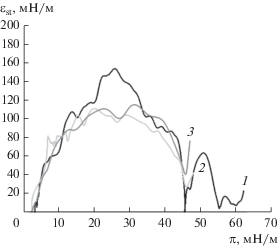
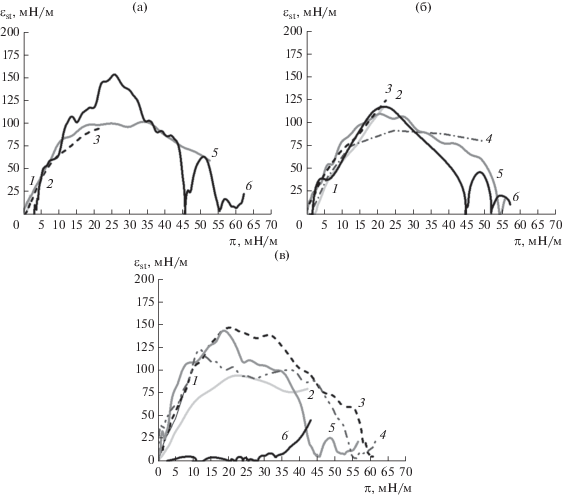
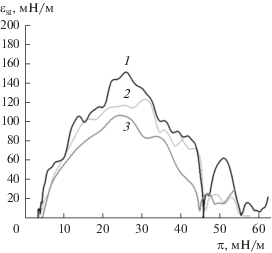
Если представить полученные результаты в виде зависимости статической упругости εst от поверхностного давления (рис. 4), то значениям поверхностного давления 45 и 55 мН/м отвечают минимальные значения упругости. Максимальная упругость, равная 130–150 мН/м, достигается при значениях поверхностного давления около 25 мН/м. При измерении кинетических зависимостей динамической поверхностной упругости методом осциллирующего кольца, когда колебания поверхности происходили в течение всего процесса формирования пленок полидофамина, такие высокие значения модуля динамической поверхностной упругости |E| не достигались [15].
Рис. 4.
Статическая упругость пленок полидофамина при временах жизни поверхности 10 (1), 30 (2), 60 (3), 120 (4), 240 (5), 720 мин (6). Исходная концентрация раствора ГДА 1 (а), 2 (б) и 5 г/л (в).
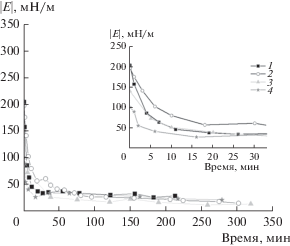
Динамическая поверхностная упругость приближается к максимальным значениям статической упругости, только если измерения методом осциллирующего кольца начинаются после примерно 10 ч формирования пленки в статических условиях (рис. 5). Пленки полидофамина на водной поверхности, сформированные в течение 12 ч, видны невооруженным глазом и не имеют заметных дефектов до начала деформации. Последующее измерение динамической поверхностной упругости приводило к значениям в диапазоне 130–200 мН/м (рис. 5). При этом поверхностное давление составляло 20–25 мН/м. Затем поверхностная упругость быстро уменьшалась до примерно 10 мН/м в течение примерно 15 мин из-за разрушения пленки. Эти результаты указывают на различия в структуре пленок, сформированных в статических и динамических условиях, и на неустойчивость пленки в первом случае к механическим возмущениям.
Рис. 5.
Зависимости динамической упругости пленок полидофамина, формировавшихся в течение 12 ч, от времени от начала колебаний площади поверхности. Начальная концентрация ГДА 1 (1), 1.5 (2), 2 (3), 5 г/л (4).
Динамическая поверхностная упругость и динамическое поверхностное натяжение сильно зависят от начальной концентрации ГДА. В области малых концентраций ГДА (≤0.5 г/л) значения динамической поверхностной упругости и динамического поверхностного натяжения близки к соответствующим значениям для воды (рис. 6 и 7). В то же время микроскопия под углом Брюстера и эллипсометрия указывают на небольшие отклонения оптических свойств от результатов для чистой воды [15]. По-видимому, это вызвано формированием на поверхности отдельных доменов полидофамина уже при низких концентрациях ГДА. Они не образуют сплошной пленки и не приводят к заметным изменениям динамической поверхностной упругости и поверхностного натяжения. Можно предположить, что начальные участки изотерм сжатия (рис. 4), когда поверхностное давление и статическая упругость близки к нулю, отвечают такому же состоянию поверхностного слоя.
Рис. 6.
Кинетические зависимости динамической поверхностной упругости пленок полидофамина, полученные методом осциллирующего кольца при значениях начальной концентрации ГДА 0.5 (1), 0.75 (2), 1 (3), 1.5 (4), 2 (5), 5 г/л (6).
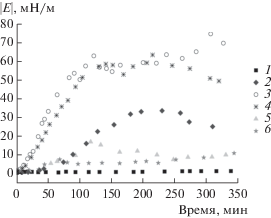
Рис. 7.
Зависимости динамической упругости от поверхностного давления для пленок полидофамина, полученные методом осциллирующего кольца, при значениях начальной концентрации ГДА 0.5 (1), 0.75 (2), 1 (3), 1.5 (4), 2 (5), 5 г/л (6).
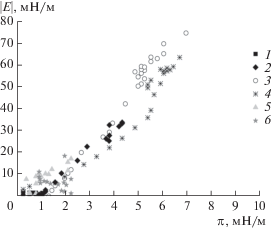
В области средних концентраций ГДА (0.75–1.5 г/л) динамическая поверхностная упругость заметно возрастает (рис. 6 и 7), в то время как эффективное динамическое поверхностное натяжение уменьшается. Увеличение исходной концентрации ГДА до 1 г/л приводит к увеличению динамической поверхностной упругости до 60 мН/м спустя 1 ч после начала формирования пленки (рис. 6). Эта величина сопоставима со значениями упругости адсорбционных слоев глобулярных белков или монослоев мягких наночастиц [26], что указывает на сильное взаимодействие между доменами полидофамина в поверхностном слое. Если представить динамическую поверхностную упругость, измеренную методом осциллирующего кольца в процессе формирования пленки полидофамина, как функцию поверхностного давления (рис. 7), то все зависимости оказываются близкими к результатам, представленным на рис. 4, в области малых значений π – от 0 до 7 мН/м. Близость зависимостей статической и динамической поверхностной упругости в этой области показывает, что пленки полидофамина при малых начальных концентрациях ГДА и малых временах жизни поверхности также представляют собой отдельные домены и рост статической поверхностной упругости обусловлен их взаимодействием.
В то же время сравнение статической и динамической упругости позволяет обнаружить два важных различия. Во-первых, при сжатии пленок полидофамина достигаются более высокие значения поверхностного давления. Статическая поверхностная упругость, соответствующая этим давлениям (рис. 4), оказывается много выше максимально достижимых значений динамической поверхностной упругости (рис. 6 и 7). Во-вторых, при π > 7 мН/м статическая поверхностная упругость имеет один или несколько экстремумов. Рост поверхностного давления до 25 мН/м приводит к росту статической поверхностной упругости до 150 мН/м. При дальнейшем увеличении поверхностного давления εst уменьшается и при π = = 45 мН/м приближается к 0, затем снова начинает расти, проходит через максимум при π = = 50 мН/м и опять снижается до 0 при π = 55 мН/м (рис. 4).
Для изотерм сжатия, полученных для растворов ГДА с концентрацией 1 г/л (рис. 3а) и 2 г/л (рис. 3б) при временах жизни поверхности 60, 120, 240 мин и для растворов ГДА с концентрацией 5 г/л (рис. 3в) при временах жизни поверхности 10 и 30 мин, достигается высокое поверхностное давление, вплоть до 50 мН/м, однако отсутствуют области плато, характерные для сплошных пленок полидофамина. В результате число экстремумов статической упругости уменьшается. Близость статической (рис. 4) и динамической (рис. 6 и 7) поверхностной упругости в области значений π до 7 мН/м и дальнейший рост εst с увеличением π связаны с тем, что пленка полидофамина состоит из отдельных доменов и ее сжатие приводит к сильному взаимодействию между доменами. Значения статической поверхностной упругости в области максимума (100–120 мН/м) оказываются меньше значений, регистрируемых при больших концентрациях ГДА и временах жизни поверхности, когда можно ожидать образования однородной сплошной пленки полидофамина. Высокие значения статической упругости (100–120 мН/м) указывают на образовании более плотной пленки. Однако ее сжатие не приводит к образованию однородной пленки и последующему появлению складок, как это происходит для сплошных пленок (рис. 1 и 2). Таким образом, свойства пленок полидофамина, формирующихся при низких концентрациях ГДА и малых временах жизни поверхности, оказываются близкими к свойствам нанесенных монослоев твердых наночастиц [28].
Для пленок второй группы на зависимостях статической поверхностной упругости от поверхностного давления (рис. 4) обнаруживаются несколько экстремумов. Первый максимум статической упругости наблюдается при поверхностном давлении 25 мН/м, как и для пленок первой группы, но оказывается выше (~150 мН/м). Минимумы статической поверхностной упругости соответствуют областям плато на изотермах сжатия и пленкам с различной морфологией (рис. 1 и 2). При сжатии такие пленки последовательно проходят через несколько состояний. Первое из них достигается при поверхностном давлении 25 мН/м и, по-видимому, отвечает предельно плотной упаковке полидофамина в поверхностном слое. Второе соответствует образованию складок при поверхностном давлении 45 мН/м (рис. 1д, 1е). На третьем этапе, при π = 55 мН/м происходит частичное разрушение пленки, на поверхности которой видны отдельные агрегаты полидофамина (рис. 1ж, 1з).
В отличие от εst динамическая упругость сплошных пленок оказывается относительно низкой. Динамическое поверхностное натяжение и динамическая поверхностная упругость достигают в течение двух часов постоянных значений и затем почти не изменяются (рис. 6). При высоких концентрациях ГДА полимеризация протекает быстрее, и пленка дофамина оказывается однородной и хрупкой даже при сравнительно небольших временах жизни поверхности (~30 мин). Так, при концентрации ГДА >2 г/л колебания площади поверхности приводят к разрушению однородной пленки, если время жизни поверхности превышает 1 ч. При сжатии также происходит разрушение пленки, приводящее к появлению полос и изгибов в области первого минимума поверхностной упругости и образованию более сложной структуры при дальнейшем сжатии.
Для оценки влияния скорости сжатия на полученные результаты изотермы поверхностного давления были измерены при трех скоростях сжатия поверхности (5, 20 и 50 мм/мин) для сплошных пленок полидофамина, полученных из растворов ГДА с начальной концентрацией 1 г/л спустя 12 часов с момента образования поверхности. С уменьшением скорости сжатия рост поверхностного давления начинается при бóльших степенях сжатия. Однако если полученные результаты представить в виде зависимости динамической поверхностной упругости от поверхностного давления (рис. 8), то они оказываются близкими.
Рис. 8.
Статическая упругость пленок полидофамина, полученных из раствора ГДА с концентрацией 1 г/л, через 12 ч после образования поверхности при значениях скорости сжатия 50 (1), 20 (2), 5 мм/мин (3).
Для оценки влияния возможного неоднородного распределения поверхностного давления в длинной ванне Ленгмюра (690 мм) на изотермы поверхностного давления были проведены измерения при различных значениях начальной площади, доступной для формирования пленки (рис. 9). При этом длина части ванны Ленгмюра между барьерами составляла 690, 490 и 290 мм; начальная концентрация ГДА и время жизни поверхности составляли 1 г/л и 12 ч соответственно. Во всех случаях зависимости статической упругости от поверхностного давления были близкими и максимум поверхностной упругости достигался при поверхностном давлении 25 мН/м.
ВЫВОДЫ
Сжатие пленок полидофамина приводит к более высоким значениям поверхностного давления и статической поверхностной упругости, чем те, что регистрируются для пленок, образующихся на поверхности раствора ГДА при постоянной площади поверхности.
Изотермы сжатия и зависимости статической поверхностной упругости от поверхностного давления можно разделить на две группы в зависимости от времени жизни поверхности и начальной концентрации ГДА. При малых концентрациях ГДА и малых временах жизни поверхности (концентрации 1 и 2 г/л при временах жизни поверхности 60, 120, 240 мин и концентрация 5 г/л при временах жизни поверхности 10 и 30 мин) пленки полидофамина состоят из отдельных несвязанных доменов. При дальнейшем сжатии домены взаимодействуют друг с другом и, по-видимому, образуют плотную, но не сплошную пленку. В этом случае поверхностная упругость достигает 100–120 мН/м при поверхностном давлении 25 мН/м. Такому же поверхностному давлению соответствует максимум статической упругости сплошных пленок дофамина, но при этом упругость оказывается выше – около 150 мН/м, что связано с достижением наиболее плотной упаковки молекул полимера в поверхностном слое. На изотермах сжатия пленок полидофамина при большой начальной концентрации ГДА (5 г/л) или больших временах жизни поверхности (>12 ч), относящихся ко второй группе, возникают области почти постоянного поверхностного давления (45 и 55 мН/м). Результаты микроскопии под углом Брюстера и атомно-силовой микроскопии показывают, что эти области характеризуются различной макроскопической и микроскопической морфологией пленок, что связано с последовательным разрушением пленки: образованием изгибов и складок на первом этапе и более сложной полислойной структуры частично разрушенной пленки на втором этапе. Таким образом, анализ изотерм сжатия, сравнение статической и динамической поверхностной упругости, а также результаты микроскопии под углом Брюстера и АСМ позволяют установить основные стадии разрушения пленки полидофамина на границе жидкость–газ при механической деформации.
Список литературы
Lynge M.E., van der Westen R., Postma A., Städler B. // Nanoscale. 2011. V. 3. P. 4916.
Ryu J.H., Messersmith P.B., Lee H. // ACS Appl. Mater. Interfaces. 2018. V. 10. P. 7523.
Ball V. // Front. Bioeng. Biotechnol. 2018. V. 6. P. 109.
Wei Q., Zhang F., Li J., Li B., Zhao C. // Polym. Chem. 2010. V. 1. P. 1430.
Cui J., Iturri J., Paez J., Shafiq Z., Serrano C., D’Ischia M., Del Campo A. // Macromol. Chem. Phys. 2014. V. 215. P. 2403.
Yang H., Luo J., Lv Y., Shen P., Xu Z. // J. Memb. Sci. 2015. V. 483. P. 42.
Qu Y., Huang R., Qi W., Su R., He Z. // ACS Appl. Mater. Interfaces. 2015. V. 7. P. 14954.
Long H., Del Frari D., Martin A., Didierjean J., Ball V., Michel M., Ahrach H.I.E. // J. Power Sources. 2016. V. 307. P. 569.
Yang Z., Sun J., Liu X., Su Q., Liu Y., Li Q., Zhang S. // Tetrahedron Lett. 2014. V. 55. P. 3239.
Farnad N., Farhadi K., Voelcker N.H. // Water. Air. Soil Pollut. 2012. V. 223. P. 3535.
Ball V. // Catal. Today. 2018. V. 301. P. 196.
Liu Y., Ai K., Lu L. // Chem. Rev. 2014. V. 114. P. 5057.
Payamyar P., King B.T., Öttinger H.C., Schlüter A.D. // Chem. Commun. 2016. V. 52. P. 18.
Ponzio F., Payamyar P., Schneider A., Winterhalter M., Bour J., Addiego F., Krafft M.P., Hemmerle J., Ball V. // J. Phys. Chem. Lett. 2014. V. 5. P. 3436.
Milyaeva O.Y., Bykov A.G., Campbell R.A., Loglio G., Miller R., Noskov B.A. // Colloids Surf. A. 2019. V. 579. P. 123637.
Dreyer D.R., Miller D.J., Freeman B.D., Paul D.R., Bielawski C.W. // Langmuir. 2012. V. 28. P. 6428.
Yu F., Chen S., Chen Y., Li H., Yang L., Chen Y., Yin Y. // J. Mol. Struct. 2010. V. 982. P. 152.
Ponzio F., Ball V. // Polym Int. 2016. V. 65. P. 1251.
Napolitano A., Ball V., Chen C., Buehler M.J. // Acc. Chem. Res. 2014. V. 47. P. 3541.
Zheng W., Fan H., Wang L., Jin Z. // Langmuir. 2015. V. 31. P. 11 671.
Della Vecchia F.N., Luchini A., Napolitano A., D’Errico G., Vitiello G., Szekely N., D’Ischia M., Paduano L. // Langmuir 2014. V. 30. P. 9811.
Yang H., Xu W., Du Y., Wu J., Xu Z. // RSC Adv. 2014. V. 4. P. 45 415.
Арсланов В.В. // Успехи химии, 2000. V. 69. P. 963.
Gaines G.L.J. Insoluble Monolayers at Liquid–Gas Interfaces. New York: Wiley, 1966.
Валькова Л.А., Глибин А.С., Valli L. // Коллоид. журн. 2008. Т. 70. С. 11.
Noskov B.A., Bykov A.G. // Curr. Opin. Colloid Interface Sci. 2018. V. 37. P. 1.
Noskov B.A., Timoshen K.A., Akentiev A.V., Chirkov N.S., Dubovsky I.M., Lebedev V.T., Lin S.-Y., Loglio G., Miller R., Sedov V.P., Borisenkova A.A. // Langmuir. 2019. V. 35. P. 3773.
Bykov A.G., Loglio G., Miller R., Noskov B.A. // Colloids Surf. A. 2015. V. 485. P. 42.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал