Коллоидный журнал, 2021, T. 83, № 1, стр. 35-50
Криоструктурирование полимерных систем. 54. Гибридные органо-неорганические криогели поливинилового спирта, наполненные образующимся in situ кремнеземом
И. В. Бакеева 1, А. В. Докторова 1, Л. Г. Дамшкалн 2, В. И. Лозинский 2, *
1 Федеральное государственное бюджетное образовательное учреждение высшего образования
"МИРЭА - Российский технологический университет",
Институт тонких химических технологий им. М.В. Ломоносова
119571 Москва, просп. Вернадского, 86, Россия
2 Институт элементоорганических соединений им. А.Н. Несмеянова РАН
119991 Москва, ул. Вавилова, 28, Россия
* E-mail: loz@ineos.ac.ru
Поступила в редакцию 27.07.2020
После доработки 10.08.2020
Принята к публикации 17.08.2020
Аннотация
Макропористые упруговязкие криогели поливинилового спирта (ПВС) образуются в результате криогенной обработки (замораживание/выдерживание в замороженном состоянии/оттаивание) концентрированных растворов этого полимера. Такие материалы представляют значительный научный и прикладной интерес. То же самое относится и к различным комплексным и композиционным криогелям ПВС, содержащим, соответственно, растворимые и нерастворимые (наполнители) добавки. В данной работе получен и исследован новый тип органо-неорганических гибридных криогелей ПВС, содержащих кремнеземные компоненты. Эти гибридные криогели образовывались в результате реакции силиката натрия с соляной кислотой, вводимых в водный раствор ПВС непосредственно перед его криогенной обработкой, т.е. когда трансформация неорганических компонентов происходила одновременно с криотропным гелеобразованием ПВС. Установлено, что физико-механические свойства полученных образцов, их теплостойкость и макропористая морфология зависят от концентрации неорганических добавок и температурных условий криогенного процесса. При этом выявлено существенное влияние образующегося NaCl, а также дополнительно поляризованных водородных связей между OH-группами ПВС и силанольными группами образующихся in situ поли/олигокремниевых кислот на характеристики формирующихся в результате гибридных криогелей.
ВВЕДЕНИЕ
Разнообразные композиционные (наполненные) гидрогели представляют значительный научный и прикладной интерес [1]. Среди этих материалов известны композиты на основе так называемых криогелей поливинилового спирта (ПВС) [2], которые благодаря своим довольно уникальным свойствам привлекают значительное внимание и востребованы в различных областях. В частности, к таковым относятся медицина [2–16], биотехнология [2, 17–26], материаловедение [2, 16, 27–31], технологии охраны окружающей среды [32, 33], строительная инженерия в районах вечной мерзлоты [2, 34–36], технология топлив [37] и др.
Собственно криогели ПВС – это нековалентные (физические) гели, образующиеся при криогенной обработке (замораживание/выдерживание в замороженном состоянии/размораживание) концентрированных растворов данного полимера (см., например, обзоры [2, 3, 6, 38–41]). Ключевой морфологической особенностью всех криогелей ПВС является их макропористость, возникающая в результате образования поликристаллов замерзшего растворителя и последующего их оттаивания. Физико-химические свойства и макропористая структура таких криогелей зависят от множества факторов, к которым относятся молекулярные характеристики используемого полимера, его концентрация в исходном растворе и условия криогенной обработки [2, 3, 6, 27, 38, 42–47].
В свою очередь, наличие различных наполнителей и их концентрация влияют на соотношение свойств и структуры соответствующих уже композитных криогелей ПВС (ККГПВС). Особенно это касается фазового состояния наполнителей, т.е. являются ли они твердыми частицами, мягкими гелеобразными частицами (например, микробными клетками или гранулами другого геля), каплями несмешивающихся жидкостей, пузырьками газа. Соответствующие ККГПВС неоднократно описаны в экспериментальных работах и различных патентах, но, насколько нам известно, информативных научных обзоров, посвященных именно ККГПВС, пока что нет.
В принципе, имеются три пути формирования наполненных криогелей ПВС [48].
1. Суспендирование дисперсного наполнителя в растворе ПВС с последующим замораживанием–оттаиванием этой системы, что приводит к получению целевого ККГПВС.
2. Приготовление исходного раствора, содержащего ПВС вместе с соответствующим растворимым предшественником “будущего” наполнителя, затем добавление агента, способного вызвать образование наполнителя, и далее быстрое замораживание смеси с целью обеспечения условий криотропного гелеобразования ПВС с одновременным формированием дискретной фазы наполнителя.
3. Приготовление исходного раствора, содержащего ПВС и соответствующий растворимый предшественник “будущего” наполнителя, криогенное структурирование такого смешанного раствора с последующей обработкой полученного криогеля агентом, способным диффундировать в пористую матрицу и тем самым вызывать образование дискретной фазы наполнителя внутри непрерывной фазы уже сформированного комплексного криогеля.
Известны публикации, описывающие получение, свойства и примеры использования различных ККГПВС, содержащих наполнители кремнеземного типа (см., например, [49–53]). Подобные органо-неорганические материалы относятся к так называемым гибридным системам [54], состоящим из органических макромолекул и неорганических включений, сохраняющих как свои собственные свойства, так и проявляющих синергетические эффекты, придающие композиту новые характеристики.
Первые два из указанных выше подходов были использованы ранее для получения ККГПВС, наполненных частицами кремнезема различного размера (включая наночастицы) и формы. Понятно, что наиболее простым является вариант 1, т.е. диспергирование наполнителя в растворе ПВС с последующим замораживанием–оттаиванием суспензии. Например, такая схема применялась при формировании образцов для изучения влияния размера пор частиц кремнезема [49] или гидрофильности/гидрофобности наполнителя [50] на физико-механические свойства соответствующих композитов. Этот же подход был реализован при получении композитных микросфер, способных функционировать в качестве систем контролируемого высвобождения лекарственных средств [51].
Вариант 2, т.е. криотропное гелеобразование ПВС параллельно с формированием дискретной фазы наполнителя трансформацией растворенного предшественника в нерастворимые включения, также применялся для создания кремнеземсодержащих ККГПВС. В этом случае алкоксисиланы, например тетраметоксисилан (ТМОС) [52] или метилтриметоксисилан [53], вводили в водный раствор ПВС, смесь быстро замораживали, и гидролитическая поликонденсация алкоксисилана (золь–гель процесс) [55] происходила в основном в замороженной системе одновременно с криотропным гелеобразованием ПВС. Полученные после размораживания композиты оказались значительно более жесткими и термостойкими по сравнению с ненаполненными криогелями при той же концентрации ПВС. В целом считается, что подобные кремнеземсодержащие ККГПВС перспективны для биомедицинского применения, например для получения искусственных хрящей, разработки систем доставки лекарств, создания биосенсоров медицинского назначения [53].
Однако в ходе реакций гидролитической поликонденсации высвобождается соответствующий спирт, токсичный метанол в случае ТМОС, поэтому требуется очень тщательная промывка полученных композитных криогелей, если предполагается их биомедицинское использование. В этой связи наше внимание было обращено на поиск способов получения SiO2-содержащих криогелей ПВС также с использованием золь–гель технологии, но без предшественников, служащих источником опасного спирта. Поиск путей решения этой проблемы и являлся целью данного исследования. Для этого мы использовали такой чрезвычайно простой неорганический предшественник кремнезема, как водно-щелочной раствор силиката натрия (т.е. “жидкое стекло”), индуцируемое подкислением превращение которого в кремнезем должно было происходить одновременно с криотропным гелеобразованием ПВС. Ранее не сообщалось о получении и исследовании подобных гибридных криогелей ПВС с использованием подхода, основанного на проведении криотропного гелеобразования ПВС параллельно с генерацией in situ кремнеземных наполнителей, формирующихся из указанных выше предшественников, т.е. Na2SiO3 + HCl.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали следующие вещества: ПВС с молекулярной массой ≈86 кДа и степенью деацетилирования 100% (Acros Organics, США), силикагель LS-5/40 (Chemapol, Чехословакия), гидроксид натрия марки “ч.” (Lachema, Чехословакия), краситель Конго красный (Aldrich, США), 6 н. соляня кислота (фиксанал), хлорид натрия (“х. ч.”), желатин (марки “фото”), фенол (“ч. д. а.”) и глицерин (“ч. д. а.”) (все – производства Реахим, РФ).
Исходные растворы применявшихся в работе компонентов в деионизированной воде получали следующим образом.
Водные растворы ПВС готовили, как описано ранее [45]. Известное количество сухого полимера суспендировали в необходимом объеме воды. Смесь выдерживали в течение ночи при комнатной температуре для набухания ПВС. Затем суспензию нагревали на кипящей водяной бане при перемешивании до полного растворения ПВС. Образцы взвешивали до и после нагревания, количество выпаренной воды компенсировали. Полученный таким образом раствор (далее обозначается как Isol) фильтровали через полиамидную сетку и термостатировали при 20°C в течение 30 мин перед смешиванием с другими компонентами, когда это требовалось.
Щелочной раствор силиката натрия (IIsol) получали растворением сухого силикагеля в 5 н. водном растворе гидроксида натрия; компоненты смешивали в мольном соотношении NaOH : SiO2 = = 2 : 1.
Формирование ненаполненных и композитных криогелей ПВС, а также кремнеземных препаратов, проводили следующим образом.
Обычные, т.е. ненаполненные криогели ПВС (Inf) получали согласно ранее описанной методике [45, 52]. Для этого раствор ПВС (Isol) с концентрацией 93.6 г/л заливали в формы, замораживали при –20°C в течение 12 ч в камере программируемого ультракриостата FP 45 HP (Julabo, Германия) и затем размораживали, нагревая со скоростью 0.03 град/мин, которая задавалась микропроцессором криостата. Общая продолжительность процессов замораживания–оттаивания – 36 ч.
Для получения ККГПВС, наполненных готовым кремнеземом, частицы сухого силикагеля LS-5/40 диспергировали в растворе полимера (Isol) из расчета 0.06, 0.12, 0.18 либо 0.24 моля SiO2 на 1 осново-моль звеньев полимера (1 моль OH-групп), суспензии заливали в формы и подвергали криогенной обработке. Сформированные таким способом композитные криогели далее обозначаются как I + LS.
При синтезе дисперсного кремнезема щелочной раствор Na2SiO3 (т.е. IIsol) и 6 н. раствор HCl быстро смешивали (при эквимолярном соотношении Na+-ионов и HCl) и сразу помещали в камеру криостата для замораживания–оттаивания в тех же условиях, что и при формировании криогелей, либо инкубировали при комнатной температуре в течение аналогичного времени. Ниже дисперсия кремнезема, полученная в криогенных условиях, обозначается как IIcryo, а дисперсия, полученная при комнатной температуре, – как IIroom.
Для формирования ККГПВС, содержащих частицы кремнезема, водные дисперсии IIcryo или IIroom смешивали с раствором ПВС Isol необходимой концентрации и добавляли, когда это требовалось, такое количество воды, чтобы получить соотношения 0.06, 0.12, 0.18 и 0.24 моля SiO2 на 1 моль OH-групп полимера. При этом концентрация ПВС в дисперсионной среде таких систем поддерживалась равной 93.6 г/л. Затем их дозировали в формы и подвергали криогенной обработке. Получаемые таким способом ККГПВС далее обозначаются как I + IIcryo и I + IIroom соответственно.
Криогели, содержащие NaCl, формировали, используя методику, описанную ранее [56]; мольное отношение NaCl : OHPVA варьировали в диапазоне 0.04–0.24. Эти криогели обозначены как I + NaCl.
Основным объектом данного исследования были ККГПВС, формируемые совмещением процессов криотропного гелеобразования ПВС и генерирования кремнеземных компонентов реакцией силиката натрия с кислотой. С этой целью раствор ПВС (Isol) требуемой концентрации смешивали со щелочным раствором силиката натрия (IIsol) в соотношениях 0.06, 0.12, 0.18 и 0.24 моля силикат-анионов (а значит, и атомов Si) на 1 моль OH-групп ПВС. Затем быстро добавляли 6 н. HCl в количестве, эквимолярном содержанию Na+-ионов в растворе IIsol, а также, когда требовалось, необходимое количество воды для достижения концентрации ПВС, равной 93.6 г/л. Последующая криогенная обработка таких композиций приводила к получению гибридных органо-неорганических криогелей, в дальнейшем обозначаемых как IIIhybr.
Для оценки физико-механических показателей полученных криогелей их формовали в разборных дюралюминиевых контейнерах с внутренним диаметром 15 мм и высотой 10 мм [52, 56], а затем измеряли кажущийся мгновенный модуль сдвига (G0), характеризующий упругие свойства материала, и модуль сдвига при 30-минутном нагружении (G30), отражающий пластическое поведение материала [45, 46, 62]. Эксперименты проводили с помощью динамометрических весов Каргина–Соголовой при нагрузке 4.905 × 10–3 Н с использованием методики пенетрации в гель сферического индентора [42].
Теплостойкость криогелей оценивали путем измерения температуры их плавления (Tf) известным методом [45, 46]. Для этого образцы объемом 5 мл готовили в прозрачных полиэтиленовых пробирках с внутренним диаметром 1 см, на дно каждой пробирки помещали шарик из нержавеющей стали диаметром 3.5 мм и массой 0.275 ± ± 0.005 г. После завершения процесса криоструктурирования плотно закрытую пробирку с криогелем помещали вверх дном в водяную баню, снабженную мешалкой. Баню нагревали со скоростью примерно 0.4 град./мин. Температура, при которой шарик, проходя через слой плавящегося геля, падал на пробку пробирки, принималась за Tf образца.
Модули сдвига криогелей, а также температуры их плавления, измеряли для четырех параллельных образцов; независимые эксперименты проводились в 3–5 повторах; полученные результаты усредняли.
Макропористую морфологию криогелей изучали с помощью оптического микроскопа Eclipse 55i (Nikon, Япония), оснащенного системой цифровой регистрации изображений. Тонкие (~10 мкм) срезы соответствующих образцов в соответствии с ранее описанной методикой [37, 45, 46, 48, 52] готовили с использованием криомикротома SM-1900 (Leica, Германия) в направлении, перпендикулярном оси цилиндра, а затем контрастировали красителем Конго красный, герметизировали в фиксирующую среду и хранили в закрытом контейнере при 4°С.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Химический состав исходных и получаемых образцов
Как указано во введении, целевыми объектами данного исследования являлись гибридные органо-неорганические композиты, представляющие собой макропористые криогели ПВС, наполненные синтезированным in situ кремнеземом. С этой целью золь–гель процессы, включавшие превращение щелочного раствора силиката натрия в кремниевую кислоту (точнее, поли/олигокремниевые кислоты [57]) и, далее, в кремнезем, проводились параллельно с криотропным гелеобразованием ПВС в замороженных многокомпонентных системах (см. Экспериментальную часть). Последовательность известных химических реакций, протекающих в ходе трансформации указанных выше неорганических соединений, выглядит следующим образом [57]:
Следовательно, целевые гибридные криогели, т.е. IIIhybr, должны содержать следующий набор химических веществ: воду, ПВС, кремнезем и хлорид натрия. Предварительные эксперименты показали, что криогели этого типа можно получить при мольном соотношении Si-содержащих добавок и мономерных звеньев ПВС, т.е. его OH-групп, не превышающем 0.25, т.к. при большем исходном содержании Na2SiO3 полимер частично коагулировал. Поэтому в последующих исследованиях мы использовали следующие значения мольного отношения Si/OHPVA: 0.06, 0.12, 0.18 и 0.24.
Вполне очевидно, что указанные нерастворимые и растворимые добавки могут влиять на свойства и макропористую морфологию соответствующих гибридных криогелей не только все вместе, но и каждая по отдельности. Именно поэтому, помимо свойств образцов IIIhybr, содержащих различные количества всех этих неорганических компонентов, мы также исследовали эффекты, вызванные включением в матрицу криогеля отдельных “представителей” таких добавок. Для этого, наряду с использованием простого кремнеземного наполнителя (в данном случае – частиц силикагеля LS), путем превращения Na2SiO3 в SiO2 при +20 и –20°C были получены образцы IIroom и IIcryo с последующим их включением в матрицу криогеля ПВС. В итоге серия образцов сравнения и целевые гибридные криогели имели составы, приведенные ниже.
Inf – ненаполненные криогели ПВС без каких-либо добавок; они содержали только воду и гелеобразующий полимер,
I + LS – ККГПВС, полученные замораживанием–оттаиванием суспензий силикагеля LS в растворе ПВС; такие наполненные криогели содержали воду, ПВС и SiO2,
I + IIroom – ККГПВС, сформированные из суспензий кремнезема IIroom, смешанных с раствором гелеобразующего полимера; эти криогели содержали воду, ПВС, SiO2 и NaCl,
I + IIcryo – ККГПВС, приготовленные на основе суспензий кремнезема IIcryo и раствора ПВС; эти криогели также содержали воду, ПВС, SiO2 и NaCl,
I + NaCl – ненаполненные солесодержащие криогели ПВС; они включали воду, ПВС и NaCl,
IIIhybr – гибридные органо-неорганические композиты, полученные сочетанием криотропного гелеобразования ПВС и превращения силиката натрия в кремнезем, когда оба процесса протекали одновременно в замороженных системах; эти криогели состояли из воды, ПВС, набора Si-содержащих соединений (см. ниже) и NaCl.
При получении перечисленных выше образцов переменными параметрами были концентрация неорганических веществ и температура криогенной обработки (Tcp), тогда как концентрация ПВС поддерживалась постоянной – 93.6 г/л. Такой дизайн экспериментов позволил выявить основные факторы, способные влиять на свойства изучаемых гибридных криогелей.
Физико-химические свойства гибридных органо-неорганических криогелей ПВС
Твердые неорганические частицы, включенные в различные полимерные гели, обычно являются так называемыми активными дисперсными наполнителями [58], способствующими повышению жесткости геля при условии их достаточной совместимости с непрерывной фазой [1]. Такой же эффект характерен и для различных ККГПВС (см., например, [15, 28, 37, 49, 50, 53, 59–61]), в том числе и для упомянутых во введении кремнеземсодержащих композитов, полученных в золь–гель процессе при гидролитической поликонденсации ТМОС, протекающей в замороженной системе одновременно с криотропным гелеобразованием ПВС [52]. Поэтому мы предположили, что очень похожая тенденция должна наблюдаться и в случае композитных криогелей IIIhybr. Однако экспериментальная проверка этого предположения выявила несколько иные эффекты.
В частности, на графиках рис. 1а и 1в приведены зависимости физико-механических характеристик (сдвиговых модулей G0 и G30) таких образцов от содержания введенных в систему кремнийсодержащих компонентов, количество которых выражено как отношение числа молей Si к числу молей OH-групп ПВС. Графики рис. 1б и 1г показывают зависимости тех же модулей от температуры криогенной обработки при получении соответствующих криогелей, содержащих различные количества неорганических добавок. Масштаб соответствующих осей ординат на этих графиках (и далее на рис. 2, 4 и 5) является одинаковым, чтобы сделать сравнение более наглядным. При этом данные для криогелей без добавок, т.е. Inf, приведены на рис. 1а и 1в как отвечающие мольному соотношению Si/OHPVA = 0, а на рис. 1б и 1г данные для этих криогелей представлены кривыми 5.
Рис. 1.
Зависимости модулей G0 (а, б) и G30 (в, г) криогелей ПВС Inf и IIIhybr от начальной концентрации Si-компонентов (а, в) и температуры криогенной обработки (б, г). Кривые 1–4 отвечают образцам, полученным замораживанием при –30, –25, –20 и –15°C, соответственно, а кривые 5–9 – образцам, сформированным при начальном мольном соотношении Si/OHPVA 0, 0.06, 0.12, 0.18 и 0.24 соответственно.
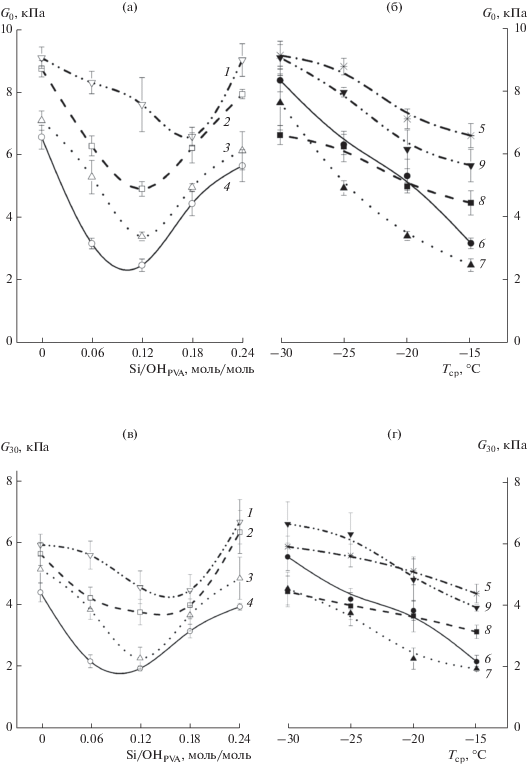
Рис. 2.
Зависимости модулей G0 (а, б) и G30 (в, г) криогелей Inf и I + LS от концентрации наполнителя – силикагеля LS (а, в) и температуры криогенной обработки (б, г). Кривые 1–4 отвечают образцам, полученным замораживанием, соответственно, при –30, –25, –20 и –15°C, а кривые 5–9 – образцам, сформированным при начальном мольном соотношении Si/OHPVA, соответственно, 0, 0.06, 0.12, 0.18 и 0.24.

Рис. 3.
Оптические микрофотографии частиц силикагеля LS (а), дисперсии IIroom (б) и дисперсии IIcryo (в).

Рис. 4.
Зависимости модулей G0 (а) и G30 (б) криогелей IIIhybr (1), I + IIroom (2) и I + IIcryo (3) от начальной концентрации Si-содержащих компонентов. Все образцы были получены замораживанием при –20°C.
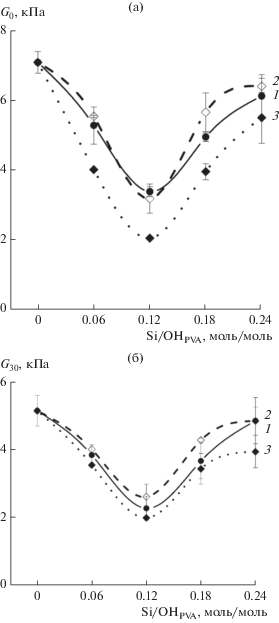
Рис. 5.
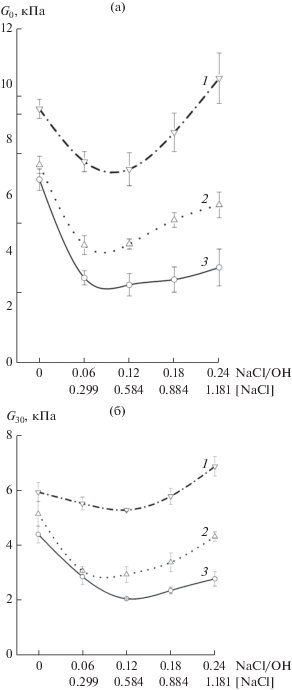
Зависимости значений модулей G0 (а) и G30 (б) криогелей I + NaCl от начальной концентрации NaCl (в величинах мольного отношения NaCl/(OH)PVA и молярной концентрации соли). Образцы получали замораживанием при –30 (1), –20 (2) и –15°C (3).
Как известно [63], теплостойкость, в частности температура плавления Tf, является существенным свойством физических (нековалентных) гелей, включая и криогели ПВС [2, 43–47, 64–66]. Фактически этот параметр является функцией количества Н-связей, которые должны термически диссоциировать, чтобы расплавились микрокристаллиты, выполняющие роль узлов надмолекулярной сетки таких криогелей [2, 44, 66, 67]. Поэтому нами также были определены значения Tf для тех образцов, физико-механические характеристики которых приведены на рис. 1. Полученные результаты такой оценки теплостойкости образцов суммированы в табл. 1.
Таблица 1.
Температура плавления ненаполненных криогелей ПВС Inf и гибридных криогелей IIIhybr*, сформированных при разной температуре криогенной обработки
| Tcp, °C | Значения Tf (°C) образцов криогелей без и с добавками Si-содержащих компонентов в количестве, выраженном как мольное отношение Si/OHPVA | ||||
|---|---|---|---|---|---|
| 0 | 0.06 | 0.12 | 0.18 | 0.24 | |
| –15 | 72.7 ± 0.3 | 76.5 ± 0.7 | 84.7 ± 0.3 | 89.4 ± 0.2** | 96.0 ± 2.0** |
| –20 | 73.0 ± 0.2 | 78.0 ± 0.2 | 83.4 ± 0.2 | 88.1 ± 1.1** | 90.5 ± 1.5** |
| –25 | 73.2 ± 0.2 | 79.6 ± 0.8 | 80.8 ± 0.4 | 85.0 ± 1.0** | 92.0 ± 1.0** |
| –30 | 73.5 ± 0.1 | 80.8 ± 0.8 | 83.5 ± 1.5 | 84.5 ± 0.5** | 85.5 ± 0.7** |
Анализ данных рис. 1 и табл. 1 позволил сделать следующие выводы, представленные ниже.
1. Постепенное повышение общего содержания неорганических компонентов в составе криогелей IIIhybr приводит к экстремальному (с минимумом) характеру зависимости их жесткости от концентрации таких добавок. При этом точки минимумов находятся в районе средних значений этих концентраций как для G0, так и для G30 (рис. 1а и 1в). Для упругих свойств (рис. 1а) минимум выражен сильнее, чем для пластических свойств (рис. 1в). Экстремальный характер кривых свидетельствует о конкуренции процессов ослабления и упрочнения таких гибридных криогелей ПВС под действием неорганических добавок.
2. В диапазоне значений Tcp от –15 до –30°C, чем ниже температура криогенной обработки, тем выше жесткость образцов с одинаковым содержанием неорганических компонентов (рис. 1б и 1г). Такая же закономерность наблюдается и в случае криогелей без добавок Inf, что согласуется и с ранее полученными результатами для подобных систем [2, 21, 45, 47].
3. В диапазоне мольных отношений Si/OHPVA от 0.06 до 0.24 жесткость гибридных криогелей не превышает жесткости соответствующих ненаполненных криогелей ПВС, полученных в идентичных условиях криогенной обработки (рис. 1б и 1г). Этот факт, очевидно, указывает на наличие определенных факторов, способствующих снижению жесткости гелевой матрицы органо-неорганических криогелей IIIhybr несмотря на включение в них Si-содержащих компонентов.
4. В случае ненаполненных криогелей ПВС Inf снижение температуры криогенной обработки с –15 до –30°C приводило к некоторому повышению их термостойкости (табл. 1), что также известно из более ранних исследований [2, 6, 45, 47, 68, 69]. В случае же гибридных криогелей IIIhybr их теплостойкость возрастала с повышением концентрации неорганических добавок при одинаковых условиях замораживания–оттаивания (горизонтальные строки в табл. 1). Однако если сравнить значения Tf в вертикальных столбцах табл. 1, то тенденция не столь очевидна и зависит от содержания неорганических добавок. При небольшом их количестве (мольное отношение Si/OHPVA = 0.06) и понижении Tcp с –15 до –30°C температура плавления полученных гибридных криогелей возрастала от 76.5 до 80.8°C. Однако при уже вдвое большем содержании тех же добавок (т.е. при Si/OHPVA = 0.12 моль/моль) этот порядок нарушался. Наконец, при еще более высокой концентрации Si-содержащих включений криогели IIIhybr теряли способность к плавлению и при повышенных температурах распадались на несколько фрагментов (образцы с индексом ** в табл. 1). Возможные причины такого эффекта будут рассмотрены ниже.
Общий вывод из данных рис. 1 и табл. 1 заключается в том, что требуется систематическое изучение влияния каждого отдельного фактора, главным образом типа включаемой добавки и ее содержания в системе, на свойства соответствующих криогелей.
Физико-химические свойства криогелей ПВС, содержащих включения индивидуальных добавок
Графики на рис. 2, 4 и 5 показывают значения модулей G0 и G30 для композитов I + LS, I + IIroom и I + IIcryo, наполненных различными частицами кремнезема, а температуры плавления этих криогелей приведены в табл. 2.
Таблица 2.
Температура плавления криогелей I + LS, I + IIroom, I + IIcryo и I + NaCl*, сформированных при разной температуре криогенной обработки
| Криогель | Tcp, °C | Значения Tf (°C) криогелей без и с добавками Si-содержащих компонентов (или NaCl) в количестве, выраженном как мольное отношение Si/OHPVA (или NaCl/OHPVA) | |||
|---|---|---|---|---|---|
| 0.06 | 0.12 | 0.18 | 0.24 | ||
| I + LS | –15 | 73.0 ± 0.2 | 73.1 ± 0.1 | 73.2 ± 0.2 | 73.4 ± 0.2 |
| –20 | 73.2 ± 0.4 | 73.3 ± 0.3 | 73.4 ± 0.2 | 73.5 ± 0.3 | |
| –25 | 73.5 ± 0.5 | 73.5± 0.3 | 73.7 ± 0.3 | 73.7 ± 0.1 | |
| –30 | 73.6 ± 0.4 | 73.6 ± 0.4 | 73.8 ± 0.4 | 74.0 ± 0.2 | |
| I + IIroom | –20 | 73.8 ± 0.4 | 75.3 ± 0.5 | 78.5 ± 0.3 | 82.0 ± 0.6 |
| I + IIcryo | –20 | 75.8 ± 0.4 | 77.7 ± 0.5 | 82.8 ± 0.2 | 84.5 ± 0.7 |
| I + NaCl** | –15 | 74.3 ± 0.3 | 77.5 ± 0.3 | 81.7 ± 0.5 | 86.5 ± 0.7 |
| –20 | 75.4 ± 0.2 | 78.7 ± 0.5 | 82.5 ± 0.7 | 87.4 ± 1.1 | |
| –30 | 76.2 ± 0.4 | 79.5 ± 0.7 | 83.3 ± 0.7 | 88.8 ± 1.0 | |
* Исходная концентрация ПВС во всех случаях – 93.6 г/л; значения Tf для ненаполненных криогелей Inf приведены в табл. 1. ** Поскольку молярная концентрация NaCl в два раза превышает молярную концентрацию Si-компонентов, отношение NaCl/OHPVA составляет соответственно 0.12, 0.24, 0.36 и 0.48.
Прежде всего, данные рис. 2 свидетельствуют, что частицы обычного кремнезема, в данном случае силикагеля LS, влияли на жесткость соответствующих композитных криогелей как типичные активные наполнители. Значения обоих сдвиговых модулей возрастали с повышением содержания дисперсной фазы (рис. 2а и 2в) аналогично уже наблюдавшемуся ранее влиянию добавок силикагелей [49, 50, 53]. При этом зависимости жесткости криогелей I + LS от температуры криотропной обработки проходили через максимум (рис. 2б и 2г), сильнее выраженный при высокой степени наполнения, а именно, при соотношении Si/OHPVA, равном 0.24 моль/моль. Интересно, что наиболее высокие значения G0 были присущи композитам I + LS, сформированным при –20°C (рис. 2б), в то время как для G30 соответствующие максимумы были смещены в сторону более низкой (Tcp = –25°C) температуры криогенной обработки (рис. 2г).
Что касается теплостойкости композитов I + LS, то существенного влияния наполнителя не выявлено (табл. 2). Значения Tf незначительно повышались с ростом содержания кремнезема, а также с понижением Tcp. Следовательно, собственно частицы SiO2 практически не участвуют в образовании термоплавких узлов трехмерной сетки криогелей ПВС, наполненных привнесенным дисперсным кремнеземом, и, таким образом, не оказывают существенного влияния на количество межцепных Н-связей.
При сравнении данных рис. 2 для композитов I + LS и физико-механических свойств гибридных криогелей IIIhybr (рис. 1) видно, что влияние эффектов, понижающих жесткость последних, наиболее выражено, в основном, в одном и том же диапазоне концентраций Si-содержащих добавок (рис. 1а и 1в). Иными словами, хотя дисперсный силикагель способствовал повышению жесткости композитов I + LS (рис. 2), в случае образцов IIIhybr, полученных с одновременным образованием in situ кремнезема, воздействие факторов и, вероятно, веществ, понижающих их жесткость, в определенном диапазоне концентраций добавки превалировало.
Такой же набор неорганических веществ, как в составе криогелей IIIhybr (вода, Si-содержащие компоненты и хлорид натрия), должен присутствовать и в суспензиях IIroom и IIcryo, приготовленных нейтрализацией щелочного раствора с невысокой концентрацией Na2SiO3, когда образование кремниевой кислоты и ее дальнейшее превращение в кремнезем происходило соответственно при +20 и –20°C.
Микрофотографии на рис. 3 показывают морфологию частиц дисперсных систем IIroom и IIcryo, а также, для сравнения, частиц силикагеля LS.
В отличие от бесформенных гранул силикагеля LS (рис. 3а), доминирующей формой SiO2 в суспензии IIroom являются анизодиаметричные частицы длиной до 150–200 мкм и толщиной 1–5 мкм (рис. 3б). В суспензии IIcryo игольчатые образования значительно короче (до 20–50 мкм) и тоньше (<1 мкм); также присутствует много мелких округлых частиц, наблюдаемых в виде темных точек (рис. 3в). Такие различия в морфологии частиц твердого вещества в этих суспензиях, очевидно, обусловлены температурным режимом и фазовым состоянием систем при реакции Na2SiO3 с HCl. Рост частиц кремнезема в замороженной системе, скорее всего, был затруднен вследствие низкой температуры и повышенной вязкости так называемой незамерзшей жидкой микрофазы (НЖМФ).
Далее были исследованы композиты I + IIroom и I + IIcryo, сформированные путем включения частиц суспензий IIroom и IIcryo в матрицу криогелей ПВС. Поскольку основной целью этих экспериментов было получение ответа на вопрос о влиянии состава и концентрации компонентов таких суспензий, введенных в указанные композитные криогели, на свойства последних, их образцы формировали только Tcp = –20°C. На рис. 4 показано, как значения сдвиговых модулей G0 и G30 полученных криогелей зависели от содержания добавок, а значения Tf для тех же образцов даны в табл. 2. Также на рис. 4а и 4б для сравнения приведены соответствующие кривые для гибридных криогелей IIIhybr, сформированных замораживанием при –20°C.
Сопоставление данных, представленных на рис. 4а и 4б, показывает очевидное сходство изменений значений G0 и G30 в зависимости от концентрации добавок. Все кривые проходят через минимум в области мольных отношений Si/OHPVA = = 0.12–0.18. Это явно свидетельствует о значимой роли компонентов химических реакций Na2SiO3 + + HCl → (H2SiO3)n + NaCl → n(SiO2 · H2O) + NaCl, исключая твердый кремнезем (см. рис. 2), в снижении жесткости этих криогелей. При этом несколько более сильное влияние на изменение модулей G0 и G30 оказывало включение в объем криогеля суспензии IIcryo по сравнению с суспензией IIroom. Кроме того, повышение содержания обеих этих добавок в соответствующих криогелях вызывало значительный рост их теплостойкости (табл. 2), как это происходило и в случае гибридных криогелей IIIhybr (табл. 1). Однако фрагментация криогелей I + IIroom и I + IIcryo при повышенных температурах еще до их плавления, в противоположность криогелям IIIhybr, не наблюдалась.
В целом, результаты, приведенные на рис. 2 и 4, а также в табл. 2, свидетельствуют о том, что “агентами”, вызывающими снижение жесткости таких ККГПВС, скорее всего, могли быть поли/олигокремниевые кислоты и NaCl. Поэтому было также исследовано влияние на свойства криогелей ПВС собственно хлорида натрия в диапазоне тех же его концентраций, что и в составе образцов I + IIroom, I + IIcryo и IIIhybr. Результаты измерений G0 и G30 для криогелей I + NaCl приведены на рис. 5, а значения их Tf даны в трех нижних строках табл. 2. Поскольку в результате реакции Na2SiO3 с HCl образуются два моля NaCl и 1 моль кремнезема, содержание соли в этих случаях выражается и молярной концентрацией (моль/л), и соотношением NaCl : OHPVA (моль/моль).
Вид кривых с минимумом на рис. 5а и 5б свидетельствует о влиянии NaCl в определенном диапазоне содержания этой соли на обсуждавшееся выше снижение жесткости гибридных криогелей IIIhybr (рис. 1), а также криогелей I + IIroom и I + IIcryo (рис. 4). Кроме того, аналогичный характер влияния концентрации NaCl на физико-механические свойства обычных ненаполненных криогелей ПВС находится в хорошем соответствии и с данными работ [56, 70–74], где было показано, что такая форма кривых обусловлена конкуренцией между факторами, положительно и отрицательно влияющими на жесткость данных систем [56]. Поскольку криотропное гелеобразование ПВС происходит [2, 21, 47, 67, 75–77] в объеме НЖМФ [78], т.е. в остающихся жидкими областях макроскопически замороженной системы, то чем выше концентрация растворенных веществ в исходном растворе, тем больше объем НЖМФ. Следовательно, концентрация ПВС там ниже по сравнению с бессолевой системой при той же отрицательной температуре. В свою очередь, чем ниже концентрация гелеобразующего полимера, тем меньше жесткость образующихся криогелей [2, 6, 13, 21, 42, 45, 47, 79]. С другой стороны, с повышением концентрации электролита возрастает ионная сила раствора полимера, способствуя тем самым высаливанию ПВС. Как следствие, усиливаются взаимодействия полимер–полимер. Когда последний эффект начинает превалировать над ослабляющим влиянием разбавления, это приводит к образование более жестких криогелей ПВС. В результате зависимости их физико-механических характеристик от концентрации NaCl имеют выраженный минимум [56].
В то же время, повышение концентрации NaCl в том же диапазоне способствовало возрастанию термостойкости криогелей I + NaCl (табл. 2) аналогично данным предыдущих исследований [56, 71, 72]. Следовательно, присутствие соли как в образцах IIIhybr, так и в криогелях I + IIroom и I + IIcryo также должно было способствовать росту значений Tf. Однако композиты I + IIroom и I + IIcryo плавились в диапазоне температур, равном примерно 74–85°C (табл. 2), тогда как гибридные криогели IIIhybr, содержавшие умеренное или высокое количество неорганических добавок, распадались на фрагменты при нагревании до аналогичных температур, а не претерпевали переход гель–золь (образцы с индексом ** в табл. 1). Такое их поведение оказалось очень похожим на поведение гетерофазных органо-неорганических криогелей, полученных замораживанием–оттаиванием водных растворов ПВС с добавками ТМОС [52]. В последнем случае причиной фрагментации криогелей являлось образование достаточно термостабильных дополнительно поляризованных связей между гидроксильными группами ПВС и силанольными группами олигосилоксанов – промежуточных продуктов гидролитической поликонденсации ТМОС. Мы полагаем, что и при нагревании гибридных криогелей IIIhybr механизм фрагментации был аналогичным.
Действительно, в этих системах наряду с образованием “обычных” межцепных водородных связей OH-группами макромолекул ПВС при его криотропном гелеобразовании в объеме НЖМФ может происходить дополнительное Н-связывание с участием кремниевых кислот. На рис. 6 изображены в качестве примера два типа химических структур, которые могут возникать в этом случае.
Рис. 6.
Типы химических структур, которые потенциально могут формироваться [52] при одновременном протекании процессов криотропного гелеобразования ПВС и превращения силиката натрия в олигомеры кремниевой кислоты.

Как давно известно, в реакции 1 моля Na2SiO3 с 2 молями HCl образуется смесь поли- и олигокремниевых кислот, которая затем медленно превращается в кремнезем и воду [80]. Поэтому силоксановые фрагменты этих неорганических поли- и олигомеров могут взаимодействовать “бок о бок” с цепями ПВС в соответствии со схемой A на рис. 6. Очевидно, что “продукты” подобных взаимодействий будут препятствовать эффективным контактам макромолекул ПВС, затрудняя образование достаточно совершенных микрокристаллитов этого полимера. Как следствие, может снижаться жесткость криогелей IIIhybr (рис. 1). С другой стороны, слабокислые силанольные группы кремниевых кислот способны образовывать водородные связи (по схеме Б на рис. 6) с имеющими неподеленную электронную пару атомами кислорода гидроксильных групп ПВС, выступающих в этом случае в качестве слабого основания. Водородные связи такого типа поляризованы сильнее, чем “обычные” H-связи типа А на рис. 6. Благодаря такой псевдосолевой природе сильнее поляризованные водородные связи Б-типа более термостойки, чем связи А-типа [52]. Поскольку поли/олигокремниевые кислоты имеют множество силанольных групп, их молекулы могут играть роль сшивающих агентов для соседних цепей ПВС, тем самым повышая теплостойкость соответствующих гибридных криогелей. Этот эффект, скорее всего, является причиной отсутствия термоиндуцированного плавления криогелей IIIhybr с высоким содержанием неорганических добавок (образцы с индексом ** в табл. 1). Однако образование структур типа Б, как и структур типа А (рис. 6), препятствует и формированию совершенных микрокристаллитов ПВС, способствуя снижению жесткости этих гибридных криогелей.
В этой связи возникает довольно очевидный вопрос: почему эффекты вызванной нагревом фрагментации, а не плавления, присущи именно органо-неорганическим криогелям IIIhybr, но не наблюдаются в случае композитов I + IIroom и I + IIcryo (табл. 2), формально содержащих те же компоненты?
С нашей точки зрения, причина такого различия обусловлена условиями приготовления соответствующих криогелей. При формировании гибридных систем IIIhybr поли/олигокремниевые кислоты образуются в объеме НЖМФ одновременно с криотропным гелеобразованием ПВС, поэтому, действительно, существует возможность возникновения химических структур типов А и Б (рис. 6), особенно, с учетом криоконцентрационных явлений. Напротив, при формировании композитных криогелей I + IIroom и I + IIcryo Si-содержащие суспензии IIroom и IIcryo были предварительно получены соответственно при положительной и отрицательной температуре и, что важно, в отсутствие ПВС, т.е. образование структур, подобных структурам А и Б на рис. 6, было невозможным. Только после этого суспензии IIroom и IIcryo вводили в исходный раствор ПВА для последующей криогенной обработки соответствующих смесей. Поскольку общая продолжительность операций по получению дисперсий IIroom и IIcryo составляла не менее 36 ч, глубина процесса “старения” поли/олигокремниевых кислот с образованием кремнезема и воды могла быть значительной. Как следствие, количество силанолсодержащих компонентов должно было существенно снижаться до тех пор, пока не останется в целом крайне небольшое число силанольных групп просто на поверхности окончательно сформировавшихся частиц кремнезема.
Микроструктура гибридных криогелей ПВС
Поскольку образование in situ неорганических Si-содержащих компонентов параллельно с криотропным гелеобразованием ПВС вызывало значительные изменения свойств гибридных криогелей IIIhybr по сравнению с ненаполненными криогелями Inf (рис. 1 и табл. 1), то важно было выяснить также, как такие изменения сказывались на микроструктуре криогелей IIIhybr. Для этого была использована оптическая микроскопия тонких срезов криогелей, которая, как было установлено при изучении самых разных ненаполненных и композитных криогелей ПВС [21, 37, 45–50, 52, 56, 81], позволяет получить адекватную информацию о макропористой морфологии таких объектов без необходимости из высушивания.
Микрофотографии на рис. 7 показывают структурные особенности следующих образцов, сформированных замораживанием исходных растворов при Tcp = –20°C:
Рис. 7.
Оптические микрофотографии окрашенных Конго красным тонких срезов образцов криогелей Inf (а) и IIIhybr (б–г) (их описание приведено в тексте).

(а) криогель ПВС без добавок, т.е. Inf,
(б) гибридный криогель IIIhybr, приготовленный с использованием наименьшего количества Si-содержащих добавок, т.е. при мольном отношении Si/OHPVA = 0.06,
(в) гибридный криогель IIIhybr, полученный при мольном отношении Si/OHPVA = 0.12, соответствующем минимальной жесткости геля (см. рис. 1а и 1в),
(г) гибридный криогель IIIhybr, сформированный с использованием наибольшего количества Si-содержащих добавок, т.е. при мольном отношении Si/OHPVA = 0.24.
Темные структурные элементы на этих черно-белых микрофотографиях представляют собой полимерную гелевую фазу стенок макропор, контрастированных Конго красным. Светлые участки – сами заполненные водой макропоры. Морфология ненаполненного криогеля Inf (рис. 7а), форма и размер его пор (несколько микрон) характерны для таких обычных, т.е. состоящих только из ПВС и воды, макропористых гелевых матриц [2, 21, 28, 45–47, 81]. В свою очередь, включение все больших количеств неорганических Si-содержащих компонентов и NaCl в гибридные криогели вызывало определенные изменения их микроструктуры. Так, в случае низкого содержания неорганических добавок, т.е. при отношении Si/OHPVA, равном 0.06, характер макропористой морфологии криогеля (рис. 7б) изменился в целом незначительно по сравнению с образцом Inf (рис. 7а). Однако уже при двукратном повышении содержания неорганических компонентов (т.е. при Si/OHPVA = 0.12), когда наблюдалось наибольшее снижение жесткости криогеля IIIhybr (рис. 1а и 1в), морфология гелевого материала заметно трансформировалась (рис. 7в). В этом случае толщина стенок пор уменьшалась, границы пор размывались, а общая текстура становилась более диффузной. Здесь следует отметить, что очень похожее влияние на микроструктуру криогелей ПВС было обнаружено и для образцов, содержащих NaCl в концентрации 0.3–0.6 моль/л [56]. Поскольку мольное отношение Si/OHPVA = 0.12 в криогелях IIIhybr соответствует концентрации NaCl, равной 0.512 моль/л (табл. 3), резонно полагать, что присутствие этой соли является одной из причин изменения микроструктуры таких гибридных криогелей.
Таблица 3.
Температура плавления криогелей I + NaCl*, сформированных при разной температуре криогенной обработки
| Tcp, °C | Значения Tf (°C) образцов криогелей, содержащих разное количество NaCl (в терминах мольного отношения NaCl/(OH)PVA или, в квадратных скобках, в моль/л) | |||
|---|---|---|---|---|
| 0.12 [0.256] | 0.24 [0.512] | 0.361 [0.768] | 0.48 [1.024] | |
| –15 | 74.3 ± 0.3 | 77.5 ± 0.3 | 82.7 ± 0.3 | 86.5 ± 0.7 |
| –20 | 75.4 ± 0.2 | 78.7 ± 0.3 | 82.5 ± 0.5 | 87.4 ± 1.2 |
| –30 | 76.2 ± 0.2 | 79.5 ± 0.5 | 83.3 ± 0.5 | 88.8 ± 0.8 |
* Исходная концентрация ПВС во всех случаях – 93.6 г/л; значения Tf для ненаполненных криогелей Inf приведены в табл. 1.
Кроме того, можно было ожидать, что и водородное связывание поли/олигокремниевых кислот с ПВС (рис. 6) также должно вызывать изменения структуры гибридных криогелей по сравнению с криогелем без добавок. При этом важно отметить, что отсутствие каких-либо частиц кремнезема, различимых в оптическом микроскопе, на изображениях рис. 7б и 7в указывает на возможность такого связывания. Возникающие H-связи не только отрицательно влияют на формирование матрицы криогеля ПВС, но и тормозят превращение кремниевых кислот в SiO2 и воду. В то же время, нельзя исключить и образования очень мелких (наноразмерных) частиц кремнезема, не детектируемых оптической микроскопией. Конечно, тонкие механизмы влияния таких H-связей на процессы с участием Si-содержащих компонентов в этих системах требуют специальных исследований, которые выходили за рамки настоящей работы.
Наконец, при еще вдвое большем содержании неорганических добавок, т.е. при Si/OHPVA = 0.24, удалось обнаружить присутствие дисперсного неорганического наполнителя в массе гибридного криогеля. Правда, количество таких микрочастиц (показаны стрелками на рис. 7в) было малым, а их форма и размер существенно отличались по сравнению с частицами SiO2 (дисперсия IIcryo), также образовавшимися в замороженной системе (рис. 3в), но в отсутствие ПВС. Эти экспериментальные результаты дополнительно свидетельствуют о взаимосвязанном влиянии гелеобразующего полимера на превращения реагирующих неорганических компонентов и Si-содержащих промежуточных продуктов на криотропное гелеобразование самого ПВС. При этом в целом морфология собственно гелевой фазы на микрофотографии рис. 7г оставалась похожей на морфологию образца с вдвое меньшим содержанием неорганических компонентов (рис. 7в). Этот факт, видимо, свидетельствует о том, что влияние наличия NaCl и поли/олигокремниевых кислот на микроструктуру гелевой фазы образцов IIIhybr с более высоким содержанием неорганических добавок в обоих случаях было примерно одинаковым.
ЗАКЛЮЧЕНИЕ
В данной работе были получены и исследованы новые макропористые гибридные органо-неорганические криогели ПВС. Такие гетерофазные материалы формировались в результате одновременного протекания двух процессов: индуцированного замораживанием–оттаиванием гелеобразования ПВС и образования поли/олигокремниевых кислот и частиц кремнезема при взаимодействии силиката натрия с соляной кислотой.
Установлено, что основными факторами, влияющими на жесткость, теплостойкость и макропористую морфологию полученных гибридных криогелей, являются образование NaCl и взаимодействие поли/олигокремниевых кислот с гидроксильными группами ПВС. Первый фактор увеличивает объем незамерзшей жидкой микрофазы, тем самым снижая эффективную концентрацию ПВС за счет сольватной воды, дополнительно удерживаемой ионами соли. С другой стороны, повышение ионной силы усиливает высаливание гелеобразующего полимера, способствуя взаимодействиям полимер–полимер. В результате зависимости жесткости криогеля от концентрации неорганических добавок проходят через минимум. В свою очередь, образование дополнительно поляризованных водородных связей между силанольными группами поли/олигокремниевых кислот и OH-группами ПВС приводит к выраженному повышению теплостойкости соответствующих гибридных криогелей. Этот эффект близок к ранее наблюдавшемуся для гибридных органо-неорганических криогелей ПВС, сформированных с добавками тетраметоксисилана, когда олигомерные продукты его гидролитической поликонденсации связывались с цепями ПВС также через дополнительно поляризованные H-связи силанол–гидроксил, существенно повышая теплостойкость гибридных криогелей [52].
Макропористая морфология полученных в данной работе криогелей IIIhybr зависела от количества Si-содержащих неорганических добавок, включенных в непрерывную фазу матрицы криогеля. Это обусловлено наличием различного количества NaCl, способного влиять на кристаллизацию порогена (т.е. льда) при замораживании исходной системы, а также взаимодействиями ПВС и поли/олигокремниевых кислот, влияющими на надмолекулярную структуру гелевой фазы – стенок макропор этих гетерофазных матриц.
Список литературы
Кудайбергенов С.Е., Ибраева Ж.Е., Яшкарова М.Г., Бектуров Е.А. Композиционные гидрогелевые материалы. Семей, Республика Казахстан: Изд-во Государственного университета им. Шакарима, 2011.
Лозинский В.И. // Успехи химии. 1998. Т. 67. С. 641.
Nambu M. // Kobunshi Ronbunshu. 1990. V. 47. P. 695 (in Japanese).
Lazzeri L. // Trends Polym. Sci. 1996. V. 4. P. 249.
Chu K.C., Rutt B.K. // Magn. Reson. Med. 1997. V. 37. P. 314.
Hassan CM, Peppas NA. // Adv. Polym. Sci. 2000. V. 153. P. 37.
Surry K.J.M., Austin H.J.B., Fenster A., Peters T.M. // Phys. Med. Biol. 2004. V. 49. P. 5529.
Hoskins P.R. // Ultrasound Med. Biol. 2008. V. 34. P. 693.
Jagur-Grodzinski J. // Polym. Adv. Technol. 2010. V. 21. P. 21.
Alves M.H., Jensen B.E.B., Smith A.A.A., Zelikin A.N. // Macromol. Biosci. 2011. V. 11. P. 1293.
Baker M.I., Walsh S.P., Schwatz Z., Boyan B.D. // J. Biomed. Mater. Res. B. 2012. V. 100. V. 1451.
Iatridis J.C., Nicoll S.B., Michalek A.J., Walter B.A., Gupta M.S. // Spine J. 2013. V. 13. P. 243.
Wan W., Bannerman A.D., Yang L., Mak H. // Adv. Polym. Sci. 2014. V. 263. P. 283.
Kumar A., Han S.S. // Int. J. Polym. Mater. Polym. Biomater. 2017. V. 66. P. 159.
Timofejeva A., D’Este M., Loca D. // Eur. Polym. J. 2017. V. 95. P. 547.
Teodorescu M., Bercea M., Morariu S. // Polym. Rev. 2018. V. 58. P. 247.
Лозинский В.И., Вакула А.С., Зубов А.Л. // Биотехнология. 1992. № 4. С. 5.
Varfolomeev S.D., Rainina E.I., Lozinsky V.I. // Pure Appl. Chem. 1992. V. 64. P. 1193.
Lozinsky V.I., Plieva F.M. // Enzyme Microb. Technol. 1998. V. 23. P. 227.
Lozinsky V.I., Plieva F.M., Galaev I.Y., Mattiasson B. // Bioseparation. 2001. V. 10. P. 163.
Лозинский В.И. // Успехи химии. 2002. Т. 71. С. 559.
Lozinsky V.I., Galaev I.Y., Plieva F.M., Savina I.N., Jungvid H., Mattiasson B. // Trends Biotech. 2003. V. 21. P. 445.
Plieva F.M., Galaev I.Y., Noppe W., Mattiasson B. // Trends Microbiol. 2008. V. 16. P. 543.
Лозинский В.И. // Известия РАН. Сер. хим. 2008. С. 996.
Mattiasson B. // Adv. Polym. Sci. 2014. V. 263. P. 245.
Efremenko E.N., Lyagin I.V., Lozinsky V.I. // Supermacroporous Cryogels: Biomedical and Biotechnological Applications. Ed. by Kumar A. Boca Raton: CRC Press, Taylor & Francis Group, LLC. 2016. P. 301.
Gutiérrez M.C., Aranaz I., Ferrer M.L., del Monte F. // Macroporous Polymers: Production, Properties and Biotechnological/Biomedical Applications. Ed. by Mattiasson B., Kumar A., Galaev I.Y. Boca Raton: CRC Press. 2010. p. 83.
Gun’ko V.M., Savina I.N., Mikhalovsky S.V. // Adv. Colloid Interface Sci. 2013. V. 187–188. P. 1.
Iijima M., Kosaka S., Hatakeyama T., Hatakeyama H. // J. Therm. Anal. Calorim. 2016. V. 123. P. 1809.
Stejskal J., Bober P. // Colloid Polym. Sci. 2018. V. 296. P. 989.
Gupta T., Pradhan A., Bandyopadhyay-Ghosh S., Ghosh S.B. // Polym. Adv. Technol. 2019. V. 30. P. 2392.
Altunina L.K., Kuvshinov V.A., Dolgikh S.N. // Advances in Geological Storage of Carbon Dioxide. Ed. by Lombardi S., Altunina L.K., Beaubien S.E. NATO Science Series IV. Springer: Heidelberg. 2006. V. 65. P. 103.
Алтунина Л.К., Фуфаева М.С., Филатов Д.А., Сваровская Л.И., Рождественский Е.А., Ганн-Эрдене Е. // Почвоведение 2014. С. 563.
Vasiliev N.K., Ivanov A.A., Sokurov V.V., Shatalina I.N., Vasilyev K.N. // Cold Reg. Sci. Technol. 2012 V. 70. P. 94.
Vasiliev N.K., Pronk A.D.C., Shatalina I.N., Janssen F.H.M.E., Houben R.W.G. // Cold Reg. Sci. Technol. 2015. V. 115. P. 56.
Лозинский В.И., Подорожко Е.А., Никитина Я.Б., Клабукова Л.Ф., Васильев В.Г., Бурмистров А.А., Кондрашов Ю.Г., Васильев Н.К. // Коллоид. журн. 2017. Т. 79. С. 449.
Glushkov D.O., Kuznetsov G.V., Nigay A.G., Yanovsky V.A., Yashitina O.S. // Power Technol. 2020. V. 360. P. 65.
Peppas N.A., Stauffer S.R. // J. Control. Release. 1991. V. 16. P. 305.
Lozinsky V.I. // Adv. Polym. Sci. 2014. V. 263. P. 1.
Suzuki A., Sasaki S. // J. Eng. Med. 2015. V. 229. P. 828.
Lozinsky V.I. // Gels. 2018. V.4. Article 77. https://doi.org/10.3390/gels4030077
Lozinsky V.I., Vainerman E.S., Domotenko L.V., Mamtsis A.M., Titova E.F., Belavtseva E.M., Rogozhin S.V. // Colloid Polym. Sci. 1986. V. 264. P. 19.
Watase M., Nishinari K. // Makromol. Chem. 1989. V. 190. P. 155.
Nishinari K., Watase M., Tanaka F. // J. Chim. Phys. (Paris) 1996. V. 93. P. 880.
Лозинский В.И., Дамшкалн Л.Г., Шаскольский Б.Л., Бабушкина Т.А., Курочкин И.Н., Курочкин И.И. // Коллоид. журн. 2007. Т. 69. С. 798.
Лозинский В.И., Дамшкалн Л.Г., Курочкин И.Н., Курочкин И.И. // Коллоид. журн. 2008. Т. 70. С. 212.
Lozinsky V.I., Okay O. // Adv. Polym. Sci. 2014. V. 263. P. 49.
Подорожко Е.А., Ульябаева Г.Р., Тихонов В.Е., Кильдеева Н.Р., Лозинский В.И. // Коллоид. журн. 2020. Т. 82. С. 47.
Lozinsky V.I., Zubov A.L., Titova E.I. // Enzyme Microb. Technol. 1997. V. 20. P. 182.
Лозинский В.И., Савина И.Н. // Коллоид. журн. 2002. Т. 64. С. 372.
Zhou H., Shi T., Zhou X. // J. Biomater. Sci. – Polym. E. 2014. V. 25. P. 641.
Lozinsky V.I., Bakeeva I.V., Presnyak E.P., Damshkaln L.G., Zubov V.P. // J. Appl. Polym. Sci. 2007. V. 105. P. 2689.
Luo X., Akram M.Y., Yuan Y., Nie J., Zhu X. // J. Appl. Polym. Sci. 2018. V. 135. Article 46895.
Помогайло А.Д. // Успехи химии. 2000. Т. 69. С. 60.
Hench L.L., West J.K. // Chem. Rev. 1990. V. 90. P. 33.
Лозинский В.И., Сахно Н.Г., Дамшкалн Л.Г., Бакеева И.В., Зубов В.П., Курочкин И.Н., Курочкин И.И. // Коллоид. журн. 2011. Т. 73. С. 225.
Iler R.K. The Chemistry of Silica: Solubility, Polymerization, Colloid and Surface Properties, and Biochemistry. N.Y.: Wiley-Interscience, 1979.
Lipatov Y.S. // Adv. Polym. Sci. 1977. V. 22. P. 1.
Pan Y., Wang J., Pan C. // Micro Nano Lett. 2012. V. 7. P. 880.
Gonzalez J.S., Alvarez V.A. // J. Mech. Behav. Biomed. Mater. 2014. V. 34. P. 47.
Zhang C., Wang J., Chi R., Shi J., Yang Y., Zhang X. // Mater. Design. 2019. V. 183. Article 108166.
Hrouz J., Ilavsky M., Havliček J., Dušek K. // Collect. Czech. Chem. Comm. 1978. V. 43. P. 1999.
Guenet J.M. Thermoreversible Gelation of Polymers and Biopolymers. London: Academic Press, 1992.
Eldridge J.E., Ferry J.D. // J. Phys. Chem. 1954. V. 58. P. 992.
Hatakeyama T., Yamauchi A., Hatakeyama H. // Eur. Polym. J. 1987. V. 23. P. 361.
Hassan C.M., Peppas N.A. // Macromolecules. 2000. V. 33. P. 2472.
Auriemma F., De Rosa C., Triolo R. // Macromolecules. 2006. V. 39. P. 9429.
Домотенко Л.В., Лозинский В.И., Вайнерман Е.С., Рогожин С.В. // Высокомолек. соед. А. 1988. Т. 30. С. 1661.
Hatakeyema T., Uno J., Yamada C., Kishi A., Hatakeyama H. // Thermochim. Acta. 2005. V. 431. P. 144.
Lozinsky V.I., Domotenko L.V., Zubov A.L., Simenel I.A. // J. Appl. Polym. Sci. 1996. V. 61. P. 1991.
Dai L.X., Ukai K., Shaheen S.M., Yamaura K. // Polym. Int. 2002. V. 51. P. 715.
Shaheen S.M., Ukai K., Dai L.X., Yamaura K. // Polym. Int. 2002. V. 51. P. 1390.
Shaheen S.M., Yamaura K. // Polym. Adv. Technol. 2003. V. 14. P. 686.
Patachia S., Florea C., Freidrich C., Thomann Y. // eXPESS Polym. Lett. 2009. V. 3. P. 320.
Gusev D.G., Lozinsky V.I., Vainerman E.S., Bakhmutov V.I. // Magn. Res. Chem. 1990. V. 28. P. 651.
Mikhalev O.I., Serpinski M., Lozinsky V.I., Kapanin P.V., Chkheidze I.I., Alfimov M.V. // Cryo-Lett. 1991. V. 12. P. 197.
De Rosa C., Auriemma F., Di Girolamo R. // Adv. Polym. Sci. 2014. V. 263. P. 159.
Сергеев Г.Б., Батюк В.А. // Успехи химии. 1976. Т. 45. С. 793.
Watase M. // Nihon Kagaku Kaisi. 1983. P. 1254 (in Japanese).
Реми Г. Курс неорганической химии. Т. 1. М.: Изд-во Иностранной литературы. 1963. С. 528.
Yokoyama F., Masada I., Shimaura K., Ikawa T., Monobe K. // Colloid Polym. Sci. 1986. V. 264. P. 595.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал


