Коллоидный журнал, 2021, T. 83, № 2, стр. 179-186
Поверхностные свойства растворов дикатионных имидазолиевых ПАВ с короткими мостиковыми фрагментами
А. А. Котенко 1, С. Л. Хилько 1, *
1 Институт физико-органической химии и углехимии им. Л.М. Литвиненко
283114 Донецк-114, ул. Р. Люксембург, 70, Украина
* E-mail: sv-hilko@yandex.ru
Поступила в редакцию 22.07.2020
После доработки 07.09.2020
Принята к публикации 25.09.2020
Аннотация
Методами формы висячей капли и осциллирующей капли исследованы поверхностное натяжение и поверхностные дилатационные реологические характеристики водных растворов дикатионных имидазолиевых ПАВ с предельно короткими мостиковыми фрагментами на границе с воздухом. Показана высокая поверхностная активность таких ПАВ. Выявлены высокие значения дилатационного модуля вязкоупругости растворов ПАВ, которые возрастают с уменьшением длины мостикового фрагмента и увеличением длины углеводородных радикалов в молекуле ПАВ.
ВВЕДЕНИЕ
Димерные ПАВ представляют собой соединения, которые состоят из двух гидрофильных головных групп, двух гидрофобных “хвостов” и мостика (спейсера), который ковалентно связывает фрагменты дифильных молекул по полярным группам или вблизи этих групп [1–8]. Димерные ПАВ характеризуются свойствами, отличающимися от свойств их мономерных аналогов. Они обладают высокой поверхностной активностью на межфазных границах и низкими значениями критической концентрации мицеллообразования (ККМ), высокой способностью к образованию в растворе структур различной морфологии (сферические, эллипсоидальные, стержневидные и червеобразные мицеллы, а также везикулы спиральной или трубчатой формы), а также эффективной способностью к эмульгированию и солюбилизации [1–9]. Кроме того – это эффективные катализаторы в органической химии (мицеллярный катализ) [10–12], стабилизаторы наночастиц [3], средства доставки лекарственных препаратов и ДНК в клетки организмов [13, 14], а также антимикробные, противогрибковые агенты [15, 16] и ионные жидкости [17, 18]. Свойства димерных ПАВ определяют их экономическую эффективность и экологическую альтернативу мономерным ПАВ.
Свойства димерных ПАВ определяются природой всех составных частей молекул этих соединений. Головная гидрофильная часть может иметь положительный заряд (дикатионные ПАВ), отрицательный заряд (дианионные ПАВ) или не иметь заряда (неионогенные димерные ПАВ). Гидрофобные радикалы, в основном, представлены неразветвленными насыщенными алкильными цепями. В большинстве случаев димерные ПАВ имеют симметричное строение, но известны примеры и несимметричных димерных ПАВ, молекулы которых имеют гидрофобные цепи разной длины [1–8]. В значительной степени свойства димерных ПАВ определяются природой мостикового фрагмента. Мостик может быть гидрофильным или гидрофобным, жестким или гибким, что решающим образом влияет на свойства водных растворов димерных ПАВ [2, 6, 19].
Большое количество работ посвящено димерным ПАВ с полиметиленовыми мостиковыми фрагментами [1, 6, 8, 9]. При этом основное внимание уделялось влиянию длины спейсера на поверхностное натяжение растворов димерных ПАВ и их агрегационное поведение на примере углеводородных мостиков с числом метиленовых групп больше 4 [6, 20–25]. В работе [6] отмечается, что для димерных аммониевых ПАВ величина ККМ зависит от длины мостикового фрагмента. Так, при увеличении числа метиленовых звеньев от 2 до 6 величина ККМ может несколько увеличиваться, а при дальнейшем росте числа метиленовых звеньев до 10 и более величина ККМ снижается. Это связано с тем, что структура димерных ПАВ может существенно изменяться в зависимости от формы мостикового фрагмента. Возможен переход молекулы ПАВ с числом метиленовых групп в мостике 8–10 в форму “шпильки”. Когда число СН2-групп в мостиковом фрагменте превышает 10, он начинает сворачиваться так, что его средняя часть погружается внутрь мицеллы и это повышает гидрофобный эффект при мицеллообразовании [26]. В работе [27] оценивалось влияние длины полиметиленового спейсера на форму агрегатов на примере диимидазолиевых ПАВ с метильными углеводородными радикалами. Для этих ПАВ отмечены снижение ККМ с увеличением длины спейсера (от 4 до 10 СН2-групп) и возможность образования разнообразных агрегатов молекул в мицеллярной фазе.
Форма молекулярных агрегатов димерных ПАВ с предельно короткими жесткими мостиковыми фрагментами и длинными углеводородными радикалами на межфазной границе раствор–воздух не выявлена.
Дилатационным реологическим свойствам поверхности растворов различных димерных ПАВ с разными мостиковыми фрагментами посвящено ограниченное число работ [6, 28–35], а применительно к растворам диимидазолиевых ПАВ с предельно короткими полиметиленовыми мостиковыми фрагментами эти свойства вообще не изучены.
Целью работы было исследование поверхностного натяжения водных растворов диимидазолиевых ПАВ с углеводородными радикалами разной длины и короткими метиленовыми мостиковыми фрагментами и дилатационных реологических характеристик их поверхностных слоев методами динамической тензиометрии и дилатационной реометрии.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе исследованы свойства межфазных слоев дикатионных имидазолиевых ПАВ с алкильными радикалами СnН2n+ 1 (n = 10–16) и мостиковыми фрагментами с числом метиленовых групп (m) от 2 до 4.
Вещества были синтезированы по усовершенствованной общей схеме, приведенной в работах [36–38]. Идентификацию и определение степени чистоты полученных соединений осуществляли методом 1Н ЯМР (спектры записаны на спектрометре Bruker Avance II (9.4 Тл) в D2O). Общая формула таких ПАВ приведена на рис. 1.
Рис. 1.
Общая формула дикатионных имидазолиевых ПАВ (дибромиды 1,3-бис(3'-алкилимидазолий-1'-ил)-2-алканов). n = 10, 12, 14, 16; m = 2, 3, 4.
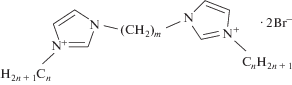
Поверхностное натяжение (γ, мН/м) водных растворов имидазолиевых ПАВ при постоянной (фиксированной) концентрации в зависимости от времени жизни поверхности (t, с) измеряли методом формы висячей капли (тензиометр PAT-2P SINTERFACE Technologies, Германия).
Дилатационные реологические характеристики поверхностных слоев растворов имидазолиевых солей изучали на тензиометре PAT-2Р. В этих экспериментах после достижения адсорбционного равновесия в системе ((5–7) × 104 с с момента формирования капли) осуществляются гармонические осцилляции капли (площадью A, объема V). Принцип работы тензиометра PAT-2P (включая дилатационную реометрию) детально описан в работах [39, 40]. При варьировании частоты осцилляции капли f от 0.005 до 0.5 Гц использовали амплитуду осцилляций 6%. Результаты экспериментов с гармоническими осцилляциями капли анализировали с помощью преобразования Фурье, используя программное обеспечение тензиометра [39, 40]:
Дилатационный модуль E характеризует вязкоупругие свойства поверхностных слоев ПАВ и учитывает все релаксационные процессы, влияющие на поверхностное натяжение.
Модуль E выражается комплексным числом и включает реальную и мнимую компоненты: $Е(i\Omega ) = {{E}_{{\text{r}}}} + i{{E}_{{\text{i}}}}$ (i – мнимая единица). Реальная часть Еr (модуль упругости) отражает накопление энергии, а мнимая часть Еi – потери энергии в поверхностном слое вследствие релаксационных процессов. Выражения для модуля вязкоупругости E и фазового угла ϕ (характеризует запаздывание изменения поверхностного натяжения при изменении площади поверхности капли) имеют следующий вид [39, 40]:
Растворы ПАВ готовили в очищенной воде (Milli-Q), имеющей поверхностное натяжение 72.0 ± 0.2 мН/м, которое не изменялось во временнóм интервале до 105 с (около 28 ч).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Исследование тензиометрических характеристик включало измерения динамического (γd) и равновесного (γe) поверхностного натяжения растворов дикатионных имидазолиевых ПАВ на границе с воздухом, расчет ККМ и определение величины γmin по экспериментальным зависимостям γe= f(СПАВ). Были рассчитаны величины адсорбции на границе фаз раствор ПАВ–воздух по известному уравнению Гиббса
В случае полной диссоциации димерных ПАВ n = 3. Однако, как следует из данных, приведенных в работах [6, 33], возможна неполная диссоциация димерных ПАВ и величина n может быть равной 2. Величина n определяется природой поверхностно-активного иона и противоиона, а также концентрацией ПАВ в растворе. При расчете величины Г в работе было использовано значение n = 3.
На рис. 2 приведены зависимости γе = f (СПАВ), откуда ожидаемо следует, что чем длиннее углеводородный радикал, тем ниже равновесное поверхностное натяжение растворов ПАВ.
Рис. 2.
Зависимости равновесного поверхностного натяжения γе от концентрации растворов дикатионных имидазолиевых ПАВ с мостиковым фрагментом с m = 2 и различной длиной углеводородного радикала n: 1 – 10, 2 – 12, 3 – 14, 4 – 16.
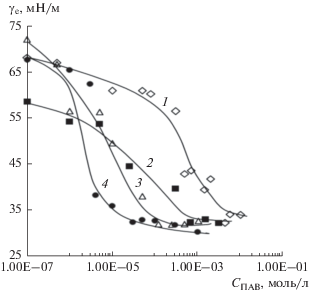
Как следует из рис. 3, изменение размера мостикового фрагмента слабо влияет на величину поверхностного натяжения. В табл. 1 приведены характеристики растворов дикатионных имидазолиевых ПАВ с разной длиной углеводородного радикала и предельно короткими мостиковыми фрагментами.
Рис. 3.
Зависимости равновесного поверхностного натяжения γе от концентрации растворов дикатионных имидазолиевых ПАВ с углеводородными радикалами с n = 16 и различной длиной мостикового фрагмента m: 1 – 2, 2 – 3, 3 – 4.

Таблица 1.
Характеристики растворов дикатионных имидазолиевых ПАВ общей формулы [СnН2n+ 1 ·· Im+(СН2)mIm+СnН2n+ 1] · 2Вr– с разным числом атомов C в углеводородных радикалах (n) и в мостиковом фрагменте (m), Im+ – катион имидазолия
| № п/п | ПАВ | ККМ, моль/л | γmin, мН/м | Гmах, моль/м2 | Еmаx, мН/м |
|---|---|---|---|---|---|
| 1 | n = 10, m = 2 | 3.8 × 10–3 | 32 | 0.42 × 10–6 | 24 |
| 2 | n = 10, m = 3 | 5.4 × 10–3 | 33 | 0.39 × 10–6 | 22 |
| 3 | n = 10, m = 4 | 5.1 × 10–3 | 33 | 0.52 × 10–6 | 20 |
| 4 | n = 12, m = 2 | 3.9 × 10–4 | 32 | 0.52 × 10–6 | 68 |
| 5 | n = 12, m = 3 | 5.0 × 10–4 | 33 | 0.41 × 10–6 | 55 |
| 6 | n = 12, m = 4 | 5.2 × 10–4 | 33 | 0.47 × 10–6 | 45 |
| 7 | n = 14, m = 2 | 5.2 × 10–5 | 32 | 0.49 × 10–6 | 79 |
| 8 | n = 14, m = 3 | 5.1 × 10–5 | 35 | 0.49 × 10–6 | 76 |
| 9 | n = 14, m = 4 | 5.6 × 10–5 | 35 | 0.64 × 10–6 | 46 |
| 10 | n = 16, m = 2 | 3.5 × 10–6 | 30 | 0.91 × 10–6 | 128 |
| 11 | n = 16, m = 3 | 3.2 × 10–6 | 32 | 0.49 × 10–6 | 105 |
| 12 | n = 16, m = 4 | 3.5 × 10–6 | 35 | 0.49 × 10–6 | 89 |
Отчетливо прослеживается зависимость ККМ от длины углеводородного радикала ПАВ. Величина ККМ уменьшается примерно на порядок при увеличении длины углеводородного радикала на две СН2‑группы. Эти результаты согласуются с данными, приведенными в работах [6, 36, 38, 41], где исследованы диимидазолиевые и дипиримидиновые ПАВ с мостиковыми фрагментами разной длины, в том числе пропиленовыми, и различным числом атомов углерода в углеводородном радикале (n = 8, 10, 12).
Величины ККМ растворов ПАВ неоднозначно изменяются при увеличении числа метиленовых групп в мостиковом фрагменте от 2 до 4 – они могут немного увеличиваться при изменении длины спейсера (при n = 10–14) или оставаться практически неизменными (при n = 16). Зависимости минимального поверхностного натяжения (γmin) и величины адсорбции (Гmах) от параметров n и m для этих ПАВ не наблюдаются, величины γmin для всех образцов находятся в диапазоне 32–35 мН/м, а величины Гmах – в диапазоне (0.39–0.64) × × 10–6 моль/м2. Для ПАВ с n = 16 и m = 2 величина Гmах = 0.91 × 10–6 моль/м2, а значение γmin несколько ниже, чем для других ПАВ, γmin = = 30 мН/м.
Для получения дополнительной информации об особенностях формирования адсорбционного слоя ПАВ на границе раствор–воздух, наряду с тензиометрией, широко используется метод дилатационной реологии, который более чувствителен к взаимодействиям между адсорбированными молекулами. Информация о динамических процессах адсорбции/десорбции на межфазных границах, полученная методом дилатационной реологии, позволяет судить о структурных особенностях адсорбционных слоев [42, 43]. Кроме того, дилатационные реологические характеристики позволяют прогнозировать свойства дисперсных систем, например, стабильность эмульсий и пен [44–46].
Согласно данным, приведенным на рис. 4, величины модулей вязкоупругости, Е, и упругости, Еr, возрастают при увеличении частоты осцилляции капли. Модуль Еi незначительно возрастает, а величина фазового угла (ϕ) уменьшается с ростом частоты осцилляции капли для всех ПАВ, при этом величины Еi и ϕ находятся в диапазоне меньше 20–30 ед. Близкие значения параметров E и Еr и низкие значения величин Еi и ϕ характеризуют адсорбционные слои этих ПАВ как упругие.
Рис. 4.
Зависимости модуля вязкоупругости Е (1–4) и его реальной компоненты Еr (5–8) от частоты осцилляции капель растворов дикатионных имидазолиевых ПАВ с постоянным размером мостикового фрагмента (m = 2) и различной длиной углеводородного радикала n: 1, 5 – 10, 2, 6 – 12, 3, 7 – 14, 4, 8 – 16. СПАВ = 10–5 моль/л.

На рис. 5 приведены зависимости модулей вязкоупругости и упругости от частоты осцилляции капли для дикатионных имидазолиевых ПАВ при различной длине мостикового фрагмента и постоянном размере углеводородного радикала (n = 16) и выбранной концентрации раствора ПАВ (СПАВ = 10–5 моль/л). Рост частоты осцилляции приводит к увеличению значений E и Еr. Прослеживается отчетливая зависимость реологических параметров от числа метиленовых групп в мостиковом фрагменте. Для дикатионного ПАВ с m = 2 при частоте осцилляции капли f = 0.5 Гц модули E и Еr достигают максимальных значений, 128 и 126 мН/м соответственно. Величины модулей E и Еr для ПАВ с m = 4 при увеличении частоты осцилляции капли изменяются незначительно, а для ПАВ с m = 3 зависимости E и Еr от f занимают промежуточное положение между соответствующими зависимостями для ПАВ с m = 4 и m = 2.
Рис. 5.
Зависимости модуля вязкоупругости Е (1–3) и его реальной компоненты Еr (4–6) от частоты осцилляции капель растворов дикатионных имидазолиевых ПАВ с постоянным размером углеводородного радикала (n = 16) и различной длиной мостикового фрагмента m: 1, 4 – 2, 2, 5 – 3, 3, 6 – 4. СПАВ = 10–5 моль/л.

Характер зависимостей модуля вязкоупругости от концентрации ПАВ с разными углеводородными радикалами и постоянной длиной мостикового фрагмента (m = 2) существенно различается (рис. 6). Зависимости E = f(СПАВ) для ПАВ с n = 10 и 12 являются убывающими функциями, тогда как для ПАВ с n = 14 и 16 – это возрастающие функции.
Рис. 6.
Зависимости модуля вязкоупругости E при f = 0.1 Гц от концентрации растворов дикатионных имидазолиевых ПАВ с постоянным размером мостикового фрагмента (m = 2) и различной длиной углеводородного радикала n: 1 – 10, 2 – 12, 3 – 14, 4 – 16.
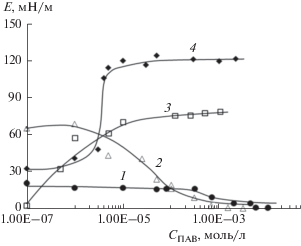
Согласно данным, приведенным на рис. 7, уменьшение количества метиленовых групп в мостиковом фрагменте дикатионных имидазолиевых ПАВ от 4 до 2 при постоянной длине углеводородного радикала (n = 16) приводит к заметному росту значений модуля вязкоупругости.
Рис. 7.
Зависимости модуля вязкоупругости E при f = 0.1 Гц от концентрации растворов дикатионных имидазолиевых ПАВ с постоянным размером углеводородного радикала (n = 16) и различной длиной мостикового фрагмента m: 1 – 2, 2 – 3, 3 – 4.

Такие различия в реологических свойствах дикатионных ПАВ с короткими мостиками могут быть связаны с разным влиянием обменных процессов между поверхностным слоем и объемом раствора.
Сопоставление реологических характеристик растворов дикатионных ПАВ с разной длиной углеводородного радикала (n = 12–16) и пропиленовыми мостиками показало, что в случае, если мостиковые фрагменты модифицированы оксимной группой, то модуль вязкоупругости адсорбционных слоев таких ПАВ выше, чем для ПАВ с немодифицированными спейсерами (рис. 8).
Рис. 8.
Зависимости модуля вязкоупругости E при f = 0.1 Гц от концентрации растворов дикатионных имидазолиевых ПАВ с постоянным размером мостикового фрагмента (m = 3) и различной длиной углеводородного радикала n: 1, 4 – 12, 2, 5 – 14, 3, 6 – 16; 1–3 – ПАВ с метиленовыми мостиковыми фрагментами, 4–6 – ПАВ с оксимными мостиковыми фрагментами.

Сравнение данных, приведенных на рис. 8 и в табл. 1 и 2 для растворов ПАВ с разной длиной углеводородного радикала и мостиковыми фрагментами, модифицированными оксимной группой (m = 3), показало, что для них значения модуля вязкоупругости ближе к значениям для ПАВ с этиленовыми мостиками, чем к значениям для ПАВ с пропиленовыми мостиками.
Таблица 2.
Экспериментальные значения максимального модуля вязкоупругости (Еmаx при f = 0.1 Гц) для некоторых димерных ПАВ
| № п/п | ПАВ | Еmаx, мН/м |
|---|---|---|
| 1 | [С16Н33Im+СН2(С=N–ОН)СН2Im+С16Н33] · 2Сl– 1,3-бис(3'-цетилимидазолий-1'-ил)-2-оксиминопропана дихлорид, n = 16, m = 3 [28] |
120 |
| 2 | [С14Н29Im+СН2(С=N–ОН)СН2Im+С14Н29] · 2Сl– 1,3-бис(3'-тетрадецилимидазолий-1'-ил)-2-оксиминопропана дихлорид, n = 14, m = 3 |
85 |
| 3 | [С12Н25Im+СН2(С=N–ОН)CН2Im+С12Н25] · 2Сl– 1,3-бис(3'-додецилимидазолий-1'-ил)-2-оксиминопропана дихлорид, n = 12, m = 3 |
80 |
| 4 | [C12Н25(СН)3N+(СН2)2N+(СН)3C12Н25] · 2Br–, n = 12, m = 2 1,2-этан-бис(диметилдодециламмония) дибромид [29] |
65 |
| 5 | Смесь желатина и [C12Н25Im+(СН2)4Im+C12Н25] · 2Br– [30] | 100 |
| 6 | [С12Н25N+(СН2СН2ОН)2(СН2)3(СН2СН2ОН)2N+С12Н25] · 2Br– 1,3-пропан-бис[ди(2-гидроксилэтил)додециламмония] дибромид [31] |
55 |
| Бетаины: | ||
| 7 | СН3(СН2)14СН2O(СН2СН2О)3СН2СH(ОН)СН2N+(СН3)2СН2СОО– [32] | 80 |
| 8 | [СН3(СН2)6СН2]2СНСН2ОСН2СH(ОН)CН2N+(СН3)2СН2СОО– [32] | 100 |
В работах [47–49] было отмечено, что сравнительно небольшие изменения в строении молекул имидазолиевых солей могут оказывать существенное влияние на свойства их агрегатов в растворах и поведение таких ПАВ на границе фаз. Влияние гибридизации атома углерода в составе мостикового фрагмента на строение и свойства дикатионных имидазолиевых солей в растворах было отмечено в работах [1, 19]. В молекулах дикатионных оксимов присутствуют sp2- и sp3‑гибридизованные атомы углерода, что придает мостиковым фрагментам дополнительную жесткость, возможность образования внутримолекулярной водородной связи и, в силу этого, вероятно, уменьшения его длины по сравнению с немодифицированным пропиленовым мостиком.
Таким образом, отчетливо прослеживается влияние размера мостикового фрагмента на дилатационные реологические характеристики адсорбционных слоев дикатионных имидазолиевых ПАВ.
Значение модуля вязкоупругости для дикатионных имидазолиевых ПАВ с метиленовым мостиковым фрагментом m = 2 и углеводородным радикалом с n = 16 превышает значения Еmаx для некоторых дикатионных ПАВ, выбранных в качестве примеров (табл. 2). При этом были использованы литературные данные и данные, полученные для дикатионных оксимов с углеводородными радикалами n = 12 и 14 при m = 3.
Можно отметить близкие значения Еmаx для дикатионных имидазолиевого (68 мН/м) и аммонийного (65 мН/м) ПАВ с одинаковыми значениями n = 12 и m = 2 (образцы 4 в табл. 1 и 2).
Высокие значения модуля вязкоупругости для димерных ПАВ могут быть связаны со способностью их молекул к образованию прочных адсорбционных слоев. Известно, что свойства адсорбционных пленок ПАВ определяются не только концентрацией молекул в поверхностном слое, но и их строением и расположением молекул на межфазной поверхности. Согласно данным, приведенным в табл. 2, разветвленные гидрофобные алкильные заместители бетаиновых молекул способны усиливать межмолекулярные взаимодействия в адсорбционном слое и, тем самым, способствовать росту динамического модуля вязкоупругости, причем увеличение размеров углеводородных радикалов приводит к значительному росту Еmаx (образцы 7 и 8) [33].
ЗАКЛЮЧЕНИЕ
Методом формы висячей капли исследованы динамическое и равновесное поверхностное натяжение водных растворов дикатионных имидазолиевых солей (дибромидов 1,3-бис(3'-алкилимидазолий-1'-ил)-2-алканов) на границе с воздухом.
Показано, что ККМ этих ПАВ уменьшается примерно на порядок при увеличении длины углеводородного радикала на две СН2‑группы. Эти результаты согласуются с литературными данными. Четких зависимостей значений ККМ, γmin, Гmах от длины мостикового фрагмента не выявлено.
Методом формы осциллирующей капли исследованы дилатационные реологические свойства адсорбционных слоев дикатионных имидазолиевых ПАВ на границе фаз водный раствор–воздух. Установлены зависимости модуля вязкоупругости от частоты осцилляций поверхности капли для растворов дикатионных ПАВ.
Выявлена отчетливая зависимость модуля вязкоупругости от размера мостикового фрагмента диимидазолиевых ПАВ. Поверхностная вязкоупругость растворов таких ПАВ зависит и от длины углеводородного радикала. ПАВ с m = 2 и n = 16 характеризуется высоким значением модуля вязкоупругости (Emax = 128 мН/м), который превышает величины Emax, характерные для некоторых дикатионных ПАВ.
Список литературы
Menger F.M., Keiper J. // Angew. Chem. Int. Ed. 2000. V. 39. P. 1906.
Menger F.M., Keiper J.S., Azov V. // Langmuir. 2000. V. 16. P. 2062.
Hait S.K., Moulik S.P. // Current Sci. 2002. V. 82. P. 1101.
Sekhon B.S. // Resonance. 2004. V. 9. № 3. P. 42.
Kamal M. S. // J. Surfact. Deterg. 2016. V. 19. P. 23.
Zana R. // J. Colloid Interface Sci. 2002. V. 248. P. 203.
Menger F., Mbadugha B.N. // J Am. Chem. Soc. 2001. V. 123. P. 875.
Menger F.M., Littau C.A. // J. Am. Chem. Soc. 1993. V. 115. P. 10 083.
Menger F.M., Littau C.A. // J. Am. Chem. Soc. 1991. V. 113. P. 1451.
Zakharova L.Ya., Mirgorodskaya A.B., Zhiltsova E.P., Kudryavtseva L., Konovalova A. // Molecular Encapsulation: Organic Reactions in Constrained Systems / Ed. by Brinker U.H., Mieusset J.-L. New-York: Wiley, 2010. P. 397.
Milton M.D., Garg P. // Appl. Organomet. Chem. 2016. V. 30. P. 727.
Прокопьева Т.М., Капитанов И.В., Белоусова И.А., Шумейко А.Е., Кострикин М.Л., Туровская М.К., Разумова Н.Г., Попов А.Ф. // Журн. орг. химии. 2015. Т. 51. С. 1105.
Sharma R., Kamal A., Abdinejad M., Mahajan R.K., Kraatz H.-B. // Adv. Colloid Interface Sci. 2017. V. 248. P. 35.
Mirgorodskaya A.B., Zakharova L.Ya., Khairutdinova E.I., Lukashenko S.S., Sinyashin O.G. // Colloids Surf. A. 2016. V. 510. P. 33.
Wettig S.D., Wang C., Verrall R.E., Foldvari M. // Phys. Chem. Chem. Phys. 2007. V. 7. P. 871.
Sheikh M.S., Khanam A.J., Matto R.H., Kabir-ud-Din // J. Surfact. Deterg. 2013. V. 16. P. 503.
Fatma N., Panda M., Kabir-ud-Din, Beg M. // J. Mol. Liq. 2016. V. 222. P. 390.
Dong K., Liu X.M., Dong H.F., Zhang X.P., Zhang S.J. // Chem. Rev. 2017. V. 117. P. 6636.
Hayes R., Warr G.G., Atkin R. // Chem. Rev. 2015. V. 115. P. 6357.
Sood R., Alakoskela J.-M., Sood A., Vitovi P., Kinnunen P.K.J. // J. Appl. Sol. Chem. Model. 2012. V. 1. P. 13.
Anderson J.L., Ding R.F., Ellern A., Armstrong, D.W. // J. Am. Chem. Soc. 2005. V. 127. P. 593.
Frizzo C.P., Gindri I.M., Bender C. R., Tier A.Z., Villetti M.A., Rodrigues D.C., Machado G., Martins M.A.P. // Colloids Surf. A. 2015. V. 468. P. 285.
Hennemann B.L., Bender C.R., Salbego P.R.S., Meyer A.R., Belladonna A.L., Zanatta N., Bonacorso H.G., Villetti M.A., Martins M.A.P., Frizzo C.P. // J. Mol. Liq. 2018. V. 252. P. 184.
Moosavi M., Khashei F., Sharifi A., Mirzaei M. // J. Chem. Thermodyn. 2017. V. 107. P. 1.
Marullo S., Rizzo C., Dintcheva N.T., Giannici F., D’Anna F. // J. Colloid Interface Sci. 2018. V. 517. P. 182.
Холмберг К., Йёнссон Б., Кронберг Б., Линдман Б. Поверхностно-активные вещества и полимеры в водных растворах. М.: БИНОМ, 2007.
Frizzo C.P., Gindri I.M., C.R. Bender, Tier A.Z., Villetti M.A., Rodrigues D.C., Machado G., Martins M.A.P. // Colloids Surf. A. 2015. V. 468. P. 285.
Хилько С.Л., Котенко А.А., Гребенюк С.А., Заречная О.М., Михайлов В.А. // Коллоид. журн. 2019. Т. 81. С. 344.
Wu D., Feng Y., Xu G., Chena Y., Cao X., Li Y. // Colloids Surf. A. 2007. V. 299. P. 117.
Ao M., Xu G., Kang W., Meng L., Gonga H., Zhoua T. // Soft Matter. 2011. V. 7. P. 1199.
Pei X., Zhang Q., Liu Zh., Song B., Li R., Zhao J., Cui Z. // Colloid Polym. Sci. 2016. V. 294. P. 1405.
Zhou Zh., Ma D.-Sh., Zhang Q., Wang H.-Zh., Zhang L., Luan H., Zhu Y., Zhang L. // Colloids Surf. A. 2018. V. 538. P. 739.
Acharya D.P., Gutiérrez J.M., Aramaki K., Aratani K., Kunieda H. // J. Colloid Interface Sci. 2005. V. 291. P. 236.
Cao X.L, Feng J., Guo L.L., Zhu Y., Zhang L., Zhang L., Luo L., Zhao S. // Colloids Surf. A. 2016. V. 490. P. 41.
Liu X.P., Feng J., Zhang L., Zhao S., Yu J. // Acta Phys.-Chim. Sin. 2010. V. 26. P. 1277.
Ao M., Huang P., Xu G., Yang X., Wang Y. // Colloid Polym. Sci. 2009. V. 287. P. 395.
Ao M., Xu G., Zhu Y., Bai Y. // J. Colloid Interface Sci. 2008. V. 326. P. 490.
Ren C., Wang F., Zhang Z., Nie H., Li N., Cui M. // Colloids Surf. A. 2015. V. 467. P. 1.
Loglio G., Pandolfini P., Miller R., Makievski A.V., Ravera F., Ferrari M., Liggieri L. Novel Methods to Study Interfacial Layers. Amsterdam: Elsevier, 2001.
Zholob S.A., Makievski A.V., Miller R., Fainerman V.B. // Adv. Colloid Interface Sci. 2007. V. 322. P. 134.
Hao J., Wang P., Zhang Y., Zhang Y. // J. Surfact. Deterg. 2016. V. 19. P. 915.
Miller R., Fainerman V.B., Makievski A.V., Kragel J., Grigoriev D.O., Kazakov V.N., Sinyachenko O.V. // Adv. Colloid Interface Sci. 2000. V. 86. P. 39.
Murray B.S., Dickinson E. // Food Sci. Technol. Int. 1996. V. 2. P. 131.
Aksenenko E.V., Kovalchuk V.I., Fainerman V.B., Miller R. // Adv. Colloid Interface Sci. 2006. V. 122. P. 57.
Ducel V., Richard J., Popineau Y., Boury F. // Biomacromolecules. 2004. V. 5. P. 2088.
Miller R., Alahverdjieva V.S., Fainerman V.B. // Soft Matter. 2008. V. 4. P. 1141.
Singh T., Kumar A. // J. Phys. Chem. B. 2007. V. 12. P. 7843.
Shi L., Zheng L. // J. Phys. Chem. B. 2012. V. 116. P. 2162.
Frizzo C.P., Bender C.R., Gindri I.M., Villetti M.A., Machado G., Bianchi O., Martins M.A.P. // J. Phys. Chem. C. 2016. V. 120. P. 14 402.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал


