Коллоидный журнал, 2022, T. 84, № 2, стр. 213-227
Вязкость и теплопроводность наножидкостей кобальта и диоксида кремния в оптимальной смеси глицерина и воды
T. R. Prasad 1, K. R. Krishna 2, K. V. Sharma 1, N. Mantravadi 2, *
1 Center for Energy Studies, JNTUH College of Engineering
Hyderabad, India
2 Department of Mechanical Engineering, Koneru Lakshmaiah Education Foundation
Vaddeswaram, India
* E-mail: nageshsarma@kluniversity.in
Поступила в редакцию 02.06.2021
После доработки 15.12.2021
Принята к публикации 23.12.2021
- EDN: ZZXEJB
- DOI: 10.31857/S0023291222020094
Аннотация
Исследованы смеси глицерина и воды для использования в качестве базовой жидкости с оптимальным по вязкости весовым соотношением компонентов. Наночастицы кобальта диаметром 80 нм и диоксида кремния диаметром 50 нм были диспергированы в выбранной базовой жидкости. Получены стабильные наножидкости без использования ПАВ с максимальной объемной концентрацией кобальта и диоксида кремния 0.18 и 0.675% соответственно. Стабильность наножидкостей оценивали по величине дзета-потенциала наночастиц. Показано, что для максимальной концентрации наночастиц в наножидкостях с кобальтом и диоксидом кремния при температуре 70°C имеет место повышение пиковой теплопроводности на 16.4 и 31.5% по сравнению с базовой жидкостью. Также в этих дисперсиях при максимальной концентрации частиц при 30°С получено увеличение вязкости на 13.1 и 47.4% по сравнению с базовой жидкостью. Рост теплопроводности для кобальтовых наножидкостей более значителен при выбранной концентрации и температуре, тогда как наножидкости диоксида кремния показывают более существенное возрастание вязкости. Согласно коэффициенту улучшения свойств, наножидкости на основе смеси глицерин–вода лучше заменяют традиционные жидкости-теплоносители.
ОБОЗНАЧЕНИЯ
BF Базовая жидкость
G Глицерин
K Теплопроводность
M Молекулярная масса базовой жидкости
m Масса
N Число Авогадро
T Температура
U Погрешность
Греческие символы
µ Вязкость
ϕ Весовая доля
ψ Объемный процент
φ Объемная доля
ρ Плотность
Индексы
bf Базовая жидкость
nf Наножидкость
p Наночастица
R Отношение
1. ВВЕДЕНИЕ
Такие жидкости как вода, этиленгликоль, глицерин широко используют для переноса тепла в различных устройствах. Системы достигли предела своей эффективности, поэтому исследования направлены на создание новых жидкостей для теплопередачи. Одно из направлений заключается в создании “наножидкостей”, которые представляют собой стабильные дисперсии твердых наноразмерных частиц в подходящей базовой жидкости, демонстрирующие более высокую скорость теплопередачи по сравнению с традиционными жидкостями. Основные, решаемые исследователями в настоящее время задачи связаны с определением свойств наножидкостей в различных базовых жидкостях, изучением влиянии состава материалов, размера частиц, рабочей температуры, стабильности наножидкостей для использования в широком спектре теплообменных устройств. Ранние исследования были, в основном, направлены на определение таких свойств наножидкостей на водной основе, как плотность, вязкость, теплопроводность и удельная теплоемкость. Отметим, что из-за низкой температуры кипения воды, наножидкости на водной основе можно использовать только для применения в теплообменниках при температурах ниже 100°C. При добавлении этиленгликоля к воде, снижается температура замерзания и повышается температура кипения композиции, что позволяет использовать составы на основе этиленгликоля в более широком диапазоне температур. Например, 40 об. % смесь этиленгликоля с водой имеет температуру замерзания – 23.5°С и точку кипения 104.4°С. Поэтому на территориях с отрицательными температурами окружающей среды, в автомобильных радиаторах используют водный раствор этиленгликоля. Поскольку этиленгликоль имеет более высокую вязкость, чем вода, смесь также более вязкая [1]. Таким образом, использование смеси в качестве базовой жидкости повышает кинетическую стабильность наножидкости, поскольку движение наночастиц подвергается воздействию силы вязкого трения, что замедляет их седиментацию [2].
Талиб и др. [3] исследовали теплопроводность и вязкость наножидкостей SiO2 в различных смесях базовых жидкостей этиленгликоля и воды с различным соотношениях компонентов по объему, таким как, 40 : 60, 50 : 50 и 60 : 40. Интересно отметить рост теплопроводности и уменьшения вязкости при снижении содержания этиленгликоля в смеси. Это можно связать с влиянием вязкости базовой жидкости на броуновское движение наночастиц, поскольку увеличение вязкости замедляет хаотичное движение частиц в наножидкости. Джанг и Чой [4], исследовавшие влияние броуновского движения на наночастицы на наноуровне, пришли к выводу, что броуновская активность отвечает за высокий уровень теплопроводности в наножидкостях. Поскольку этиленгликоль более вязкий, чем вода, увеличение количества этиленгликоля в смеси снижает броуновское движение взвешенных частиц, замедляя теплоперенос. Акилу и др. [5] предложили аналогичное объяснение снижению теплопроводности из-за увеличения вязкости базовой жидкости. Ваэли и др. [6] исследовали несоответствие теплофизических характеристик и стабильности трех типов наножидкостей с использованием частиц SiC в качестве дисперсной фазы. Воду, 35% водные растворы этиленгликоля и пропиленгликоля использовали в качестве базовых жидкостей. При добавлении 0.5% SiC к базовым жидкостям плотность и вязкость тестируемых наножидкостей возрастали. В исследуемом диапазоне температур не было выявлено существенного различия в теплопроводности этих трех наножидкостей. SiC в гликолевых дисперсиях более стабилен, чем SiC, диспергированный в воде. Эти данные показывают, что увеличение вязкости базовой жидкости улучшает стабильность наножидкостей.
Глицерин является потенциальной заменой этиленгликоля из-за его более низкой стоимости, более широкого диапазона рабочих температур и экологичности. Безводный глицерин не летуч в атмосферных условиях, а давление паров практически равно нулю. При низких температурах он обладает высокой вязкостью и более низкой теплопроводностью, чем вода [5, 7]. Однако исследования с глицерином в качестве базовой жидкости очень ограничено представлены в литературе. Акилу и др. [5] анализировали теплопроводность и распределение SiO2, диспергированного в этиленгликоле и глицерине, в диапазоне концентраций 0.5–2.0 об.% и диапазоне температур 30–80°С. Результаты показывают, что с ростом концентрации и температуры теплопроводность увеличивается. Для наножидкости с 2.0 об. % концентрацией SiO2 в базовых жидкостях этиленгликоля и глицерина при 60°C, сообщается о максимальном увеличение теплопроводности на 6.1 и 11.5% соответственно, по сравнению с базовой жидкостью. Реологические результаты показывают, что обе наножидкости являются ньютоновскими в диапазоне рабочих условий. Падение вязкости для SiO2 было более существенным в глицерине, чем в этиленгликоле, примерно на 95 и 80% соответственно. Согласно выводам авторов, увеличение теплопроводности частиц SiO2 больше в этиленгликоле, чем в глицерине при выбранной температуре. По мнению авторов, глицерин более вязкий и препятствует броуновскому движению дисперсных частиц SiO2, замедляя передачу тепловой энергии.
Шарифпур и др. [7] провели эксперименты по определению теплопроводности в диапазоне температур от 20 до 45°C наножидкости Al2O3 на основе глицерина. В экспериментах использовали частицы с различными диаметрами 31, 55 и 134 нм. Наножидкости с частицами меньшего диаметра продемонстрировали значительное увеличение теплопроводности из-за дополнительных прямых столкновений более мелких частиц в базовой жидкости. Рост теплопроводности на 19.5% был зафиксирован для жидкости с 4 об. % наночастиц Al2O3 размером 31 нм. Температура практически не влияет на коэффициент теплопроводности, однако Акилу и др. [5] обнаружили, что коэффициент теплопроводности растет с температурой. Авторы предполагают, что коэффициент теплопроводности полностью определяется материалами, используемыми для приготовления наножидкости. Чиманга и др. [8] сообщают, что коэффициент теплопроводности линейно увеличивается с объемной долей наночастиц MgO при выбранной температуре. Исследователи использовали частицы размерами 21.1, 103.7 и 123.7 нм. По их данным, повышение теплопроводности сильнее для частиц меньшего размера, что согласуется с исследованиями Шарифпура и др. [7]. Отмечается максимальное увеличение примерно на 19% при объемной доле 0.04 для наночастиц MgO в глицерине. Согласно данным Шарифпура и др. [7], коэффициент теплопроводности остается стабильным при изменении температуры. Назарабад и др. [9] исследовали влияние структуры частиц на транспортные характеристики наножидкости оксида вольфрама в глицерине. Частицы многоугольной формы приводят к более высокому увеличению вязкости, чем сферические частицы. Этот результат объясняется тем, что суспензии полигональных вытянутых частиц имеют более высокую вязкость из-за структурно ограниченного броуновского движения. Также отмечается, что наножидкости, содержащие сферические частицы, имеют наиболее значительное увеличение теплопроводности, за счет большего отношения поверхности к объему, по сравнению с другими формами частиц. Частицы с большим отношением поверхности к объему могут инициировать межфазные эффекты на поверхности, что повышает эффективность теплопроводности наножидкости.
Гохаршади и др. [10] исследовали реологию наножидкостей на основе глицерина с квантовыми точками графена при различных концентрациях. К своему удивлению, авторы обнаружили, что увеличение концентрации снижает вязкость наножидкости. Было высказано предположение, что это происходит из-за того, что квантовые точки графена действуют как смазка после диспергирования в глицерине. Сообщается, что добавление графеновых квантовых точек размером 20 нм снижает вязкость глицерина на 49.97% при концентрации 2.0 об. %. Акилу и др. [11] измеряли вязкость и теплопроводность наножидкости диоксида кремния в соотношении смеси глицерин/этиленгликоль 60:40 при концентрации частиц от 1.0 до 4.0 об. % в диапазоне температур 20–80°C. Обнаружено линейное увеличение коэффициента теплопроводности с температурой, которое авторы связали с усилением броуновского движения частиц в жидкости.
Для улучшения теплопроводности с температурой Назарабад и др. [9] использовали аналогичный подход для наножидкостей с оксидом вольфрама. Заметное увеличение теплопроводности происходит при повышенных температурах с наибольшим значением в 13% при 4 об. % оксида вольфрама и 60°С. Другие исследователи наблюдали характерное увеличение вязкости с концентрацией частиц и постоянство вязкости при различных температурах [5]. Рост вязкости при увеличении концентрации SiO2 от 1.0 до 4.0 об. % составил около 85%, в температурном диапазоне от 20 до 80°C. Харикришнан и др. [12] оценили теплофизические свойств наножидкостей на основе водно-глицериновой смеси, содержащих частицы CuO. В качестве базовой жидкости использовали смесь глицерина с водой в соотношении 20 : 80 по весу. При низких концентрациях частиц увеличение теплопроводности носит линейный характер, но при более значительных концентрациях зависимость становится нелинейной. Это может быть связано с возможной агломерацией частиц при значительных концентрациях, что существенно влияет на свойства переноса тепла. Максимальное увеличение теплопроводности на 40.24% зафиксировано при наполнении наножидкости наночастицами до 1 мас. %. В этой работе отмечается, что по мере увеличения концентрации наночастиц вязкость наножидкостей увеличивается и значительно падает при повышении рабочей температуры. Представленные авторами данные о вязкости соответствуют общей концепции, согласующейся с данными других исследователей [3, 5].
Глицерин хорошо смешивается с водой, что приводит к изменению вязкости и теплопроводности. Анализ, проведенный Такамура и др. [13], показывает, что растворы глицерин/вода обеспечивают изменение вязкости водной фазы более чем на три порядка. Повышение вязкости смеси глицерин/вода носит сильно нелинейный характер с увеличением процентного содержания глицерина. Резкое увеличение вязкости смесей глицерин/вода можно лучше понять из исследований База и др. [14] и Йенсена и др. [15]. Когда содержание глицерина в смеси повышается, водородные связи “вода–вода” заменяются водородными связями “глицерин–вода”, что приводит к значительному увеличению сдвиговой вязкости. Для демонстрации такого поведения Баз и др. [14] использовали моделирование методом молекулярной динамики. Полученные в работе [14] результаты согласуются с данными Йенсена и др. [15], которые использовали спектроскопию механического сдвига для исследования смесей глицерин/вода при молярных долях глицерина в диапазоне от 1 (чистый глицерин) до 0.3. Авторы предположили, что вода выполняет роль в этих смесях выполняет роль смазки, ослабляя водородные связи в глицериновой матрице.
Ченг [16] предложил экспоненциальное соотношение для оценки вязкости водного раствора в диапазоне концентраций 0–100 мас. % и диапазоне температур 0–100°С, с отклонением от экспериментальных данных менее 5%. Зависимость между теплопроводностью и физико-химическими свойствами, справедливая в интервале температур от 15 до 90°С была сформулирована Филипповым для 83 различных растворов [17]. В работе описаны девять существенно новых экспериментальных методов измерения теплопроводности. Была предложена линейная зависимость теплопроводности от массовой концентрации для прогнозирования наблюдаемых значений теплопроводности с максимальным отклонением 3%.
Подбор наножидкостей, обладающих хорошей дисперсионной устойчивостью и химической инертностью, необходим для обеспечения подходящих свойств. Увеличение вязкости базовой жидкости может улучшить стабильность наножидкости, ограничивая при этом перенос тепла за счет снижения теплопроводности. Соответственно, чтобы предотвратить экранирование теплового преимущества наножидкости, следует выбирать соответствующий процент глицерина в воде для использования в качестве базовой жидкости.
Исследования показали, что добавление воды к глицерину уменьшает вязкость и повышает теплопроводность смеси. Определение оптимального соотношения глицерина и воды будет полезно для получения наножидкостей с требуемыми функциональными свойствами. В представленном исследовании оптимальное соотношение глицерина и воды определено путем сравнения вязкости и теплопроводности смесей с разным соотношением компонентов. Насколько известно авторам, ранее о таких исследованиях в литературе не сообщалось.
Кроме того, предполагается определить влияние концентрации частиц и температуры на теплопроводность и вязкость наножидкостей, содержащих диоксид кремния и кобальта, приготовленных с использованием водного раствора глицерина оптимального состава. Наножидкости недавно были исследованы на предмет их потенциального использования для охлаждения электронных схем [18]. В электронных устройствах создаются магнитные и электрические поля. Потенциально, магнитное поле может оказывать влияние на теплоперенос в наножидкостях, содержащих магнитные частицы кобальта. Теплопроводность и вязкость наножидкости влияют на теплоперенос, и данное исследование направлено на выявление этого влияния. Когда наножидкость течет в трубе теплообменника, согласно исследованию Шарма и др. [19], частицы с более высокой плотностью мигрируют к оси, а частицы с более низкой плотностью – к стенке. Поэтому, разработка гибридной наножидкости из кобальта и частиц более низкой плотности, позволит получить равномерное распределение композитных частиц по поперечному сечению трубки. Равномерное распределение твердых частиц в протекающем потоке способствует улучшению теплопередачи. Наночастицы диоксида кремния были выбраны наряду с кобальтом из-за низкой плотности. Кроме того, большинство базовых жидкостей инертны по отношению к наночастицам SiO2 [5]. Предполагается определить улучшение свойств приготовленных наножидкостей для дальнейшего улучшения теплообмена в турбулентном диапазоне течений.
2. МАТЕРИАЛЫ И МЕТОДЫ
2.1. Материалы
Наноразмерный диоксид кремния (SiO2) размером 50 нм и степенью чистоты 99.5% был получен от Nano Research Lab, Джамшедпур, Индия.
Изображение автоэмиссионной растровой электронной микроскопии (РЭМ) наночастиц SiO2 приведено на рис. 1. Кобальтовая наножидкость со средним размером частиц 80 нм и концентрацией 1.5 мас. % в выбранном соотношении смеси глицерин/вода произведена в Nanowings, Хаммам, Индия. Изображение автоэмиссионной РЭМ наночастиц кобальта приведено на рис. 2.
Глицерин лабораторного качества и чистоты 99.5% произведен Pon Pure Chemicals, Ченнаи, Индия. Свойства закупленных частиц SiO2 и Co приведены в табл. 1.
Изображения, демонстрирующие морфологию наночастиц SiO2 и Co, получены с помощью автоэмиссионного растрового электронного микроскопа (FEI Teneo LV SEM) и представлены на рис. 1 и 2. На микрофотографиях РЭМ видно, что наночастицы SiO2 и Co имеют сферическую форму. Согласно данным производителя, средний диаметр наночастиц SiO2 и Co составляет 50 нм. Однако определенный по изображениям РЭМ размер наночастиц кобальта оказался равен 80 нм.
2.2. Приготовление образцов смесей глицерин/вода
Процедура предназначена для определения оптимального соотношения смеси глицерина и воды в качестве базовой жидкости. Выбор был сделан на основе измеренных данных вязкости смесей глицерин/вода (ГВ) при различном процентном содержании глицерина по массе. Были приготовлены девять образцов смеси базовых жидкостей с содержанием глицерина, в пределах от 10 до 90% с шагом 10%. Образцы смеси имеют маркировку 10ГВ, 20ГВ, 30ГВ, … 90ГВ, с номером, указывающим на весовую долю глицерина в смеси.
2.3. Приготовление наножидкостей, оценка стабильности
Наножидкости с SiO2 получали двухстадийным способом [5] с массовыми концентрациями 0.25, 0.5, 1.0 и 1.5%. Относительные массы наночастиц SiO2 и базовой жидкости для приготовления выбранной массовой концентрации определяли по формуле:
где ϕ, mp, и mbf– массовая доля, масса наночастиц и масса базовой жидкости, соответственно. Массу наночастиц и базовой жидкости определяли с помощью электронных весов. Наножидкость кобальта с концентрацией 1.5 мас. % разбавляли до 1.0 и 0.5 мас. % путем смешения с необходимым количеством базовой жидкости. Для сравнения экспериментальных данных массовые концентрации приготовленных наножидкостей SiO2 и Co были переведены в объемные концентрации по формуле:(2)
$\psi = \frac{{\frac{{{{m}_{{\text{p}}}}}}{{{{\rho }_{{\text{p}}}}}}}}{{\frac{{{{m}_{{\text{p}}}}}}{{{{\rho }_{{\text{p}}}}}} + \frac{{{{m}_{{{\text{bf}}}}}}}{{{{\rho }_{{{\text{bf}}}}}}}}} \times 100,$Таблица 2.
Концентрации наножидкостей диоксида кремния и кобальта
| Наножидкости диоксида кремния | Наножидкости кобальта | |
|---|---|---|
| массовая доля, % | объемная доля, % | объемная доля, % |
| 0.5 | 0.225 | 0.06 |
| 1.0 | 0.450 | 0.12 |
| 1.5 | 0.675 | 0.18 |
Каждый образец наножидкости перемешивали на магнитной мешалке в течение 30 минут. Ультразвуковая обработка наносуспензий обеспечивает однородность дисперсии за счет разрушения кластеров частиц [5]. Многие исследователи используют метод обработки ультразвуком для приготовления стабильных наносуспензий [2, 20]. Джамшиди и др. [21] установили, что 60 мин ультразвуковой обработки наножидкости позволяют получить устойчивую, хорошо гомогенизированную суспензию. Поэтому в представленном исследовании образцы наножидкостей SiO2 и Co обрабатывали ультразвуком в течение 60 мин с использованием ультразвуковой ванны (Sonoplusserie 2000.2).
В представленном исследовании улучшение стабильности наножидкости осуществляли путем регулирования поверхностного заряда за счет изменения pH. Суспендированные наночастицы с большим поверхностным зарядом интенсивно отталкиваются друг от друга. Для определения этой силы отталкивания определяли дзета-потенциал наножидкостей [2]. Начальное значение рН, приготовленных наножидкостей SiO2 и Co при их максимальной концентрации, составляет 8.0 и 7.3 соответственно. Пять образцов с рН в диапазоне от 1.5 до 12.5 были приготовлены с использованием наножидкостей 0.675 об. % SiO2 и 0.18 об. % Co. Основанием для выбора наибольшей концентрации наножидкостей является более высокая вероятность нестабильности из-за агломерации. При более высоких концентрациях агрегации способствует уменьшение расстояния между частицами [2]. Растворы электролитов HCl или NaOH обычно используют [22] для изменения pH наножидкостей. Значение pH изменяли до 1.5, 4.5, 7.5, 9.5 и 12 путем добавления нескольких капель HCl или NaOH с последующим перемешиванием. Данные дзета-потенциала получали с помощью анализатора размеров и зарядов частиц Zetasizer (Nano ZS 90, Malvern Panalytical Inc) при 30°С. Дзета-потенциал образца измеряли в день приготовления и повторяли через 30 дней. Повторяемость результатов теста гарантирует стабильность наножидкостей в течение указанного периода времени.
2.4 Измерение вязкости и теплопроводности наножидкостей
Вязкость смесей глицерин/вода, а также наножидкостей SiO2 и Co измеряли с помощью реометра Brookfield LVDV III Ultra, а KD2 Pro использовали для измерения теплопроводности. Реометр Brookfield LVDV III Ultra может измерять широкий диапазон вязкости от 1 до 6 × 106 сП. Образец жидкости для измерения наливали в мерный контейнер объемом около 16 мл и подсоединяли к прибору. Температура испытуемой жидкости поддерживалась постоянной с помощью водяной бани. Для задания выбранных значений скорости сдвига и температуры, а также определения вязкости использовали встроенное программное обеспечение Rheocal [23]. Расчет вязкости повторяли пять раз для каждого образца, а в таблицу заносили среднее значение.
При использовании нестационарного источника тепла прибор KD2 Pro позволяет получить данные по теплопроводности. Устройство имеет портативный блок управления и игольчатый датчик. Водяная баня используется для поддержания желаемой температуры тестовой жидкости с точностью до 0.10°C. Для каждого образца выполняли не менее пяти измерений и заносили в таблицу среднее значение. Теплопроводность и вязкость чистого глицерина были протестированы для проверки точности реометра Brookfield и KD2 Pro. В измерениях, направленных на проверку точности прибора (табл. 3) было обнаружено, что максимальное наблюдаемое отклонение находится в пределах 2%.
3. РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
3.1 Выбор базовой жидкости
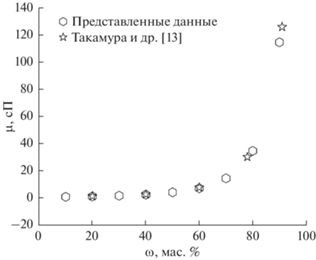
Вязкость и теплопроводность смесей глицерин/вода измеряли при 30°С. Как и ожидалось, вязкость смесей глицерин/вода увеличивается с ростом процентного содержания глицерина (рис. 3). Полученные экспериментальные данные хорошо согласуются с ранее полученным результатом, опубликованным Такамура и др. [13], при среднем отклонении менее 5%.
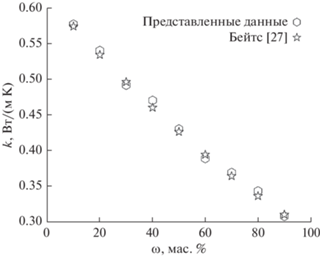
Экспериментальные значения теплопроводности от процентного содержания глицерина в смеси показаны на рис. 4. Наблюдается снижение теплопроводности смеси глицерин/вода с увеличением процентного содержания глицерина. Измеренные данные теплопроводности близки к значениям, сообщенным Бейтсом [27]. Среднее расхождение между экспериментальными и опубликованными данными теплопроводности для смесей глицерин/вода составляет менее 1%.
Теплопроводность глицерина составляет 0.281 Вт/(м К), а вязкость 912 сП при 25°C [5]. В свою очередь, при 25°C теплопроводность воды 0.605 Вт/(м К) и вязкость 0.89 сП [24]. Таким образом, повышение процентного содержания глицерина в смеси увеличивает вязкость и снижает теплопроводность жидкости, что можно увидеть на рис. 3 и 4. В табл. 4 приведены значения теплопроводности, вязкости и их градиент для различных процентных содержаний глицерина в воде. Создавать наножидкости с высокими значениями вязкости нецелесообразно, поскольку в дальнейшем это требует увеличения мощности прокачки нанофлюида [25].
Таблица 4.
Теплопроводность и вязкость смесей глицерин/вода
| Содержание глицерина в смеси, мас. % | Теплопроводность, Вт/(м К) | Вязкость, сП |
|---|---|---|
| 10 | 0.576 | 1.04 |
| 20 | 0.539 | 1.32 |
| 30 | 0.491 | 1.89 |
| 40 | 0.469 | 2.63 |
| 50 | 0.429 | 4.32 |
| 60 | 0.388 | 7.33 |
| 70 | 0.368 | 14.66 |
| 80 | 0.342 | 34.84 |
| 90 | 0.307 | 114.63 |
Кроме того, эффективность теплопередачи снижается из-за уменьшения теплопроводности с увеличением процентного содержания глицерина. Акилу и др. [5] и Цай и др. [26] исследовали влияние вязкости базовой жидкости на общее улучшение теплопроводности наножидкостей, и обнаружили, что повышение вязкости базовой жидкости подавляет броуновское движение и приводит к снижению роста теплопроводности. Следовательно, оптимальное процентное содержание глицерина в воде выбирается на основе компромисса между вязкостью и теплопроводностью смесей глицерин/вода. Измеренные данные показали, что вязкость и теплопроводность в смеси 30ГВ составляют 1.89 сП и 0.469 Вт/(м К) соответственно. Смесь 30ГВ имеет вязкость примерно в два раза больше, чем у воды, и на 67% более высокую теплопроводность, чем у глицерина. Использовании в качестве базовой жидкости раствора 30ГВ приводит к относительному увеличению вязкости и способствует повышению стабильности наножидкости без значительной потери теплопроводности [2]. Поэтому смесь 30ГВ была выбрана в качестве базовой жидкости для приготовления наножидкостей SiO2 и Co.
3.2. Стабильность наножидкостей Co и SiO2
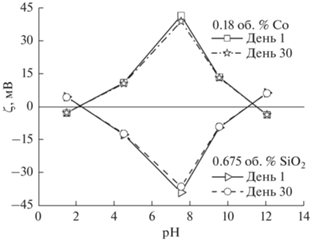
На рис. 5 показана зависимость дзета-потенциала от pH для исследованного интервала значений рН. Из рисунка видно, что приготовленная наножидкость с содержанием SiO2 0.675 об. % при рН 7.5 имеет дзета-потенциал ‒38.7 и ‒37.1 мВ на первый и тридцатый день соответственно. Аналогично дзета-потенциал для наножидкости с 0.18 об. % Со при рН 7.5 на первый и тридцатый день составляет 41.2 и 39.6 мВ. Таким образом, в течение 30 дней изменение дзета-потенциала не превышает 5%, что свидетельствует о хорошей стабильности наножидкости в течение рассматриваемого времени. При рН 7.5 приготовленные наножидкости имеют дзета-потенциал более значительный, чем минимально необходимый для стабильности: ±30 мВ [2, 28]. Поскольку приготовленные наножидкости 0.675 об. % SiO2 и 0.18 об. % Co демонстрируют более высокий дзета-потенциал при pH 7.5, другие смеси также поддерживали при этом pH для хорошей стабильности.
3.3. Вязкость наножидкостей SiO2 и Co
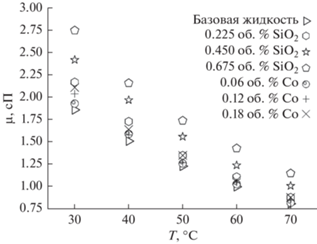
Вязкость приготовленных наножидкостей SiO2 и Co на основе базовой жидкости 30ГВ измерена в температурном диапазоне от 30 до 70°C. Изменение вязкости наножидкостей от концентрации и температуры показано на рис. 6. Вязкость приготовленных наножидкостей больше, чем у базовой жидкости, и увеличивается с концентрацией. Более высокое сопротивление течению, вызванное добавлением наночастиц, и взаимодействие между взвешенными частицами и молекулами базовой жидкости приводит к более высокой вязкости наножидкостей, по сравнению с базовыми жидкостями [28, 29]. С ростом числа частиц в жидкости происходит образование более крупных агломератов из-за ван-дер-ваальсовых взаимодействий между частицами. При образовании более крупных агломератов из-за возникновения сдвиговых напряжений внутри агрегата для диспергирования таких агрегатов требуется больше энергии. В результате этого явления вязкость наножидкости повышается с концентрацией [28, 30].
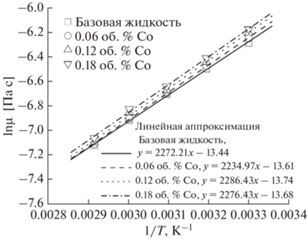
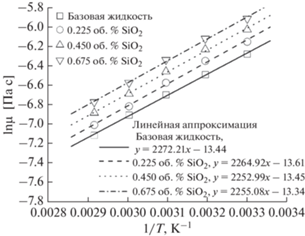
Другой ключевой вывод из рис. 6 заключается в том, что вязкость базовых жидкостей и наножидкостей уменьшается с повышением температуры. Уравнение Аррениуса, представленное ниже как уравнение (3), позволяет предсказать взаимное влияние температуры и вязкости жидкости.
Из этого уравнения следует, что натуральный логарифм вязкости линейно зависит от величины обратной температуры [29, 30] поскольку это уравнение (3) может быть представлено в форме: где T 1, R, Ea и A – абсолютная температура, газовая постоянная, энергия активации и предэкспоненциальный множитель для наножидкости, соответственно. На рис. 7 и 8 приведена зависимость натурального логарифма измеренной вязкости ln(µ) от обратной величины абсолютной температуры 1/(T + 273.15) для наножидкостей с Co и SiO2. В согласии с уравнением (4) эта зависимость носит линейный характер. Энергию активации рассчитывали с использованием наклона линий Ea/R, принимая газовую постоянную R равной 8.314 Дж/(моль К). Расчетные значения энергий активации Ea приведены в табл. 5.Таблица 5.
Энергия активации, Ea, базовой жидкости, наножидкостей Co и SiO2
| Жидкость | Ea, кДж/моль |
|---|---|
| Базовая | 18.89 |
| 0.06% Co | 18.58 |
| 0.12% Co | 19.01 |
| 0.18% Co | 18.92 |
| 0.225% SiO2 | 18.83 |
| 0.45% SiO2 | 18.73 |
| 0.675% SiO2 | 18.74 |
Мессаади и др. [31] ранее установили, что для воды Ea = 15.749 кДж/моль и для глицерина Ea = = 59.608 кДж/моль. Джиап [32] утверждает, что высокое значение Ea отражает тот факт, что вязкость жидкости быстро меняется с изменением температуры. Основываясь на полученном значении Ea для смеси 30ГВ, мы можем сделать вывод, что по температурной чувствительности вязкость смеси 30ГВ ближе к вязкости воды. С другой стороны, Ea всех наножидкостей Co и SiO2 практически совпадает с Ea для смеси 30ГВ, поскольку зависимость вязкости всех исследованных наножидкости от температуры аналогична зависимости для базовой жидкости. Точно также Али и др. [29] обнаружили, что наножидкости с частицами TiO2 в смесях этиленгликоль/вода имеют такое же температурное поведение вязкости, как и базовая жидкость. Джаранежад и др. [30] обнаружили аналогичную закономерность для температурной зависимости вязкости базовой жидкости и наножидкостей на водной основе с частицами TiO2 и Al2O3.
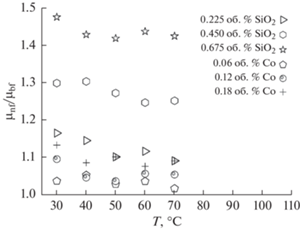
Относительная вязкость (µR) представляет собой отношение вязкости наножидкости (µnf) к вязкости базовой жидкости (µbf), согласно уравнению:
Изменения относительной вязкости приведены на рис. 9 для наножидкостей SiO2 и Co. Многие исследователи обращали внимание на изменение коэффициента вязкости наножидкостей [5, 28]. Из рис. 9 видно, что коэффициенты вязкости наножидкостей SiO2 и Co увеличиваются с концентрацией и незначительно меняются с температурой. Аналогичный вывод был сделан ранее несколькими исследователями [28, 33]. Эти результаты означают, что приготовленные наножидкости могут быть эффективны в приложениях, требующих постоянной прокачки при различных температурах. Пиковое увеличение вязкости наножидкости SiO2 при концентрации 0.675 об. % составляет 47.4%. Максимальное увеличение вязкости для наножидкостей Co составляет 13.1% при концентрации 0.18 об. %. В обеих наножидкостях пиковое повышение наблюдалось при 30°С.Измеренные вязкости наножидкостей SiO2 и Co сравнивали со значениями, оцененными по теоретическим моделям. Вязкость наножидкостей можно предсказать с помощью классической корреляции, предложенной Бэтчелором [34]:
где φ объемная доля наночастиц. Различные исследователи [5, 33] сообщают, что вязкость, рассчитанная по Бэтчелору имеет сильно заниженные значения, по сравнению с экспериментальными данными. Расхождения между рассчитанными по классическому соотношению (6) и измеренными данными, связаны с исключением из рассмотрения принципа ослабления молекулярных связей [5]. Кроме того, классическая модель учитывает объемную долю наночастиц, тогда как наночастицы образуют кластеры в жидкостях и адсорбируются на поверхностях. Гидродинамический диаметр наночастиц увеличивается за счет кластеризации и поверхностной адсорбции, что приводит к увеличению относительной вязкости [33]. Чтобы исключить существенные теоретические несоответствия в предсказании вязкости наножидкости, Гарузи [35] разработал модель вязкости, которая учитывает температуру, природу, диаметр, форму частиц и природу базовой жидкости. Корреляция может быть выражена следующим соотношением:(7)
${{\mu }_{{{\text{nf}}}}} = \left( {1 + 49.6{{{\left( {\frac{{{{d}_{{\text{p}}}}}}{{{{d}_{{{\text{bf}}}}}}}} \right)}}^{{ - 0.414}}}{{\varphi }^{{0.908}}}{{e}^{{10.8\varphi }}}} \right){{\mu }_{{{\text{bf}}}}},$(8)
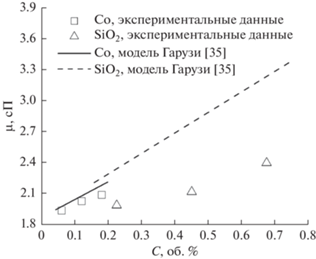
${{d}_{{{\text{bf}}}}} = 0.1{{\left( {\frac{{6M}}{{N\prod {{\rho }_{{f0}}}}}} \right)}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}},$В обзоре [36] Муршед и Эстель описали различные модели для описания вязкости наножидкостей и обнаружили, что большинство этих моделей основаны на результатах измерений определенного типа наножидкости и недостаточны для прогнозирования вязкости других видов наносуспензий. Анализируя экспериментальные значения вязкости наножидкостей с частицами SiO2 и Co, представленные на рис. 10, можно сделать вывод, что при выбранной концентрации частиц и температуре наножидкости с частицами Co демонстрируют значительно большее увеличение вязкости, чем наножидкости с частицами SiO2. Объяснение этому может быть связано с тем, что частицы Co имеют больший диаметр по сравнению с SiO2. Об аналогичной зависимости вязкости наножидкостей от размера наночастиц ранее сообщали различные исследователи [37, 38].
В данном исследовании воспроизводимость экспериментальных данных по вязкости наножидкостей использовали для оценки их стабильности в течение 30 дней. Также стабильность дисперсии наножидкостей путем анализа воспроизводимости данных по вязкости была исследована Махбубул и др. [39] и Хагиги и др. [40]. Вязкость наножидкостей с наночастицами SiO2 и Co измеряли на первый и тридцатый день после приготовления. В табл. 6 представлены измеренные значения вязкости при 30°С. Максимальное отклонение значений вязкости на 30-й день от вязкости в первый день для наножидкостей с частицами SiO2 и Co составляет 5%, что свидетельствует о хорошей стабильности суспензий в течение 30 дней.
3.4. Теплопроводность наножидкостей SiO2 и Co
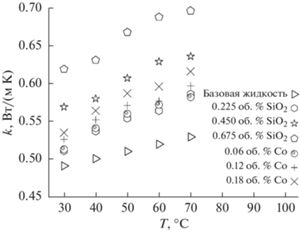
Теплопроводность наножидкостей с частицами SiO2 и Co на основе базовой жидкости 30ГВ измеряли в диапазоне температур 30–70°C. На рис. 11 показано изменение теплопроводности наножидкостей с частицами SiO2 и Co в зависимости от концентрации и температуры. Теплопроводность наножидкостей с частицами SiO2 и Co, увеличивающаяся с температурой и концентрацией, как показано на рис. 11, выше, чем соответствующие значения для базовой жидкости. Как отмечалось ранее, различные исследователи показали, что наножидкости имеют более значительную теплопроводность, чем базовые жидкости [5, 28]. Согласно Рамачандрану и др. [41], статические факторы, связанные с наночастицами, такие как формирование межфазного слоя и связывание частиц, улучшают теплопроводность в наножидкостях. Динамические факторы, которые повышают теплопроводность, включают наноконвекцию и броуновское движение частиц. Молекулы базовой жидкости создают твердоподобный слой на внешней стороне частиц, который работает как энергетический мост, увеличивая передачу энергии между частицей и окружающей жидкостью. Агрегирование частиц создает более низкое тепловое сопротивление вдоль структуры, формируемой частицами в наножидкости, что приводит к уменьшению сопротивления тепловому потоку и к лучшей теплопередаче. Под действием броуновского движения молекул наночастицы в жидкости всегда находятся в случайном движении, даже если сама жидкость статична. Броуновское движение является вероятным способом передачи тепла в наножидкостях, поскольку самопроизвольное движение частиц в жидкости приводит к их столкновениям. Частица увлекает молекулы базовой жидкости во время броуновского движения, образуя наноконвекции и повышая теплопроводность наножидкости.
По данным Ленина и др. [44], комбинированный эффект объема наночастиц и межфазного слоя может определять улучшение теплопроводности наножидкости. Из-за высокой теплопроводности твердоподобного слоя вокруг частицы, его вклад в теплопроводность жидкости необходимо оценивать вместе с вкладом от частиц, диспергированных в наножидкости. При этом сам межфазный слой также дает вклад в объемную долю частиц и, таким образом, оказывает значительное влияние на концентрационную зависимость теплопроводности. Рост числа частиц в жидкости приводит к увеличению объемной доли частиц и увеличению доли молекул жидкости, адсорбированных на частицах. Температура влияет на скорость броуновского движения и толщину межфазного слоя, следовательно, теплопроводность наножидкости изменяется с температурой. На плотность адсорбированных молекул на поверхности частицы также влияет температура наножидкости, которая напрямую влияет на толщину межфазного слоя [45]. Cогласно Фану и др. [46], толщина нанослоя увеличивается с температурой. Такое поведение объясняется тем, что с повышением температуры связь между молекулами в твердом и жидком слое ослабевает, и молекулы жидкости формируют более разреженную упаковку на поверхности, увеличивая толщину межфазного слоя. По мнению исследователей, увеличение толщины межфазного слоя увеличивает теплопроводность наножидкости. Увеличение теплопроводности за счет адсорбции молекул базовой жидкости на поверхности частиц было исследовано Камалвандом и Карами [47] при различных температурах. Было обнаружено линейное увеличение теплопроводности c количеством адсорбированных молекул базовой жидкости. Авторы полагают, что уровень адсорбции молекул базовой жидкости увеличивается с повышением температуры наножидкости.
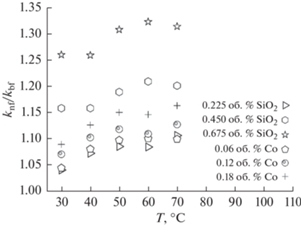
Чтобы лучше характеризовать изменение теплопроводности наножидкостей, удобно использовать коэффициент (${{k}_{R}}$) равный отношению теплопроводности наножидкости (${{k}_{{{\text{nf}}}}}$) к теплопроводности базовой жидкости (${{k}_{{{\text{bf}}}}}$):
Коэффициенты теплопроводности наножидкостей были определены в работе [5]. Изменение коэффициента теплопроводности наножидкостей с наночастицами SiO2 и Co в зависимости от температуры и концентрации, полученное в данной работе, показано на рис. 12. Видно существенное увеличение коэффициента теплопроводности наножидкостей SiO2 и Co с концентрацией наночастиц. Также для коэффициента теплопроводности обнаружено постепенное увеличение с повышением температуры как для наножидкостей Co, так и для SiO2. Максимальное улучшение теплопроводности на 31.5% для наножидкости с частицами SiO2 обнаружено при концентрации частиц 0.675%. Для наножидкости с частицами Co улучшение составляет 16.4% при концентрации 0.18%. При одинаковой температуре 70°C обе наножидкости демонстрируют максимальное увеличение теплопроводности.Для анализа характеристик теплопередачи чистых жидкостей, таких как вода, свойства обычно можно предсказать с помощью эмпирических корреляций. Эти эмпирические корреляции широко доступны для чистых жидкостей. Однако единых эмпирических корреляций для оценки свойств наножидкостей не существует. В результате ряд исследователей работали над установлением этих корреляций. Много десятилетий назад были разработаны классические модели, позволяющие предсказывать коэффициент теплопроводности двухфазных сред, в том числе и наножидкостей. Для оценки коэффициента теплопроводности суспензии, содержащей твердые частицы, взвешенные в жидкости, с использованием теории эффективной среды, Максвелл [48] предложил соотношение:
(10)
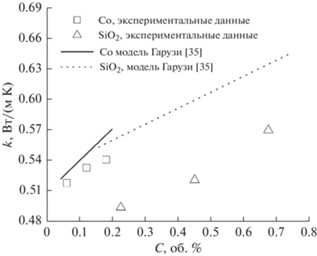
$\frac{{{{k}_{{{\text{nf}}}}}}}{{{{k}_{{{\text{bf}}}}}}} = \frac{{{{k}_{{\text{p}}}} + 2{{k}_{{{\text{bf}}}}} + 2\varphi \left( {{{k}_{{\text{p}}}} - {{k}_{{{\text{bf}}}}}} \right)}}{{{{k}_{{\text{p}}}} + 2{{k}_{{{\text{bf}}}}} - \varphi \left( {{{k}_{{\text{p}}}} - {{k}_{{{\text{bf}}}}}} \right)}},$По-видимому, к недооценке коэффициента ${{k}_{R}}$ в классической модели по сравнению с экспериментальными данными может приводить неучет образования двойного электрического слоя на поверхности частиц, особенностей поведения дисперсии и влияния диаметра наночастиц на теплопроводность [33]. Поскольку классическая модель Максвелла не может корректно предсказать результаты, Гарузи [35] использовал другую модель теплопроводности. Полученное им соотношение для расчета knf учитывает температуру, материал, диаметр, форму частиц и базовую жидкость:
(11)
$\begin{gathered} {{k}_{{{\text{nf}}}}} = \left( {\frac{{{{k}_{{\text{p}}}} + 2{{k}_{{{\text{bf}}}}} + 2\left( {{{k}_{{\text{p}}}} - {{k}_{{{\text{bf}}}}}} \right)\varphi }}{{{{k}_{{\text{p}}}} + 2{{k}_{{{\text{bf}}}}} - 2\left( {{{k}_{{\text{p}}}} - {{k}_{{{\text{bf}}}}}} \right)\varphi \omega }}} \right. + \\ \left. { + \,\,3.762{{{\left( {\frac{T}{{{{T}_{0}}}}} \right)}}^{{8.661}}}{\kern 1pt} {{{\left( {\frac{{{{d}_{{\text{p}}}}}}{{{{d}_{{{\text{bf}}}}}}}} \right)}}^{{ - 0.4351}}}{\kern 1pt} {{{\left( {\frac{{{{k}_{{\text{p}}}}}}{{{{k}_{{{\text{bf}}}}}}}} \right)}}^{{0.08235}}}{{\varphi }^{{0.64}}}{{e}^{{ - 5.742\varphi }}}} \right){{k}_{{{\text{bf}}}}}, \\ \end{gathered} $Модель теплопроводности Гарузи [35] предсказывает данные наножидкости c наночастицами Co с максимальным отклонением менее 5%. С другой стороны, расхождение для наножидкости с частицами SiO2 довольно значительное, с максимальным отклонением 15.5% при 30°С. Как обсуждалось Кочча [49], как правило, классические модели теории эффективной среды дают неточные значения теплопроводности для наножидкостей. Согласно анализу, проведенному авторами [49], такое неточное предсказание связано с тем, что явления теплопереноса в наножидкостях не могут быть описаны теорией эффективной среды, рассматривающей в качестве механизма теплопроводности только термодиффузию. Поскольку объединение экспериментальных данных позволяет получить более совершенные теоретические модели, требуются дополнительные исследования и проверка. Важный вывод, который можно сделать из рис. 13, заключается в том, что экспериментальные данные по теплопроводности наножидкостей с частицами SiO2 и Co указывают на более значительное улучшение теплопроводности для наножидкости с частицами Co, по сравнению с наножидкостью с частицами SiO2, при данной концентрации и температуре. Наножидкости с частицами Co на основе 30ГВ имеют более высокую теплопроводность, чем наножидкости с частицами SiO2, поскольку Co является металлом с более высокой теплопроводностью, чем SiO2. В своем исследовании Аладе и др. [50] обнаружили, что металлические наножидкости демонстрируют более значительное увеличение теплопроводности, чем оксидные наножидкости.
Измеряя свойства с течением времени, можно определить потенциальные проблемы седиментации и стабильности наножидкостей. Садри и др. [51] использовали указанный метод для проверки стабильности суспензии многослойных углеродных нанотрубок в воде, тестируя теплопроводность с интервалом в 4 дня в течение 28 дней. Изменение теплопроводности наножидкостей SiO2 и Co на первый и тридцатый день после приготовления, использовали в данной работе в качестве критерия стабильности в представленном исследовании. В табл. 7 приведены измеренные значения теплопроводности при 30°С. Отклонения общей теплопроводности наножидкостей c частицами Co и SiO2 составляют менее 4% и 5% за 30 дней соответственно, что позволяет предположить, что приготовленные наножидкости стабильны. Повышенная вязкость базовой жидкости при добавлении глицерина в воду и изменение pH наножидкостей, приводящее к более высокого дзета-потенциалу может объяснить хорошую стабильность наножидкостей SiO2 и Co.
Таблица 7.
Зависимость теплопроводности от времени
| Параметр | Теплопроводность, Вт/(м К) | |||||
|---|---|---|---|---|---|---|
| наножидкость Co | наножидкость SiO2 | |||||
| Концентрация, об. % | 0.06 | 0.12 | 0.18 | 0.225 | 0.45 | 0.675 |
| День 1 | 0.513 | 0.526 | 0.535 | 0.586 | 0.636 | 0.696 |
| День 30 | 0.506 | 0.514 | 0.518 | 0.576 | 0.615 | 0.667 |
| Отклонение, % | 1.36 | 2.28 | 3.17 | 1.70 | 3.30 | 4.16 |
4. ТЕПЛОВЫЕ ХАРАКТЕРИСТИКИ НАНОЖИДКОСТЕЙ С ЧАСТИЦАМИ SiO2 И Co
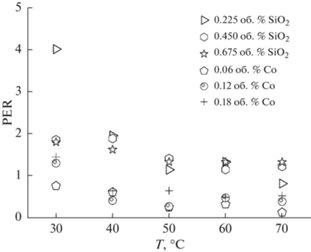
Чтобы оценить преимущество тепловых характеристик наножидкостей, исследователи рассчитывают коэффициент улучшения свойств (property enhancement ratio, PER) [23]. PER представляет собой отношение улучшения вязкости к улучшению теплопроводности, согласно следующему уравнению:
(12)
${\text{PER}} = \frac{{\frac{{{{\mu }_{{{\text{nf}}}}}}}{{{{\mu }_{{{\text{bf}}}}}}} - 1}}{{\frac{{{{k}_{{{\text{nf}}}}}}}{{{{k}_{{{\text{bf}}}}}}} - 1}},$Гарг и др. [52] указали, что PER наножидкости должен быть ниже 5, для получения значительного теплового преимущества при ее использовании в теплообменниках с турбулентным потоком. На рис. 14 приведен сравнительный график PER наножидкостей с частицами SiO2 и Co. Оказалось, PER ниже 5 для обеих наножидкостей и уменьшается с температурой. Кроме того, PER для наножидкостей с частицами Co меньше, чем для наножидкостей SiO2. Наблюдаемые особенности свидетельствуют, что эти наножидкости являются подходящими заменителями традиционных теплоносителей.
5. ПОГРЕШНОСТИ В ОЦЕНКЕ СВОЙСТВ
Оценку погрешностей при измерениях теплопроводности и вязкости наножидкостей SiO2 и Co осуществляли с учетом ошибок измерений связанных параметров. Погрешности связаны с ошибками измерения в данных массового отношения наночастиц и температуры. Изменение теплопроводности и вязкости в процессе измерения также влияют на погрешность.
Погрешность измерений определяли с учетом точности используемых приборов. Точность используемого измерителя теплопроводности и вискозиметра составляет ±1%. Водяная баня имеет точность поддержания стабильной температуры 0.1°C. Электронные весы, используемые для взвешивания наночастиц, имеют точность 0.01 г. Погрешности в измерении теплопроводности и вязкости определяли согласно уравнениям (13) и (14) предложенным Тенгом и др. [53]. Наибольшие погрешности составляют ±2.26% и ±2.25% при измерении теплопроводности и вязкости соответственно.
6. ВЫВОДЫ
Добавление глицерина к воде увеличивает вязкость и снижает теплопроводность полученной смеси. Для приготовления наножидкостей с частицами SiO2 и Co в качестве базовой жидкости выбрана смесь 30% глицерина + 70% воды (30ГВ). Измеренные теплофизические характеристики смеси глицерин/вода хорошо согласуются с литературными данными. Дзета-потенциал частиц в процессе приготовления наножидкостей с частицами SiO2 и Co при разных значениях pH проходит через максимум при pH 7.5. Установлено, что приготовленные наножидкости SiO2 и Co стабильны в течение 30 дней. Максимальное улучшение теплопроводности для наножидкостей SiO2 и Co составляет 31.5% при концентрации 0.675 об. % и 16.4% при концентрации 0.18 об. %, соответственно, при 70°C. Максимальное улучшение вязкости наножидкостей SiO2 и Co составляет 47.4 и 13.1% при концентрациях 0.675 об. % и 0.18 об. % соответственно, при 30°C. При концентрации 0.18 об. % наножидкости диоксида кремния и кобальта демонстрируют улучшение теплопроводности на 8.3 и 16.4% при 70°C соответственно.
Аналогично при концентрации 0.18 об. % и 30°C наножидкость кобальта демонстрирует немного большее увеличение вязкости (13.1%), по сравнению с наножидкостью диоксида кремния (11.8%) при одинаковых условиях. Воспроизводимость данных измерений вязкости и теплопроводности за 30 дней показывает, что отклонение составляет менее 5%. Значения коэффициента усиления свойств (PER) показывают, что наножидкости на основе SiO2 и Co в базовой жидкости 30ГВ являются потенциальной заменой традиционных жидких теплоносителей.
Список литературы
Sekrani G., Poncet S. // Appl. Sci. 2018. V. 8. P. 2311.
Yu F., Chen Y., Liang X., Xu J., Lee C., Liang Q., Tao P., Deng T. // Prog. Nat. Sci. 2017. V. 27. № 5. P. 531.
Talib S.F.A., Azmi W.H., Zakaria I., Mohamed WANW., Mamat A.M.I., Ismail H., Daud W.R.W. // Energy Procedia. 2015. V. 79. P. 366.
Jang S.P., Choi S.U. // Appl. Phys. Lett. 2004. V. 84. P. 4316.
Akilu S., Baheta A.T., Minea A.A., Sharma K.V. // Int. Commun. Heat Mass Transf. 2017. V. 88. P. 245.
Al-Waeli A.H.A., Chaichan M.T., Sopian K., Kazem H.A. // Case Stud. Therm. Eng. 2018. V. 13. P. 100340.
Sharifpur M., Tshimanga N., Meyer J.P., Manca O. // Int. Commun. Heat Mass Transf. 2017. V. 85. P. 12.
Tshimanga N., Sharifpur M., Meyer J.P. // Heat Transf. Eng. 2016. V. 37. № 18. P. 1538.
Karimi-Nazarabad M., Goharshadi E.K., Youssefi A. // J. Mol. Liq. 2016. V. 223. P. 828.
Goharshadi E.K., Niyazi Z., Shafaee M., Moghaddam M.B., Ludwig R., Namayandeh-Jorabchi M. // J. Mol. Liq. 2017. V. 241. P. 831.
Akilu S., Baheta A.T., Sharma K.V., Vandragi S.K. // ARPN J. Eng. Appl. Sci. 2016. V. 11. № 22. P. 13019.
Harikrishnan S., Roseline A.A., Kalaiselvam S. // IEEE Trans. Nanotechnol. 2013. V. 12. № 4. P. 629.
Takamura K., Fischer H., Morrow N.R. // J. Pet. Sci. Eng. 2012. V. 98–99. P. 50.
Baz J., Held C., Pleiss J., Hansen N. // Phys. Chem. Chem. Phys. 2019. V. 21. № 12. P. 6467.
Jensen M.H., Gainaru C., Alba-Simionesco C., Hecksher T., Niss K. // Phys. Chem. Chem. Phys. 2018. V. 20. № 3. P. 1716.
Cheng N.S. // Ind. Eng. Chem. Res. 2008. V. 47. P. 3285.
Filippov L.P. // Int. J. Heat Mass Transf. 1968. V. 11. P. 331.
Colangelo G., Favale E., Milanese M., de Risi A., Laforgia D. // Appl. Therm. Eng. 2017. V. 127. P. 421.
Sharma K.V., Azmi W.H., Kamal S., Sarma P.K., Vijayalakshmi B. // Can. J. Chem. Eng. 2016. V. 94. № 3. P. 565.
Setia H., Gupta R., Wanchoo R.K. // Mater. Sci. Forum 2013. V. 757. P. 139.
Jamshidi N., Farhadi M., Ganji D.D., Sedighi K. // Int. J. Eng. Trans. B: Appl. 2012. V. 25. P. 201.
Choudhary R., Khurana D., Kumar A., Subudhi S. // J. Exp. Nanosci. 2017. V. 12. № 1. P. 140.
Nabil M.F., Azmi W.H., Abdul Hamid K., Mamat R., Hagos F.Y. // Int. Commun. Heat Mass Transf. 2017. V. 86. P. 181.
Kothandaraman C.P., Subramanyan S. Heat and Mass Transfer Data Book, 5th ed., New Delhi: New Age International Publishers, 2004.
Pak B.C., Cho Y.I. // Exp. Heat Transf. 1998. V. 11. P. 151.
Tsai T.-H., Kuo L.-S., Chen P.-H., Yang C.-T. // Appl. Phys. Lett. 2008. V. 93. P. 233121.
Bates O.K. // J. Ind. Eng. Chem. 1936. V. 28. № 4. P. 494.
Akilu S., Baheta A.T., Kadirgama K., Padmanabhan E., Sharma K.V. // J. Mol. Liq. 2019. V. 284. P. 780.
Ali A., Ilyas S.U., Garg S., Alsaady M., Maqsood K., Nasir R., Abdulrahman A., Zulfiqar M., Mahfouz A.B., Ahmed A., Ridha S. // Int. Commun. Heat Mass Transf. 2020. V. 118. P. 104882.
Jarahnejad. M., Haghighi E.B., Saleemi M. // Rheol. Acta. 2015. V. 54. P. 411.
Giap S.G.E. // J. Phys. Sci. 2010. V. 21. № 1. V. 29.
Messaâdi A., Dhouibi N., Hamda H., Belgacem F.B.M., Adbelkader Y.H., Ouerfelli N., Hamzaoui A.H. // J. Chem. 2015. V. 1015. P. 163262.
Suresh S., Venkitaraj K.P., Selvakumar P., Chandrasekar M. // Colloids Surf. A: Physicochem. Eng. Asp. 2011. V. 388. P. 41.
Batchelor G.K. // J. Fluid Mech. 1977. V. 83. P. 97.
Garoosi F. // Powder Technol. 2020. V. 366. P. 788.
Murshed S.M.S., Estellé P. // Renew. Sust. Eng. Rev. 2017. V. 76. P. 1134.
Nguyen C., Desgranges F., Roy G., Galanis N., Mare T., Boucher S., Mintsa H.A. // Int. J. Heat Fluid Flow. 2007. V. 28. P. 1492.
He Y., Jin Y., Chen H., Ding Y., Cang D., Lu H. // Int. J. Heat Mass Transf. 2007. V. 50. P. 2272.
Mahbubul I.M., Elcioglu E.B., Amalina M.A., Saidur R. // Powder Technol. 2019. V. 345. P. 668.
Haghighi E.B., Nikkam N., Saleemi M., Behi M., Mirmohammadi S.A., Poth H., Khodabandeh R., Toprak M.S., Muhammed M., Palm B. // Meas. Sci. Technol. 2013. V. 24. P. 105301.
Ramachandran K., Kadirgama K., Awad O.I., Ramasamy D., Samykano M., Azmi W.H. // Int. Commun. Heat Mass Transf. 2018. V. 98. P. 13.
Leong K.C., Yang C., Murshed S.M.S. // J. Nanoparticle Res. 2006. V. 8. № 2. P. 245.
Wu C., Cho T.J., Xu J., Lee D., Yang B., Zachariah M.R. // Phys. Rev. E Stat. Nonlin. Soft Matter Phys. 2010. V. 81. P. 011406.
Lenin R., Joy P.A., Bera C. // J. Mol. Liq. 2021. V. 338. P. 116929.
Eastman J.A., Phillpot S.R., Choi S.U.S., Keblinski P. // Annu. Rev. Mater. Res. 2004. V. 34. P. 219.
Fan W., Zhong F. // ACS Omega. 2020. V. 5. P. 27972.
Kamalvand M., Karami M. // Int. J. Therm. Sci. 2013. V. 65. P. 189.
Maxwell J.C. Treatise on Electricity and Magnetism, 2-nd ed., Oxford: Clarendon Press, 1881.
Coccia C., Tomassetti S., Nicola G.D. // Renew. Sust. Energ. Rev. 2021. V. 151. P. 111573.
Alade I.O., Oyehan T.A., Popoola I.K., Olatunji S.O., Aliyu B. // Adv. Powder Technol. 2018. V. 29. № 1. P. 157.
Sadri R., Ahmadi G., Togun H., Dahari M., Kazi S.N., Sadeghinezhad E., Zubir N. // Nanoscale Res. Lett. 2014. V. 9. P. 151.
Garg J., Poudel B., Chiesa M., Gordon J., Ma J., Wang J., Ren Z., Kang Y., Ohtani H., Nanda J. // J. App. Phys. 2008. V. 103. № 7. P. 074301.
Teng T.P., Hung Y.H., Teng T.C., Mo H.E., Hsu H.G. // Appl. Therm. Eng. 2010. V. 30. № 14. P. 2213.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал