Координационная химия, 2019, T. 45, № 10, стр. 579-583
Квантово-химическое изучение магнитных свойств дикатионных о-хиноновых комплексов железа с пиридинофановыми лигандами
А. Г. Стариков 1, М. Г. Чегерев 1, А. А. Старикова 1, *, В. И. Минкин 1
1 Научно-исследовательский институт физической и органической химии
Южного федерального университета
Ростов-на-Дону, Россия
* E-mail: alstar@ipoc.sfedu.ru
Поступила в редакцию 28.03.2019
После доработки 04.04.2019
Принята к публикации 10.04.2019
Аннотация
Проведено компьютерное моделирование дикатионных о-бензохиноновых комплексов железа с 2,11-диаза[3.3]-(2,6)пиридинофановыми лигандами. Основным состоянием изученных соединений являются низкоспиновые изомеры. Сильные антиферромагнитные обменные взаимодействия предсказаны между неспаренными электронами трехвалентного иона железа и анион-радикальной формы редокс-активного лиганда. Посредством варьирования заместителей в тетраазамакроциклическом основании выявлено соединение, способное претерпевать спин-кроссовер.
Координационные соединения переходных металлов с радикальными лигандами благодаря их необычному магнитному поведению вызывают повышенный интерес специалистов в области координационной и металлоорганической химии [1, 2]. Рациональный дизайн таких структур открывает широкие перспективы при разработке динамических материалов, устройств хранения информации, записывающих элементов и квантовых компьютеров [3, 4]. Распространенным типом радикальных лигандов являются производные о-бензохинона, обладающие редокс-активными свойствами [5]. Комплексы переходных металлов с такими органическими молекулами способны демонстрировать перегруппировки по механизмам спин-кроссовера (СКО) [4] или валентной таутомерии (ВТ) [6–8], сопровождающиеся переключением спиновых состояний.
Существует несколько способов построения магнитно-активных координационных соединений с о-хинонами. Первый включает два редокс-лиганда и моно- или бидентатные основания с донорными атомами азота, достраивающими координационную сферу металла до октаэдра [9]. Такие комплексы представляют собой классические ВТ системы. Недавно был предложен другой структурный мотив, представляющий собой электронейтральный аддукт бис-хелата переходного металла с одним о-бензохиноновым лигандом, в котором реализуются термически инициированные спиновые перегруппировки [10, 11]. К третьему типу соединений, демонстрирующих магнитную бистабильность, относятся катионные комплексы, содержащие один редокс-активный лиганд и тетрадентатное макроциклическое азотсодержащее основание [12–14]. Сконструированные таким образом молекулы в зависимости от природы тетраазамакроцикла и металла могут проявлять как ВТ [12], так и СКО [13, 14].
Ранее был получен дикатионный ди-трет-бутил-о-бензохиноновый комплекс железа с N,N'-диметил-2,11-диаза[3.3]-(2,6)пиридинофаном, представляющий собой первый пример соединения, включающего низкоспиновый трехвалентный ион железа и семихиноновую (SQ) форму редокс-активного лиганда [15]. Интерес авторов статьи заключался в исследовании окисления, каталитической активности и способности к мимикрии под диоксигеназу этой системы. Данное соединение – структурный аналог монокатионного комплекса железа с N,N'-ди-трет-бутил-2,11-диаза[3.3]-(2,6)пиридинофаном, проявляющего СКО [14].
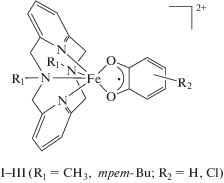
В настоящей работе с использованием методов квантовой химии изучены геометрические, энергетические и магнитные характеристики о-бензохиноновых комплексов железа I (R1 = CH3; R2 = H), II (R1 = CH3; R2 = Cl) и III (R1 = трет-Bu; R2 = H) с производными пиридинофана. Задача исследования состояла в выяснении влияния заместителей в редокс-активном и тетраазамакроциклическом лигандах на возможность протекания термически инициированного спинового перехода.
МЕТОДИКА РАСЧЕТОВ
Расчеты проводили с помощью программы Gaussian 09 [16] методом теории функционала плотности (DFT) с использованием функционала UTPSSh [17, 18] и расширенного базиса 6‑311++G(d,p), сочетание которых корректно воспроизводит энергетические характеристики СКО в катионных комплексах [19–25]. Локализацию стационарных точек на поверхности потенциальной энергии (ППЭ) осуществляли путем полной оптимизации геометрии молекулярных структур с проверкой стабильности DFT волновой функции. Вычисление параметров обменного взаимодействия (J, см–1) осуществляли в рамках формализма “нарушенной симметрии” (broken symmetry, BS) [26] с применением формулы, предложенной в [27]. Графические изображения молекулярных структур получали при помощи программы ChemCraft [28].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Согласно расчетам, основным состоянием соединения I (R1 = CH3; R2 = H) является низкоспиновый изомер LSFeIIISQ на дублетной ППЭ, включающий трехвалентный ион металла и SQ-форму редокс-активного лиганда (рис. 1, табл. 1). Вычисленные длины связей в координационном узле и бензохиноновом кольце хорошо коррелируют со значениями, установленными при помощи РСА [15]. В обсуждаемом электронном изомере (электромере [29]) предсказаны сильные обменные взаимодействия антиферромагнитного характера (J = –1603 см–1, см. табл. 2), что также находится в согласии с экспериментальными данными, указывающими на диамагнетизм комплекса [15]. Значительное перекрывание орбиталей атомов железа и кислорода (рис. 2) приводит к уменьшению количества спиновой плотности на металле и редокс-активном лиганде в состоянии BS (табл. 1).
Рис. 1.
Геометрические характеристики и распределение спиновой плотности в изомерах дикатионных комплексов I–III (R1 = CH3, трет-Bu; R2 = H, Cl), рассчитанные методом DFT UTPSSh/6-311++G(d,p). Атомы водорода опущены для ясности, длины связей даны в ангстремах, все структуры имеют заряд +2, cutoff = 0.02.
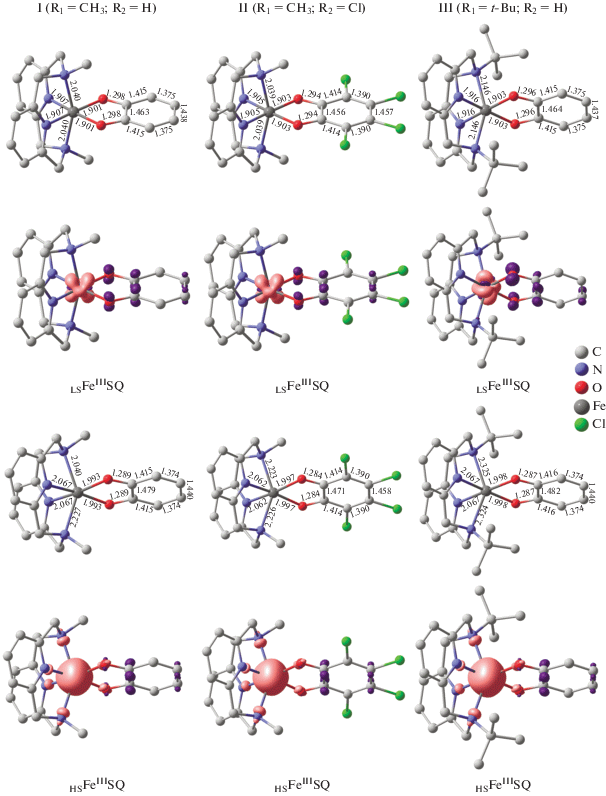
Таблица 1.
Спин (S), полная энергия (Е), значение оператора квадрата спина (S2), спиновая плотность на ионе железа $\left( {q_{{\text{s}}}^{{\text{M}}}} \right)$ и редокс-активном лиганде $\left( {q_{{\text{s}}}^{{\text{L}}}} \right)$ в изомерах дикатионных комплексов I–III (R1 = CH3, трет-Bu; R2 = H, Cl), рассчитанные методом DFT UTPSSh/6-311++G(d,p)
| Изомер | S | Е, ат. ед. | S2 | $q_{{\text{s}}}^{{\text{M}}}$ | $q_{{\text{s}}}^{{\text{L}}}$ |
|---|---|---|---|---|---|
| I (R1 = CH3; R2 = H) | |||||
| LSFeIIISQ | 2/2 | –2485.93717 | 2.042 | 1.13 | 1.02 |
| BS | 0 | –2485.94721 | 0.667 | 0.72 | –0.74 |
| HSFeIIISQ | 6/2 | –2485.91384 | 12.014 | 4.23 | 1.38 |
| BS | 4/2 | –2485.92421 | 6.662 | 4.04 | –0.47 |
| II (R1 = CH3; R2 = Cl) | |||||
| LSFeIIISQ | 2/2 | –4324.40185 | 2.043 | 1.07 | 1.05 |
| BS | 0 | –4324.41189 | 0.691 | 0.74 | –0.75 |
| HSFeIIISQ | 6/2 | –4324.38017 | 12.015 | 4.14 | 1.40 |
| BS | 4/2 | –4324.38940 | 6.679 | 4.03 | –0.47 |
| III (R1 = трет-Bu; R2 = H) | |||||
| LSFeIIISQ | 2/2 | –2721.88466 | 2.062 | 1.11 | 1.06 |
| BS | 0 | –2721.89029 | 0.752 | 0.78 | –0.79 |
| HSFeIIISQ | 6/2 | –2721.86755 | 12.014 | 4.03 | 1.49 |
| BS | 4/2 | –2721.87801 | 6.649 | 3.84 | –0.43 |
Таблица 2.
Спин (S), относительная энергия с учетом обменных взаимодействий (ΔE) и величина параметра обменных взаимодействий (J) в изомерах дикатионных комплексов I–III (R1 = CH3, трет-Bu; R2 = H, Cl), рассчитанные методом DFT UTPSSh/6-311++G(d,p)
| Изомер | S | ΔE*, ккал/моль | J, см–1 |
|---|---|---|---|
| I (R1 = CH3; R2 = H) | |||
| LSFeIIISQ | 2/2 | 0.0 | –1603 |
| HSFeIIISQ | 6/2 | 14.4 | –425 |
| II (R1 = CH3; R2 = Cl) | |||
| LSFeIIISQ | 2/2 | 0.0 | –1630 |
| HSFeIIISQ | 6/2 | 14.1 | –380 |
| III (R1 = трет-Bu; R2 = H) | |||
| LSFeIIISQ | 2/2 | 0.0 | –943 |
| HSFeIIISQ | 6/2 | 7.7 | –428 |
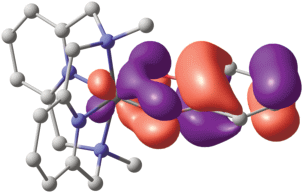
Рис. 2.
Форма магнитной орбитали изомера LSFeIIISQ комплекса I (R1 = CH3; R2 = H), согласно расчетам методом DFT UTPSSh/6-311++G(d,p). Атомы водорода опущены для ясности, cutoff = 0.036.
На секстетной ППЭ локализован изомер HS-FeIIISQ, содержащий высокоспиновый трехвалентный ион железа и семихинон. Как следует из данных, приведенных в табл. 1, количество спиновой плотности на атоме металла составляет 4.23, что меньше значения, ожидаемого для пяти неспаренных электронов. В то же время этот параметр на редокс-активном лиганде равен 1.38 (табл. 1). Следовательно, в высокоспиновом изомере HSFeIIISQ имеет место перенос спиновой плотности с иона металла на донорные атомы о‑бензохинона и N,N'-диметил-2,11-диаза[3.3]-(2,6)пиридинофана (рис. 1). Расчет состояния BS и последующий анализ обменных взаимодействий указывает на сильное антиферромагнитное связывание, приводящее, как и в низкоспиновом изомере LSFeIIISQ, к уменьшению $q_{{\text{s}}}^{{\text{M}}}$ и $q_{{\text{s}}}^{{\text{L}}}$ (табл. 1). Вычисленная разность энергий между электромерами комплекса I (R1 = CH3; R2 = H) превышает значения, характерные для СКО комплексов железа [1], и не позволяет ожидать протекания в нем термически инициированного спинового перехода (табл. 2).
Известно [13], что введение электроноакцепторных заместителей в редокс-активный фрагмент облегчает протекание термически индуцированного СКО в о-семихиноновых комплексах железа с тетраазамакроциклическими лигандами. С целью поиска соединения, способного претерпевать спиновые переходы на ионе Fe3+, изучено производное II (R1 = CH3; R2 = Cl). Расчеты показали, что хлорные заместители в радикальном лиганде не оказывают существенного влияния на энергетические и магнитные характеристики электромеров данного комплекса (табл. 1, 2, рис. 1). Дестабилизация изомера HSFeIIISQ по отношению к низкоспиновой структуре LSFeIIISQ на 14.1 ккал/моль свидетельствует о термической недостижимости высокоспинового состояния. В электромере на дублетной ППЭ ожидаются сильные антиферромагнитные обменные взаимодействия (J = –1630 см–1), приводящие к диамагнетизму комплекса II (R1 = = CH3; R2 = Cl) в широком диапазоне температур.
Ранее экспериментально [14] и теоретически [21, 22] была показана способность объемистых заместителей при донорных атомах тетраазамакроциклических лигандов затруднять формирование низкоспинового изомера, характеризующегося более короткими координационными связями. Этот эффект приводит к сокращению разности энергий между электромерами до величин, благоприятствующих протеканию термически управляемого СКО. С учетом вышеизложенного, изучен комплекс III (R1 = трет-Bu; R2 = H). Расчеты показали, что замена метильных заместителей при атомах азота пиридинофанового лиганда на трет-бутильные группы сопровождается изменениями геометрических и энергетических характеристик электромеров (табл. 1, 2, рис. 1). Так, расстояния Fe–N увеличиваются на 0.1 Å по сравнению со значениями, вычисленными для изомеров комплекса I (R1 = CH3; R2 = Н). Это приводит к понижению устойчивости низкоспиновой структуры и сужению энергетической щели между электромерами LSFeIIISQ и HSFeIIISQ до 7.7 ккал/моль, что делает возможным реализацию спинового перехода на ионе железа. Обменные взаимодействия в соединении III (R1 = трет-Bu; R2 = H), как и в рассмотренных выше системах, носят сильный антиферромагнитный характер. Следовательно, ожидаемая перегруппировка LSFeIIISQ ⇄ HSFeIIISQ будет сопровождаться переходом комплекса из диамагнитного (S = 0) в парамагнитное квинтетное (S = = 4/2) состояние, что позволяет рассматривать комплекс III (R1 = трет-Bu; R2 = H) в качестве кандидата для дизайна молекулярных переключателей.
Таким образом, посредством квантово-химического моделирования дикатионных о-семихиноновых комплексов железа с производными пиридинофана установлено, что электроноакцепторные группы в радикальном лиганде не оказывают заметного влияния на свойства изученных координационных соединений, в то время как варьирование заместителей при атомах азота тетрадентатного основания сопровождается изменением геометрических и энергетических характеристик изомеров. Между спинами неспаренных электронов трехвалентного иона железа и анион-радикальной формы о-хинона предсказаны сильные антиферромагнитные обменные взаимодействия, приводящие к диамагнетизму основного состояния. Предложен дикатионный о-бензохиноновый комплекс железа с N,N'-ди-трет-бутил-2,11-диаза[3.3]-(2,6)пиридинофаном, способный проявлять термически инициированный спин-кроссовер. Выполненный ранее синтез координационного соединения I (R1 = CH3; R2 = H) [15] позволяет ожидать получения его аналога, включающего трет-бутильные группы при донорных атомах азота.
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
Stable Radicals: Fundamentals and Applied Aspects of Odd-Electron Compounds / Ed. Hicks R.G. Chichester: John Wiley & Sons, Ltd., 2010. 606 p.
Demir S., Jeon I.-R., Long J.R., Harris T.D. // Coord. Chem. Rev. 2015. V. 289–290. P. 149.
Sato O. // Nature Chem. 2016. V. 8. № 7. P. 644.
Spin-Crossover Materials: Properties and Applications / Ed. Halcrow M.A. Chichester: John Wiley & Sons, 2013. 564 p.
Shultz D.A. // Magnetism: Molecules to Materials II / Eds. Miller J.S., Drillon M. N.Y.: Wiley, 2001. P. 281.
Tezgerevska T., Alley K.G., Boskovic C. // Coord. Chem. Rev. 2014. V. 268. P. 23.
Золотухин А.А., Бубнов М.П., Черкасов В.К., Абакумов Г.А. // Коорд. химия. 2018. Т. 44. № 2. С. 123 (Zolotukhin A.A., Bubnov M.P., Cherkasov V.K. et al. // Russ. J. Coord. Chem. 2018. V. 44. № 4. Р. 272).https://doi.org/10.1134/S1070328418040085
Protasenko N.A., Poddel’sky A.I., Bogomyakov A.S. et al. // Inorg. Chim. Acta. 2019. V. 489. P. 1.
Buchanan R.M., Pierpont C.G. // J. Am. Chem. Soc. 1980. V. 102. P. 4951.
Старикова А.А., Минкин В.И. // Успехи химии. 2018. Т. 87. № 11. С. 1049 (Starikova A.A., Minkin V.I. // Russ. Chem. Rev. 2018. V. 87. № 11. Р. 1049).
Ивахненко Е.П., Кощиенко Ю.В., Князев П.А. и др. // Коорд. химия. 2016. Т. 42. № 4 С. 221 (Ivakhnenko E.P., Koshchienko Y.V., Knyazev P.A. et al. // Russ. J. Coord. Chem. 2016. V. 42. № 4. Р. 252).https://doi.org/10.1134/S1070328416040011
Bencinia A., Caneschia A., Carbonera C. et al. // J. Mol. Struct. 2003. V. 656. № 1–3. P. 141.
Floquet S., Simaan A.J., Rivière E. et al. // Dalton Trans. 2005. № 9. P. 1734.
Graf M., Wolmershäuser G., Kelm H. et al. // Angew. Chem. Int. Ed. 2010. V. 49. № 5. P. 950.
Koch W.O., Schünemann V., Gerdan M. et al. // Chem. Eur. J. 1998. V. 4. № 7. P. 1255.
Frisch M.J., Trucks G.W., Schlegel H.B. et al. Gaussian-09. Revision E. 01. Wallingford: Gaussian, 2013.
Tao J.M., Perdew J.P., Staroverov V.N., Scuseria G.E. // Phys. Rev. Lett. 2003. V. 91. № 14. P. 146401.
Staroverov V.N., Scuseria G.E., Tao J., Perdew J.P. // J. Chem. Phys. 2003. V. 119. № 23. P. 12129.
Bannwarth A., Schmidt S.O., Peters G. et al. // Eur. J. Inorg. Chem. 2012. № 16. P. 2776.
Cirera J., Paesani F. // Inorg. Chem. 2012. V. 51. № 15. P. 8194.
Стариков А.Г., Старикова А.А., Минкин В.И. // До-кл. РАН. 2016. Т. 467. № 3. С. 300. (Starikov A.G., Starikova A.A., Minkin V.I. // Dokl. Chem. 2016. V. 467. № 1. Р. 83).
Starikova A.A., Chegerev M.G., Starikov A.G., Minkin V.I. // Comp. Theor. Chem. 2018. V. 1124. P. 15.
Старикова А.А., Минкин В.И. // Коорд. химия. 2018. Т. 44. № 4. С. 229 (Starikova A.A., Minkin. V.I. // Russ. J. Coord. Chem. 2018. V. 44. № 8. Р. 483).https://doi.org/10.1134/S1070328418080079
Стариков А.Г., Старикова А.А., Чегерев М.Г., Минкин В.И. // Коорд. химия. 2019. Т. 45. № 2. С. 92 (Starikov A.G., Starikova A.A., Chegerev M.G., Minkin V.I. // Russ. J. Coord. Chem. 2019. V. 45. № 2. Р. 105).https://doi.org/10.1134/S1070328419020088
Старикова А.А., Метелица Е.А., Минкин В.И. // Коорд. химия. 2019. Т. 45. № 6. 350. (Starikova A.A., Metelitsa E.A., Minkin V.I. // Russ. J. Coord. Chem. 2019. V. 45. № 6. P. 411. https://doi.org/10.1134/S1070328419060095
Noodleman L. // J. Chem. Phys. 1981. V. 74. № 10. P. 5737.
Shoji M., Koizumi K., Kitagawa Y. et al. // Chem. Phys. Lett. 2006. V. 432. № 1–3. P. 343.
Chemcraft. Version 1.7. 2013. http://www.chemcraftprog.com.
Bally T. // Nature Chem. 2010. V. 2. № 3. P. 165.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия