Координационная химия, 2019, T. 45, № 7, стр. 404-410
Гетероспиновый катехолатный комплекс меди(II) c TEMPO-иминопиридиновым лигандом
А. В. Черкасова 1, К. А. Кожанов 1, А. А. Золотухин 1, А. С. Богомяков 2, А. В. Черкасов 1, В. К. Черкасов 1, *
1 Институт металлоорганической химии им. Г.А. Разуваева РАН
Нижний Новгород, Россия
2 Международный томографический центр СО РАН
Новосибирск, Россия
* E-mail: cherkasov@iomc.ras.ru
Поступила в редакцию 11.12.2018
После доработки 22.01.2019
Принята к публикации 11.02.2019
Аннотация
Получен и охарактеризован методами ИК-спектроскопии, магнетохимии, ЭПР и РСА гетероспиновый комплекс меди(II) – (пиридин-2-илметилен)-4-амино-2,2,6,6-тетраметилпиперидин-1-оксил)-3,6-ди-трет-бутилкатехолатомедь(II) (I). Одноэлектронное окисление I AgBF4 приводит к образованию бирадикального комплекса меди(I) – бис[(пиридин-2-илметилен)-4-амино-2,2,6,6-тетраметилпиперидин-1-оксил)]медь(I) (II). Анализ параметров изотропных спектров ЭПР I и II свидетельствует о том, что они относятся к бирадикалам с быстрым (I) и промежуточным (II) обменным взаимодействием между радикальными центрами.
Одним из активно развивающихся направлений в дизайне молекулярных магнетиков является поиск новых гетероспиновых металлокомплексов, содержащих наряду с магнитным металлоцентром парамагнитный лиганд [1, 2]. B качестве таких радикальных лигандов наиболее часто используют нитроксильные (нитронилнитроксильные) радикалы [1–4] и анион-радикалы о-семихинонов [5–11]. К настоящему времени синтезировано большое число парамагнитных лигандов – функционализированных производных 2,2,6,6-тетраметилпиперидин-1-оксила, содержащих кроме нитроксильного магнитного центра группу, обеспечивающую координацию с металлом [3, 4]. Один из таких лигандов – (пиридин-2-илметилен)-4-амино-2,2,6,6-тетраметилпиперидин-1-оксил (L1), содержащий хелатный иминопиридильный сайт, способный прочно связываться с металлоцентром – впервые предложен в [4] для изучения методом ЭПР в растворе обменных взаимодействий металл–нитроксил. Целый ряд металлокомплексов марганца, кобальта, никеля и меди был исследован с помощью этой методики [12–15]. Однако молекулярная структура ни одного из изученных комплексов не была определена. Недавно мы синтезировали и охарактеризовали методами РСА и магнетохимии шестикоординационный гетероспиновый бис-о-семихиноновый комплекс кобальта с этим радикальным лигандом [16].
Настоящая работа посвящена синтезу, исследованию молекулярной структуры, магнитных свойств и изучению методом ЭПР катехолатного комплекса меди(II) с лигандом L1 – (пиридин-2-илметилен)-4-амино-2,2,6,6-тетраметилпиперидин-1-оксил)-3,6-ди-трет-бутилкатехолатомеди(II) (I).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все работы с комплексами проводили в вакуумированных ампулах с использованием очищенных по стандартным методикам органических растворителей [17]. Исходные лиганды [12, 18] и бис-о-семихинолят меди [19] получали согласно известным литературным данным.
Спектры ЭПР регистрировали на спектрометре BrukerEMX, оснащенном температурной приставкой, ЯМР-магнитометром и прецизионным частотометром. Параметры спектров ЭПР получали путем моделирования в пакете EasySpin [20] с использованием компенсации уширения линий за счет эффекта затрудненного вращения [21].
РСА кристаллического образца I (0.44 × 0.11 × × 0.10 мм) проведен на дифрактометре Bruker D8 Quest (ω-сканирование, МоКα-излучение, λ = = 0.71073 Å, T = 100 K, 2θ = 56.93°). Измерение и интегрирование экспериментальных наборов интенсивностей, учeт поглощения и уточнение структуры проведены с использованием программных пакетов APEX3 [22], SADABS [23] и SHELX [24]. Кристаллы I (C29H41CuN3O3 ∙ 1/2C7H8) моноклинные, пр. гр. P21/n, a = 12.3955(4), b = 12.7099(4), c = 20.2488(6) Å, β = 105.2380(10)°, V = 3077.95(17) Å3, Z = 4, ρ(выч.) = 1.272 мг/м3, μ = 0.746 мм–1. Измерено 36 942 отражения; 7712 независимых рефлексов (Rint = 0.0269) использованы для уточнения 463 параметров структуры полноматричным МНК по $F_{{hkl}}^{2}$ в анизотропном приближении для неводородных атомов. Атомы водорода помещены в геометрически рассчитанные положения и уточнены изотропно с фиксированными тепловыми параметрами U(H)изо = 1.2U(C)экв (U(H)изо = 1.5U(C)экв для метильных групп).
Анализ синтеза Фурье электронной плотности показал, что иминопиридинатный лиганд и сольватная молекула толуола в I разупорядочены каждый по двум положениям. Инструкции SADI, DFIX, ISOR, EADP и RIGU использованы для ограничения геометрических характеристик и анизотропных параметров атомных смещений при уточнении разупорядоченных фрагментов. После финального уточнения wR2 = 0.0827 и S(F 2) = 1.027 для всех отражений (R1 = 0.0316 для I > 2σ(I)). Остаточные максимум и минимум электронной плотности составили 0.50/–0.53 e/Å3.
Структура I зарегистрирована в Кембриджском банке структурных данных (CCDC № 1882883; ccdc.cam.ac.uk/structures).
Магнитную восприимчивость (χ) поликристаллического образца измеряли на SQUID-магнетометре MPMSXL фирмы Quantum Design в температурном интервале 2–300 K при напряженности магнитного поля 5 кЭ. Парамагнитные составляющие магнитной восприимчивости определяли с учетом диамагнитного вклада, оцененного из констант Паскаля. Эффективный магнитный момент (μэфф) вычисляли по формуле [3kχT/$\left( {{{N}_{{\text{A}}}}\mu _{{\text{B}}}^{{\text{2}}}} \right)$]1/2, где NA, μB и k – число Авогадро, магнетон Бора и постоянная Больцмана соответственно.
Синтез комплекса I. В вакуумированной ампуле к раствору бис-(3,6-ди-трет-бутилбензосемихиноляту-1,2)меди(II) (0.0504 г, 10–4 моль) в толуоле (30 мл) добавляли раствор L1 (0.0260 г, 10–4 моль) в толуоле (15 мл). Реакционную смесь выдерживали при комнатной температуре в течение суток. Выделившийся кристаллический продукт темно-синего цвета отфильтровывали, промывали холодным толуолом и высушивали в вакууме. Продукт включает молекулу толуола на две молекулы комплекса. Выход 0.055 г (93%).
ИК-спектр (ν, см–1): 509 сл, 533 сл, 575 ср, 593 ср, 651 с, 693 с, 715 сл, 742 с, 762 с, 777 с, 808 ср, 887 сл, 923 ср, 938 с, 977 с, 1026 с, 1043 сл, 1067 сл, 1082 сл, 1107 ср, 1145 ср, 1160 сл, 1177 ср, 1194 сл, 1207 сл, 1258 с, 1279 ср, 1292 сл, 1305 сл, 1314 сл, 1347 сл, 1353 сл, 1362 сл, 1378 с, 1402 с, 1447 сл, 1462 с, 1482 л, 1493 сл, 1553 сл, 1568 сл, 1596 с, 1633 ср, 2854 с, 2924 с, 2950 с.
| Найдено, %: | C 67.15; | H 7.98; | N 7.05; | Cu 10.63. |
| Для C32.5H46N3O3Cu | ||||
| вычислено, %: | C 66.13; | H 7.86; | N 7.12; | Cu 10.77. |
Синтез комплекса ((пиридин-2-илметилен)-4-амино-циклогексил)-3,6-ди-трет-бутилкатехолатомеди(II) (I') выполняли по аналогичной для I методике, но с использованием лиганда с циклогексильным заместителем (L1') (0.019 г, 10–4 моль) вместо L1. Подобно комплексу I, продукт включает молекулу толуола на две молекулы комплекса. Выход 0.046 г (89%).
ИК-спектр (ν, см–1): 550 сл, 621 сл, 697 сл, 722 сл, 760 ср, 846 сл, 887 сл, 922 сл, 964 сл, 994 сл, 1042 с, 1078 сл, 1135 сл, 1247 ср, 1342 с, 1376 с, 1459 с, 1465 ср, 1561 с, 1640 с, 2852 с, 2923 с, 2944 с.
| Найдено, %: | C 68.75; | H 8.09; | N 5.35; | Cu 12.18. |
| Для C29.5H40N2O2Cu | ||||
| вычислено, %: | C 68.38; | H 7.78; | N 5.41; | Cu 12.26. |
Синтез комплекса бис[(пиридин-2-илметилен)-4-амино-2,2,6,6-тетраметилпиперидин-1-оксил)]меди(I) (II). а) К смеси комплекса I (0.0295 г, 5 × 10–5 моль) и AgBF4 (0.0097 г, 5 × × 10–5 моль) приконденсировали 5 мл ТГФ в вакууме. Реакционную смесь анализировали методом ЭПР без выделения.
б) К смеси CuCl (0.0050 г, 5 × 10–5 моль), KPF6 (0.0092 г, 5 × 10–5 моль) и L1 (0.0260 г, 10–4 моль) приконденсировали 15 мл ТГФ в вакууме. С течением времени в спектре ЭПР наблюдается постепенная трансформация сигнала L1 в сигнал комплекса II. Продукт в индивидуальном виде не выделяли.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
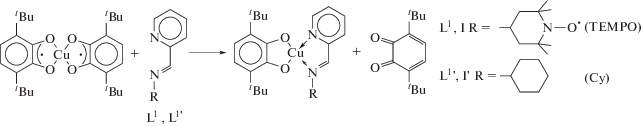
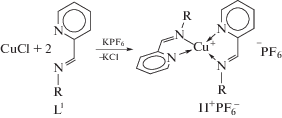
Катехолатные комплексы, содержащие TEMPO-иминопиридиновый L1 (I) и его нерадикальный аналог циклогексилиминопиридиновый L1' (I') лиганды, синтезировали по реакции замещения из бис-о-семихинолята меди(II) [19]:
Комплекс I, выделенный в индивидуальном виде, представляет собой кристаллическое вещество темно-синего цвета, хорошо растворимое в тетрагидрофуране, хлористом метилене и полностью нерастворимое в толуоле и предельных углеводородах. Его состав и строение охарактеризованы методами РСА, спектроскопии ЭПР, ИК и магнетохимии.
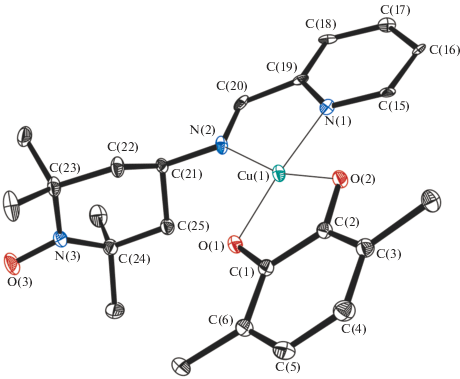
По данным РСА, соединение I представляет собой комплекс меди(II), в котором катион Cu2+ связан с двумя атомами кислорода катехолатного лиганда и двумя атомами азота иминопиридинатного лиганда (рис. 1). В симметрически независимой области кристаллической ячейки, помимо молекулы комплекса, содержится также центросимметричная сольватная молекула толуола. Таким образом, соединение I кристаллизуется в форме (Cat)Cu(TEMPO-ImPy) ∙ 1/2(C7H8). Координационный полиэдр атома Cu(II) – искаженный квадрат. Двугранный угол между плоскостями O(1)C(1)C(2)O(2) и N(1)C(19)C(2)N(2) хинонового и иминопиридинатного фрагментов равен 13.4(2)°. Атом Cu(II) практически не отклоняется (всего на 0.02(2) Å) от средней плоскости O(1)O(2)N(1)N(2), а сумма валентных углов при атоме меди составляет 361.1(5)°, что близко к значению для идеальной плоской квадратной структуры (360°). Длины связей C–O и С–С в хиноновом фрагменте (1.344(2)–1.345(2) и 1.421(2) Å соответственно) позволяют однозначно охарактеризовать структуру хинонового лиганда как катехолатную. Длины связей Cu–O 1.869(2)–1.880(2) Å также соответствуют значениям, характерным для катехолатных комплексов меди(II) [25].
Рис. 1.
Молекулярная структура комплекса I. Тепловые эллипсоиды приведены с 30% вероятностью. Атомы водорода и метильные группы трет-бутильных заместителей не изображены для ясности.
Иминопиридинатный лиганд в I полностью разупорядочен по двум положениям в соотношении ~50/50%. Поскольку геометрические характеристики разупорядоченных фрагментов близки, ниже приведены длины связей и углы для одного из положений лиганда. Длины связей Cu–N(1) и Cu–N(2) сопоставимы между собой и составляют 2.04(2) и 2.055(9) Å соответственно. Связь N(2)–C(20) (1.274(9) Å) значительно короче, чем C(19)–C(20) (1.453(5) Å), что типично для лигандов такого типа. Фрагмент TEMPO в I находится в конформации кресла: двугранный угол между плоскостями C(21)C(22)C(25) и C(22)C(23)C(24)C(25) равен 55.4(3)°, между C(22)C(23)C(24)C(25) и C(23)N(3)C(24) – 32.8(5)°. Гетероцикл практически перпендикулярен иминопиридинатному фрагменту: двугранный угол между плоскостями N(1)C(19)C(20)N(2) и C(21)C(22)C(23)N(3)C(24)C(25) составляет 82.5(3)°.
Анализ кристаллической упаковки показал, что в I реализуются межмолекулярные взаимодействия O···H между атомом кислорода нитроксильной и атомом водорода CH-групп иминопиридиновых фрагментов соседних молекул. Расстояние O···HIm (1.93(4) Å) значительно меньше суммы ван-дер-ваальсовых радиусов O и H (2.7 Å). Расстояние O···HРy заметно больше, чем O···HIm, и равно 2.50(4) Å. Также в I имеют место многочисленные межмолекулярные взаимодействия H···H, расстояния H···H лежат в широком интервале значений 2.16(5)–2.39(5) Å.
В ИК-спектре комплекса I содержатся интенсивные полосы при 1246 и 1258 см–1 ν(C–O), соответствующие двум одинарным связям CO катехолатного фрагмента [25]. Также присутствует полоса 1635 см–1 ν(C=N), относящаяся к двойной связи CN координированного иминонитроксильного фрагмента [14].
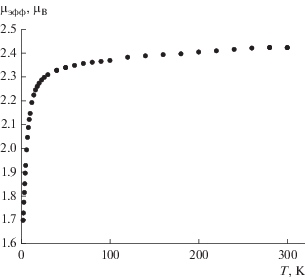
Комплекс I парамагнитен. Значение µэфф составляет 2.47 µB при 300 К и при понижении температуры до 50 K практически не меняется, после чего уменьшается до 1.77 µB при 2 K (рис. 2). Высокотемпературное значение µэфф согласуется с теоретической чисто спиновой величиной 2.45 µB для двух парамагнитных центров со спинами S = 2 – одного иона Cu2+ и одного нитроксила. Уменьшение µэфф ниже 50 K указывает на наличие антиферромагнитных обменных взаимодействий между магнитными центрами, и значение µэфф при 2 K согласуется с теоретической величиной для одного парамагнитного центра. В соответствии со структурными данными, такими каналами межмолекулярного антиферромагнитного обмена в I могут служить межмолекулярные взаимодействия O···H между атомом кислорода нитроксильной и атомом водорода CH-групп иминопиридиновых фрагментов. Таким образом, парамагнетизм комплекса при низких температурах обусловлен только спинами ионов Cu2+. Анализ зависимости µэфф(T) проводили в рамках модели для обменно-связанного димера (H = –2JS1S2, gR = 2 фиксированы с учетом вклада в магнитную восприимчивость ионов Cu2+ согласно закону Кюри). Оптимальные значения параметра межмолекулярного обменного взаимодействия (J') и gCu составляют 4.1 см–1 и 2.04 соответственно.
Спектр ЭПР комплекса I (рис. 3а) представляет собой квартет (1 : 1 : 1 : 1), обусловленный сверхтонким взаимодействием (СТВ) с магнитными изотопами 63Cu, 65Cu атома меди(II) (gi = = 2.0552, aCu11 = 4.8 мТл, где aCu – константа СТВ). В спектре также наблюдается примесный сигнал исходного иминопиридинового лиганда в виде триплета 1 : 1 : 1 (gi = 2.0057, aN = 1.55 мТл), интегральная интенсивность которого менее 1%.
Рис. 3.
Спектры ЭПР комплексов (эксп.) и их компьютерная симуляция (сим.): I (а), I' (б), ${\text{I}}{{{\text{I}}}^{ + }}{\text{BF}}_{{\text{4}}}^{--}$ (в) (ТГФ (а, в), толуол (б); комнатная температура).
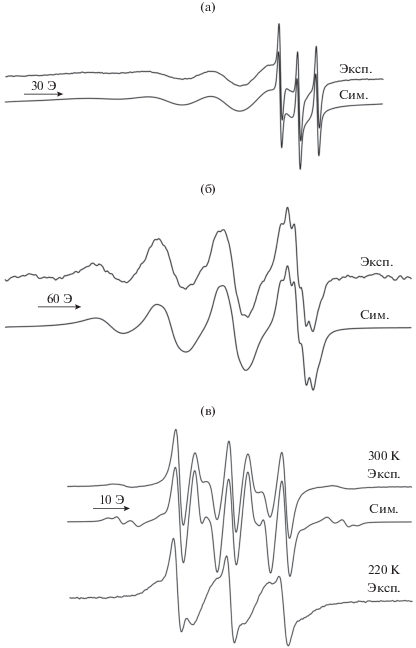
Наблюдаемые значения gi = 2.0552 и aCu = 4.8 мТл для комплекса I существенно отличаются от соответствующих значений, характерных для аналогичных катехолатных комплексов меди (II) с диазалигандами [25]. Так, изотропный спектр ЭПР аналогичного катехолатного комплекса с диамагнитным иминопиридиновым лигандом L1' (I') (рис. 3б) имеет характерные для производных меди(II) параметры спектра ЭПР (gi = 2.0927, aCu = = 9.5 мТл). Дополнительно наблюдается сверхтонкое расщепление на ядрах азота 14N иминопиридинового фрагмента (aN(1) = 1.14 мТл, aN(2) = 1.02 мТл).
Параметры спектра ЭПР комплекса I характерны для бирадикальных соединений, в которых величина константы электрон-электронного взаимодействия (J) значительно превышает константу СТВ (J $ \gg $ a) [26]. Быстрый обмен между радикальными центрами в таких системах приводит к усреднению их параметров. Наблюдаемые экспериментальные значения комплекса I удовлетворяют этому правилу: величина gi = 2.0552 составляет ~1/2 от суммы значений gi = 2.0927 и 2.0057. Константа СТВ, равная 4.8 мТл, с магнитными изотопами вдвое меньше соответствующей aCu = 9.5 мТл в комплексе I'. Отсутствие явно выраженной сверхтонкой структуры на ядрах азота 14N нитроксильной группы (ожидаемое значение aN ≈ 0.77 мТл) и иминопиридинового фрагмента (ожидаемое значение aN ≈ 0.55 мТл) в спектре ЭПР комплекса I связано, по-видимому, с тем, что величина сверхтонкого расщепления существенно меньше ширины линии (~2.0 мТл).
Таким образом, комплекс I имеет бирадикальный характер с локализацией парамагнитных центров на ионе меди(II) и нитроксильной группе TEMPO-фрагмента.
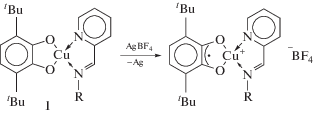
Исходя из свойственной диоксоленовым комплексам редокс-активности [27], мы предприняли попытку одноэлектронного окисления катехолатного лиганда в I с целью получения о-семихинонового производного, содержащего сразу три радикальных центра (о-семихинон, нитроксил и Cu(II)):
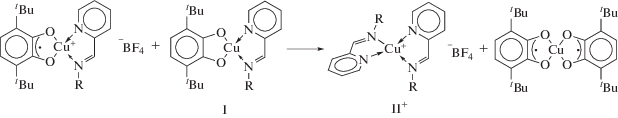
Однако окисление комплекса I не приводит к желаемому результату. При действии AgBF4 на раствор комплекса I в ТГФ появляется спектр ЭПР (рис. 3в), типичный для бис-нитроксильных бирадикалов c J ≈ a [26]. Сверхтонкое взаимодействие с магнитными изотопами 63Cu, 65Cu отсутствует. Наблюдаемый спектр ЭПР соответствует бис-иминопиридиновому комплексу Cu(I) – ${\text{I}}{{{\text{I}}}^{ + }}{\text{BF}}_{{\text{4}}}^{--},$ содержащему два радикальных лиганда L1, координированных с ионом Cu+. Его образование возможно в результате обмена лигандами первичного продукта окисления с исходным комплексом I:
Аналогичный бис-лигандный комплекс ${\text{I}}{{{\text{I}}}^{ + }}{\text{PF}}_{{\text{6}}}^{--},$ содержащий идентичный катион, образуется непосредственно при взаимодействии L1 с CuPF6. Параметры его изотропного спектра ЭПР полностью совпадают с соответствующими значениями комплекса II+BF4:
Температурная зависимость спектров ЭПР ${\text{I}}{{{\text{I}}}^{ + }}{\text{BF}}_{{\text{4}}}^{--}$ и ${\text{I}}{{{\text{I}}}^{ + }}{\text{PF}}_{{\text{6}}}^{--}$ полностью соответствует поведению нитроксильных бирадикальных систем, для которых характерна зависимость параметра J от температуры [26]. Анализ температурной зависимости параметров спектров ЭПР II+ показывает, что константа J монотонно уменьшается от J ≈ 26 Э при 300 К до J ≈ 7 Э при 220 К и ниже.
Таким образом, на базе радикального TEMPO-иминопиридинового лиганда L1 синтезированы два новых гетероспиновых комплекса – (пиридин-2-илметилен)-4-амино-2,2,6,6-тетраметилпиперидин-1-оксил)-3,6-ди-трет-бутил-катехолатомедь(II) (I) и бис[(пиридин-2-илметилен)-4-амино-2,2,6,6-тетраметилпиперидин-1-оксил)]медь(I) (II+B${\text{F}}_{4}^{ - }$). Анализ параметров изотропных спектров ЭПР I и II показывает, что они относятся к бирадикалам с быстрым (J $ \gg $ a, I) или промежуточным (J ≈ a, II) обменным взаимодействием между радикальными центрами.
БЛАГОДАРНОСТИ
Авторы благодарят Российский научный фонд за финансовую поддержку (грант № 14-13-01296).
Рентгенодифракционные исследования проведены в рамках госзадания (тема № 44.2, рег. № АААА-А16-116122110053-1) с использованием научного оборудования Центра коллективного пользования “Аналитический центр ИМХ РАН”.
Список литературы
Ovcharenko V. Metal-Nitroxide Complexes: Synthesis and Magnetostructural Correlations. Ch. 13 // Stable Radicals: Fundamentals and Applied Aspects of Odd-Electron Compounds. John Wiley & Sons: Ltd., 2010. P. 461.
Fedin M.V., Veber S.L., Bagryanskaya E.G. et al. // Coord. Chem. Rev. 2015. V. 289–290. P. 341.
Eaton S.S. // Coord. Chem. Rev. 1978. V. 26. P. 20.
Eaton S.S., Eaton G.R. // Coord. Chem. Rev. 1988. V. 83. P. 29.
Pierpont C.G., Buchanan R.M. // Coord. Chem. Rev. 1981. V. 38. P. 45.
Pierpont C.G. // Coord. Chem. Rev. 2001. V. 219–221. P. 415.
Pierpont C.G. // Coord. Chem. Rev. 2001. V. 216−217. P. 99.
Hendrickson D.N., Pierpont C.G. Valence Tautomeric Transition Metal Complexes. Spin Crossover in Transition Metal Compounds II. Berlin: Springer, 2004. V. 234. P. 63.
Pierpont C.G., Lange C. W. The Chemistry of Transition Metal Complexes Containing Catechol and Semiquinone Ligands. Progress in Inorganic Chemistry. N.Y.: John Wiley & Sons, Inc., 2007. P. 331.
Pierpont C.G., Kelly J.K. Coordination Chemistry of o‑Semiquinones. PATAI’S Chemistry of Functional Groups. N.Y.: John Wiley & Sons, Ltd., 2009.
Poddel’sky A.I., Cherkasov V.K., Abakumov G.A. // Coord. Chem. Rev. 2009. V. 253. P. 291.
Boymel P.M., Eaton G.R., Eaton S.S. // Inorg. Chem. 1980. V. 19. № 3. P. 727.
Boymel P.M., Braden G.A., Eaton G.R. et al. // Inorg. Chem. 1980. V. 19. № 3. P. 735.
Hard S., Eaton G.R. // J. Magnetic Resonance. 1983. V. 51. P. 470.
More J.K., More K.M., Eaton G.R. et al. // J. Am. Chem. Soc. 1984. V. 106. P. 5395.
Zolotukhin A.A., Bubnov M.P., Arapova A.V. et al. // Inorg. Chem. 2017. V. 56. P. 14751.
Armarego W.L.F., Chai C. Purification of Laboratory Chemicals. Butterworth-Heinemann, 2013. 1002 p.
Kim S., Kim E., Lee H.J. et al. // Polyhedron. 2014. V. 69. P. 149.
Abakumov G.A., Lobanov A.V., Cherkasov V.K. et al. // Inorg. Chim. Acta. 1981. V. 49. P. 135.
Stoll S., Schweiger A. // J. Magnetic Resonance. 2006. V. 178. P. 42.
Kozhanov K.A., Bubnov M.P., Teplova I.A. et al. // J. Mol. Struct. 2017. V. 1147. P. 541.
APEX3. Version 2016-9. Madison (WI, USA): Bruker AXS Inc., 2016.
Krause L., Herbst-Irmer R., Sheldrick G.M. et al. // J. Appl. Cryst. 2015. V. 48. P. 3.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3.
Davidson R.A., Hao J., Rheingold A.L. et al. // Polyhedron. 2017. V. 133. P. 348.
Бучаченко А.Л., Вассерман А.М. Стабильные радикалы. Электронное строение, реакционная способность и применение. М.: Химия, 1973. 408 с.
Абакумов Г.А., Черкасов В.К., Неводчиков В.И. и др. // Изв. АН. Сер. хим. 1996. № 2. С. 464.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия