Координационная химия, 2019, T. 45, № 8, стр. 497-503
Природа конформационного полиморфизма в кристаллах комплекса Ph3Sb(O2CCH2–CH=CH2)2
Г. К. Фукин 1, *, Е. В. Баранов 1, А. В. Черкасов 1, Р. В. Румянцев 1
1 Институт металлоорганической химии им. Г.А. Разуваева РАН
Нижний Новгород, Россия
* E-mail: gera@iomc.ras.ru
Поступила в редакцию 27.12.2018
После доработки 01.02.2019
Принята к публикации 14.03.2019
Аннотация
В процессе кристаллизации комплекса Ph3Sb(O2CCH2−CH=CH2)2 при быстром испарении растворителя (бензол) образуются моноклинные кристаллы (I), тогда как при медленном – триклинные (II). Кроме того, моноклинные кристаллы в течение полугода самопроизвольно трансформируются в триклинные. Показано, что наличие пустот около одного из карбоксилатных лигандов в моноклинной фазе комплекса Ph3Sb(O2CCH2−CH=CH2)2 приводит к уменьшению энергии межмолекулярных взаимодействий и, как следствие, к изменению его конформации с заметным понижением энергии кристаллической решетки. Другими словами, наличие пустот в кристалле моноклинной фазы позволяет реализовать более термодинамически выгодную конформацию молекул в кристалле. Определено несколько структурных моделей комплекса Ph3Sb(O2CCH2−CH=CH2)2 (СIF files № 1 887 561 (IIAM) – модель невзаимодействующих атомов, 1 887 562 (I) – мультипольная модель, 1887563 (IIIAM) – модель невзаимодействующих атомов, 1 887 564 (II) – мультипольная модель).
Карбоксилатные комплексы триарилсурьмы проявляют противоопухолевую активность [1–8], что потенциально важно при лечении онкологических заболеваний. Однако существуют и побочные эффекты, основным из которых является высокая токсичность таких препаратов. Поэтому большинство исследований карбоксилатных производных Sb(V) направлены на изучение взаимосвязи химических и фармакологических свойств этих соединений с целью минимизации побочных эффектов и повышения их эффективности. Широкий практический интерес представляют работы по использованию карбоксилатных комплексов триарилсурьмы в полимеризации [9–11], реакциях кросс-сочетания [12–14], а также при создании фоторезистов в микроэлектронике [15]. В свою очередь, мы обнаружили, что в процессе кристаллизации комплекса Ph3Sb(O2CCH2−CH=CH2)2 (I) при быстром испарении растворителя (бензол) образуются моноклинные кристаллы, тогда как при медленном – триклинные. Моноклинные кристаллы в течение полугода самопроизвольно трансформируются в триклинные.
Настоящее исследование посвящено причинам самопроизвольной трансформации моноклинных кристаллов комплекса Ph3Sb(O2CCH2−CH=CH2)2 (I) в триклинные.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез винилуксусного комплекса трифенилсурьмы(V) I проводили по известной методике, описанной в [16].
Прецизионный РСА комплекса I и его конформационной полиморфной модификации (II) при 100 К проведен на автоматических дифрактометрах (графитовые монохроматоры, MoKα-излучение, λ = 0.71073 Å) Oxford Xcalibur (Eos детектор) для I и Bruker D8 QUEST (CMOS детектор) для II. Экспериментальные наборы интенсивностей интегрированы с помощью программ CrysAlisPro [17] и SAINT [18]. Программы SCALE3 ABSPACK [19] и SADABS [20] использованы для введения поправок на поглощение. Структуры расшифрованы прямым методом и уточнены полноматричным МНК по F 2 (SHELXTL) [21]. Все неводородные атомы уточнены в анизотропном приближении. Атомы водорода помещены в геометрически рассчитанные положения и уточнены изотропно в модели “наездника”.
Мультипольное уточнение комплексов I и II проведено в рамках модели Хансена–Коппенса [22] с использованием программного пакета MoPro [23]. Все атомы водорода в прецизионном РСА перед мультипольным уточнением нормализованы на идеальные нейтронографические расстояния [24]. Уровень мультипольного разложения был гексадекапольным для атома сурьмы, октапольным для всех неводородных атомов и дипольным для атомов водорода. Все связанные пары атомов удовлетворяют тесту Хиршфельда [25]. Топологический анализ экспериментальной функции ρ(r) проведен при помощи программного пакета WINXPRO [26].
Наличие разупорядоченного аллильного фрагмента в II приводит к некоторым отклонениям от стандартной схемы мультипольного уточнения, в которой координаты атомов, их тепловые и мультипольные параметры уточняются последовательно. Здесь мы “разбили” молекулу на два блока. Первый содержал атомы комплекса со 100- и 80%-ной заселенностью позиций, а второй блок только с 20%-ной. Сначала уточняли одинаковые параметры в одном блоке (100%-ная + 80%-ная заселенность позиций), а затем (20%-ная заселенность позиций) в другом и так для каждого уточняемого параметра. Кроме того, разупорядоченность аллильного фрагмента привела к тому, что мы отдельно использовали программу WINXPRO для анализа топологии электронной плотности двух различных конформаций II (IIa и IIб). Заселенности позиций для каждого разупорядоченного аллильного фрагмента в этом случае были равны единице.
Основные кристаллографические характеристики и параметры РСА для мультипольной модели уточнения в комплексах I и II приведены в табл. 1.
Таблица 1.
Основные кристаллографические характеристики и параметры прецизионного РСА для мультипольной модели уточнения в комплексах I и II
| Параметр | Значение | |
|---|---|---|
| I | II | |
| Брутто-формула | C26H25O4Sb | C26H25O4Sb |
| М | 523.216 | 523.216 |
| Сингония | Моноклинная | Триклинная |
| Пр. гр. | P21/c | P1 |
| а, Å | 12.4174(2) | 8.1823(3) |
| b, Å | 22.1246(4) | 8.8194(3) |
| c, Å | 8.8020(2) | 17.9141(7) |
| α, град | 90 | 77.880(1) |
| β, град | 104.647(2) | 89.821(1) |
| γ, град | 90 | 62.885(1) |
| V, Å3 | 2339.59(8) | 1118.62(7) |
| Z | 4 | 2 |
| ρ(выч.), г см–3 | 1.486 | 1.554 |
| μ, мм–1 | 1.208 | 1.263 |
| F(000) | 1056 | 528 |
| Размер кристалла, мм | 0.45 × 0.35 × 0.20 | 0.46 × 0.18 × 0.16 |
| Область θ, град | 3.02–51.42 | 2.34–51.43 |
| Число собранных/независимых отражений | 971 802/25 476 | 336 077/28 905 |
| R1/wR2 (I > 2σ(I)) | 0.0394/0.0314 | 0.0177/0.0144 |
| GOOF | 0.993 | 0.998 |
| Остаточная электронная плотность, e Å–3 | 0.320/–0.449 | 0.311/–0.856 |
Структуры депонированы в Кембриджском банке структурных данных (КБСД) (№ 1 887 561 (IIAM) – модель невзаимодействующих атомов, 1 887 562 (I) – мультипольная модель, 1887563 (IIIAM) – модель невзаимодействующих атомов, 1887564 (II) – мультипольная модель; http://www.ccdc.cam.ac.uk/data_request/cif).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
С целью изучения самопроизвольного фазового перехода моноклинных кристаллов I в триклинные II были проведены их прецизионные РСА. Молекулярное строение комплексов представлено на рис. 1. Координационное окружение центрального атома Sb в комплексах I и II промежуточное между тригонально-бипирамидальным и тетрагонально-пирамидальным. Параметр τ для обоих комплексов равен 0.50 [27]. Комплексы I и II имеют цис-расположение карбоксилатных групп. Основные расстояния Sb(1)−O(1, 3), Sb(1)−O(2, 4) и Sb(1)−C(Ph) в комплексах I и II лежат в диапазонах 2.1196(3)–2.1512(8), 2.7778(9)–2.9816(4) и 2.1063(4)–2.1190(3) Å соответственно. Анализ КБСД [28] показывает, что такие расстояния характерны для карбоксилатных комплексов трифенилсурьмы(V). Следует отметить, что трансформация моноклинных кристаллов I в триклинные II приводит к появлению двух конформеров вследствие разупорядочения одного из аллильных фрагментов карбоксилатного лиганда в II с заселенностью позиций 80% (IIа) и 20% (IIб) (рис. 1б). Разупорядоченные фрагменты в триклинной фазе II приближенно связаны между собой зеркальной плоскостью, проходящей через карбоксилатную группу О(3)О(4)С(5). Суперпозиция молекул комплекса Ph3Sb(O2CCH2−CH=CH2)2 для моноклинной (I) и триклинной (IIa, IIб) фаз представлена на рис. 2. Наибольшие конформационные различия в структуре молекул комплекса I наблюдаются между фрагментами С(6)С(7)С(8) моноклинной (I) и триклинной (IIа) фаз (рис. 2а), а также фрагментами С(6)С(7)С(8) и С(6')С(7')С(8') в I и IIб (рис. 2б). Аллильный фрагмент С(6)С(7)С(8) винилуксусного лиганда (80%-ная заселенность позиций) в IIа развернут относительно аналогичного фрагмента С(6)С(7)С(8) в I вокруг оси С2, проходящей вдоль связей С(5)–С(6) на ~170° (рис. 2а). В свою очередь, фрагмент С(6')С(7')С(8') винилуксусного лиганда (20%-ная заселенность позиций) в IIб и С(6)С(7)С(8) в I приблизительно связаны между собой зеркальной плоскостью. Таким образом, самопроизвольная трансформация моноклинных кристаллов I приводит к образованию двух конформационных изомеров в триклинной фазе.
Рис. 1.
Молекулярное строение Ph3Sb(O2CCH2−CH=CH2)2: а − молекула моноклинной фазы (I); б − молекула триклинной фазы (II). Один из карбоксилатных лигандов в триклинной фазе разупорядочен по двум положениям с заселенностью позиций 80% (фрагмент С(6)С(7)С(8), соединение IIа) и 20% (фрагмент С(6')С(7')С(8'), соединение IIб). Тепловые эллипсоиды приведены с 30%-ной вероятностью. Атомы водорода для наглядности не показаны.
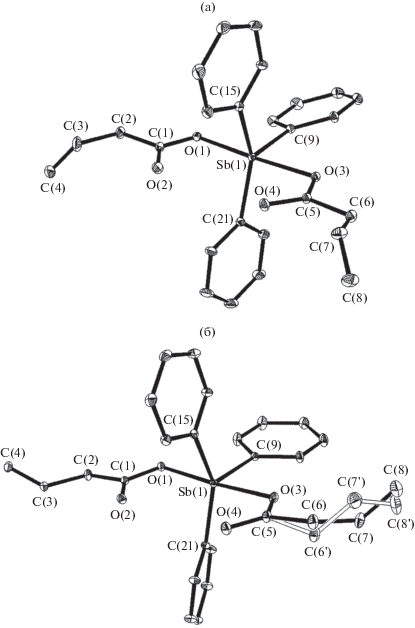
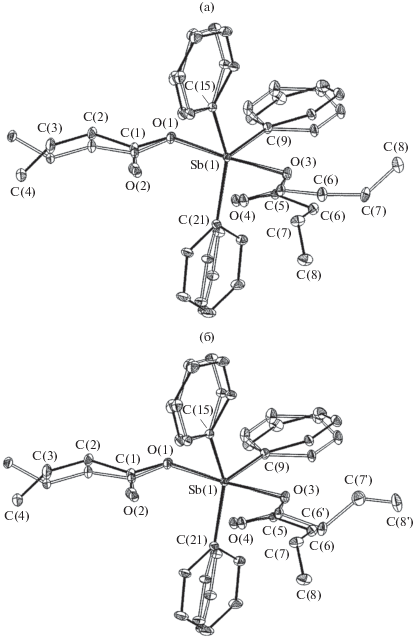
Рис. 2.
Суперпозиция молекул комплекса Ph3Sb(O2CCH2−CH=CH2)2 в моноклинной (I) и триклинной (IIа (а) и IIб (б)) фазах. Связи в молекулах моноклинной фазы представлены сплошными линиями, а в триклинной − контурными. Тепловые эллипсоиды приведены с 30%-ной вероятностью. Атомы водорода для наглядности не показаны.
Для изучения природы химических связей в координационной сфере атомов Sb в I и II, мы использовали теорию Бейдера [29], согласно которой связи Sb(1)−O(1, 3) и Sb(1)−C(15, 21) в I относятся к типу промежуточных взаимодействий (∇2ρ(r) > 0, he(r) < 0), тогда как связь Sb(1)−C(9) является взаимодействием обобществленного типа (∇2ρ(r) < 0, he(r) < 0) (табл. 2). В II все взаимодействия в координационной сфере атома сурьмы промежуточные. Отметим, что в ранее исследованных дикарбоксилатных комплексах трифенилсурьмы связи Sb−C(Ph) характеризовались как взаимодействия промежуточного типа [30, 31], так и обобществленные [32].
Таблица 2.
Расстояния и основные топологические параметры в КТ(3, −1)* в координационной сфере атома сурьмы в комплексе Ph3Sb(O2CCH2−CH=CH2)2 в моноклинной и триклинной фазах
| Связь | Расстояние, Å | ν(r), а.е. | ρ(r), а.е. | ∇2ρ(r), а.е. | he(r), а.е. |
|---|---|---|---|---|---|
| Моноклинная фаза (I) | |||||
| Sb(1)−O(1) | 2.1255(9) | –0.102 | 0.077 | 0.272 | –0.017 |
| Sb(1)−O(3) | 2.1512(8) | –0.092 | 0.071 | 0.257 | –0.014 |
| Sb(1)…O(2) | 2.8384(10) | –0.017 | 0.024 | 0.068 | 0.0001 |
| Sb(1)…O(4) | 2.7778(9) | ||||
| Sb(1)−C(9) | 2.1166(11) | –0.205 | 0.137 | –0.040 | –0.108 |
| Sb(1)−C(15) | 2.1102(12) | –0.166 | 0.117 | 0.063 | –0.075 |
| Sb(1)−C(21) | 2.1081(12) | –0.191 | 0.128 | 0.055 | –0.089 |
| Триклинная фаза (II) | |||||
| Sb(1)−O(1) | 2.1196(3) | –0.138 | 0.099 | 0.198 | –0.044 |
| Sb(1)−O(3) | 2.1277(3) | –0.128 | 0.094 | 0.205 | –0.039 |
| Sb(1)…O(2) | 2.8021(4) | ||||
| Sb(1)…O(4) | 2.9816(4) | ||||
| Sb(1)−C(9) | 2.1190(3) | –0.147 | 0.105 | 0.161 | –0.053 |
| Sb(1)−C(15) | 2.1089(3) | –0.161 | 0.113 | 0.116 | –0.066 |
| Sb(1)−C(21) | 2.1063(4) | –0.174 | 0.121 | 0.058 | –0.080 |
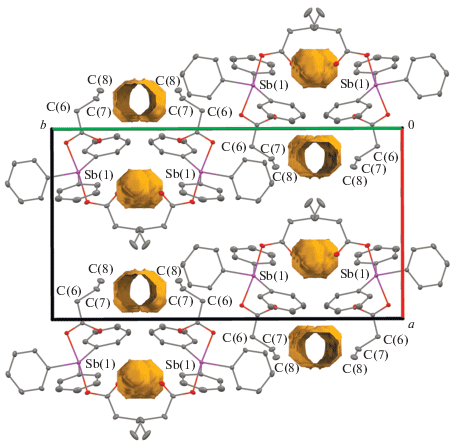
Для изучения природы конформационного полиморфизма в кристаллах Ph3Sb(O2CCH2−CH= CH2)2 были найдены все взаимодействия между молекулами комплекса в моноклинной I и триклинной II фазах и оценена их энергия по корреляции Эспинозы–Моллинса–Лекомта [33]. Интересно отметить, что энергия межмолекулярных контактов лиганда О(1, 2)С(1−4) в моноклинной фазе I (–9.41 ккал/моль) практически совпадает с аналогичным значением энергии для этого лиганда в триклинной фазе II (‒9.49 ккал/моль). Это согласуется с относительно небольшими конформационными изменениями лиганда О(1.2)С(1−4) при переходе в триклинную фазу II. В свою очередь, лиганд О(3, 4)С(5−8) при переходе из моноклинной фазы I в триклинную II подвержен существенно бóльшим конформационным изменениям. Энергия межмолекулярных контактов этого лиганда в I составляет –8.01 ккал/моль, что меньше, чем в IIа (–10.25 ккал/моль) и IIб (–8.42 ккал/моль). В результате фазового перехода энергия кристаллической решетки понижается на ∼5 ккал/моль в IIа и ∼3.5 ккал/моль в IIб, а также уменьшаются объемы молекул и, как следствие, возрастает плотность и коэффициент упаковки (табл. 3). Следует отметить, что объем аллильного фрагмента С(6)С(7)С(8) в I с учетом атомов водорода, полученный как сумма объемов атомных бассейнов, составляет 76.3 Å3, что заметно превышает объем аналогичного фрагмента в II (73.9 Å3 в IIа и 72.9 Å3 в IIб). Такое различие можно интерпретировать наличием пустот около аллильного фрагмента С(6)С(7)С(8) в I, что позволяет изменять ему свою конформацию без разрушения кристалла (рис. 3).
Таблица 3.
Энергетические и кристаллические характеристики комплекса Ph3Sb(O2CCH2−CH=CH2)2
| Моноклинная фаза (I) | Триклинная фаза (II)* |
|---|---|
| Энергия всех межмолекулярных контактов, ккал/моль | |
| –40.04 | –45.72/–43.50 |
| Плотность, г/см3 | |
| 1.486 | 1.554 |
| Коэффициент упаковки, % | |
| 70.2 | 73.3/73.1 |
| Объем молекулы (сумма объемов полиэдров Вороного–Дирихле), Å3 | |
| 596.2 | 565.5 |
| Объем молекулы (сумма объемов атомных бассейнов), Å3 | |
| 582.8 | 557.3 |
Таким образом, наличие пустот около одного из карбоксилатных лигандов в моноклинной фазе I комплекса Ph3Sb(O2CCH2−CH=CH2)2 приводит к уменьшению энергии межмолекулярных взаимодействий и, как следствие, к возможности изменения его конформации с заметным понижением энергии кристаллической решетки. Другими словами, наличие пустот в кристалле моноклинной фазы I позволяет реализовать более термодинамически выгодную конформацию молекул в кристалле.
Список литературы
Bajpai K., Singhal R., Srivastava R.C. // Indian J. Chem. A. 1979. V. 18. P. 73.
Singhal K., Rastogi R., Raj. P. // Indian J. Chem. A. 1987. T. 26. P. 146.
Ma Y., Li J., Xuan Z., Liu R. // J. Organomet. Chem. 2001. V. 620. № 1–2. P. 235.
Liu R.-C., Ma Y.-Q., Yu L. et al. // Appl. Organomet. Chem. 2003. V. 17. № 9. P. 662.
Yu L., Ma Y.-Q., Liu R.-C. et al. // Polyhedron. 2004. V. 23. № 5. P. 823.
Yu L., Ma Y.-Q., Wang G.-C. et al. // Heteroat. Chem. 2004. V. 15. № 1. P. 32.
Hadjikakou S.K., Ozturk I.I., Banti C.N. et al. // J. Inorg. Biochem. 2015. V. 153. P. 293.
Islam A., Rodrigues B.L., Marzano I.M. et al. // Eur. J. Med. Chem. 2016. V. 109. P. 254.
US Patent № 3.287.210 (C1 167–30). November 22. 1966. Appl. December 26. 1967. V. 66. № 19. 85070.
Карраер Ч., Морган М. Металлоорганические полимеры. М.: Мир, 1981. С. 121.
Котон М.M. Металлоорганические соединения и радикалы. Наука, 1985. С. 13.
Gushchin A.V., Moiseev D.V., Dodonov V.A. // Russ. Chem. Bull. 2001. V. 50. № 7. P. 1291.
Moiseev D.V., Gushchin A.V., Shavirin A.S. et al. // J. Organomet. Chem. 2003. V. 667. № 1–2. P. 176.
Qin W., Yasuike S., Kakusawa N. et al. // J. Organomet. Chem. 2008. V. 693. № 17. P. 2949.
Passarelli J., Murphy M., Del Re R. et al. // SPIE Advanced Lithography. 2015. V. 9425. P. 94250T.
Гущин А.В., Шарутин Д.В., Прыткова Л.К. и др. // Журн. общ. химии. 2011. Т. 81. № 3. С. 397.
Data Collection. Reduction and Correction Program. CrysAlis Pro-Software Package. Agilent Technologies, 2012.
SAINT. Data Reduction and Correction Program. Version 8.27B. Madison (WI, USA): Bruker AXS Inc., 2012.
SCALE3 ABSPACK: Empirical Absorption Correction. CrysAlis Pro-Software Package. Agilent Technologies, 2012.
Sheldrick G.M. SADABS-2012/1. Bruker/Siemens A-rea Detector Absorption Correction Program. Madison (WI, USA): Bruker AXS Inc., 2012.
Sheldrick G.M. SHELXTL. V.6.14. Structure Determination Software Suite. Madison (WI, USA): Bruker AXS, 2003.
Hansen N.K., Coppens P. // Acta Crystallogr. A. 1978. V. 34. № 6. P. 909.
Jelsch C., Guillot B., Lagoutte A. et al. // J. Appl. Crystallogr. 2005. V. 38. № 1. P. 38.
Allen F.H., Kennard O., Watson D.G. et al. // Perkin Trans. 2. 1987. № 12. P. S1.
Hirshfeld F. // Acta Crystallogr. A. 1976. V. 32. № 2. P. 239.
Stash A., Tsirelson V. // J. Appl. Crystallogr. 2002. V. 35. № 3. P. 371.
Addison A.W., Rao T.N., Reedijk J. et al. // Dalton Trans. 1984. № 7. P. 1349.
Groom C.R., Bruno I.J., Lightfoot M.P. et al. // Acta Crystallogr. 2016. V. 72. № 2. P. 171.
Bader R.F.W. Atoms in Molecules – A Quantum Theory. Oxford: Oxford Univ. Press, 1990.
Fukin G.K., Samsonov M.A., Kalistratova O.S. et al. // Struct. Chem. 2016. V. 27. № 1. P. 357.
Fukin G.K., Samsonov M.A., Arapova A.V. et al. // J. Solid State Chem. 2017. V. 254. P. 32.
Фукин Г.К., Самсонов М. А., Баранов Е. В. и др. // Коорд. химия. 2018. Т. 44. № 5. С. 325 (Fukin G.K., Samsonov M.A., Baranov E.V. et al. // Russ. J. Coord. Chem. 2018. V. 44. № 10. P. 626.https://doi.org/10.1134/ S1070328418100020).
Espinosa E., Molins E., Lecomte C. // Chem. Phys. Lett. 1998. V. 285. № 3–4. P. 170.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия