Координационная химия, 2020, T. 46, № 2, стр. 104-111
Синтез, термическая стабильность, кристаллическая структура и оптические свойства бромовисмутатов 1,1'-(1,N-алкандиил)-бис-пиколинов
П. А. Буйкин 1, 2, *, А. Ю. Руденко 2, 3, А. Б. Илюхин 1, Н. П. Симоненко 1, Х. Э. Ёров 1, 4, В. Ю. Котов 1, 5
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
2 Высший химический колледж РАН, Российский химико-технологический университет
им. Д.И. Менделеева
Москва, Россия
3 Институт органической химии им. Н.Д. Зеленского РАН
Москва,, Россия
4 Московский государственный университет им. М.В. Ломоносова, химический факультет
Москва, Россия
5 Научно-исследовательский университет “Высшая школа экономики”
Москва, Россия
* E-mail: peterzzz@mail.ru
Поступила в редакцию 09.09.2019
После доработки 25.09.2019
Принята к публикации 28.09.2019
Аннотация
Синтезированы в концентрированной HBr и охарактеризованы физико-химическими методами гибридные бромовисмутаты N-алкилированных производных 2- и 3-метилпиридина: (C15H20N2)2Bi2Br10 (I), (C17H24N2)2Bi2Br10 (II), (C18H26N2)3(Bi2Br9)2 (III), (C14H18N2)(H3O)BiBr6 ∙ 2H2O (IV), (C14H18N2)2BiBr6IBr2 (V), (C16H22N2)3(Bi2Br9)2 (VI), (C18H26N2)3(Bi2Br9)2 (VII). Строение комплексов I–VII изучено методом РСА (CIF files CCDC № 1946844–1946850). Комплексы I и II имеют в своем составе анионы [Bi2Br10]4–. В структуре соединений III, VI и VII обнаружены анионы [Bi2Br9]3–. Бромовисмутат бис(3-метил-1-пиридино)этана IV содержит катионы H3O+ и анионы [BiBr6]3– и, в отличие от других бромовисмутатов, разлагается при низких температурах. В присутствии паров HI наряду с IV кристаллизуется двойной бромовисмутат V, содержащий анионы [BiBr6]3– и ${\text{IBr}}_{2}^{ - }.$
Гибридные галовисмутаты представляют собой перспективные материалы для солнечной энергетики [1–4]. Они обладают низкой токсичностью и высокой устойчивостью к внешним воздействиям, в частности к высокой влажности. Среди многочисленных легко образующихся гибридных галовисмутатов можно найти соединения с низкими значениями оптической ширины запрещенной зоны (Eg < 1.8 эВ) [5–9], из них смешанный хлороиодовисмутат [7] и иодовисмутат [8] метилвиологена имеют в своей структуре линейные 1D-цепи $[{\text{Bi}}{{{\text{X}}}_{5}}]_{n}^{{2n--}}.$ В ходе поиска соединений с линейными полимерными анионами мы получили несколько бромо- и иодовисмутатов N‑замещенных пиколинов [9–12]. Интересующий нас линейный анион $[{\text{Bi}}{{{\text{I}}}_{5}}]_{n}^{{2n--}}$ обнаружен в структуре иодовисмутата производного 4-метилпиридина. Ширина запрещенной зоны для этого соединения составила 1.73 эВ [9]. В структурах полученных бромовисмутатов производных пиколинов обнаружены изолированные анионы [Bi2Br10]4–, [Bi2Br11]5– и [BiBr6]3– [10], а также зигзагообразный полимерный анион $[{\text{BiB}}{{{\text{r}}}_{5}}]_{n}^{{2n--}}$ [11]. В структуре бромовисмутата 1,1'-(1,4-фенилен-бис(метилен))бис(3-метилпиридин-1-ия) обнаружен необычный линейный анионный агломерат [(BiBr6)···(BiBr5)···(BiBr6)]8–. Высокие значения Eg для этого соединения [12] и соединений с зигзагообразным полимерным анионом ${\text{[BiB}}{{{\text{r}}}_{5}}]_{n}^{{2n--}}$ [11] согласуются с заключением, что только наличие линейной анионной цепи в соединении является условием снижения ширины запрещенной зоны полупроводника. В литературе известны бромовисмутаты, иодовисмутаты и смешанные бромоиодовисмутаты однозарядных производных пиколина [13–15]. Однако среди них соединения с низкими значениями Eg не были обнаружены.
Цель настоящей работы – исследование ранее не изученных гибридных бромовисмутатов дикатионов N-алкилированных 2- и 3-пиколинов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
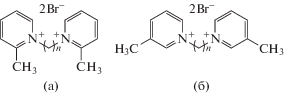
Синтез бромидов бис(2-метил-1-пиридино)-1,1'-алканов (а) и бис(3-метил-1-пиридино)-1,1'-алканов (б) проводили на воздухе.
Смесь метилпиридина, взятого в избытке (6 экв.), и дибромалкана (1 экв.) растворяли в ацетонитриле. Полученный раствор кипятили в течение 20 ч. Выпавший осадок отфильтровывали и промывали ацетонитрилом. Чистоту образовавшихся продуктов проверяли методом ЯМР 1Н.
Бромид бис(2-метил-1-пиридино)-1,1'-пропана: ЯМР 1Н (300 MГц; DMSO-d6; δ, м.д.): 9.08 (d., J = 6.0 Гц, 2H), 8.46 (t., J = 7.8 Гц, 2H), 8.13 (d., J = = 8.1 Гц, 2H), 8.05–7.95 (m., 2H), 4.57 (s., 4H), 2.87 (s., 6H), 1.95 (s., 2H).
Бромид бис(2-метил-1-пиридино)-1,1'-пентана: ЯМР 1Н (300 MГц; DMSO-d6; δ, м.д.): 9.18 (s., 2H), 8.50 (s., 2H), 8.11 (s., 2H), 7.99 (s., 2H), 4.64 (s., 4H), 2.90 (s., 6H), 1.97 (s., 4H), 1.51 (s., 2H).
Бромид бис(2-метил-1-пиридино)-1,1'-гексана: ЯМР 1Н (300 MГц; DMSO-d6; δ, м.д.): 9.11 (d., J = 6.1 Гц, 2H), 8.48 (t., J = 7.8 Гц, 2H), 8.14–7.90 (m., 2H), 4.70–4.49 (m., 4H), 2.87 (s., 6H), 1.88 (s., 4H), 1.45 (s., 4H).
Бромид бис(3-метил-1-пиридино)-1,1'-этана: ЯМР 1Н (300 MГц; DMSO-d6; δ, м.д.): 9.15 (s., 2H), 8.88 (d., J = 5.9 Гц, 2H), 8.53 (d., J = 7.9 Гц, 2H), 8.06 (t., J = 7.0 Гц, 2H), 5.31 (s., 4H), 2.50 (s., 6H).
Бромид бис(3-метил-1-пиридино)-1,1'-бутана: ЯМР 1Н (300 MГц; DMSO-d6; δ, м.д.): 9.18 (s., 2H), 9.05 (d., J = 5.8 Гц, 2H), 8.48 (d., J = 7.9 Гц, 2H), 8.07 (t., J = 6.9 Гц, 2H), 4.72 (s., 4H), 2.50 (s., 6H), 2.02 (s., 4H).
Бромид бис(3-метил-1-пиридино)-1,1'-гексана: ЯМР 1Н (300 MГц; DMSO-d6; δ, м.д.): 9.15 (s., 2H), 9.03 (d., J = 6.0 Гц, 2H), 8.46 (d., J = 8.0 Гц, 2H), 8.09–8.02 (m., 2H), 4.62 (t., J = 7.4 Гц), 2.51 (s., 6H), 1.99–1.91 (m., 4H), 1.34 (s., 4H).
Синтез (C15H20N2)2Bi2Br10 (I). Навеску бромида бис(2-метил-1-пиридино)пропана (0.50 г) растворяли в 6.25 мл 4 М водного раствора KBr. В реакционную смесь добавляли раствор, содержащий 23.8 г KBr и 4.75 г Bi(NO3)3 · 5H2O в 75 мл Н2О. Выпавший зеленоватый осадок отфильтровывали под вакуумом, промывали водой и этанолом, после чего высушивали на воздухе. Выход 0.82 г. Полученный осадок растворяли в минимальном количестве концентрированной HBr и оставляли упариваться при комнатной температуре. Через несколько суток образовавшееся мелкокристаллическое вещество отделяли от раствора и высушивали на воздухе. По данным РСА, полученные кристаллы представляют собой соединение состава (C15H20N2)2Bi2Br10 (I). РФА показал, что полученное после перекристаллизации вещество однофазное. Детали уточнения по Ритвельду: P21/n, a = 11.1050(3), b = 10.0430(4), c = 19.9647(6) Å, β = 101.993(2)°, Rexp 3.10, Rwp 8.08, Rp 5.38%, GOОF 2.61.
Синтез (C17H24N2)2Bi2Br10 (II). Навеску бромида бис(2-метил-1-пиридино)пентана (0.50 г) растворяли в 6.25 мл 4 М водного раствора KBr. В реакционную смесь добавляли раствор, содержащий 23.8 г KBr и 4.75 г Bi(NO3)3 · 5H2O в 75 мл Н2О. Выпавший зеленоватый осадок отфильтровывали под вакуумом, промывали водой и этанолом, после чего высушивали на воздухе. Выход 0.635 г. Полученный осадок растворяли в минимальном количестве концентрированной HBr и оставляли упариваться при комнатной температуре. Через несколько суток образовавшееся мелкокристаллическое вещество отделяли от раствора и высушивали на воздухе. По данным РСА, полученные кристаллы представляют собой соединение со-става (C17H24N2)2Bi2Br10 (II). РФА показал, что полученное после перекристаллизации вещество содержит в качестве основной фазы соединение II, а также неидентифицированную примесь с наиболее интенсивными пиками при 2θ = 20.0, 30.1 и 40.3. Детали уточнения по Ритвельду: C2/m, a = 14.4137(6), b = 18.0306(9), c = 9.8775(4) Å, β = 114.822(4)°, Rexp = 3.49%, Rwp = 14.41%, Rp = 9.67%, GOОF 4.13.
Синтез кристаллов (C18H26N2)3(Bi2Br9)2 (III). Навеску бромида бис(2-метил-1-пиридино)гексана (0.50 г) растворяли в 6.25 мл 4 М водного раствора KBr. В реакционную смесь добавляли раствор, содержащий 23.8 г KBr и 4.75 г Bi(NO3)3 · 5H2O в 75 мл Н2О. Выпавший зеленоватый осадок отфильтровывали под вакуумом, промывали водой и этанолом, после чего высушивали на воздухе. Выход: 1.02 г. Полученный осадок растворяли в минимальном количестве концентрированной HBr и оставляли упариваться при комнатной температуре. Через несколько суток образовавшийся порошок отделяли от раствора и высушивали на воздухе. Из него удалось выделить несколько кристаллов III, пригодных для РСА. По данным РФА III не является основным веществом выделенного продукта.
Синтез (C14H18N2)(H3O)BiBr6 ∙ 2H2O (IV). Навеску бромида бис(3-метил-1-пиридино)этана (0.50 г) растворяли в 6.25 мл 4 М водного раствора KBr. В реакционную смесь добавляли раствор, содержащий 23.8 г KBr и 4.75 г Bi(NO3)3 · 5H2O в 75 мл Н2О. Выпавший бесцветный осадок отфильтровывали под вакуумом, промывали водой и этанолом, после чего высушивали на воздухе. Выход 1.57 г. Полученный осадок растворяли в минимальном количестве концентрированной HBr и оставляли упариваться при комнатной температуре. Через несколько суток образовавшуюся смесь отделяли от раствора и высушивали на воздухе. В смеси обнаружили кристаллы двух видов, пригодные для РСА: IV и (C14H18N2)2BiBr6IBr2 (V). По данным РФА, продукт содержал IV в качестве основной фазы, а также неидентифицированную примесь, отличную от V с наиболее интенсивными пиками при 2θ = 9.4°, 10.6°, 11.8°, 12.1° и 16.8°. Детали уточнения по Ритвельду: P21/n, a = 10.4093(4), b = 18.2135(8), c = 13.8881(6) Å, β = 99.444(5)°, Rexp 2.05, Rwp 12.72, Rp 8.70%, GOОF 6.21. Образование минорной фазы V в продукте наиболее вероятно связано с воздействием паров HI на реакционную смесь при одновременном выдерживании серии растворов, содержащих HBr или HI в вытяжном шкафу.
Синтез (C16H22N2)3(Bi2Br9)2 (VI). Навеску бромида бис(3-метил-1-пиридино)бутана (0.50 г) растворяли в 6.25 мл 4 М водного раствора KBr. В реакционную смесь добавляли раствор, содержащий 23.8 г KBr и 4.75 г Bi(NO3)3 · 5H2O в 75 мл Н2О. Выпавший бледно-зеленый осадок отфильтровывали под вакуумом, промывали водой и этанолом, после чего высушивали на воздухе. Выход 1.168 г. Полученный осадок растворяли в минимальном количестве концентрированной HBr и оставляли упариваться при комнатной температуре. Через несколько суток образовавшиеся кристаллы отделяли от раствора и высушивали на воздухе. РСА показал, что полученные кристаллы представляют собой соединение состава (C16H22N2)3(Bi2Br9)2 (VI). По данным РФА, полученное после перекристаллизации вещество однофазное. Детали уточнения по Ритвельду: P21/n, a = 16.4908(9), b = = 11.3762(10), c = 41.7608(26) Å, β = 95.189(5)°, Rexp 2.88, Rwp 12.56, Rp 8.06%, GOОF 4.37.
Синтез кристаллов (C18H26N2)3(Bi2Br9)2 (VII). Навеску бромида бис(3-метил-1-пиридино)гексана (0.50 г) растворяли в 6.25 мл 4 М водного раствора KBr. В реакционную смесь добавляли раствор, содержащий 23.8 г KBr и 4.75 г Bi(NO3)3 · 5H2O в 75 мл Н2О. Выпавший бледно-зеленый осадок отфильтровывали под вакуумом, промывали водой и этанолом, после чего высушивали на воздухе. Выход 1.07 г. Полученный осадок растворяли в минимальном количестве концентрированной HBr и оставляли упариваться при комнатной температуре. Через несколько суток образовавшийся осадок отделяли от раствора и высушивали на воздухе. Из него удалось выделить несколько кристаллов VII, пригодных для РСА. По данным РФА, VII не является основным веществом выделенного продукта.
РСА. Экспериментальные данные для соединений I–VI получены на дифрактометре Bruker SMART APEX2 (MoKα-излучение, λ = 0.71073 Å, графитовый монохроматор) [16]. Поглощение учтено полуэмпирическим методом по эквивалентам (SADABS) [17]. Данные для соединения VII получены на дифракционной станции ВМ01 Европейского центра синхротронных исследований (дифрактометр PILATUS@SNBL, Гренобль, Франция) [18]. Обработка экспериментальных данных проведена c помощью программ SNBL ToolBox [18] и CrysAlis software (Rigaku Oxford Diffraction). Структуры определены комбинацией прямого метода и Фурье-синтезов и уточнены полноматричным анизотропно-изотропным МНК. Величины заселенности разупорядоченых фрагментов в структурах IV и VI получены при изотропном уточнении с фиксированными тепловыми параметрами разупорядоченных атомов и в последующем уточнении фиксированы. Все расчеты выполнены по программам SHELXS и SHELXL [19]. Основные кристаллографические данные приведены в табл. 1, 2.
Таблица 1.
Основные кристаллографические данные и результаты уточнения структур I–IV
| Параметр | Значение | |||
|---|---|---|---|---|
| I | II | III | IV | |
| Формула | C30H40N4Br10Bi2 | C34H48N4Br10Bi2 | C54H78N6Br18Bi4 | C14H25N2O3Br6Bi |
| М | 1673.72 | 1729.82 | 3085.52 | 957.80 |
| T, К | 150(2) | 150(2) | 150(2) | 150(2) |
| Сингония | Моноклинная | Моноклинная | Моноклинная | Моноклинная |
| Пр. гр.; Z | P21/n; 2 | C2/m; 2 | P21/n; 2 | P21/n; 4 |
| a, Å | 11.0210(4) | 14.2567(5) | 9.9964(4) | 10.3705(4) |
| b, Å | 10.0180(4) | 17.9650(6) | 16.4091(7) | 18.0471(7) |
| c, Å | 19.8331(7) | 9.8582(3) | 24.7686(11) | 13.8346(5) |
| β, град | 101.7340(10) | 114.6920(10) | 95.401(2) | 99.5630(10) |
| V, Å3 | 2143.98(14) | 2294.04(13) | 4044.8(3) | 2553.27(17) |
| ρ(выч.), г/см3 | 2.593 | 2.504 | 2.533 | 2.492 |
| μ, мм–1 | 17.542 | 16.399 | 17.602 | 16.311 |
| F(000) | 1528 | 1592 | 2812 | 1760 |
| Размер образца, мм | 0.28 × 0.28 × 0.14 | 0.24 × 0.24 × 0.12 | 0.2 × 0.1 × 0.08 | 0.32 × 0.32 × 0.28 |
| Область измерений по θ, град | 2.098–31.022 | 2.267–31.512 | 2.278–26.058 | 2.257–30.058 |
| Интервалы индексов отражений | –15 ≤ h ≤ 15, –14 ≤ k ≤ 14, –28 ≤ l ≤ 28 |
–20 ≤ h ≤ 20, –26 ≤ k ≤ 25, –13 ≤ l ≤ 14 |
–12 ≤ h ≤ 12, –20 ≤ k ≤ 20, –30 ≤ l ≤ 30 |
–14 ≤ h ≤ 14, –25 ≤ k ≤ 25, –19 ≤ l ≤ 19 |
| Число измеренных отражений | 54 585 | 16 735 | 43 742 | 47 092 |
| Число независимых отражений (Rint) | 6793 (0.0644) | 3794 (0.0464) | 7987 (0.0870) | 7490 (0.0727) |
| Полнота до θ = 25.242°, % | 100.0 | 100.0 | 99.9 | 100.0 |
| Max, min пропускание | 0.1007, 0.0319 | 0.1015, 0.0286 | 0.0926, 0.0322 | 0.099, 0.0314 |
| Метод уточнения | МНК по F 2 | МНК по F 2 | МНК по F 2 | МНК по F 2 |
| Число ограничений/ параметров | 0/209 | 0/121 | 0/373 | 0/236 |
| S | 1.033 | 1.002 | 0.974 | 1.037 |
| R1, wR2 (I > 2σ(I)) | 0.0269, 0.0564 | 0.0270, 0.0610 | 0.0369, 0.0617 | 0.0360, 0.0768 |
| R1, wR2 (все данные) | 0.0383, 0.0593 | 0.0366, 0.0643 | 0.0719, 0.0716 | 0.0537, 0.0830 |
| ∆ρmax/∆ρmin, е/Å3 | 2.253/–0.942 | 1.703/–0.970 | 1.214/–1.522 | 2.532/–1.291 |
Таблица 2.
Основные кристаллографические данные и результаты уточнения структур V–VII
| Параметр | Значение | ||
|---|---|---|---|
| V | VI | VII | |
| Формула | C28H36N4Br8IBi | C48H66N6Br18Bi4 | C54H78N6Br18Bi4 |
| М | 1403.77 | 3001.36 | 3085.52 |
| T, К | 150(2) | 100(2) | 150(2) |
| Сингония | Триклинная | Моноклинная | Моноклинная |
| Пр.гр.; Z | – P1; 1 | P21/n; 4 | P21/n; 2 |
| a, Å | 9.7162(4) | 16.4918(7) | 10.6567(3) |
| b, Å | 10.1351(5) | 11.2389(5) | 16.5173(4) |
| c, Å | 11.5665(5) | 41.1424(18) | 23.2031(5) |
| α, град | 82.1770(10) | 90 | 90 |
| β, град | 65.5040(10) | 94.7070(10) | 92.411(3) |
| γ, град | 68.6170(10) | 90 | 90 |
| V, Å3 | 964.99(8) | 7600.0(6) | 4080.59(18) |
| ρ(выч.), г/см3 | 2.416 | 2.623 | 2.511 |
| μ, мм–1 | 13.674 | 18.732 | 15.261 |
| F(000) | 648 | 5432 | 2812 |
| Размер образца, мм | 0.16 × 0.14 × 0.08 | 0.24 × 0.16 × 0.12 | 0.04 × 0.02 × 0.01 |
| Область измерений по θ, град | 2.158–31.509 | 2.066–27.118 | 1.669–26.750 |
| Интервалы индексов отражений | –13 ≤ h ≤ 14, –14 ≤ k ≤ 14, –16 ≤ l ≤ 16 |
–21 ≤ h ≤ 21, –14 ≤ k ≤ 14, –52 ≤ l ≤ 51 |
–13 ≤ h ≤ 13, –22 ≤ k ≤ 22, –30 ≤ l ≤ 30 |
| Число измеренных отражений | 18 762 | 63 868 | 25 299 |
| Число независимых отражений (Rint) | 6095 (0.0459) | 16 731 (0.0791) | 8782 (0.0421) |
| Полнота до θ = 25.242°, % | 100.0 | 99.9 | 92.3 |
| Max, min пропускание | 0.1015, 0.0342 | 0.0285, 0.0054 | 1, 0.39459 |
| Метод уточнения | МНК по F 2 | МНК по F 2 | МНК по F 2 |
| Число ограничений/ параметров | 0/195 | 9/695 | 0/370 |
| S | 1.019 | 0.990 | 1.016 |
| R1, wR2 (I > 2σ(I)) | 0.0332, 0.0812 | 0.0571, 0.1388 | 0.0658, 0.1590 |
| R1, wR2 (все данные) | 0.0435, 0.0851 | 0.0881, 0.1546 | 0.0925, 0.1755 |
| ∆ρmax/∆ρminе/Å3 | 1.749/–2.333 | 2.028/–2.209 | 3.229/–3.492 |
Экспериментальные данные для структур I–VII депонированы в Кембриджском банке структурных данных (CCDC 1946844–1946850); deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk).
Рентгенофазовый анализ (РФА) проведен на дифрактометре Bruker D8 Advance (CuKα, Ni-фильтр, LYNXEYE детектор, геометрия на отражение). Полнопрофильный анализ порошков проведен с помощью программы TOPAS 4.2 [20]. Уточнение по Ритвельду проводили с использованием структурных моделей I, II, IV, VI.
Спектры диффузного отражения (СДО) регистрировали на спектрофотометре Ocean Optics модель QE65000 в диапазоне частот 11 000–50 000 см–1 при комнатной температуре. Спектры перестроили в координатах зависимости функции Кубелка–Мунка [21] от энергии света. Для получения функции Кубелка–Мунка использовали уравнение:
где F(Rd) – абсолютное отражение слоя образца. Ширину запрещенной зоны оценивали экстраполяцией линейной части соответствующей кривой на F(Rd) = 0.
Термогравиметрический (ТГ) анализ образцов проводили с использованием тепловизора SDT Q600 V8.3 Build 101 Module DSC-TGA. Образец нагревали в режиме 10°С/мин от 25 до 300°C с потоком воздуха 250 мл/мин в открытой алюминиевой посуде.
Спектры ЯМР 1Н регистрировали на спектрометре Bruker AM300 (300 МГц) в DMSO-d6.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
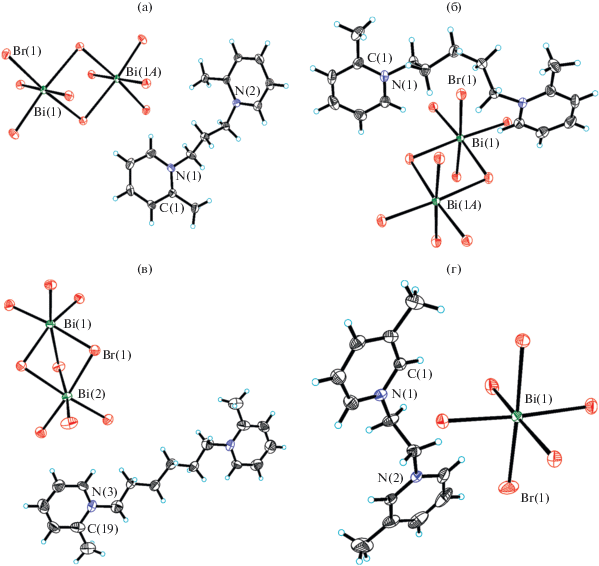
Структура I образована катионами бис(2-метил-1-пиридино)пропана и центросимметричными анионами Bi2Br10 (рис. 1a). Пиридиновый фрагмент N(2) участвует в стекинг-взаимодействии с образованием центросимметричного димера (кратчайшие контакты C…C 3.46, 3.53, 3.54 Å). Кратчайшие контакты Br…Br 4.15, 4.16 Å.
В структуре II катион бис(2-метил-1-пиридино)пентан расположен на оси 2, анион Bi2Br10 имеет кристаллографическую симметрию 2/m (рис. 1б). Пиридиновый фрагмент участвует в стекинг-взаимодействии (кратчайшие контакты C…C 3.25, 3.35, 3.43 Å) с двумя симметрически зависимыми фрагментами, что приводит к образованию 2D-слоев. Кратчайший контакт Br…Br 4.20 Å.
В структуре III присутствуют два кристаллографически независимых катиона бис(2-метил-1-пиридино)гексана, один расположен в общей позиции, второй на центре инверсии, анион Bi2Br9 расположен в общей позиции (рис. 1в). Кратчайший контакт Br…Br 3.92 Å объединяет анионы в 1D-цепочки.
Структура IV образована катионами бис(3-метил-1-пиридино)этана, анионами BiBr6 (рис. 1г), ионами оксония и молекулами кристаллизационной воды. Все позиции атомов O ионов оксония и молекул воды разупорядочены (заселенность 0.24–0.76), что не позволяет объективно локализовать атомы H.
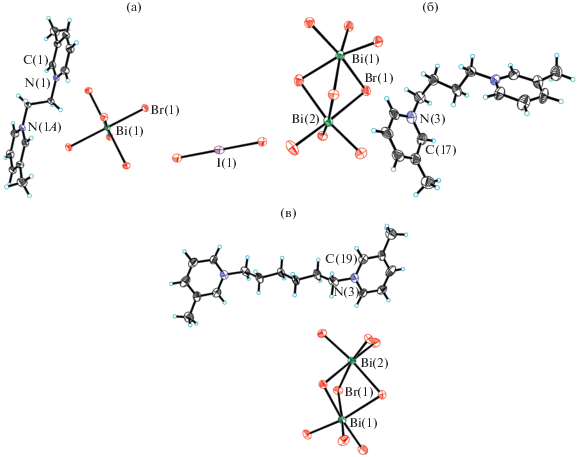
Все структурные единицы в примесной фазе V – два кристаллографически независимых катиона бис(3-метил-1-пиридино)этана, анионы BiBr6 и IBr2 (рис. 2а) – находятся в частных позициях (центры инверсии). Один из катионов посредством стекинг-взаимодействий пиридинового фрагмента образует 1D-цепочку. Контакт I…Br (4.16 Å) связывает анионы в 1D-цепочку.
В структуре VI присутствуют два кристаллографически независимых аниона Bi2Br9 и четыре независимых катиона бис(3-метил-1-пиридино)бутана (рис. 2б). Один из анионов разупорядочен по двум позициям в соотношении (0.85 : 0.15), два катиона находятся в общей позиции, третий – на центре инверсии, четвертый разупорядочен вокруг центра инверсии. В кратчайшем контакте Br…Br 3.73 Å участвует разупорядоченный атом Br с заселенностью 0.15.
Структура VII образована анионами Bi2Br9 и двумя кристаллографически независимыми катионами бис(3-метил-1-пиридино)гексана, один из которых расположен на центре инверсии (рис. 2в). Хотя конформацию алифатических цепочек в катионах можно описать как ttttt интервал абсолютных величин торсионных углов NCCC и CCCC в центросимметричном (174°–180°) и находящемся в общей позиции катионе (148°–174°) указывает на менее искаженную конформацию первого катиона. Кратчайший контакт Br…Br 3.90 Å.
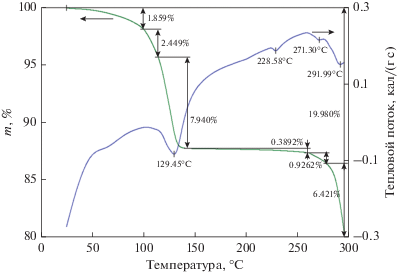
Термический анализ кристаллического порошка IV (рис. 3) показал, что соединение теряет молекулу HBr и две молекулы H2O при достижении 140°С. Другие соединения более устойчивы. Соединение I стабильно до 270°С, после чего плавится с разложением при 279°С. Разложение II начиналось уже при 250°С. Плавление III происходит при 250°С, VI – при 234°С и VII – при 250°С.
По данным СДО, значения ширины запрещенной зоны соединений I, II, IV и VI составили 2.83, 2.85, 2.88 и 2.85 эВ. Формальные значения для продуктов, содержащих III и VII, равны и составляют 2.86 эВ. Таким образом, все выделенные соединения имеют спектральные характеристики, характерные для 0D-гибридных бромовисмутатов.
Полученные из концентрированных растворов HBr гибридные бромовисмутаты N-замещенных 2- и 3-пиколинов содержат в своем составе различные анионы, а именно [BiBr6]3–, [Bi2Br9]3– и [Bi2Br10]4–. Ранее в структурах бромовисмутатов N-замещенных 2- и 4-пиколинов [10, 11] мы обнаружили также анионы $[{\text{BiB}}{{{\text{r}}}_{5}}]_{n}^{{2n--}}$ и [Bi2Br11]5–. Таким образом, мы не можем предсказать возможный состав и строение анионной части бромовисмутатов в ряду N-замещенных пиколинов даже при одинаковом исходном стехиометрическом соотношении реагентов (двухзарядный органический катион : висмут). Мы отметили, что для бромовисмутатов N-замещенных 4-пиколинов во всех изученных случаях кристаллизуются продукты с соотношением органический катион : висмут = 1 : 1. Для бромовисмутатов N-замещенных 2-пиколинов отклонение от этого соотношения наблюдается только для соединения, в котором катион имеет алкановую цепочку, содержащую шесть атомов углерода, а для бромовисмутатов N-замещенных 3-пиколинов уже для соединений с алкановой цепочкой из четырех и шести атомов углерода. Однако тот факт, что продукты взаимодействия катионов бис(n-метил-1-пиридино)гексана с бромовисмутат-анионами не являются однофазными, не позволяет нам утверждать об обнаружении тенденции изменения соотношения органический катион : висмут в ряду выделенных соединений.
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
Singh T., Kulkarni A., Ikegami M., Miyasaka T. // ACS Appl. Mater. Interfaces. 2016. V. 8. P. 14542.
Zhang Z., Li X.W., Xia X.H. et al. // J. Phys. Chem. Lett. 2017. V. 8. P. 4300.
Sanders S., Stummler D., Pfeiffer P. et al. // MRS Advances. 2018. V. 3. P. 3085.
Fabian D.M., Ardo S. // J. Mater. Chem. A. 2016. V. 4. P. 6837.
Kotov V.Y., Ilyukhin A.B., Sadovnikov A.A. et al. // Mendeleev Commun. 2017. V. 27. P. 271.
Kotov V.Y., Ilyukhin A.B., Birin K.P. et al. // New J. Chem. 2016. V. 40. P. 10041.
Leblanc N., Mercier N., Zorina L. et al. // J. Am. Chem. Soc. 2011. V. 133. P. 14924.
Chen Y., Yang Z., Guo C.X. et al. // Eur. J. Inorg. Chem. 2010. P. 5326.
Kotov V.Y., Ilyukhin A.B., Korlyukov A.A. et al. // New J. Chem. 2018. V. 42. P. 6354.
Kotov V.Y., Ilyukhin A.B., Simonenko N.P., Kozyukhin S.A. // Polyhedron. 2017. V. 37. P. 122.
Buikin P.A., Rudenko A.Y., Baranchikov A.E. et al. // Russ. J. Coord. Chem. 2018. V. 44. P. 373. https://doi.org/10.1134/S1070328418060015
Kotov V.Y., Safiullina,E.S., Ilyukhin A.B. et al. // J. Mol. Structure. 2019. V. 119. P. 944.
Li H.H., Wang M., Huang S.W. et al. // Synth. React. Inorg. Met.-Org. Nano-Metal Chem. 2011. V. 41. P. 1351.
Adonin S.A., Gorokh I.D., Novikov A.S. et al. // Polyhedron. 2018. V. 13. P. 282.
Adonin S.A. Gorokh I.D. Samsonenko D.G. et al. // Polyhedron. 2019. V. 15. P. 318.
APEX2 and SAINT. Madison (WI, USA): Bruker AXS Inc., 2007.
Sheldrick G.M. SADABS. Göttingen (Germany): Univ. of Göttingen, 1997.
Dyadkin V., Pattison P., Dmitriev V., Chernyshov D. // J. Synchrotron Radiation. 2016. V. 23. P. 825.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3.
Caelho A.A. TOPAS-Academic. Version 4.2. Brisbane (Australian): Caelho Software, 2009.
Kubelka P., Munk F. // Z. Techn. Phys. 1931. V. 12. P. 593.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия