Координационная химия, 2020, T. 46, № 2, стр. 98-103
Необычный шестиядерный пиразол-пиразолат-пивалат Fe(II, III), образующийся при η5,π-связывании мостикового пиразолат-аниона с катионами калия
М. А. Уварова 1, С. Е. Нефедов 1, *
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
* E-mail: snef@igic.ras.ru
Поступила в редакцию 27.09.2019
После доработки 29.09.2019
Принята к публикации 30.09.2019
Аннотация
Pеакция водного сульфата железа(II) с пивалатом калия в MeCN с последующим удалением растворителя, растворением остатка в Et3N и гексане приводит к образованию коричневого раствора и белого осадка. При взаимодействии маточного раствора с избытком 3,5-диметилпиразола (HDmpz) получен гексаядерный комплекс {[Fe3(µ3-O)(µ-OOCtBu)4(OOCtBu)2(HDmpz)(µ,η5-Dmpz)(µ-K)]2 ∙ 2HDmpz} (I), охарактеризованный методами элементного анализа, ИК-спектроскопии, РСА (СIF file CCDC № 1956015). Комплекс I формируется в результате впервые наблюдаемого в присутствии карбоксилатов железа депротонирования HDmpz, что приводит к возникновению пиразолат-мостикового аниона, собирающего через необычную η5,π-координацию с катионом калия два трехядерных фрагмента Fe3(µ3-O)(µ-OOCtBu)4(OOCtBu)2(HDmpz) в шестиядерный кластер.
Комплексы железа(II, III), содержащие карбоксилат-анионы и координированные гетероциклические молекулы (пиразол или имидазол и их аналоги) во многих случаях рассматриваются как структурные аналоги активной части природных металлоферментов, отвечающих за различные каталитические процессы, прежде всего за реакции окисления-восстановления H2O до H2, CO2 до CO, N2 до NH3 и O2 до H2O и др. [1–8].
Кроме того, такие комплексы активно изучаются в качестве потенциальных молекулярных магнетиков, катализаторов различных химических реакций, а также исходных соединений для синтеза необычных гомо-, гетерометаллических материалов, в том числе мелкодисперсных различной размерности, получаемых в результате восстановления в атмосфере водорода или термолиза [9–11].
Ранее было обнаружено, что гетероциклический 3,5-диметилпиразол (HDmpz) в мягких условиях может депротонироваться в присутствии простейщих димеров-фонариков M2(µ-OOCtBu)4(NEt3)2 (M = Zn, Co(II)) с образованием пиразолат-мостиковых димеров M2(µ-Dmpz)2(HDmpz)2(OOCtBu)2, при протонировании которых сильной трифторметансульфоновой кислотой образуются ком-плексы [M2(µ-OOCtBu)2(HDmpz)4]Otf2, содержащие координационный узел MO2N2, присутствующий в активной части природных металлоферментов [12].
В настоящей работе рассмотрен подход для получения пиразолат-мостиковых комплексов на основе пивалата железа(II), изучено строение продукта реакции водного сульфата железа с пивалатом калия в ацетонитриле и последующей реакции с триэтиламином и HDmpz – {[Fe3(µ3-O)-(µ-OOCtBu)4-(OOCtBu)2 (HDmpz)(µ,η5-Dmpz)(µ-K)]2 ∙ 2HD-mpz} (I).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все операции по синтезу и выделению комплекса проводили в атмосфере чистого аргона с использованием абсолютированных растворителей.
Синтез комплекса I. Сухие порошки FeSO4 ∙ ∙ 7H2O (1.00 г, 3.60 мМ) и KOOCtBu (0.76 г, 5.42 мМ) помещали в двугорлую колбу, вакуумировали и растворяли в 20 мл абсолютного ацетонитрила. Полученный слабо-окрашенный коричневый раствор отфильтровывали от белого осадка. Фильтрат концентрировали досуха в вакууме водоструйного насоса и добавляли последовательно 1 мл Et3N (частично растворяется) и 20 мл гексана. Коричневый раствор смешивали с раствором HDmpz (0.53 г, 5.51 мМ) в 5 мл гексана. Реакционную смесь концентрировали до ~15 мл и выдерживали при комнатной температуре в течение суток. Образовавшиеся при этом коричневые монокристаллы отделяли от маточного раствора декантацией, промывали холодным гексаном и сушили в токе аргона. Выход монокристаллического продукта 0.3 г (25%).
| Найдено (порошок), %: | C 48.02; | H 6.95; | N 4.88. |
| Для C100H170N12O30K2Fe6 | |||
| вычислено, %: | C 49.35; | H 7.04; | N 6.91. |
ИК-спектр (KBr; ν, см–1): 3021 сл, 2957 сл, 2870 сл, 1591 ср, 1567 ср, 1524 сл, 1483 ср, 1419 с, 1355 ср, 1333 ср, 1304 ср, 1224 с, 1082 с, 1032 с, 784 ср, 735 ср, 659 о.сл, 562 сл.
ИК-спектры кристаллических образцов регистрировали в интервале 4000–550 см–1 в таблетках KBr на ИК-Фурье спектрометре NEXUS фирмы NICOLET с использованием приставки MIRacle фирмы Pike Technologies с алмазным кристаллом.
РСА I выполнен по стандартной методике на автоматическом дифрактометре Bruker SMART Apex II, оборудованном CCD-детектором (MoKα, λ = 0.71073 Å, графитовый монохроматор, ω-сканирование) при Т = 150 К. Расчет структуры проведен с использованием комплекса программ SHELXTL PLUS (PC версия). Уточнение структур выполнено с использованием программы SHELXTL-97 [13–16]. Разупорядоченная по нескольким позициям сольватная молекула гексана удалена из уточнения программой SQUEEZE. Кристаллографические данные и детали уточнения приведены в табл. 1, основные геометрические параметры изученного комплекса в табл. 2.
Таблица 1.
Кристаллографические параметры и детали уточнения структуры комплекса I
| Параметр | Значение |
|---|---|
| М | 2433.77 |
| Цвет | Коричневыйй |
| T, K | 150(2) |
| Сингония | Триклинная |
| Пр. гр. | P1 |
| a, Å | 11.448(2) |
| b, Å | 14.618(3) |
| c, Å | 21.660(4)) |
| α, град | 90.78(3) |
| β, град | 97.58(3) |
| γ, град | 110.31(3) |
| V, Å3 | 3362.8(13) |
| Z | 1 |
| ρ(выч.), мг/м3 | 1.202 |
| µ, мм–1 | 0.758 |
| F(000) | 1288 |
| Размеры кристалла, мм | 0.24 × 0.22 × 0.20 |
| Oбласть θ, град | 1.48–26.00 |
| Интервалы индексов отражений | –13 ≤ h ≤ 14,
–16 ≤ k ≤ 18, –26 ≤ l ≤ 26 |
| Число отражений | 12 781 |
| Число независимых отражений (Rint) | 3803 (0.1254) |
| GOOF | 0.908 |
| R (I > 2σ(I)) | R1 = 0.0763, wR2 = 0.1738 |
| R (по всем рефлексам) | R1 = 0.2243, wR2 = 0.2305 |
| Остаточная электронная плотность (min/max), e/Å3 | 0.570/–0.693 |
Таблица 2.
Основные длины связей и валентные углы в комплексе I
| Связь | d,Å | Связь | d,Å |
|---|---|---|---|
| Fe(1)–O(15) | 1.897(5) | Fe(1)–O(7) | 1.935(6) |
| Fe(1)–O(3) | 2.003(6) | Fe(1)–O(1) | 2.036(6) |
| Fe(1)–O(5) | 2.056(6) | Fe(1)–N(3) | 2.105(7) |
| Fe(2)–O(15) | 1.855(5) | Fe(2)–O(11) | 1.996(6 |
| Fe(2)–O(9) | 1.995(5) | Fe(2)–O(4) | 2.004(6) |
| Fe(2)–O(2) | 2.012(6) | Fe(2)–N(1) | 2.152(7) |
| Fe(3)–O(15) | 1.914(5) | Fe(3)–O(13) | 1.949(5) |
| Fe(3)–O(12) | 2.007(6) | Fe(3)–O(10) | 2.024(6) |
| Fe(3)–O(6) | 2.057(6) | Fe(3)–N(4) | 2.084(7) |
| Fe(3)–K(1) | 3.836(3) | K(1)–O(8) | 2.593(6) |
| K(1)–O(14) | 2.627(6) | K(1)–O(14) | 2.733(6) |
| K(1)–O(6) | 2.812(6) | K(1)–N(4) | 2.854(7) |
| K(1)–N(3) | 2.866(7) | K(1)–C(36) | 3.126(10) |
| K(1)–C(39) | 3.155(9) | K(1)–C(38) | 3.288(9) |
| K(1)–C(11) | 3.291(9) | K(1)–C(13) | 3.467(10) |
| K(1)–C(35) | 3.537(11) | O(14)–K(1)) | 2.627(6) |
| N(1)–N(2) | 1.325(8) | N(3)–N(4) | 1.373(8) |
| N(5)–N(6) | 1.322(10) | ||
| Угол | ω, град | Угол | ω, град |
| O(15)Fe(1)O(7) | 170.5(2) | O(15)Fe(1)O(3) | 96.9(2) |
| O(7)Fe(1)O(3) | 91.8(2) | O(15)Fe(1)O(1) | 94.4(2) |
| O(7)Fe(1)O(1) | 90.0(2) | O(3))Fe(1)O(1) | 86.1(2) |
| O(15)Fe(1)O(5) | 87.7(2) | O(7)Fe(1)O(5) | 84.6(2) |
| O(3)Fe(1)O(5) | 167.6(2) | O(1)Fe(1)O(5) | 82.0(2) |
| O(15)Fe(1)N(3) | 85.1(2) | O(7)Fe(1)N(3) | 92.0(3) |
| O(3)Fe(1)N(3) | 84.1(3) | O(1)Fe(1)N(3) | 170.1(3) |
| O(5)Fe(1)N(3) | 107.9(3) | O(15)Fe(2)O(11) | 96.5(2) |
| O(15)Fe(2)O(9) | 96.5(2) | O(11)Fe(2)O(9) | 88.4(2) |
| O(15)Fe(2)O(4) | 91.4(2) | O(11)Fe(2)O(4) | 89.3(2) |
| O(9)Fe(2)O(4) | 171.9(2) | O(15)Fe(2)O(2) | 93.5(2) |
| O(11)Fe(2)O(2) | 169.5(2) | O(9)Fe(2)O(2) | 87.3(2) |
| O(4)Fe(2)O(2) | 93.6(2) | O(15)Fe(2)N(1) | 171.0(2) |
| O(11)Fe(2)N(1) | 86.7(3) | O(9)Fe(2)N(1) | 92.0(3) |
| O(4-Fe(2)N(1) | 80.2(3) | O(2)Fe(2)N(1) | 83.9(3) |
| O(15-Fe(3)O(13) | 178.5(3) | O(15)Fe(3)O(12) | 95.0(2) |
| O(13-Fe(3)O(12) | 86.3(2) | O(15)Fe(3)O(10) | 92.1(2) |
| O(13)Fe(3)O(10) | 88.6(2) | O(12)Fe(3)O(10) | 88.9(2) |
| O(15)Fe(3)O(6) | 92.5(2) | O(13)Fe(3)O(6) | 86.2(2) |
| O(12)Fe(3)O(6) | 172.0(2) | O(10)Fe(3)O(6) | 88.3(2) |
| O(15)Fe(3)N(4) | 85.0(2) | O(13)Fe(3)N(4) | 94.2(2) |
| O(12)Fe(3)N(4) | 93.4(3) | O(10)Fe(3)N(4) | 176.4(3) |
| O(6)Fe(3)N(4) | 89.8(2) | O(15)Fe(3)K(1) | 101.06(16) |
| O(13)Fe(3)K(1) | 77.51(18) | O(12)Fe(3)K(1) | 134.63(17) |
| O(10)Fe(3)K(1) | 131.94(18) | O(6)Fe(3)K(1) | 45.61(16) |
| N(4)Fe(3)K(1) | 46.97(19) | O(8)K(1)O(14) | 110.2(2) |
| O(8K(1)O(14) | 151.1(2) | O(14)K(1)O(14) | 92.81(19) |
| O(8K(1)O(6) | 84.49(19) | O(14)K(1)O(6) | 155.03(18) |
| O(14)K(1)O(6) | 68.16(18) | O(8)K(1)N(4) | 98.01(19) |
| O(14)K(1)N(4) | 131.7(2) | O(14)K(1)N(4) | 77.84(19) |
| O(6)K(1)N(4) | 62.07(19) | O(8)K(1)N(3) | 71.90(19) |
| O(14)K(1)N(3) | 133.4(2) | O(14)K(1)N(3) | 105.3(2) |
| O(6)K(1)N(3) | 69.6(2) | N(4)K(1)N(3) | 27.77(17) |
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (CCDC № 1956015; deposit@ccdc.cam.ac.uk или http:// www.ccdc.cam.ac.uk/data_request/cif).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Обнаружено, что реакция водного сульфата железа(II) с пивалатом калия (1 : 2) в ацетонитриле при комнатой температуре с последующим полным удалением растворителя, растворением остатка в триэтиламине и гексане приводит к образованию коричневого раствора и белого осадка. Взаимодействие полученного раствора с избытком HDmpz и кристаллизация при комнатной температуре дает c выходом 25% коричневые монокристаллы гексаядерного комплекса I.
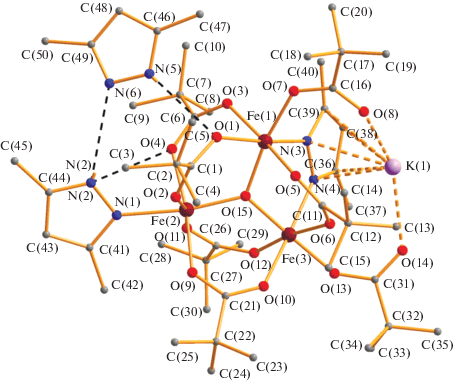
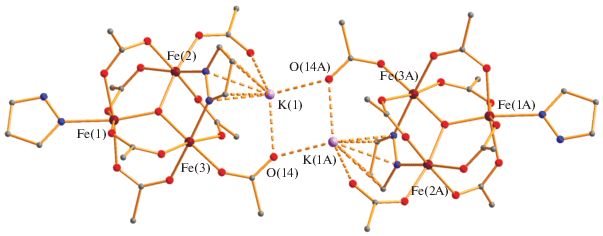
По данным РСА в независимой части кластера I (рис. 1, табл. 1, 2) три атома железа, расположенные на несвязывающих расстояниях Fe(1)...Fe(2) 3.2767(9), Fe(1)...Fe(3) 3.2501(9), Fe(2)...Fe(3) 3.2834(9) Å соединены тридентато-мостиковым атомом кислорода (Fe(1)–O(15) 1.897(5), Fe(2)–O(15) 1.855(5), Fe(3)–O(15) 1.914(5) Å; отклонение атома О(15) от плоскости Fe3 0.030 Å). Атом Fe(2), содержащий в аксиальной позиции молекулу HDmpz (Fe(2)–N(1) 2.152(7) Å), связан с каждым из двух других атомов железа двумя µ-пивалат-анионами (Fe(2)–O 1.996(6)–2.012(6), Fe(1)–O 2.003(6), 2.036(6), Fe(3)–O 2.007(6), 2.024(6) Å) и имеет искаженное октаэдрическое окружение. Аналогичное окружение имеют и атомы Fe(1) и Fe(3), которое помимо µ3-атома кислорода и атомов кислорода, принадлежащих пивалатным мостикам (Fe(1)–O(5) 2.056(6), Fe(3)–O(6) 2.057(6) Å), дополнено атомами азота депротонированного мостикового пиразолат-аниона (Fe(1)–N(3) 2.105(7), Fe(3)–N(4) 2.084(7) Å) и атомами кислорода концевого аниона OOCtBu (Fe(1)–O(7) 1.935(6), Fe(3)–O(13) 1.949(5)Å). Некоординированные атомы кислорода концевых пивалат-анионов имеют контакты с катионом калия (K(1)···O(8) 2.593(6), K(1)–O(14) 2.733(6) Å), который координирован по η5,π-типу с делокализованной электронной π-плотностью мостикового Dmpz (K(1)...N 2.854(7), 2.866(7), K(1)...C 3.126(10)–3.288(9) Å). Длина связи азот–азот в пиразолат-анионе (1.373(8) Å) заметно увеличена по сравнению с длинами связей в координированном (1.325(8) Å) и сольватном пиразолах (1.322(10) Å). Катион калия связан также с атомом кислорода О(14A) (K(1)–O(14A) 2.627(6) Å), принадлежащем другой молекуле треугольника Fe3, формируя шестиядерный кластер I (рис. 2).
Рис. 2.
Строение кластера I. Для ясности в трет-бутильных заместителях карбоксилат-анионов показаны только опорные атомы углерода, опущены метильные заместители HDmpz и атомы водорода. Цвет атомов: кислород – красный, азот – синий, углерод – серый.
В кристаллической ячейке комплекса I присутствуют две сольватные молекулы пиразола, NH-фрагменты которых образуют водородные связи с атомом кислорода мостикового пивалат-аниона (N(5)...O(1) 2.899(8) Å). Пиррольные атомы азота связаны с NH-фрагментами координированного Dmpz (N(6)...N(2) 3.164(11) Å), соединенного, в свою очередь, с атомом кислорода мостикового карбоксилата (N(2)...O(4) 2.830(9) Å) (рис. 1).
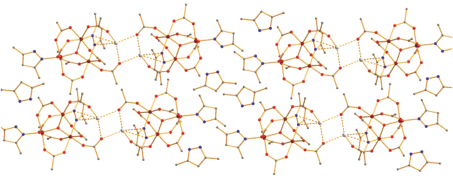
В кристалле молекулы локализованы и не образуют заметных контактов (рис. 3).
Рис. 3.
Упаковка молекул комплекса I в кристалле. Для ясности в трет-бутильных заместителях карбоксилат-анионов показаны только опорные атомы углерода. Цвет атомов: железо – коричневый, кислород – красный, азот – синий, углерод – серый.
Cтруктурно охарактеризованные комплексы карбоксилатов железа, содержащие мостиковые пиразолат-анионы, не известны. Однако ряд соединений с другими анионами получен в ходе реакций галогенидов железа(II, III) c пиразолатами щелочных металлов, а также в результате депротонирования пиразолов посредством синтеза. Так, при взаимодействии Fe(NO)I с NaDmpz образуется пиразолат-мостиковый димер Fe2(µ-Dmpz)2(NO)4 c длинами связей Fe–N 2.009(5) Å и расстоянием металл–металл 3.3359(3) Å [17]. Депротонирование незамещенного пиразола (HPz) ферроценом в вакууме при 145°С в течение 5 cут приводит к образованию пиразолат-мостикового полимера незамещенного пиразола [Fe(Pz)2]n (Fe–N 2.027(1) Å) [18]. Синтезированы трехядерные комплексы железа(III) Fe3(µ3-O)(µ-4-RPz)6X3 (R = NO2, X = Br [19], NCS [20], четырехядерные комплексы [LFe3(µ-3-PhPz)3OFe][OTf]2 (L = лиганд на основе 1,3,5-триарилбензольного фрагмента [21]), а также пиразолат-мостиковые кластеры, содержащие кубановый металлоостов Fe4(µ3-O)4, Fe8(µ4-O)4-(µ-Рz)12Cl4 [22], Fe8(µ4-O)4(µ-4-RРz)12X4, (X = Cl, Br; R = H, Me, Cl, tBu) [23–25].
Показано, что реакции карбоксилатов железа(II), содержащих стерически нагруженные анионы 2,6-ди(пара-толил)бензоат и 2-фенилбензоат с HDmpz, приводят к образованию моноядерных и биядерных комплексов со структурой китайского фонарика и координированными молекулами пиразола. Такие комплексы рассматриваются как структурные аналоги активной части природных металлоферментов [26–29].
Известно также, что пиразолат-анионы могут выступать в качестве η5,π-лигандов, например, в соединениях [Na(Dmpz)(Thf)]4, [Na{Al(Dmpz)2Me2}]n [28]; Na(η6-PhMe){Ln(3,5-tBu2Pz)4} (Ln = Tb, Ho), [K(η6-PhMe){Ln(3,5-tBu2Pz)4}] ∙ 2PhMe (Ln = La, Sm, Tb, Yb, Lu) (K–N 2.83(1)–3.01(1), K–C 3.07(1)–3.41(1) Å [30]; K[(OC)3Mn(μ-Pz)3Mn(CO)3], где катион калия является мостиковым и связан с четырьмя мостиковыми пиразолат-анионами двух димеров Mn2 (K-центр Pz 2.903–3.371 Å) [31]; (Thf)6Ba6(Dmpz)8{(OSiMe2)2O}2 [32]. Отметим, что расстояния K–η5,π-RPz в исследованных комплексах вполне соответствуют расстояниям в исследованном кластере I.
Таким образом, в результате проведенных исследований обнаружено, что одним из конечных продуктов реакции водного сульфата железа(II) с пивалатом калия в присутствии Et3N как депротонирующего агента и HDmpz в мягких условиях является не ожидаемый биядерный комплекс M2(µ-Dmpz)2(HDmpz)2(OOCtBu)2, аналог комплексов цинка и кобальта, а необычный кластер {[Fe3(µ3-O)(µ-OOCtBu)4(OOCtBu)2(HDmpz)(µ,η5-Dmpz)(µ-K)]2 ∙ 2HDmpz}, возникающий в результате частичного окисления атомов металла, связанных с сильными донорными пивалат-анионами.
БЛАГОДАРНОСТИРентгеноструктурные исследования комплексов выполнены с использованием оборудования ЦКПФМИ ИОНХ РАН, функционирующего при поддержке государственного задания ИОНХ РАН в области фундаментальных научных исследований.ФИНАНСИРОВАНИЕРабота выполнена в рамках государственного задания ИОНХ РАН в области фундаментальных научных исследований.
Список литературы
Lippard S.J., Berg J.M. Principles of Bioinorganic Chemistry. Mill Valley (CA, USA): University Science Books, 1994.
Solomon E.I., Sundaram U.M., Machonkin T.E. // Chem. Rev. 1996. V. 96. P. 2563. https://doi.org/10.1021/cr950046o
Dance I.Z., Lubitz W. // Anorg. Allg. Chem. 2015. V. 641. P. 91. https://doi.org/10.1002/zaac.201400120
Lubitz W., Ogata H., Rüdiger O., Reijerse E. // Chem. Rev. 2014. V. 114. P. 4081. https://doi.org//10.1021/cr4005814
Kaim W., Rall J. // J. Angew. Chem., Int. Ed. 1996. V. 35. P. 43. https://doi.org/10.1002/anie.199600431
Holm R.H., Kennepohl P., Solomon E.I. // Chem. Rev. 1996. V. 96. P. 2239. https://doi.org/0.1021/cr9500390
Eady R.R. // Coord. Chem. Rev. 2003. P. 237. https://doi.org/10.1016/S0010-8545(02)00248-5
Baran P., Boca R., Chakraborty I. et al. // Inorg. Chem. 2008. V. 47. P. 645. https://doi.org/10.1021/ic7020337
Ruiter G. de, Thompson N.B., Lionetti D. // J. Am. Chem. Soc. 2015. V. 137. P. 14094. https://doi.org/10.1021/jacs.5b07397
Mehrotra R.C., Bohra R. Metal Carboxylates. London: Acad. Press, 1983. P. 396.
Cotton F.A., Wilkincon G., Murillo C.A., Bochmann M. Advanced Inorganic Chemistry. John Wiley & Sons, Inc., 1999.
Kiskin M.A., Eremenko I.L. // Russ. Chem. Rev. 2006. V. 75. P. 559. https://doi.org/10.1070/RC2006v075n07ABEH003636
Nefedov S.E. // Russ. J. Inorg. Chem. 2006. V. 51. Suppl. 1. P. S49. https://doi.org/10.1134/S0036023606130031
SMART (control) and SAINT (integration) Software. Version 5.0. Madison (WI, USA): Bruker AXS Inc., 1997.
SAINT: Area-Detector Integration Sofware. Madison (WI, USA). Bruker AXS Inc., 2012.
Sheldrick G.M. SADABS. Program for Scaling and Correction of Area Detector Data. Göttingen (Germany): Univ. of Göttingen, 1997.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3. https://doi.org/10.1107/S2053229614024218
Chong K.S., Rettig S.J., Storr A., Trotter J. // Can. J. Chem. 1979. V. 57. P. 3119. https://doi.org/10.1139/v79-509
Patrick B.O., Reiff W.M., Sanchez V.A. et al. // Polyhedron 2001. V. 20. P. 1577. https://doi.org/10.1016/S0277-5387(01)00657-X
Sameera W.M.C., Pinero D.M., Herchel R. et al. // Eur. J. Inorg. Chem. 2012. P. 3500. https://doi.org/1002/ejic.201200206
Govor E.V., Al-Ameed K., Chakraborty I. et al. // Angew. Chem., Int. Ed. 2017. V. 56. P. 582. https://doi.org/10.1002/anie.201610534
de Ruiter G., Thompson N.B., Lionetti D., Agapie T. // J. Am. Chem. Soc. 2015. V. 137. P. 14094. https://doi.org/14094 10.1021/jacs.5b07397
Raptis R.G., Georgakaki I.P., Hockless D.C.R. // Angew. Chem. Int. Ed. 1999. V. 38. P. 1632. https://doi.org/10.1002/(SICI)1521-3773(19990601)38:11< 1632::AID-ANIE1632>3.0.CO;2-O
Chakraborty I., Baran P., Sanakis Y., Simopoulos A. et al. // Inorg. Chem. 2008. V. 47. P. 11734. https://doi.org/10.1021/ic801459s
Baran P., Boca R., Chakraborty I. et al. // Inorg. Chem. 2008. V. 47. P. 645. https://doi.org/10.1021/ic7020337
Deutscher J., Corona T., Warm K. et al // Eur. J. Inorg. Chem. 2018. V. 45. P. 4925. https://doi.org/10.1002/ejic.201800269
Sungho Yoon, Lippard S.J. // J. Am. Chem. Soc. 2004. V. 126. P. 2666. https://doi.org/10.1021/ja031603o
Reisner E., Telser J., Lippard S.J. // Inorg. Chem. 2007. V. 46. P. 10754. https://doi.org/10.1021/ic701663j
Cortes-Llamas S., Velazquez-Carmona M.-A., Munoz-Hernandez M.-A. // Inorg. Chem. Commun. 2005. V. 8. P. 155. https://doi.org/10.1016/j.inoche.2004.11.028
Deacon G.B., Delbridge E.E., Evans D.J. et al. // Chem. Eur. J. 2004. V. 10. P. 1193. https://doi.org/10.1002/chem.200305444
Morawitz T., Zhang F., Bolte M. et al. // Organometallics. 2008. V. 27. P. 5067. https://doi.org/10.1021/om800504r
Steiner A., Lawson G.T., Walfort B. et al. // Dalton Trans. 2001. P. 219. https://doi.org/10.1039/b009121i
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия