Координационная химия, 2021, T. 47, № 9, стр. 535-542
Координационные полимеры скандия(III) и тиофендикарбоновой кислоты
А. А. Лысова 1, *, В. А. Дубских 1, К. Д. Абашеева 1, 2, А. А. Васильева 1, 2, Д. Г. Самсоненко 1, **, Д. Н. Дыбцев 1, ***
1 Институт неорганической химии им. А.В. Николаева СО РАН
Новосибирск, Россия
2 Новосибирский государственный университет
Новосибирск, Россия
* E-mail: lysova@niic.nsc.ru
** E-mail: denis@niic.nsc.ru
*** E-mail: dan@niic.nsc.ru
Поступила в редакцию 23.03.2021
После доработки 16.04.2021
Принята к публикации 19.04.2021
Аннотация
Синтезированы три новых металл-органических координационных полимера на основе катионов скандия(III) и 2,5-тиофендикарбоновой кислоты (H2Tdc): [Sc(Tdc)(OH)] · 1.2DMF (I), [Sc(Tdc)(OH)] · · 2/3DMF (II), (Me2NH2)[Sc3(Tdc)4(OH)2] · DMF (III) (DMF = N,N-диметилформамид). Структура соединений установлена методом монокристального рентгеноструктурного анализа (CCDC № 2067819 (I), 2067820 (II), 2067821 (III)), методами элементного, термогравиметрического и рентгенофазового анализов и ИК-спектроскопии доказана химическая и фазовая чистота соединения I.
Металл-органические координационные полимеры (МОКП) представляют собой уже относительно известный класс неорганических соединений, состоящих из ионов или кластеров металлов, связанных друг с другом мостиковыми лигандами с образованием одно- (1D), двух- (2D) или трехмерных (3D) периодичных структур [1–3]. Такие соединения могут сохранять свою пористость после удаления гостевых молекул растворителя и быть использованы в качестве сорбентов для самого широкого круга приложений [4–6]. Значительная часть прикладных задач, таких как гетерогенный катализ [7], очистка антропогенных отходов от вредных веществ, тяжелых и радиоактивных металлов [8], селективное извлечение ионов металлов из природных источников [9] и т.д. требует относительно высокой гидролитической стабильности пористого материала. На сегодняшний момент известно несколько сотен тысяч различных МОКП, но высокая гидролитическая стабильность показана лишь для ограниченного круга систем, среди которых можно выделить каркасы на основе карбоксилатных мостиковых лигандов и высокозарядных катионов оксофильных металлов: Sc(III), Cr(III), Al(III), Ti(IV) и Zr(IV) [10–14]. Очевидно, что в условиях ограниченного выбора металлов основным способом варьирования функциональных свойств пористого МОКП должны стать органические мостиковые лиганды. Недавно было показано, что включение в структуру МОКП гетероциклических фрагментов на основе тиофена существенно повышает их сорбционные и люминесцентные характеристики [15–18]. Однако следует отметить, что число известных МОКП на основе высокозарядных ионов, имеющих в своем составе гетероциклические тиофеновые фрагменты, невелико; например, для скандия(III) известно только два таких МОКП с 2,5-тиофендикарбоксилатными анионом [19, 20]. В этой связи разработка синтетических подходов для кристаллизации новых МОКП на основе вышеперечисленных катионов металлов и карбоксилатных лигандов с гетероциклическими фрагментами представляет несомненный научный интерес и перспективную практическую значимость.
В настоящей работе описано получение и кристаллическая структура трех новых МОКП на основе катионов скандия(III) и 2,5-тиофендикарбоновой кислоты (H2Tdc).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали исходные вещества трифторметансульфонат скандия(III) (ДАлХИМ), 2,5-тиофендикарбоновая кислота (Sigma-Aldrich), гидроксид натрия (Вектон), муравьиная кислота (Реактив), N,N-диметилформамид (Вектон), ацетон (Вектон), ацетонитрил (Криохром) квалификации не ниже “х. ч.” без дополнительной очистки. ИК-спектры регистрировали в диапазоне 4000–400 см–1 в таблетках с KBr на Фурье-спектрометре VERTEX 80. Элементный анализ выполняли в аналитической лаборатории ИНХ СО РАН на CHNS-анализаторе “Vario MICRO cube”. Данные РФА получены на порошковом дифрактометре Shimadzu XRD 7000S (излучение CuKα). Термогравиметрический анализ (ТГА) проводили в атмосфере Ar на термоанализаторе NETZSCH TG 209 F1 при линейном нагревании образцов со скоростью 10°C/мин.
Синтез [Sc(Тdc)(OH)] · 1.2DMF (I). 0.25 мл 0.1 М раствора трифторметансульфоната скандия(III) в N,N-диметилформамиде (DMF), 0.25 мл 0.1 М раствора 2,5‑тиофендикарбоновой кислоты в DMF, 0.25 мл 10–4 М раствора NaOH в воде и 0.25 мл ацетона запаивали в стеклянной ампуле и выдерживали при 60°С в течение 5 сут. Состав и строение прозрачных ромбических кристаллов I установили методом РСА. Кристаллы отфильтровывали, промывали DMF (3 × 1 мл) и сушили на воздухе. Выход 6.1 мг (69%).
ИК-спектр (ν, см–1): 3384 ш.ср νs(O–H), 3080 сл ν(C–H), 2940 сл ν(C–H), 2854 сл ν(C–H), 1666 с νas(C=O), 1561 с γ(C=C), 1529 с γ(C=C), 1380 с νs(C=O), 1244 сл ν(C–N), 1089 ср ν(C–N), 1035 сл ν(C–N), 772 с δoop(C–H), 678 ср δoop(C–H), 504 сл δoop(C–H) (оор = внеплоскостные колебания).
Синтез [Sc(Tdc)(OH)] · 2/3DMF (II). 0.25 мл 0.1 М раствора трифторметансульфоната скандия(III) в DMF, 0.25 мл 0.1 М раствора 2,5‑тиофендикарбоновой кислоты в DMF, 0.25 мл 10–2 М раствора NaOH в воде и 0.25 мл ацетонитрила запаивали в стеклянной ампуле и выдерживали при 130°С в течение 2 сут. Состав и строение прозрачных ромбических кристаллов II установили методом РСА.
Синтез (Me2NH2)[Sc3(Tdc)4(OH)2] · DMF (III). 0.25 мл 0.1 М раствора трифторметансульфоната скандия(III) в DMF, 0.25 мл 0.1 М раствора 2,5‑тиофендикарбоновой кислоты в DMF, 0.25 мл воды, 0.25 мл ацетонитрила и 9.5 мкл муравьиной кислоты запаивали в стеклянной ампуле и выдерживали при 120°С в течение 2 сут. Состав и строение прозрачных ромбических кристаллов III установлены методом РСА.
РCA. Дифракционные данные для монокристаллов соединений I–III получены на автоматическом дифрактометре Agilent Xcalibur, оснащенном двухкоординатным детектором AtlasS2 (графитовый монохроматор, λ(MoKα) = 0.71073 Å, ω-сканирование с шагом 0.5°) при 130 К. Интегрирование, учет поглощения, определение параметров элементарной ячейки проведены с использованием пакета программ CrysAlisPro [21]. Кристаллические структуры расшифрованы с использованием программы SHELXT [22] и уточнены полноматричным МНК в анизотропном (за исключением атомов водорода) приближении с использованием программы SHELXL [23]. Позиции атомов водорода органических лигандов рассчитаны геометрически и уточнены по модели “наездника”. Гостевой состав соединения I определен согласно процедуре PLATON/SQUEEZE [24] (1502 e− в 7330 Å3) и данных элементного анализа (C, H, N). Кристаллографические данные и детали дифракционных экспериментов приведены в табл. 1.
Таблица 1.
Кристаллографические характеристики и детали дифракционного эксперимента для I–III
| Параметр | Значение | ||
|---|---|---|---|
| I | II | III | |
| Формула | C9.6H11.4N1.2O6.2SSc | C8H7.67N0.67O5.67SSc | C29H25N2O19S4Sc3 |
| M | 319.82 | 280.83 | 968.63 |
| Сингония | Ромбическая | Моноклинная | Моноклинная |
| Пр. гр. | Pbam | I2/m | P21/c |
| a, Å | 21.9009(7) | 11.6287(5) | 10.8919(4) |
| b, Å | 25.7997(9) | 14.8227(6) | 18.9016(4) |
| c, Å | 22.4066(8) | 19.7730(11) | 19.2160(5) |
| α, град | 90 | 90 | 90 |
| β, град | 90 | 106.885(5) | 99.915(3) |
| γ, град | 90 | 90 | 90 |
| V, Å3 | 12660.6(8) | 3261.3(3) | 3897.0(2) |
| Z | 32 | 12 | 4 |
| ρ(выч.), г/см3 | 0.974 | 1.716 | 1.651 |
| μ, мм−1 | 0.588 | 0.878 | 0.802 |
| F(000) | 3712 | 1712 | 1968 |
| Размер кристалла, мм | 0.28 × 0.20 × 0.18 | 0.18 × 0.12 × 0.04 | 0.18 × 0.11 × 0.05 |
| Область сканирования по θ, град | 3.29–28.38 | 3.31–28.84 | 3.29–28.94 |
| Диапазон индексов hkl | −28 ≤ h ≤ 26, −18 ≤ k ≤ 34, −29 ≤ l ≤ 21 | −14 ≤ h ≤ 12, −19 ≤ k ≤ 15, −18 ≤ l ≤ 25 | −11 ≤ h ≤ 13, −25 ≤ k ≤ 23, −25 ≤ l ≤ 18 |
| Число измеренных/независимых отражений | 36 039/14 159 | 8268/3726 | 19 490/8521 |
| Rint | 0.0240 | 0.0760 | 0.0277 |
| Число отражений с I > 2σ(I) | 11 426 | 3157 | 6544 |
| GOOF | 1.037 | 1.059 | 1.049 |
| R-факторы (I > 2σ(I)) | R1 = 0.0353, wR2 = 0.0955 |
R1 = 0.0594, wR2 = 0.1517 | R1 = 0.0452, wR2 = 0.1117 |
| R-факторы (по всем отражениям) | R1 = 0.0461, wR2 = 0.0995 |
R1 = 0.0681, wR2 = 0.1616 |
R1 = 0.0658, wR2 = 0.1234 |
| Остаточная электронная плотность (min/max), e/Å3 | −0.475/0.384 | −1.099/0.803 | −0.877/1.028 |
Полные таблицы межатомных расстояний и валентных углов, координаты атомов и параметры атомных смещений депонированы в Кембриджский банк структурных данных (CCDC № 2067819 (I), 2067820 (II), 2067821 (III); deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk), а также могут быть получены у авторов.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Синтезы всех соединений проводили в близких условиях (эквимолярное соотношение Sc : H2Tdc, одинаковый объем и состав растворителя с точностью до природы слабокоординирующейся добавки: ацетон (синтез соединения I) или ацетонитрил (синтез соединений II и III)). Ключевым отличием является температура синтеза и наличие модуляторов кислотности. При низких температурах (40–70°С) кристаллизуется соединение [Sc(Tdc)(OH)] · 1.2DMF (I). При более высокой температуре (130°С) образуется соединение [Sc(Tdc)(OH)] · 2/3DMF (II), имеющее такую же стехиометрию координационного каркаса, что и I, но другую кристаллическую структуру. В ходе оптимизации условий синтеза I было обнаружено, что добавление в реакционную смесь небольших количеств NaOH (от 0.1 до 10% в сравнении с количеством Sc(III) или H2Tdc) повышает выход и кристалличность продукта, однако чистое соединение I в виде ромбических кристаллов можно получить и без таких добавок. При использовании более высоких концентраций NaOH наблюдалось образование аморфного осадка и новой фазы с игловидными кристаллами, состав и строение которых не удалось установить. Добавление в систему муравьиной кислоты (20-кратный избыток по отношению к Sc(III) и H2Tdc) приводит к образованию соединения (Me2NH2)[Sc3(Tdc)4(OH)2] · DMF (III) при 120°С. Очевидно, что кислая среда и высокая температура приводит к частичному гидролизу N,N‑диметилформамида и образующиеся катионы Me2NH2+ встраиваются в структуру соединения III при его кристаллизации. Состав и строение всех соединений установлены с помощью монокристального РСА. Для соединения I эти данные дополнительно подтверждены химическим, термогравиметрическим, рентгенофазовым анализами и ИК-спектроскопией. Низкий выход и невозможность масштабирования синтезов соединений II и III не позволили провести их дополнительную характеризацию.
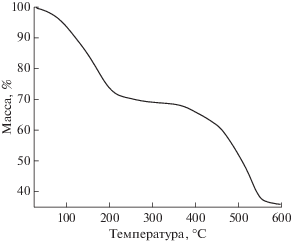
Согласно данным РСА, в структуре I присутствуют пять кристаллографически независимых катионoв скандия(III), каждый из которых находится в октаэдрическом координационном окружении из шести атомов кислорода двух гидроксильных групп OH– и четырех карбоксилатных групп лигандов Tdc2–, занимающих мостиковое положение между двумя соседними катионами скандия(III) (рис. 1а). Мостиковые гидроксильные OH– и карбоксилатные группы связывают катионы скандия(III) в цепочки, расположенные вдоль кристаллографической оси b ромбической группы Pbam (последовательность –Sc(1)–Sc(2)–Sc(3)–Sc(4)–Sc(5)–Sc(4)–Sc(3)–Sc(2)–Sc(1)–). Длины связей Sc–O находятся в диапазоне: Sc(1)–O 2.0321(13)–2.1471(13), Sc(2)–O 2.0462(13)–2.1322(13), Sc(3)–O 2.0277(13)–2.1228(13)Å, Sc(4)–O 2.0413–2.1404(13), Sc(5)–O 2.0354(13)–2.1222(13) Å. Мостиковые лиганды Tdc2– соединяют такие цепочечные мотивы вдоль кристаллографических осей а и с с образованием трехмерного металл-органического каркаса (рис. 1б, 1в). В направлении оси b в пористой структуре присутствуют каналы размером 5 × 6 Å, занятые гостевыми молекулами DMF (рис. 1в). Объем свободного пространства после удаления гостевых молекул растворителя составляет 56.7% (по данным программы PLATON [24]).
Рис. 1.
Координационное окружение катионов скандия(III) (а) и фрагмент кристаллической структуры соединения I: проекция на плоскости bc (б) и ac (в).
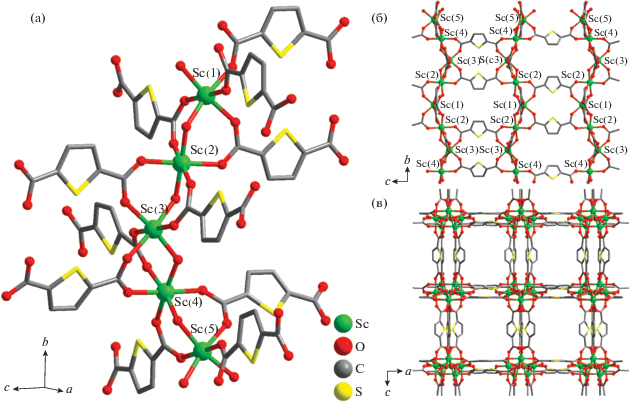
Ромбические кристаллы соединения II имеют в своей структуре два кристаллографически независимых катиона скандия(III), каждый из которых находится в октаэдрическом координационном окружении из шести атомов кислорода двух гидроксильных групп OH– и четырех карбоксилатных групп лигандов Tdc2–, занимающих мостиковое положение между двумя соседними катионами скандия(III) (рис. 2а). Две мостиковые гидроксильные OH– и четыре карбоксилатные группы Tdc2–связывают два катиона Sc(2) и один катион Sc(1) в сложные двойные цепочки, идущие вдоль кристаллографической оси a (рис. 2б). В каждой такой цепочке можно выделить линейную последовательность катионов –Sc(2)–Sc(1)–Sc(2)–Sc(2)–Sc(1)–Sc(2)–, связанных мостиковыми карбоксилатными группами и лигандами μ2-ОН–. Катионы Sc(1) и Sc(2) связываются через один лиганд ОН– и две группы RCOO–, а катионы Sc(2) и Sc(2) связываются через две группы RCOO–. Такие последовательности соединяются дополнительными боковыми мостиками μ2-ОН–, связывающими соседние катионы Sc(2) вдоль направления b c образованием двойных цепочек, упомянутых выше. Длины связей Sc–O находятся в диапазоне Sc(1)–O 2.068(2)–2.117(2), Sc(2)–O 2.0700(19)–2.166(2) Å. При формировании кристаллической упаковки двойные цепочки связываются через мостиковые лиганды Tdc2– в шести направлениях, перпендикулярных оси а, с образованием тригональных каналов размером 4 × 3 Å, занятых разупорядоченными молекулами DMF. Объем свободного пространства каналов по данным программы PLATON [24] составляет 31.8%.
Рис. 2.
Фрагмент двойной цепочки из катионов скандия(III) (а) и фрагмент кристаллической структуры соединения II: проекция на плоскость bc (б). Гостевые молекулы растворителя не показаны.
Соединения I и II обладают идентичной формулой координационного каркаса и являются полиморфными модификациями. При сопоставлении условий их кристаллизации и строения можно отметить закономерность, нередко наблюдающуюся для других МОКП: более низкая температура синтеза приводит к более рыхлым структурам в сравнении с более высокими температурами, которые, как правило, приводят к формированию более компактных фаз с меньшей пористостью [25–27]. Действительно, низкотемпературная фаза I имеет кристаллографическую плотность каркаса ρ = 0.97 г/см3 и объем пор 56.7%, в то время как высокотемпературная фаза II имеет плотность ρ = 1.42 г/см3 и объем пор 31.8%.
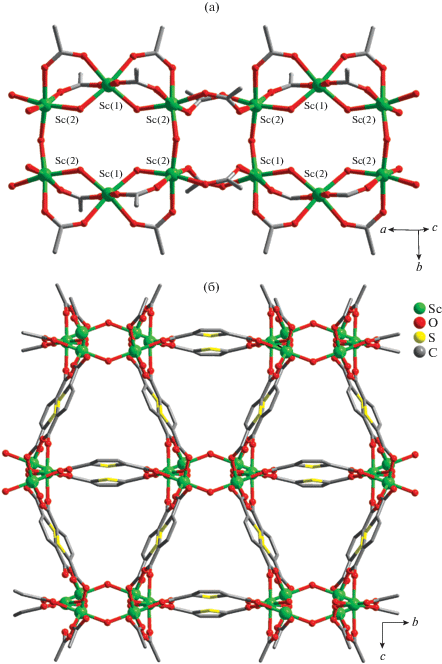
Подкисление реакционного раствора избытком муравьиной кислоты при высокой температуре (120°С) способствует гидролизу DMF с образованием катиона диметиламмония ${\text{M}}{{{\text{e}}}_{{\text{2}}}}{\text{NH}}_{2}^{ + },$ выступающего противоионом для анионного каркаса III. По данным РСА, в структуре III присутствуют три кристаллографически независимых катиона скандия(III). Катионы Sc(1) и Sc(3) находятся в октаэдрическом координационном окружении из шести атомов кислорода одной мостиковой гидроксильной группы OH– и пяти карбоксилатных групп лигандов Tdc2–, две из которых занимают мостиковое положение между катионами Sc(1) и Sc(2) или Sc(3) и Sc(2) (рис. 3а). Катион Sc(2) находится в октаэдрическом координационном окружении из шести атомов кислорода двух мостиковых гидроксильных групп OH– и четырех мостиковых карбоксилатных групп лигандов Tdc2–, связывающих катионы Sc(1) и Sc(2), а также Sc(3) и Sc(2). Катионы Sc(1), Sc(2) и Sc(3) образуют трехядерный вторичный строительный блок {Sc3(RCOO)8(OH)2}. С помощью карбоксилатных мостиковых групп лигандов Tdc2– такие блоки соединяются друг с другом по принципу “голова к голове”, образуя карбоксилатные цепочки (рис. 3а). Такие цепочки связываются между собой мостиковыми лигандами Tdc2– с образованием металл-органического каркаса, в котором наблюдаются ромбовидные каналы (рис. 3б) размером 8 × 3 Å, занятые гостевыми молекулами DMF и катионами диметиламмония. Объем свободного пространства после удаления гостевых молекул растворителя и катионов диметиламмония, по данным программы PLATON [24], составляет 25.5%. Длины связей Sc–O находятся в диапазонах Sc(1)–O 2.069(2)–2.137(2) Å, Sc(2)–O 2.0401(19)–2.1040(19) Å, Sc(3)–O 2.0596(18)–2.158(2) Å.
Рис. 3.
Фрагмент цепочки из катионов скандия(III) (а) и фрагмент кристаллической структуры соединения III (б). Гостевые молекулы растворителя и катионы диметиламмония не показаны.
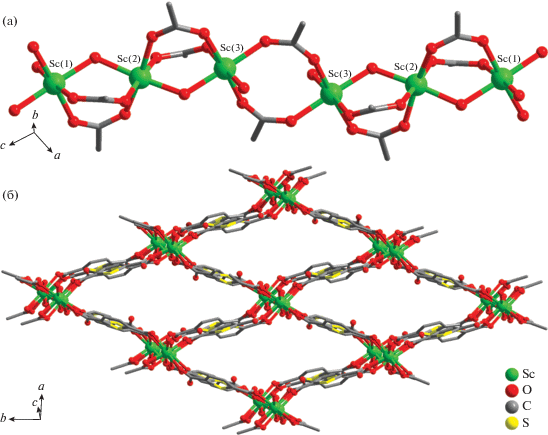
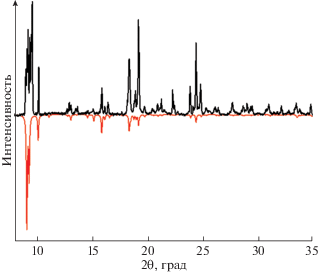
Методику синтеза соединения I удалось оптимизировать для получения представительных количеств продукта, достаточных для его характеризации методами рентгенофазового, элементного анализов, ТГА и ИК-спектроскопии. Как видно из рис. 4, экспериментальная дифрактограмма хорошо согласуется с рассчитанной из данных монокристального РСА, что доказывает фазовую чистоту образца. Согласно кривой ТГА, соединение I теряет 30% массы до температуры 310°С (рис. 5), что соответствует потере 1.4 гостевой молекулы DMF. Данный результат хорошо согласуется с данными РСА и химического анализа. При температуре выше 310°С наблюдается необратимое разложение металл-органического каркаса.
Рис. 4.
Сравнение экспериментальной (черный) и рассчитанной (красный) порошковых дифрактограмм для соединения I.
ИК-спектр соединения I содержит сильную полосу при 772 см–1, относящуюся к деформационным внеплоскостным колебаниям связи C–H в тиофеновом фрагменте лиганда Tdc2–. Группа полос в интервале от 1035 до 1244 см–1 принадлежит валентным колебаниям связи C–N в гостевой молекуле DMF. Характерные интенсивные полосы валентных симметричных и асимметричных колебаний связи С=О находятся при 1380 и 1666 см–1 соответственно. Интенсивные полосы в интервале от 1529 до 1561 см–1 относятся к скелетным колебаниям связи С=С в гетероцикле лиганда Tdc2–. Ряд полос различной интенсивности от 2854 до 3080 см–1 принадлежит валентным колебаниям связи С–Н, а широкая полоса при 3384 см–1 соответствует валентным колебаниям связи О–Н в координированной гидроксильной группе и в гостевой молекуле воды.
Следует отметить, что на сегодняшний день известно только два металл-органических координационных полимера на основе катионов скандия(III) и тиофеновых лигандов [19, 20], в качестве которых выступал 2,5-тиофендикарбоксилат. В 2011 году Ибарра с соавторами получил трехмерный металл-органический координационный полимер [Sc(Tdc)(OH)] · 2.6H2O, названный NOTT-401 [19], который по своему химическому составу похож на соединения I и II, однако отличен от них по строению: NOTT-401 кристаллизуется в тетрагональной группе симметрии I41/amd и состоит из биядерных вторичных строительных блоков {Sc2(μ2-OH)(RCOO)4}. В 2020 году Ванг с соавторами синтезировали трехмерный металл-органический полимер [Sc2(Tdc)2(OH)2] · · 4H2O, который по строению похож на МОКП II, однако в данном случае ОН-группы в октаэдрах {Sc(OH)2O4} располагаются в транс-положении, в то время как в II ОН- группы занимают цис-положение, в результате чего упаковка металл-органического каркаса оказывается отличной от таковой в [20].
Таким образом, результаты данной работы существенно расширяют весьма ограниченный класс металл-органических координационных полимеров на основе Sc(III) и гетероциклических тиофеновых лигандов, которые могут быть использованы как стабильные адсорбенты и катализаторы.
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
Maurin G., Serre C., Cooper A., Férey G. // Chem. Soc. Rev. 2017. V. 46. P. 3104.
Morris R.E., Brammer L. // Chem. Soc. Rev. 2017. V. 46. P. 5444.
Kirchon A., Feng L., Drake H.F. et al. // Chem. Soc. Rev. 2018. V. 47. P. 8611.
Wu D., Zhang P.-F., Yang G.-P. et al. // Coord. Chem. Rev. 2021. V. 434. P. 213709.
Mukherjee S., Sensharma D., Qazvini O.T. et al. // Coord. Chem. Rev. 2021. V. 437. P. 213852.
Zhang G., Hua B., Dey A. et al. //Acc. Chem. Res. 2021. V. 54. V. 155.
Gao C., Lyu F., Yin Y. // Chem. Rev. 2021. V. 121. P. 834.
Hasanpour M., Hatami M. // Adv. Colloid Interface Sci. 2020. V. 284. P. 102247.
Ghomi G.A., Asasian-Kolur N., Sharifian S. et al. // J. Environ. Chem. Eng. 2020. V. 8. P. 103996.
Барсукова М.О., Сапченко С.А., Дыбцев Д.Н. и др. // Успехи химии. 2018. Т. 87. С. 1139.
Serre C., Millange F., Thouvenot C. et al. // J. Am. Chem. Soc. 2002. V. 124. P. 13519.
Loiseau T., Serre C., Huguenard C. et al. // Chem. Eur. J. 2004. V. 10. P. 1373.
Assi H., Mouchaham G., Steunou N. et al. // Chem. Soc. Rev. 2017. V. 46. P. 3431.
Cavka J.H., Jakobsen S., Olsbye U. et al. // J. Am. Chem. Soc. 2008. V. 130. P. 13850.
Bolotov V.A., Kovalenko K.A., Samsonenko D.G. et al. // Inorg. Chem. 2018. V. 57. P. 5074.
Lysova A.A., Samsonenko D.G., Dorovatovskii P.V. et al. // J. Am. Chem. Soc. 2019. V. 141. P. 17260.
Hua C., D’Alessandro D.M. // Cryst. Growth Des. 2017. V. 17. P. 6262.
Zhao J., Shi X., Li G. et al. // Inorg. Chim. Acta. 2012. V. 383. P. 185.
Ibarra I.A., Yang S., Lin X. et al. // Chem. Commun. 2011. V. 47. P. 8304.
Wang P., Zhang L., Zhu Z. et al. // Inorg. Chim. Acta. 2020. P. 119304.
CrysAlisPro Software System. Version 1.171.38.46. Rigaku Oxford Diffraction. Wrocław (Poland): Rigaku Corporation, 2015.
Sheldrick G.M. // Acta Crystallogr. A. 2015. V. 71. P. 3.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3.
Spek A.L. // Acta Crystallogr. С. 2015. V. 71. P. 9.
Dubskikh V.A., Lysova A.A., Samsonenko D.G. et al. // CrystEngComm. 2020. V. 22. P. 6295.
Lysova A., Samsonenko D., Dybtsev D. et al. // Crystals. 2018. V. 8. P. 7.
Hou S.-S., Huang X., Guo J.-G. et al. // CrystEngComm. 2015. V. 17. P. 947.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия